
Früherkennung von AMI durch Einsatz schneller Triage-Algorithmen
Klinik für Kardiologie und Cardiovascular<br>Research Institute Basel (CRIB) <br>Universitätsspital Basel, Schweiz<br>E-Mail: Jasper.Boeddinghaus@usb.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Früherkennung des akuten Myokardinfarkts ist essenziell, um möglichst unmittelbar eine evidenzbasierte Therapie zu initiieren und die Herzmuskulatur zu schützen („Zeit ist Muskel“). Die wichtigsten diagnostischen Eckpfeiler sind hierbei die Anamnese, das 12-Kanal-EKG und die serielle Messung eines herzspezifischen Biomarkers, des kardialen Troponins. Dieses sollte idealerweise unter Verwendung hochsensitiver Assays im peripheren Blut gemessen werden. Durch die von der Europäischen Gesellschaft für Kardiologie empfohlenen Triage-Algorithmen ist es möglich, einen Myokardinfarkt auf der einen Seite sicher und schnell auszuschließen und ihn auf der anderen Seite mit einer hohen Wahrscheinlichkeit zu erkennen.
Keypoints
-
Beim AMI gilt: „Zeit ist Muskel.“
-
Diagnostisch gilt: ausführliche Anamnese, 12-Kanal-EKG und serielle Messung von cTnT/I.
-
hs-cTn-Assays erhöhen die diagnostische Genauigkeit im Vergleich zu konventionellen Assays.
-
Der ESC-0/1h-Algorithmus bei der cTnT/I-Messung ist der bevorzugte Algorithmus.
-
Der 0/1h-Algorithmus scheint auch bei Patienten, die sich später als 12 Stunden nach Symptombeginn vorstellen, vorteilhaft zu sein.
Früherkennung eines akuten Koronarsyndroms
Der Sammelbegriff „akutes Koronarsyndrom“ (ACS) umfasst den akuten Myokardinfarkt (AMI) und die instabile Angina pectoris und stellt somit die unmittelbar lebensbedrohlichen Phasen der koronaren Herzerkrankung dar. In diesem Zusammenhang sei erwähnt, dass kardiovaskuläre Erkrankungen, insbesondere die koronare Herzerkrankung, nach wie vor die häufigste Todesursache in Europa sind.1
Bei Verdacht auf ein ACS wird anhand des 12-Kanal-Elektrokardiogramms (EKG) in ST-Hebungsinfarkt (STEMI) und bei fehlender ST-Hebung durch (serielle) Messung des kardialen Troponins T/I in Nicht-ST-Hebungsinfarkt (NSTEMI) und bei nicht erhöhtem Troponin bzw. fehlender Troponin-Dynamik instabile Angina pectoris unterteilt (Abb. 1).2–6 Die frühzeitige Diagnose ist beim AMI von größter Bedeutung für den rechtzeitigen Beginn einer evidenzbasierten Therapie.2, 4, 5 Eine bisher nicht untersuchte Subpopulation sind jene Patientinnen und Patienten, die sich erst 12 Stunden oder später nach Beginn der Symptome vorstellen.
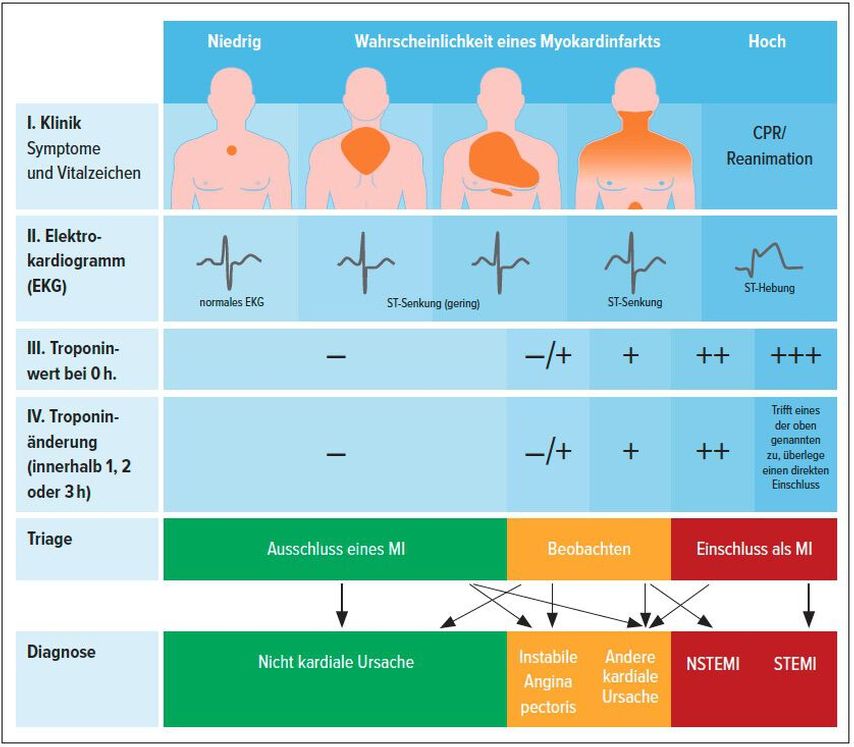
Abb. 1: Diagnostischer Algorithmus und Triage beim akuten Koronarsyndrom ohne persistierende ST-Hebungen (adaptiert nach Roffi M et al.4). Die initiale Einschätzung basiert auf der Integration von Merkmalen mit niedriger bis hoher Wahrscheinlichkeit für einen AMI, abgeleitet aus der klinischen Präsentation (Symptome, Vitalparameter), dem 12-Kanal-EKG und der seriellen Messung des kardialen Troponins. Andere kardiale Diagnosen sind – unter anderem – Myokarditis, Tako-Tsubo-Syndrom oder Herzinsuffizienz. Kardiale Troponine und ihre Dynamik bei der seriellen Messung sollten als quantitative Marker interpretiert werden: je höher der Wert bei Vorstellung in der Notaufnahme beziehungsweise je höher die absolute Veränderung während der seriellen Messung, desto höher die Wahrscheinlichkeit eines AMI. Bei instabilen Patienten (Herzstillstand oder hämodynamische Instabilität) sollte direkt nach dem 12-Kanal-EKG eine Echokardiografie durch erfahrenes Fachpersonal durchgeführt und interpretiert werden. Falls die initiale Beurteilung auf eine Aortendissektion oder Pulmonalarterienembolie hinweist, sollten gegebenenfalls D-Dimere abgenommen und eine Multidetektor-Computertomografie veranlasst werden.9, 10 CPR = kardiopulmonale Reanimation; ECG = Elektrokardiogramm; NSTEMI = Nicht-ST-Hebungsinfarkt, STEMI = ST-Hebungsinfarkt.
Hochsensitives kardiales Troponin
Die hochsensitiven kardialen Troponine (hs-cTn) T und I sind aufgrund ihrer hohen Sensitivität und Spezifität die bevorzugten Biomarker für die Früherkennung des AMI. Diese myofibrillären Proteine sind Bestandteile des kontraktilen Apparats der Myokardzellen (dünnes Filament) und werden fast ausschließlich im Herzen exprimiert (im Gegensatz zum Troponin C). Dementsprechend sind die kardialen Troponine T und I sensitive und spezifische biochemische Marker für jede Art von Kardiomyozytenschaden, nicht nur für den AMI.3, 7, 8
Verglichen mit konventionellen Troponin-T/I-Tests haben die neuen hs-cTn-Assays vor allem den „Rule-out“-Prozess verbessert und durch Reduktion der Notwendigkeit einer kardialen Stresstestung sowie vor allem durch Verkürzung der Zeit bis zur Entlassung aus der Notaufnahme die Kosten reduziert.11 Konzentrationen von hs-cTnT/I sollten immer als quantitative Variablen betrachtet werden und absolute Konzentrationsänderungen sollten gegenüber relativen bevorzugt werden, um zwischen dem Vorliegen eines AMI und anderen Ursachen des Thoraxschmerzes zu unterscheiden (Tab. 1).12, 13 Je ausgeprägter die Dynamik (Anstieg/Abfall) der gemessenen hs-cTn Werte, desto höher ist die Wahrscheinlichkeit eines AMI.12–14

Tab. 1:Klinische Bedeutung hochsensitiver kardialer Troponin-Assays. AMI:akuter Myokardinfarkt; NSTEMI: Nicht-ST-Hebungsinfarkt; hs-cTn: hochsensitives kardiales Troponin; NPV: negativ prädiktiver Wert; PPV = positiver prädiktiver Wert (adaptiert nach Roffi M et al.4)
ESC-0/1h- und -0/2h-Algorithmen
Im letzten Jahrzehnt wurden mehrere Algorithmen zum schnellen Ein-/Ausschluss von AMI basierend auf der seriellen Messung von hs-cTn entwickelt.4, 15–19 Der ESC-0/3h-Algorithmus wurde 2011 erstmals durch die ESC-Richtlinien für NSTE-ACS eingeführt und war der erste auf hs-cTnT/I basierende Triage-Algorithmus mit einem negativ prädiktiven Wert (NPV) >98% für den Ausschluss eines AMI. Mehrere Studien deuten allerdings darauf hin, dass das Gleichgewicht zwischen Wirksamkeit und Sicherheit des ESC-0/3h-Algorithmus durch schnellere Protokolle verbessert werden könnte, die auf niedrigeren Ausschlusskonzentrationen basieren, einschließlich der ESC-0/1h- und -0/2h-Algorithmen.20–23 Die sehr hohe Sicherheit und Wirksamkeit der Anwendung des ESC-0/1h-Algorithmus wurden kürzlich in drei realen Implementierungsstudien bestätigt, darunter eine randomisierte kontrollierte Studie.23–25 Der ESC-0/1h-Algorithmus ist demnach der bevorzugte Algorithmus, da er Sicherheit und Wirksamkeit bestmöglich in Einklang bringt (Abb. 2). Er wurde für alle klinisch verfügbaren hochsensitiven kardialen Troponin-T/I-Assays abgeleitet und validiert. Als erste Alternative wird von den aktuellen Richtlinien der ESC-0/2h-Algorithmus empfohlen.
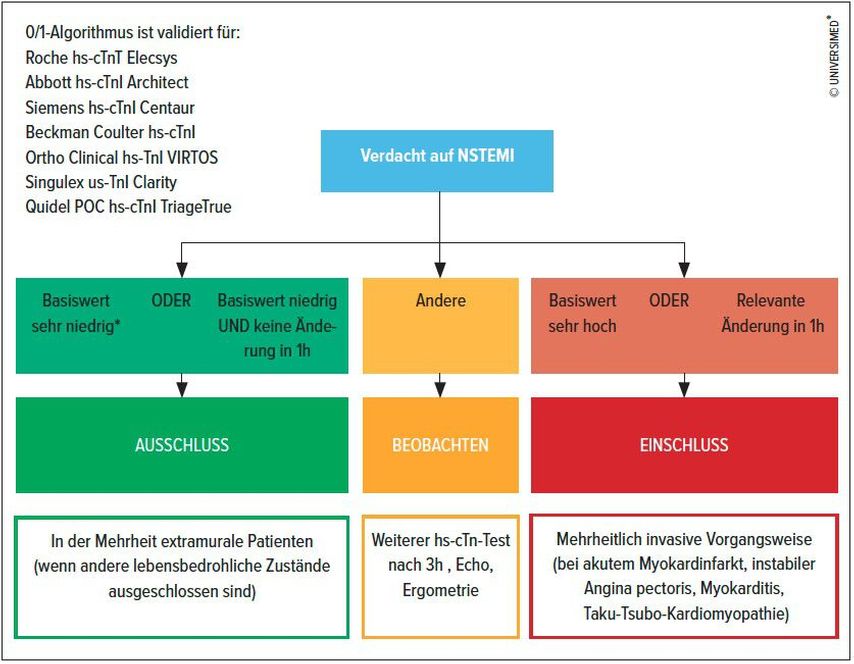
Abb. 2: ESC 0/1h-hs-cTn-Algorithmus zum schnellen Ein- und Ausschluss eines Nicht-ST-Hebungsinfarkts bei Patientinnen und Patienten mit Brustschmerzen auf der Notfallstation. *falls Schmerzbeginn vor mehr als 3 Stunden (adaptiert nach Roffi M, et al.4)
Die wichtige Subpopulation der „late presenters“
Die Performance der schnellen Triage-Algorithmen, insbesondere die des ESC-0/1h-Algorithmus, wurde bis zum heutigen Zeitpunkt ausschließlich bei Patientinnen und Patienten untersucht, welche sich
innerhalb von 12 Stunden nach Brustschmerzbeginn auf der Notaufnahme vorgestellt hatten. Nun beschäftigte man sich, wie im Rahmen eines Posters beim diesjährigen Kongress der Europäischen Gesellschaft für Kardiologie vorgestellt, zum ersten Mal mit der Frage, ob die ausgezeichnete Performance des ESC-0/1h-Algorithmus auch bei den sogenannten „late presenters“ bestehen bleibt. Die jüngsten Forschungsresultate belegen eindrücklich, dass auch bei dieser sehr wichtigen Subpopulation eine sehr hohe Sicherheit mit einer Sensitivität und einem NPV von 100% gegeben ist. Ebenfalls möglich bleibt weiterhin, mit einer hohen Genauigkeit zu sagen, dass ein NSTEMI vorliegt (positiv prädiktiver Wert, PPV, 75% und Spezifität 95%). Diese Resultate tragen erheblich zum besseren Verständnis der Performance des ESC-0/1h-Algorithmus bei dieser Patientenpopulation bei und zeigen auf, dass der 0/1h-Algorithmus auch bei Patientinnen und Patienten angewendet werden kann, die sich sehr lange nach Beginn ihrer Symptome auf der Notaufnahme vorstellen.
Schlussfolgerungen
Die Früherkennung des AMI ist essenziell, um so viel gefährdetes Myokard wie möglich zu schützen („Zeit ist Muskel“). Erhöhte Konzentrationen von cTnT/I sind im Rahmen einer akuten oder chronischen Kardiomyozytenschädigung zu interpretieren und nicht zwangsläufig beweisend für das Vorliegen eines AMI. Die genaue klinische Untersuchung inklusive ausführlicher Anamnese, des 12-Kanal-EKGs und der seriellen Messung von cTnT/I als quantitativer Variable sind grundlegend, um einen AMI von anderen Ursachen der Kardiomyozytenschädigung zu unterscheiden. Die Anwendung von hs-cTn-Assays (versus konventionelle Assays) erhöht die diagnostische Genauigkeit in Bezug auf das Vorliegen eines AMI bei Vorstellung in der Notaufnahme und verkürzt das Zeitintervall bis zur zweiten Messung. Der ESC-0/1h-Algorithmus ist aktuell der bevorzugte Algorithmus, da er ein optimales Gleichgewicht zwischen Sicherheit und Wirksamkeit bietet und für alle klinisch verfügbaren hs-cTnT/I-Assays validiert wurde. Diese hervorragenden Eigenschaften des ESC-0/1h-Algorithmus scheinen auch bei Patientinnen und Patienten, die sich später als 12 Stunden nach Symptombeginn vorstellen, erhalten zu bleiben.
Literatur:
1 Naghavi M et al.: Global, regional, and national age-sex specifc mortality for 264 causes of death, 1980-2016: A systematic analysis for the Global Burden of Disease Study 2016. Lancet 2017; 390: 1151-210 2 Thygesen K et al.: Fourth universal definition of myocardial infarction (2018). Eur Heart J 2019; 40: 237-69 3 Thygesen K et al.: How to use high-sensitivity cardiac troponins in acute cardiac care. Eur Heart J 2012; 33: 2252-7 4 Roffi M et al.: 2015 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation: Task Force for the Management of Acute Coronary Syndromes in Patients Presenting without Persistent ST-Segment Elevation. Eur Heart J 2016; 37: 267-315 5 Ibanez B et al.: 2017 ESC Guidelines for the management of acute myocardial infarction in patients presenting with ST-segment elevation: The Task Force for the management of acute myocardial infarction in patients presenting with ST-segment elevation of the European Society of Cardiology (ESC). Eur Heart J 2017: doi: 10.1093/eurheartj/ehx393 6 Collet J-P et al.: 2020 ESC Guidelines for the management of acute coronary syndromes in patients presenting without persistent ST-segment elevation. Eur Heart J 2020: 1-79 7 Mueller C: Biomarkers and acute coronary syndromes: an update. Eur Heart J 2014 35: 552-6 8 Giannitsis E et al.: Analytical validation of a high-sensitivity cardiac troponin T assay. Clin Chem 2010; 56: 254-61 9 Konstantinides S V et al.: 2019 ESC Guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur Respir J 2019. doi: 10.1183/13993003.01647-2019 10 Erbel R et al.: 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European. Eur Heart J 2014; 35: 2873-926 11 Twerenbold R et al.: Impact of high-sensitivity cardiac troponin on use of coronary angiography, cardiac stress testing, and time to discharge in suspected acute myocardial infarction. Eur Hear J 2016; 37: 3324-32 12 Reichlin T et al.: Utility of absolute and relative changes in cardiac troponin concentrations in the early diagnosis of acute myocardial infarction. Circulation 2011; 124: 136-45 13 Mueller M et al.: Absolute and relative kinetic changes of high-sensitivity cardiac troponin T in acute coronary syndrome and in patients with increased troponin in the absence of acute coronary syndrome. Clin Chem 2012 58: 209-18 14 Neumann JT et al.: Application of high-sensitivity troponin in suspected myocardial infarction. N Engl J Med 2019; 380: 2529-40 15 Boeddinghaus J et al.: Direct comparison of 4 very early rule-out strategies for acute myocardial infarction using high-sensitivity cardiac troponin I. Circulation 2017: doi: 10.1161/CIRCULATIONAHA.116.025661 16 Wildi K et al.: Comparison of fourteen rule-out strategies for acute myocardial infarction. Int J Cardiol 2019; 283: 41-7 17 Rubini Gimenez M et al.: One-hour rule-in and rule-out of acute myocardial infarction using high-sensitivity cardiac troponin I. Am J Med 2015; doi: 10.1016/j.amjmed.2015.01.046 18 Wildi K et al.: Safety and efficacy of the 0h/3 h protocol for rapid rule out of myocardial infarction. Am Heart J 2016: doi: 10.1016/j.ahj.2016.07.013 19 Reichlin T et al.: One-hour rule-out and rule-in of acute myocardial infarction using high-sensitivity cardiac troponin T. Arch Intern Med 2012 172: 1211-8 20 Badertscher P et al.: Direct comparison of the 0/1h and 0/3h algorithms for early rule-out of acute myocardial infarction. Circulation 2018; 137: 2536–8 21 Chapman AR et al.: Comparison of the efficacy and safety of early rule-out pathways for acute myocardial infarction. Circulation 2017; 135: 1586-96 22 Chapman AR et al.: Novel high-sensitivity cardiac troponin I assay in patients with suspected acute coronary syndrome. Heart 2019; 105: 616-22 23 Chew DP et al.: A randomized trial of a 1-hour troponin T protocol in suspected acute coronary syndromes: the rapid assessment of possible acute coronary syndrome in the emergency department with high-sensitivity troponin T study (RAPID-TnT). Circulation 2019; 140: 1543-56 24 Stoyanov KM et al.: RAPID-CPU: a prospective study on implementation of the ESC 0/1-hour algorithm and safety of discharge after rule-out of myocardial infarction. Eur Hear J Acute Cardiovasc Care 2019: 204887261986191 25 Twerenbold R et al.: Outcome of applying the ESC 0/1-hour algorithm in patients with suspected myocardial infarction. J Am Coll Cardiol 2019: 74: 483–94
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...


