Eisensubstitution: New kid on the block or more of the same?
Autor:innen:
Dr. Noel G. Panagiotides
Dr.in Henrike Arfsten, PhD, FHFA
Medizinische Universität Wien
Universitätsklinik für Innere Medizin II, Abteilung für Kardiologie, Wien
E-Mail: henrike.arfsten@meduniwien.ac.at
Eisenmangel ist eine häufige Komorbidität chronischer Erkrankungen. Mit einer Prävalenz von bis zu 50% leidet ein signifikanter Teil symptomatischer Patienten im gesamten Herzinsuffizienzspektrum an einem Eisenmangel. Dieser tritt bei einer großen Zahl der Patienten unabhängig vom Vorliegen einer Anämie auf.1 Eisenmangel bei Herzinsuffizienz wirkt sich auf die Symptomatik, gemessen am NYHA-Stadium, die körperliche Leistungsfähigkeit, die Lebensqualität und die Prognose aus.2–4
Keypoints
-
Die Definition von Eisenmangel bei Herzinsuffizienz ist: Ferritin <100ng/ml oder 100–300ng/ml und TSAT <20%.
-
Eisenmangel betrifft etwa die Hälfte aller Herzinsuffizienzpatienten und beeinträchtigt Symptome, Leistungsfähigkeit, Lebensqualität und Prognose unabhängig von anderen Risikofaktoren oder Anämie.
-
Orale Eisentherapie wird bei Eisenmangel in der Herzinsuffizienz nicht empfohlen.
-
Die intravenöse Eisentherapie mit Eisen-Carboxymaltose oder Eisen-Derisomaltose wird bei Eisenmangel in der Herzinsuffizienz empfohlen und lindert Symptome, verbessert die Lebensqualität, steigert die körperliche Leistungsfähigkeit und verringert das Risiko für Krankenhausaufenthalte.
Die Diagnostik eines Eisenmangels sollte unabhängig vom roten Blutbild durchgeführt werden und wird in der Herzinsuffizienz definiert als:
-
Serum-Ferritin-Konzentration <100ng/ml
-
oder Serum-Ferritin-Konzentration von 100–300ng/ml + Transferrinsättigung (TSAT) <20%.
Ursachen und Stellenwert des Eisenmangels in der Herzinsuffizienz
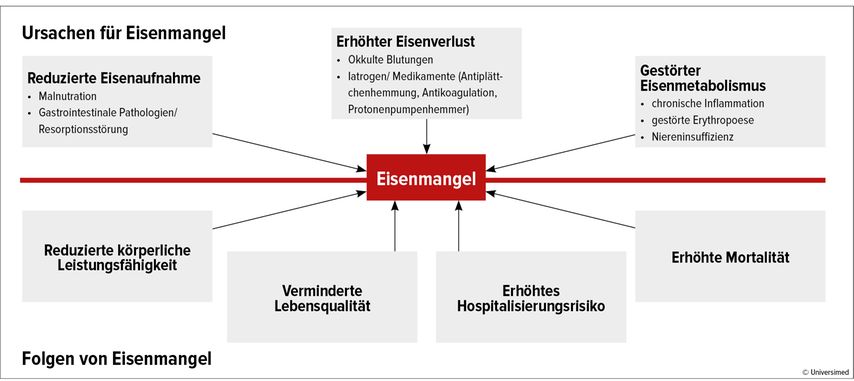
Die Entwicklung des Eisenmangels bei Patienten mit Herzinsuffizienz ist oft multifaktoriell, wobei drei Einflussgrößen eine wesentliche Rolle spielen (Abb. 1):5,6
-
eine gestörte Darmabsorption,
-
ein erhöhter Eisenverlust (okkulter Blutverlust) und
-
als wahrscheinlich wesentlichster Faktor eine metabolische Dysregulation.
Abb. 1:Ursachen und Folgen von Eisenmangel in der Herzinsuffizienz: 1) Reduzierte Eisenaufnahme/Eisenabsorption, 2) gestörter Eisenmetabolismus und 3) erhöhter Eisenverlust bedingen bei Patienten mit Herzinsuffizienz die Entwicklung eines Eisenmangels. Zu den daraus entstehenden Folgen gehören reduzierte körperliche Leistungsfähigkeit, geringere Lebensqualität, höhere Rehospitalisierungsraten und eine erhöhte Sterblichkeit
Die zentrale Stellschraube in der Regulation des Eisenhaushalts ist Hepcidin, ein von den Hepatozyten synthetisiertes und sezerniertes Protein.7 Hepcidin steuert die Aktivität des Transmembranproteins Ferroportin, das für den Eisenexport sowohl aus den Darm-Enterozyten (Absorption) als auch aus den Hepatozyten und Makrophagen des retikuloendothelialen Systems der Leber (Mobilisierung) verantwortlich ist.7,8 Die Bindung von Hepcidin an Ferroportin führt zu Inaktivierung der Eisenabsorption und Blockierung der Eisen-mobilisierung.7 Bei inflammatorischen Krankheitsbildern, wie auch der Herzinsuffizienz, kommt es zu chronisch erhöhten Hepcidin-Spiegeln, was die Eisenhomöostase behindert und unweigerlich zu einem funktionellen und schließlich absoluten Eisenmangel führt.7,9
Eisen ist jedoch ein wichtiger Kofaktor und Katalysator vieler enzymatischer Reaktionen und ein Schlüsselbestandteil von Strukturproteinen.7 Es ist wesentliche Komponente von Sauerstoffspeicherung, Sauerstofftransport und oxidativer Reaktionen und somit von grundlegender Bedeutung für die Funktion der Mitochondrien und die aerobe Atmung.10 Besonders vulnerabel auf einen Eisenmangel reagieren, im Sinne einer unzureichenden zellulären Energieversorgung, Zellen mit hohem Energiebedarf (z.B. Kardio-/und Myozyten).11 Diese Beeinträchtigung der Substratnutzung und der Energieversorgung in Herz- und Skelettmuskel ist eine Erklärung für die Auswirkungen eines Eisenmangels auf die Symptomatik und die Krankheitsprogression in der Herzinsuffizienz.12
Evidenz und Therapieempfehlung zur Eisentherapie in der Herzinsuffizienz
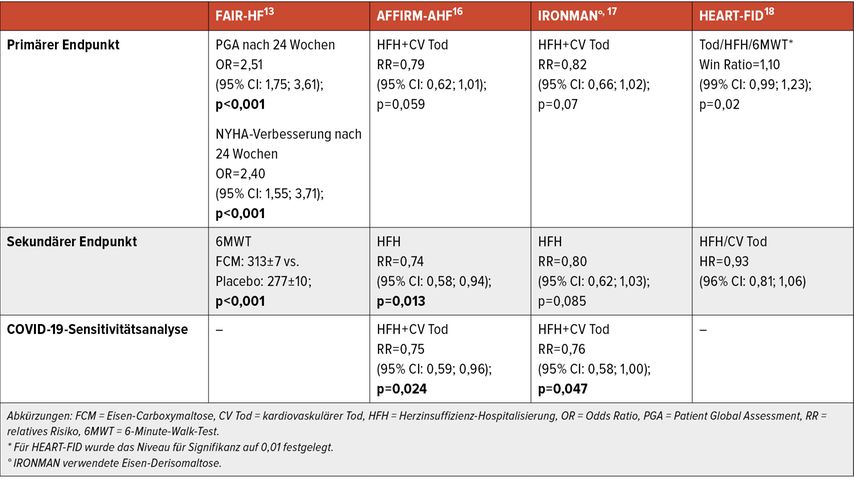
Vor dem Hintergrund, dass einem Eisenmangel hinsichtlich der Symptomatik und der Krankheitsprogression bei Patienten mit Herzinsuffizienz ein wesentlicher Stellenwert zukommt, wächst in den letzten Jahren auch die therapeutische Evidenz. Die wichtigsten Ergebnisse rezenter prospektiv randomisierter klinischer Studien, die sich zum aktuellen Stand nur auf Patienten mit HFrEF oder HFmrEF (LVEF <50%) beschränken, sind in Tabelle 1 zusammengefasst.
Zu den ersten Studien, die als prospektive randomisierte Studien den Nutzen und die Sicherheit einer intravenösen Eisentherapie bei Patienten mit Eisenmangel und Herzinsuffizienz und einer LVEF ≤45% untersuchten, gehören FAIR-HF, CONFIRM-HF und EFFECT-HF.13-15 Die Studien zeigten, dass die intravenöse Therapie mit Eisen-Carboxymaltose sicher ist und in einer Verbesserung der körperlichen Leistungsfähigkeit und Lebensqualität im Vergleich zur Placebogabe resultierte.
Diesen Resultaten schlossen sich die Studien AFFIRM-AHF, IRONMAN und HEART-FID mit nun harten klinischen Endpunkten (Herzinsuffizienz-Hospitalisierung und/oder Tod) an.16–18
In AFFIRM-AHF wurden 1132 Herzinsuffizienzpatienten (LVEF <50%) mit Eisenmangel nach einem akuten Event inkludiert. Nach einem Beobachtungszeitraum von 52 Wochen zeigte sich der primäre kombinierte Studienendpunkt aus Herzinsuffizienz-Hospitalisierung (HFH) oder kardiovaskulärem (CV) Tod nicht signifikant reduziert (p=0,059).16 Es konnte aber eine signifikante Reduktion der HFH gezeigt werden.
IRONMAN untersuchte den Einsatz von intravenöser Eisen-Derisomaltose bei Patienten mit chronischer Herzinsuffizienz bzw. nach einem rezenten akuten Event (n=1132, LVEF ≤45%) und zeigte ebenfalls keinen signifikanten Therapievorteil hinsichtlich des kombinierten primären Studienendpunkts HFH oder CVTod.17
Eine wesentliche Limitation in der Durchführung beider Studien war die Covid-19-Pandemie, die u.a. Ereignisraten in beiden Studiengruppen beeinflusst haben könnte. Denn in prädefinierten Covid-19-Sensitivitätsanalysen zeigte sich ein Therapie-Benefit mit signifikanter Reduktion von HFH oder CVTod durch die intravenöse Therapie mit Eisen-Carboxymaltose (AFFIRM-AHF) oder Eisen-Derisomaltose (IRONMAN).16,17
HEART-FID ist die rezenteste und bislang größte Studie zur Eisentherapie in der Herzinsuffizienz (n=3065; LVEF ≤40%). Hier zeigte sich ein ähnliches Bild wie bei den vorigen Studien, wobei der hierarchisch kombinierte Endpunkt aus CVTod, HFH und Änderung der 6-Minute-Walk-Distanz (6MWD) verfehlt wurde (p=0,02; Signifikanzniveau p<0,01).18Auch in HEART-FID wurde die Mehrzahl der Patienten während der Pandemie rekrutiert, was möglicherweise die Eventraten und Datenvollständigkeit beeinflusst hat.
Zusammenfassend zeigen die vorliegenden randomisierten Studien und Metaanalysen Sicherheit und gute Verträglichkeit der intravenösen Eisensupplementierung bei Patienten mit HFrEF/HFmrEF und Eisenmangel.13,14,16,19 Die Therapie geht mit einer Verbesserung der Leistungsfähigkeit und Lebensqualität sowie einer Reduktion von HFH einher und stellt somit eine wesentliche Komponente im Therapiemanagement der Herzinsuffizienzpatienten dar.12,14,19 Der Einfluss auf die CV oder Gesamtmortalität ist nach wie vor inkonklusiv.19,26
Es sei hier angemerkt, dass die orale Eisentherapie keinen Stellenwert in der Therapie des Eisenmangels in der Herzinsuffizienz hat. Dies ist durch prospektive Daten klar nachgewiesen (u.a. IRONOUT-Studie).27
Therapieempfehlung
Basierend auf der aktuellen Evidenz, empfehlen die Leitlinien der European Society of Cardiology (ESC), Patienten mit Herzinsuffizienz regelmäßig auf das Vorliegen eines Eisenmangels zu untersuchen (Blutbild, Serum-Ferritin-Konzentration, Transferrin-Sättigung).28,29
Auf der Grundlage von Studien und neueren Metaanalysen wird die intravenöse Eisensupplementierung mit Eisen-Carboxymaltose oder Eisen-Derisomaltose bei Patienten mit symptomatischer HFrEF oder HFmrEF und Eisenmangel empfohlen, um die Symptome und Lebensqualität zu verbessern (Klasse I, Evidenz-Level A).29 Eine Klasse-IIa-, Evidenz-Level-A-Empfehlung gibt es bei diesen Patienten mit dem Ziel der Risikoreduktion für HFH (Tab. 2).29
Ausblick
Ein in vielen Aspekten hinsichtlich existierender Evidenz und Therapieoptionen häufig hinten angestelltes Patientenkollektiv in der Herzinsuffizienz ist die Herzinsuffizienz mit erhaltener Auswurffraktion (HFpEF). Wir wissen, dass die Prävalenz des Eisenmangels in der HFpEF mindestens jener der HFmrEF oder HFrEF entspricht.1 Ob auch Patienten mit HFpEF und Eisenmangel von einer intravenösen Eisensupplementierung profitieren, wird aktuell in den Studien FAIR-HFpEF und IRONMET-HFpEF untersucht.
Literatur:
1 Lindberg F et al.: Iron deficiency in heart failure: screening, prevalence, incidence and outcome data from the Swedish Heart Failure Registry and the Stockholm CREAtinine Measurements collaborative project. Eur J Heart Fail 2023; 25(8): 1270-80 2 Enjuanes C et al.: Iron deficiency and health-related quality of life in chronic heart failure: Results from a multicenter European study. Int J Cardiol 2014; 174(2): 268-75 3 Martens P et al.: Impact of iron deficiency on exercise capacity and outcome in heart failure with reduced, mid-range and preserved ejection fraction. Acta Cardiol 2018; 73(2): 115-123 4 Jankowska EA et al.: Iron deficiency: an ominous sign in patients with systolic chronic heart failure. Eur Heart J 2010; 31(15): 1872-80 5 Anand IS et al.: Current Concepts and Emerging Therapies. Circulation 2018; 138(1): 80-98 6 Van Der Wal HH et al.: Iron deficiency in worsening heart failure is associated with reduced estimated protein intake, fluid retention, inflammation, and antiplatelet use. Eur Heart J 2019; 40(44): 3616-25 7 Von Haehling S et al.: Iron deficiency and cardiovascular disease. Nat Rev Cardiol 2015; 12(11): 659-69 8 Ganz T, Nemeth E: Iron imports. IV. Hepcidin and regulation of body iron metabolism. Am J Physiol - Gastrointest Liver Physiol 2006; 290(2): 199-203 9 Nicolas G et al.: The gene encoding the iron regulatory peptide hepcidin is regulated by anemia, hypoxia, and inflammation. J Clin Invest 2002; 110(7): 1037-44 10 Neubauer S: The Failing Heart — an engine out of fuel. https://doi.org/101056/NEJMra063052 2007; 356(11): 1140-51 11 Boyman L et al.: Regulation of mitochondrial ATP production: Ca2+ signaling and quality control. Trends Mol Med 2020; 26(1): 21-39 12 Brown DA et al.: Expert consensus document: Mitochondrial function as a therapeutic target in heart failure. Nat Rev Cardiol 2017; 14(4): 238-50 13 Anker SD et al.: Ferric carboxymaltose in patients with heart failure and iron deficiency. N Engl J Med 2009; 361(25): 2436-48 14 Ponikowski P et al.: Beneficial effects of long-term intravenous iron therapy with ferric carboxymaltose in patients with symptomatic heart failure and iron deficiency†. Eur Heart J 2015; 36(11): 657-68 15 Van Veldhuisen DJ et al.: Effect of Ferric Carboxymaltose on Exercise Capacity in Patients With Chronic Heart Failure and Iron Deficiency. Circulation 2017; 136(15): 1374-83 16 Ponikowski P et al.: Ferric carboxymaltose for iron deficiency at discharge after acute heart failure: a multicentre, double-blind, randomised, controlled trial. Lancet (London, England) 2020; 396(10266): 1895-1904 17 Kalra PR et al.: Intravenous ferric derisomaltose in patients with heart failure and iron deficiency in the UK (IRONMAN): an investigator-initiated, prospective, randomised, open-label, blinded-endpoint trial. Lancet (London, England) 2022; 6736(22): 1-11 18 Mentz RJ et al.: Ferric carboxymaltose in heart failure with iron deficiency. N Engl J Med 2023; 389(11): 975-86 19 Anker SD et al.: Effect of intravenous iron replacement on recurrent heart failure hospitalizations and cardiovascular mortality in patients with heart failure and iron deficiency: A Bayesian meta-analysis. Eur J Heart Fail 2023; 25(7): 1080-90 20 Comin-Colet J et al.: The effect of intravenous ferric carboxymaltose on health-related quality of life in patients with chronic heart failure and iron deficiency: a subanalysis of the FAIR-HF study. Eur Heart J 2013; 34(1): 30-8 21 Anker SD et al.: Ferric carboxymaltose in patients with heart failure and iron deficiency. N Engl J Med 2009; 361(25): 2436-48 22 Vukadinović D et al.: Efficacy and safety of intravenous iron repletion in patients with heart failure: a systematic review and meta-analysis. Clin Res Cardiol 2023; 112(7): 954-66 23 Salah HM et al.: Intravenous iron infusion in patients with heart failure: a systematic review and study-level meta-analysis. ESC Hear Fail 2023; 10(2): 1473-80 24 Jhund PS et al.: Heart Failure Hospitalization in Adults Receiving Hemodialysis and the Effect of Intravenous Iron Therapy. JACC Heart Fail 2021; 9(7): 518-27 25 Macdougall IC et al.: Intravenous iron in patients undergoing maintenance hemodialysis. N Engl J Med 2019; 380(5): 447-58 26 Graham FJ et al.: Intravenous iron in patients with heart failure and iron deficiency: an updated meta-analysis. Eur J Heart Fail 2023; 25(4): 528-37 27 Lewis GD et al.: Effect of oral iron repletion on exercise capacity in patients with heart failure with reduced ejection fraction and iron deficiency: the IRONOUT HF randomized clinical trial. JAMA 2017; 317(19): 1958-66 28 McDonagh TA et al.: 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021; 42(36): 3599-726 29 McDonagh TA et al.: 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failureDeveloped by the task force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC) Wit. Eur Heart J. Published online 2023
Das könnte Sie auch interessieren:
ESC gibt umfassende Empfehlung für den Sport
Seit wenigen Tagen ist die erste Leitlinie der ESC zu den Themen Sportkardiologie und Training für Patienten mit kardiovaskulären Erkrankungen verfügbar. Sie empfiehlt Training für ...
ESC-Guideline zur Behandlung von Herzvitien bei Erwachsenen
Kinder, die mit kongenitalen Herzvitien geboren werden, erreichen mittlerweile zu mehr 90% das Erwachsenenalter. Mit dem Update ihrer Leitlinie zum Management kongenitaler Vitien bei ...
Inclisiran bei Patienten mit Statinintoleranz wirksam und sicher
Eine Analyse statinintoleranter Patienten aus dem Phase III Studienprogramm ORION zeigt, dass Inclisiran die LDL-Cholesterinspiegel kardiovaskulärer Hochrisikopatienten, die kein Statin ...