Eine Fülle an neuen Daten zu urogenitalen Tumoren
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Am diesjährigen virtuellen Meeting der European Society for Medical Oncology (ESMO) wurden zahlreiche interessante Daten zu urogenitalen Tumoren präsentiert. PD Dr. med. Aurelius Omlin vom Kantonsspital St. Gallen schildert seine Highlights zu den Karzinomen der Niere, der Prostata und des Urothels und spricht dabei u.a. über vielversprechende Ergebnisse zu unterschiedlichen Kombinationen, welche Inhibitoren wie Immuncheckpoint-, PARP- bzw. AKT-Inhibitoren inkludieren, und die kontinuierliche Suche nach prädiktiven Biomarkern. Zudem verrät er, von welchen grossen Phase-III-Studien er sich durchaus mehr erhofft hätte.
Was waren Ihre ESMO-Highlights zum Nierenzellkarzinom?
A. Omlin: Ich würde gern mit der CheckMate-9ER-Studie beginnen, einer Erstlinienstudie bei Patienten mit metastasiertem Nierenzellkarzinom mit hellzelliger Komponente, welche Nivolumab und Cabozantinib in der Kombination verglichen mit Sunitinib erhielten. Es gab bereits einige Studien, die einen Checkpoint-Inhibitor mit einem Tyrosinkinase-Inhibitor kombiniert und mit Sunitinib verglichen haben. Von daher vermag es vielleicht wenig überraschen, dass die Resultate positiv waren: Es konnte eine Verdoppelung des progressionsfreien Überlebens von 8,3 auf 16,6 Monate gezeigt werden (Abb. 1) sowie eine deutliche Verbesserung des Ansprechens von 27% unter Sunitinib im Vergleich zu 55,7% unter der Kombination von Cabozantinib und Nivolumab. Interessanterweise zeigte sich sogar eine bessere Lebensqualität im Kombinationsarm verglichen mit Sunitinib. Auch die Nebenwirkungsprofile unterschieden sich nicht wesentlich.Die Studie hat etwa 20% «Poor risk»-Patienten nach IMDC-Kriterien eingeschlossen, was ich als sehr wichtig erachte. Wenn man eine gute Response erreichen möchte, ist diese Kombination also eine attraktive Kombination in der Erstlinie – sofern sie denn zugelassen wird. Die Alternative wäre Pembrolizumab und Axitinib oder möglicherweise die Immunkombination mit Ipilimumab und Nivolumab.
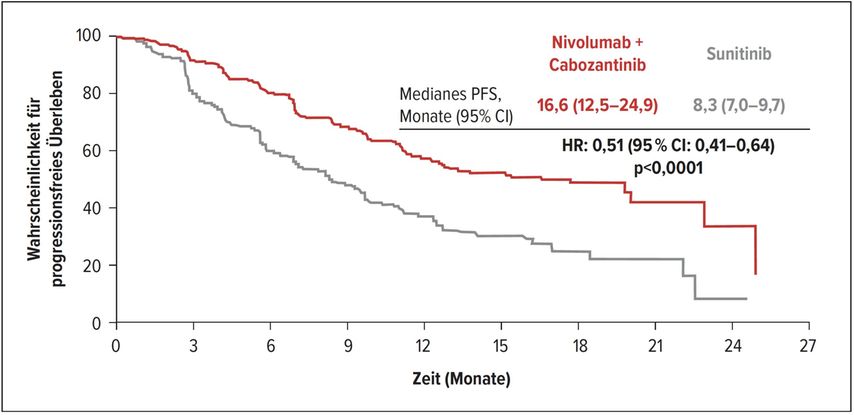
Abb. 1: Progressionsfreies Überleben in der CheckMate-9ER-Studie (nach Choueiri T et al.: ESMO 2020, Abstr. #696O_PR)
Am ESMO-Meeting wurde eine weitere, allerdings nur Phase-Ib-Studie vorgestellt, die ebenfalls Cabozantinib in der Kombination mit einem Checkpoint-Inhibitor, in diesem Fall Atezolizumab, untersucht. Es zeigten sich ein gutes Ansprechen und ebenso ein sehr langes progressionsfreies Überleben von fast 20 Monaten. Da es sich bei den Studienteilnehmern aber um selektionierte Phase-I-Patienten handelt, sind die Ergebnisse jedoch mit Vorsicht zu interpretieren. Cabozantinib wurde, genauso wie auch in anderen Studien, in einer Dosierung von 40mg täglich verabreicht. In der PhaseIb gab es auch eine 60-mg-Kohorte. Diese Dosis war jedoch toxischer und einige Patienten mussten die Dosis dementsprechend reduzieren. Die Kombination aus Cabozantinib und Atezolizumab wird weiter untersucht und es läuft bereits eine Phase-III-Studie zu dieser Kombination.
Ausserdem gab es zum Nierenzellkarzinom zwei interessante Beiträge zu prädiktiven Markern. Erstens wurde im Rahmen der NIVOREN-Studie gewonnenes Gewebe von Patienten, die Nivolumab zur Therapie des metastatierten Nierenzellkarzinoms erhalten hatten, mittels RNA-Sequenzierung untersucht. Patienten mit einem hohen Score für T-Effektor-Zellen und einem niedrigen Score für Angiogenese scheinen besonders gut auf die Immuntherapie anzusprechen. Das muss allerdings sicher noch weiter untersucht werden.
Zweitens wurde in einer am ESMO-Meeting präsentierten wissenschaftlichen Arbeit nach Genveränderungen sowohl in zirkulierender Tumor-DNA als auch in Gewebeproben von Patienten mit metastasiertem Nierenzellkarzinom gesucht. Die Analyse von zirkulierender Tumor-DNA ist machbar und zeigt insgesamt auch eine gute Korrelation mit Alterationen, welche am Tumorgewebe gefunden wurden. Solche Untersuchungen könnten in Zukunft helfen die Systemtherapie unter Umständen frühzeitig anzupassen, wenn sich z.B. Resistenzmechanismen anhand der zirkulierenden Tumor-DNA feststellen lassen.
Zwar können die besprochenen Ergebnisse nicht direkt im Alltag eingesetzt werden, aber es wird gut aufgezeigt, dass mit dem Gewebe, das im Rahmen der Studien gewonnen wird, Forschungsarbeiten betrieben werden können und dies auch tatsächlich geschieht. In Zukunft können sich also möglicherweise prädiktive Marker herauskristallisieren.
Welche der am ESMO-Meeting zum Prostatakarzinom präsentierten Daten waren für Sie besonders wichtig?
A. Omlin: Eines der Highlights war die IPATential-150-Studie, bei welcher im Juni einer der koprimären Endpunkte erreicht worden war. In dieser Studie wurden Patienten mit wenig symptomatischem oder asymptomatischem Prostatakarzinom in der ersten Linie der kastrationsresistenten Situation eingeschlossen und randomisiert zu entweder Abirateron + Placebo oder Abirateron + Ipatasertib, einem AKT-Inhibitor. Es gab verschiedene Stratifikationsfaktoren, darunter PTEN-Verlust. Der koprimäre Endpunkt war das radiografisch progressionsfreie Überleben in der gesamten Population und auch in der Population mit PTEN-Verlust. Bei Patienten mit Verlust von PTEN hat die Kombination aus Abirateron + Ipatasertib zu einem 2 Monate längeren radiografisch progressionsfreien Überleben geführt. Auch die Ansprechrate war unter der Kombination besser als im Behandlungsarm mit Abirateron + Placebo. Jedoch zeigte die Kombination mit Ipatasertib eine nicht unwesentliche Toxizität von 10–15% an Nebenwirkungen vom Grad 3–4, u.a. Hautausschlag, Durchfall, Hyperglykämie und Leberwerterhöhung. Der koprimäre Endpunkt in der Gesamtpopulation wurde nicht erreicht. Insgesamt gilt die Studie also als formal negativ, obwohl in der Subgruppe mit PTEN-Verlust der Endpunkt erreicht wurde. Ich bin gespannt, ob diese Kombination eine Zulassung erreichen wird. Ein Update vor allem auch zum Gesamtüberleben wird folgen.
Ein weiteres interessantes Update gab es am ESMO-Meeting zur PROfound-Studie, die Patienten mit kastrationsresistentem Prostatakarzinom miteinschloss, welche nach Therapie mit Abirateron oder Enzalutamid oder beidem progredient waren. Zwei Drittel hatten auch eine Chemotherapie erhalten. In der Kohorte A waren Patienten BRCA1-, BRCA2- oder ATM-Alterationen eingeschlossen, in der Kohorte B waren Patienten mit verschiedenen weiteren Genmutationen inkludiert, welche möglicherweise auf eine PARP-Inhibition mit Olaparib ansprechen. Als primärer Endpunkt galt das radiologisch nachgewiesene progressionsfreie Überleben, welches bereits vorgestellt worden war. Am ESMO-Meeting wurden nun die Ergebnisse zum Gesamtüberleben gezeigt. Es konnte das Gesamtüberleben bei Patienten der Kohorte A mit Olaparib im Vergleich zum Kontrollarm mit Abirateron oder Enzalutamid deutlich verlängert werden. Es lässt sich ein fast 5-monatiger Gesamtüberlebensvorteil erkennen (Abb.2). Werden dann noch die Patienten exkludiert, welche ein Cross-over durchgeführt haben, ist der Überlebensvorteil sogar noch grösser.
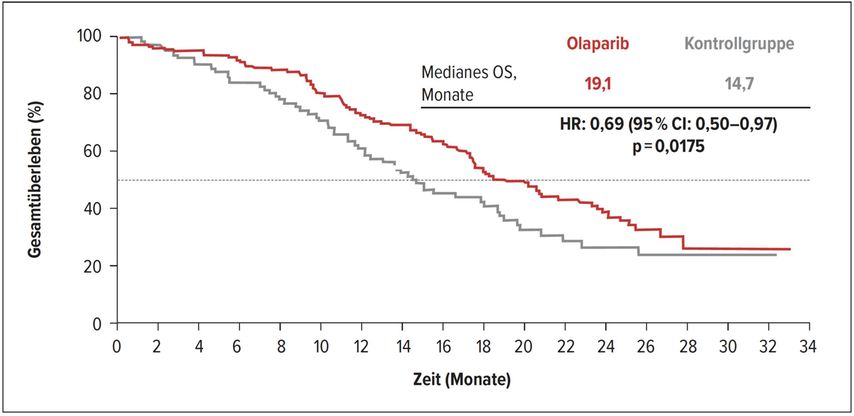
Abb. 2: Gesamtüberleben in der PROfound-Studie (nach De Bono JS et al.: ESMO 2020, Abstr. #610O)
Von besonderem Interesse sind die einzelnen Subgruppen. Am meisten konnten Patienten mit BRCA2-Alterationen von der Therapie mit Olaparib profitieren. In den USA ist Olaparib bei Patienten mit kastrationsresistentem metastasiertem Prostatakarzinom, welche Mutationen in diesen Genen der homologen Rekombinationsreparatur aufweisen, bereits zugelassen. In der Schweiz ist eine Zulassung noch ausständig und wir werden sehen, wie sich dies entwickeln wird. Im Moment ist Olaparib sicher eine gute Option für Patienten mit nachgewiesen Mutationen in BRCA1/2. Die Anwendung von Olaparib bei anderen Mutationen muss wahrscheinlich noch genauer untersucht werden.
Zur STAMPEDE-Studie sind nun die Daten eines 6-Jahres-Follow-up präsentiert worden. In der Studie ist Androgendeprivation (ADT) alleine mit ADT und Abirateron + Prednison verglichen worden. Verschiedene Patientenkollektive waren eingeschlossen, sowohl Patienten mit nicht metastasierten als auch mit metastasierten Karzinomen. BeiPatienten mit metastasierter Erkrankung zeigt sich weiterhin ein sehr klarer Vorteil im medianen Gesamtüberleben von mehr als 4Jahren Differenzfür ADT plus Abirateron gegenüber ADT alleine. Wenn die Patienten zusätzlich nach den LATITUDE-Low-Risk/High-Risk-Kriterien klassifiziert werden, lässt sich in der Low-Risk-Population der genau gleiche Überlebensvorteil wie in der High-Risk-Population erkennen (HR: 0,54 vs. 0,55; 95% CI: 0,43—0,69 vs. 0,41—0,76). Im Moment ist die Zulassung von Abirateron vor allem auf Patienten mit hohem Risiko analog denKriterien der LATITUDE-Studie fokussiert, aber die nun präsentierten Daten weisen darauf hin, dass Abirateron auch bei Low-Risk- und Low-Volume-Patienten evaluiert werden sollte.
Welche Neuigkeiten gab es zum Urothelkarzinom?
A. Omlin: Zum Urothelkarzinom gab es leider etwas enttäuschende Neuigkeiten zu zwei grossen Phase-III-Studien, die nicht das zeigen konnten, was wir uns erhofft hätten.
Zum einen wurden Daten der KEYNOTE-361-Studie präsentiert, welche die Immuntherapie in der Erstlinie bei Patienten mit fortgeschrittenem, nicht resezierbarem Urothelkarzinom untersuchte. Es handelt sich um eine dreiarmige Studie, die Patienten 1:1:1 zu Immun-Monotherapie mit Pembrolizumab, zu Immuntherapie + Chemotherapie mit Pembrolizumab + Gemcitabin, Cisplatin oder Carboplatin oder zu alleiniger Chemotherapie randomisierte. Es gab einen dualen primären Endpunkt zum progressionsfreien Überleben und zum Gesamtüberleben. Leider hat die Studie die primären Endpunkte nicht erreicht.
Ein minimaler Vorteil im progressionsfreien Überleben für die Kombination aus Pembrolizumab + Chemotherapie versus alleinige Chemotherapie konnte gezeigt werden, aber kein signifikanter Vorteil im Gesamtüberleben für die Kombination versus Chemotherapie. Das Ansprechen und auch die Zahl der kompletten Remissionen waren etwas höher im Arm Chemotherapie + Immuntherapie verglichen mit Immuntherapie alleine. Dies ist aber leider in diesem Setting nicht ausreichend. Es war bereits bekannt, dass eine alleinige Immuntherapie in der ersten Linie nur bei Patienten eingesetzt werden sollte, welche eine hohe PD-L1-Expression aufweisen. Diese Subgruppe wurde ebenfalls untersucht: Pembrolizumab versus Chemotherapie bei Patienten mit einem CPS ≥10. Jedoch zeigt sich auch hier leider kein signifikanter Vorteil für die Immuntherapie.
Bei der zweiten Studie, DANUBE, handelt es sich ebenfalls um eine dreiarmige Studie zur Erstlinien-Immuntherapie. Patienten mit fortgeschrittenem oder metastasiertem Urothelkarzinom erhielten 1:1:1 randomisiert entweder eine Immun-Monotherapie mit Durvalumab, eine Kombinationstherapie aus Durvalumab und Tremelimumab oder den Standard of Care, also Gemcitabin und Cisplatin oder Carboplatin. Als koprimäre Endpunkte waren das Gesamtüberleben unter Durvalumab versus Chemotherapie bei Patienten mit hoher PD-L1-Expression sowie das Gesamtüberleben unter Tremelimumab + Durvalumab versus Chemotherapie bei allen Patienten definiert. Beide koprimären Endpunkte wurden leider nicht erreicht. Bei Betrachtung der besonders interessanten Subgruppe von Patienten mit hoher PD-L1-Expression zeigt sichein positiver Trend im Überleben zugunsten der Kombination von Durvalumab + Tremelimumab im Vergleich zur Chemotherapie. Möglicherweise gibt es also einen Vorteil durch die Behandlung mit Immuntherapeutika. Leider handelt es sich hierbei nur um einen sekundären Endpunktund damit reicht das nicht für eine Änderung der Praxis.
In den klinischen Alltag wird es wahrscheinlich so Eingang finden: Cisplatin-fitte Patienten erhalten Cisplatin/Gemcitabin in der Erstlinie ohne Immuntherapeutika. Carboplatin-fitte Patienten werden mit Carboplatin und Gemcitabin behandelt. Bei einer Krankheitsstabilisierung oder einem Ansprechen auf die Chemotherapie wird dann auf Avelumab gewechselt (Switch-Maintenance) – analog der JAVELIN-Bladder-100-Studie, die inzwischen bereits im New England Journal of Medicine publiziert worden ist.
Am diesjährigen ESMO-Meeting wurden auchinteressante Analysen der JAVELIN-Bladder-100-Studiepräsentiert. Es wurden verschiedene Biomarker untersucht, wie die PD-L1-Expression, die Tumormutationslast oder auch Mutationssignaturen. Keiner dieser Biomarker hatte einen ausgesprochen prädiktiven Wert, aber es zeigt sich ähnlich wie beim Nierenzellkarzinom, dass mit dem Gewebe, welches im Zuge grosser Patientenstudien gesammelt wird, wertvolle weitere Untersuchungen gemacht werden können.
Ausserdem wurden die Ergebnisse einer Phase-II-Studie zu einem Antikörper-Wirkstoff-Konjugat Sacituzumab-Govitecan beim metastasierten Urothelkarzinom vorgestellt. Bei Sacituzumab handelt es sich um einen monoklonalen Antikörper, der gegen das Oberflächenantigen Trophoblasten-Zelloberflächen-Antigen-2 (Trop-2) gerichtet ist. Die Gesamtansprechrate bei vorbehandelten Patienten lag bei 27%. Diese Substanz ist sicher vielversprechend und wird in einer Phase-III-Studie weiter untersucht werden. Beim tripelnegativen Brustkrebs wurde dieser Wirkstoff von der FDA bereits dieses Jahr zugelassen.
Vielen Dank für das Gespräch!
Das Interview führte
Dr. Nicole Leitner
Unser Gesprächspartner:
PD Dr. med. Aurelius Omlin
Klinik für Medizinische Onkologie und Hämatologie
Kantonsspital St. Gallen
E-Mail: aurelius.omlin@kssg.ch
Das könnte Sie auch interessieren:
„Die Lebensqualität ist sehr variabel, auch innerhalb der Subtypen“
Im Rahmen eines JATROS-Interviews mit Ao. Univ.-Prof. Dr. Wolfgang Reinhard Sperr, MedUni Wien, wollten wir einen Einblick in den Umgang mit der seltenen Erkrankung „systemische ...
Anamnese oder präoperatives Gerinnungsscreening?
Blutgerinnungsstörungen können zu intra- wie auch postoperativen Blutungen führen, die abhängig von Lokalisation und Schweregrad ernste Folgen nach sich ziehen können. Ziel einer ...
CAR-T-Zellen: Stellenwert – klinische Evidenz – Herausforderungen
„Chimeric antigen receptor“(CAR)-T-Zellen sind eine der bedeutendsten Innovationen der modernen Hämatologie. Es handelt sich dabei um autologe, genetisch modifizierte T-Zellen, die ex ...