Update Pap- und HPV-Abstrich
Autor:
Dr. med. Gian Piero Ghisu
Praxis für Gynäkologie
Privatklinik Bethanien
Zürich
E-Mail: praxis-ghisu@hin.ch
Das Zervixkarzinom ist weltweit die vierthäufigste Krebserkrankung der Frau, wobei 85% der Fälle in Entwicklungsländern diagnostiziert werden. Dies liegt vor allem an unzureichendem Zugang zu Screeningprogrammen, HPV-Impfungen und Behandlungen von Krebsvorstufen sowie an Risikofaktoren wie HIV-Infektionen, die das Erkrankungsrisiko deutlich erhöhen. Um die Inzidenz global zu senken, hat die WHO eine Strategie entwickelt, die bis 2030 darauf abzielt, a) 90% der Mädchen bis 15 Jahre zu impfen, b) 70% der Frauen bis 35 und erneut bis 45 Jahre einem Screening zu unterziehen und c) 90% der Betroffenen zu behandeln.
Das Zervixkarzinom kann durch regelmässige Vorsorgeuntersuchungen weitgehend verhindert werden. In der Schweiz, die eine der niedrigsten Inzidenzraten weltweit aufweist (ca. 240 neu diagnostizierte Fälle pro Jahr), zählt die unzureichende Screeningteilnahme zu den Hauptrisikofaktoren: Rund ein Drittel der Betroffenen hat nie an einem Screening teilgenommen, und etwa 15% der Frauen im Alter von 25–65 Jahren halten die empfohlenen Intervalle nicht konsequent ein.1
Seit der Einführung des opportunistischen Screenings in den 1960er-Jahren ist die Inzidenz des Zervixkarzinoms in der Schweiz um über 60% zurückgegangen. Es wird ein Screening alle drei Jahre zwischen 21 und 70 Jahren empfohlen, wobei von 21–29 Jahren zytologisch gescreent wird und ab 30 Jahren auch HPV-basierte Verfahren möglich sind. Da für Letztere die Kostenübernahme nicht gesetzlich geregelt ist, wird in der Praxis fast ausschliesslich zytologisch gescreent.2
Optimierungspotenziale im Screening
Neue Strategien zur Senkung der weltweiten Inzidenz von Zervixkarzinomen sind dringend erforderlich. Bereits die Einführung von Screenings in Ländern ohne Programme könnte viele Fälle verhindern. Auch in industrialisierten Ländern gibt es Optimierungsansätze, etwa Strategien zur Erreichung der Frauen, die nicht oder unregelmässig zum Screening gehen, bzw. die Fortführung des Screenings über das 70. Lebensjahr hinaus. Zytologische und HPV-basierte Screeningmethoden gelten als Goldstandard, stehen jedoch vor spezifischen Herausforderungen: Ein effektives Screening sollte Erkrankungen zuverlässig erkennen, gleichzeitig aber unnötige Untersuchungen und Kosten vermeiden. Der bewährte Pap-Test hat eine geringe Sensitivität und erkennt daher nicht alle Fälle. Zudem zeigt er vor allem bei leichten Veränderungen eine hohe Interobserver-Variabilität. Zudem setzt die Beurteilung der Zytologien eine grosse Expertise der Fachpersonen voraus. Der HPV-Test ist zwar deutlich sensitiver, aber weniger spezifisch, wodurch unnötige Tests und Behandlungen ausgelöst werden können.
Internationale Entwicklungen im Screening
Nachbarländer haben vielfach eigene, organisierte Screeningsysteme entwickelt, wobei zunehmend HPV-basierte Verfahren oder Co-Tests (Zytologie plus HPV-Test) zum Einsatz kommen. Diese Methoden verbessern die diagnostische Genauigkeit und erlauben längere Screeningintervalle. Insbesondere in Skandinavien sind Co-Tests mit erweiterten Genotypisierungen populär. In Deutschland dominiert ein zytologiebasiertes Screening: Die Risikostratifizierung erfolgt durch einen zusätzlichen HPV-Test. Die Algorithmen sehen bei Auffälligkeiten in der Regel mehrere Screeningrunden vor.
Erweiterte Diagnostik und neue Technologien
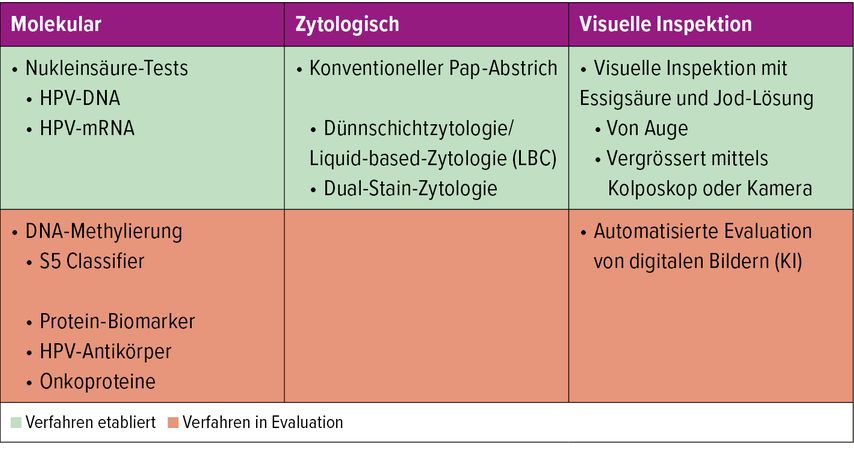
Zur Identifikation von Frauen mit Zervixdysplasie oder einem erhöhten Risiko für Gebärmutterhalskrebs stehen verschiedene Testverfahren zur Verfügung. Dabei lassen sich grundsätzlich drei Ansätze zur Früherkennung sowie zukünftige Testmethoden unterscheiden. Diese sind in Tabelle 1 zusammengefasst.3
Visuelle Beurteilung
In ressourcenarmen Regionen wird oft die Inspektion mit Essiglösung und Jod, mit oder ohne Kolposkop, angewandt. Diese Methode gilt für das Screening als ungenügend. Künstliche Intelligenz könnte künftig durch automatisierte Bildauswertung die Diagnostik vereinfachen.
Zytologie-basiertes Screening
Der sog. Pap-Test hat die Zervixkarzinominzidenz erheblich gesenkt. Heute wird häufig die Dünnschichtzytologie (LBC) eingesetzt, da sie weniger inadäquate Ergebnisse liefert und automatisierbar ist. Die Sensitivität der LBC liegt bei etwa 55%, verglichen mit 51% beim traditionellen Pap-Test; die Spezifität liegt bei 78% vs. 67%.4
Dual-Stain-Test
Der p16/Ki-67-Dual-Stain-Test kann als Zusatzanalyse aus einer LBC zur Triage HPV-positiver Frauen erfolgen. Die Co-Expression von p16 und des Proliferationsmarkers Ki-67 geht mit einem erhöhten Risiko für eine CIN2+ einher. Die diagnostische Genauigkeit variiert dabei nach zytologischem Befund. Bei ASCUS («atypical squamous cells of undetermined significance») liegt die Sensitivität zwischen 64 und 92,2%, die Spezifität zwischen 53 und 80,6%, bei LSIL («low-grade squamous intraepithelial lesion») zwischen 81,6 und 100% resp. 43 und 75%.5 Der Test reduziert unnötige Kolposkopien und ermöglicht längere Kontrollintervalle bei höherer Sensitivität und Spezifität im Vergleich zu herkömmlichen Pap-Tests.
HPV-basiertes Screening und Genotypisierung
Von rund 200 HPV-Typen können etwa 40 die Zervix infizieren, wobei die meisten Zervixkarzinome durch die Typen 16, 18 und 45 verursacht werden. Eine US-Studie mit über 42000 Frauen ab 25 Jahren ergab, dass ein Screening mittels HPV-16/18-Genotypisierung eine bessere Risikoeinschätzung ermöglicht als die Zytologie. Die Sensitivität für CIN 3+ lag bei 47,8% für die Zytologie und 76,1% für das HPV-Screening (+28%), während die Spezifität bei 97,1% bzw. 93,5% lag.6 Eine NL-Studie mit >45000 Frauen zwischen 29 und 56 Jahren zeigte, dass durch das HPV-Screening eine CIN2+ früher erkannt und die Inzidenz von CIN3 und Zervixkarzinomen in Folgerunden um 60% gesenkt werden können.7
DNA-Methylierung
Die Dysregulation der Genexpression durch eine abweichende DNA-Methylierung spielt eine zentrale Rolle in der Krebsentstehung. Die DNA-Methylierung wird als Triagewerkzeug für HPV-positive Frauen genutzt, um Hochrisikoläsionen besser zu identifizieren. Eine Metaanalyse von 23 Studien8 zeigte das Potenzial der Methylierungsanalyse, Risikoläsionen besser zu identifizieren und unnötige Kolposkopien zu vermeiden. Die Methode ist noch nicht validiert.
S5 Classifier
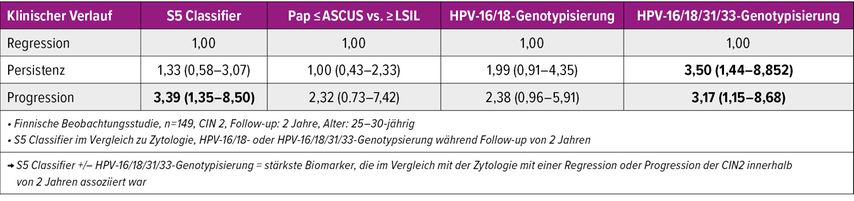
Der S5 Classifier ist ein Verfahren zur Analyse der DNA-Methylierung. Der Nachweis epigenetischer DNA-Modifikationen in einem Tumorsuppressorgen sowie in den HPV-Regionen 16, 18, 31 und 33 ermöglicht eine genauere Differenzierung zwischen Dysplasien mit Potenzial zur Progression zum Zervixkarzinom und solchen mit einem persistierenden oder regressiven Verlauf. In einer Studie mit 257 HPV-positiven Frauen wurde eine Sensitivität von 93,2% für CIN3+ mit dem S5 Classifier erreicht, im Vergleich zu 86% beim Co-Test bzw. 61% bei der Zytologie alleine (Tab. 2).9 In einer finnischen Studie zeigte der S5 Classifier die stärkste Assoziation mit einer Progression von CIN2 (OR: 3,39), gefolgt von der HPV-16/18/31/33-Genotypisierung (OR: 3,17).10,11
Self-Sampling
Eine Metaanalyse von 33 Studien ergab eine hohe Akzeptanz für das Self-Sampling bei mit konventionell entnommenen Abstrichen vergleichbarer Sensitivität und gering abweichender Spezifität. Ein Self-Sampling könnte somit die Teilnahme am Screening erhöhen12,13 und in der Schweiz zumindest einen Teil der gut 20% Frauen ansprechen, die unregelmässig oder nicht am Screening teilnehmen.
Screening über 70 Jahre hinaus
Eine dänische Studie zeigte ein erhöhtes Zervixkarzinomrisiko bei Frauen über 70 Jahre.14 Ursächlich dafür könnten Kohorteneffekte, geringere Hysterektomieraten und unzureichende HPV-Impfungen sein. In der Schweiz besteht ein ähnlicher Trend.15 Individuelle Risikofaktoren und Anamnese sollten bestimmen, ob das Screening über 70 Jahre hinaus weitergeführt wird. Angesichts eines Anteils von bis zu 70% inadäquater Kolposkopien in dieser Altersgruppe könnten HPV-Tests für diese Population besonders effektiv sein. Ob das Screening nach einem negativen HPV-Test gestoppt werden darf, bleibt unklar, zumal bei Status nach CIN3 oder AIS ein erhöhtes Zervixkarzinomrisiko persistiert.16, 17
Fazit
Das Zervixkarzinom ist eine vermeidbare Krebserkrankung, deren Inzidenz durch Screeningprogramme und HPV-Impfungen deutlich reduziert werden kann. Weltweit bestehen jedoch erhebliche Unterschiede im Zugang zu Vorsorge und Behandlung, insbesondere in Entwicklungsländern. Fortschritte in der Diagnostik, wie HPV-basierte Tests, Genotypisierungen und innovative Ansätze wie DNA-Methylierung oder Self-Sampling, bieten Potenzial, die Teilnahmean Screenings sowie deren Effektivität zu erhöhen. Eine globale Strategie und lokale Anpassungen sind entscheidend, um die Krankheitslast zu senken.
Literatur:
1 ICO/IARC Information Centre on HPV and Cancer - Switzerland: HPV & Related Cancers, Fact Sheet 2023 (2023-03-10) 2 SGGG: Expertenbrief Nr. 50, Empfehlungen für die Gebärmutterhalskrebsvorsorge, 03/2018 3 WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, 2nd edition. 2024 4 Kisser A, Zechmeister-Koss I: LBI-HTA Projektbericht Nr. 72, 2013 5 WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention: Use of dual-stain cytology to triage women after a positive test for human papillomavirus (HPV) [Internet]. 2nd edition. Geneva: 2024 6 Wright TC et al.: Primary cervical cancer screening with human papillomavirus: end of study results from the ATHENA study using HPV as the first-line screening test. Gynecol Oncol 2015; 136(2): 189-97 7 Rijkaart DC et al.: Human papillomavirus testing for the detection of high-grade cervical intraepithelial neoplasia and cancer: final results of the POBASCAM randomised controlled trial. Lancet Oncol; 13(1): 78-88 8 Salta S et al.: DNA methylation as a triage marker for colposcopy referral in HPV-based cervical cancer screening: a systematic review and meta-analysis. Clin Epigenetics 2023; 15(1): 125 9 Cook DA et al.: Evaluation of a validated methylation triage signature for human papillomavirus positive women in the HPV FOCAL cervical cancer screening trial. Int J Cancer 2018; 144(10): 2587 10 Louvanto K et al.: Methylation in predicting progression of untreated high-grade cervical intraepithelial neoplasia. Clin Infect Dis 2019; 70(12): 2582 11 Burdier FR et al.: DNA methylation as a triage tool for cervical cancer screening - a meeting report. Prev Med Rep 2024; 6: 41 12 Colonetti T et al.: Self-sampling for HPV testing in cervical cancer screening: A scoping review. Eur J Obstet Gynecol Reprod Biol 2024; 296: 20 13 Bhatla N et al.: Can human papillomavirus DNA testing of self-collected vaginal samples compare with physician-collected cervical samples and cytology for cervical cancer screening in developing countries? Cancer Epidemiol 2009; 33(6): 446 14 Andersen B et al.: HPV-prevalence in elderly women in Denmark. Gynecol Oncol 2019; 154(1): 118 15 Die Statistiken zur nationalen Krebsinzidenz – Gesamtschweiz und Sprachregionen; letzte Aktualisierung: 12.03.2020 16 Kalliala I et al.: Incidence and mortality from cervical cancer and other malignancies after treatment of cervical intraepithelial neoplasia: a systemic review and meta-analysis of the literature. Ann Oncol 2020; 31(2): 213 17 Costales AB et al.: Risk of residual disease and invasive carcinoma in women treated for adenocarcinoma in situ of the cervix. Gynecol Oncol 2013; 129(3): 10
Das könnte Sie auch interessieren:
Von Impfung bis Kontrazeption: aktuelle Empfehlungen für den Praxisalltag
Wie ist die beste Vorgehensweise in der Beratung impfskeptischer Schwangerer, worauf ist bei der Behandlung vaginaler Dysbiosen zu achten und welche Faktoren beeinflussen die Wahl der ...
Von der Rolle des Mikrobioms bis zur Umsetzung der Vakzinierungsprogramme
Im Rahmen des diesjährigen EUROGIN-Kongresses wurde ein Fazit über 20 Jahre HPV-Impfung gezogen und ausführlich über die Implementierung von Screeningmaßnahmen und ...
Ein geschützter Raum für Freude, Frust und Trauer
Viele Menschen mit Kinderwunsch fühlen sich mit ihren Emotionen oft allein gelassen. Um dieser Einsamkeit entgegenzuwirken, hat fertisuisse das kostenlose Online-Angebot «fertisuisse ...