Operative Therapie und Risikoreduktion bei BRCA-Mutations-Trägerinnen
Autorinnen:
Dr. Melitta B. Köpke
Dr. Johanna Veh
Prof. Dr. Nina Ditsch
Universitätsklinikum Augsburg
Korrespondenz:
E-Mail: melitta.koepke@uk-augsburg.de
Familiäre Krebserkrankungen, besonders durch pathogene Genveränderungen bedingt, sind vermehrt in den Fokus der Forschung gerückt. Dies zeigt sich vor allem bei Brustkrebs (BC). Das Wissen um eine pathogene Mutation zieht therapeutische wie auch präventive Konsequenzen nach sich. Der vorliegende Artikel möchte daher einen Überblick über mögliche operative Therapien sowie Risikoreduktion bei Trägerinnen der BRCA(„BReast CAncer gene“)-Mutation bieten.
Keypoints
-
Patientinnen mit BRCA-Mutation haben ein erhöhtes Lebenszeitrisiko für Brust- und Eierstockkrebs.
-
Neben der operativen Therapie bei bereits eingetretener Brustkrebserkrankung besteht die Option risikoreduzierender operativer Maßnahmen (Mastektomieder Gegenseite oder bilaterale Oophorektomie).
-
Es bestehen vielfältige Möglichkeiten der allogenen sowie autologen Brustrekonstruktion.
Pathogene Varianten
Unter einer pathogenen Variante (PV) versteht man eine Mutation, die krankheitsverursachend wirkt. Es kann sich dabei entweder um Keimbahnmutationen handeln, die an folgende Generationen vererbt werden, oder um somatische Mutationen, die nur das Individuum betreffen. Nach derzeitigem Kenntnisstand sind etwa 10% aller BC und 20% aller Ovarialkarzinome (OC) auf PV in bestimmten Genen zurückzuführen.
BRCA1 und -2 gehören hierbei zu den häufigen PV mit einem hohen Erkrankungsrisiko und werden autosomal-dominant vererbt.1 Daneben ist auch die Modulation des Krebsrisikos durch nichtgenetische Faktoren, zum Beispiel Alter oder Parität, relevant.
Lebenszeitrisiko für Karzinome durch BRCA-PV
Während das mittlere Erkrankungsalter bei sporadischen BC-Fällen bei 65 Jahren liegt,2 liegt es für einen BRCA-bedingten BC bei etwa 44 Jahren. Bei einer PV in BRCA1 liegt das BC-Lebenszeitrisiko bei 61,8%, bei BRCA2 bei 43,2%.3 Darüber hinaus wird durch eine BRCA-Mutation auch das Lebenszeitrisiko für OC erhöht und liegt mit 44% bei BRCA1 und 18% bei BRCA2 deutlich über dem Lebenszeitrisiko der Allgemeinbevölkerung von 1,2%.4
Auch bei Männern steigt das Lebenszeitrisiko für ein BC bei BRCA-Mutation auf bis zu 9% im Vergleich zu 0,11% ohne PV,5 jedoch ist hier die Datenlage deutlich eingeschränkter.
Chirurgische Optionen bei erkrankten BRCA-Mutations-Trägerinnen
Die Empfehlungen zur chirurgischen Therapie bereits an BC erkrankter BRCA-Mutations-Trägerinnen richten sich nach den individuellen Voraussetzungen. In die Beratung ist neben der onkologischen Sicherheit hinsichtlich der aktuellen Erkrankung auch das Risiko für eine Erkrankung der Gegenseite sowie für ein OC miteinzubeziehen. Die erkrankte Seite kann hierbei nach aktuellem Wissensstand brusterhaltend operiert werden, da im Vergleich zu einer Mastektomie (ME) kein Unterschied in Bezug auf das Gesamtüberleben gezeigt wurde.6 In das operative Konzept sollte bei BRCA1- oder BRCA2-PV immer die Planung für die kontralaterale Seite integriert werden. Denn: Vor allem jung an BC erkrankte Frauen mit guter Prognose profitieren hinsichtlich des Überlebens von einer kontralateralen ME.7–9
Möglichkeiten der Brustrekonstruktion
Der Wunsch nach einer Brustrekonstruktion ist auch bei BRCA-PV bei gleicher onkologischer Sicherheit umsetzbar.10 Es bestehen je nach Art der Brustdrüsenentfernung verschiedene Optionen. Hierbei wird grundsätzlich zwischen allogener Rekonstruktion mit Fremdmaterial und autologer Rekonstruktion mit Eigengewebe unterschieden. Eine gute Aufklärung zu möglichen Komplikationen, Spätfolgen und Folgeeingriffen ist obligat.
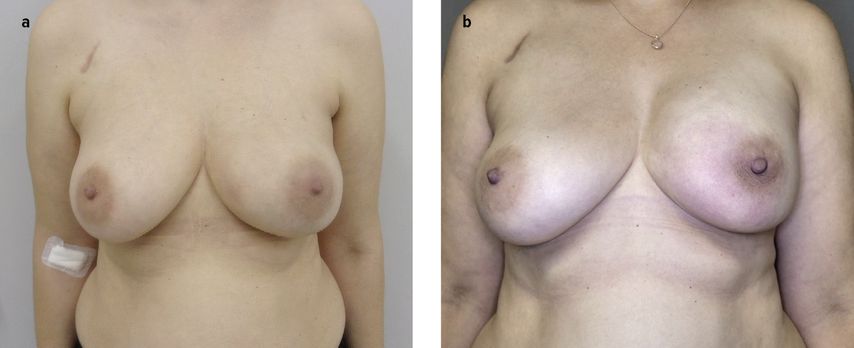
Entscheidet sich eine Frau für eine ME mit Implantatrekonstruktion, kann im Regelfall hautsparend bzw. brustwarzenerhaltend operiert werden. Das Implantat wird hierbei meist nach Entfernung des Brustdrüsengewebes über einen Schnitt in der Submammärfalte eingebracht, Netze oder azelluläre Matrizes können hier stabilisierend unterstützen (Abb. 1a/b). Auch hautsparende Verfahren ohne Brustwarzenerhalt sind möglich: Die Schnittführung kann zum Beispiel als umgekehrter T-Schnitt gewählt werden.
Abb. 1: Implantatbasierte Brustrekonstruktion links: a) präoperativ, b) drei Monate postoperativ (Bilddarstellung mit freundlicher Genehmigung der Patientin)
Ist der Hautmantel aufgrund des ungünstigen Tumorsitzes nicht zu erhalten, besteht bei Ablatio simplex die Option einer gleichzeitigen Expandereinlage. Der Expander wird in einem zweiten Eingriff durch ein Implantat ersetzt. Zunächst wird er postoperativ schrittweise mit NaCl aufgefüllt, um eine langsame und schonende Dehnung des Hautmantels zu ermöglichen. Nach Wunsch ist eine Brustwarzenrekonstruktion mit unterschiedlichen Methoden, etwa mittels Star-Flap oder Tätowierung, möglich.
Entscheidet sich eine Patientin für eine Eigengewebsrekonstruktion, können verschiedene Optionen angeboten werden. Die Auswahl hängt ab von der Gewebeverfügbarkeit, vorangegangenen Operationen oder Bestrahlungen sowie dem individuellen Risikoprofil der Patientin (z.B. Adipositas, Nikotinabusus). Es wird grundsätzlich zwischen gestielten Lappen, die ihre Blutversorgung über die Spenderregion erhalten, und freien Lappen mit der Blutversorgung nach Setzen einer Gefäßanastomose unterschieden. Als Goldstandard der autologen Mammarekonstruktion hat sich der DIEP-Lappen („deep inferior epigastric artery perforator“), ein freier Perforatorlappen vom Unterbauch, durchgesetzt.11 Der Lappen wird als Neo-Brust formiert, für die Patientin ergibt sich der positive Nebeneffekt einer „Bauchdeckenstraffung“.
Alternativen zum DIEP bieten Muskellappen vom Rumpf (z.B. transverser Rectus-abdominis-Muskel, TRAM) oder Oberschenkel (z.B. Gracilislappen). Auch freie Perforatorlappen aus der Gesäßregion haben ihren Stellenwert bei passenden Patientinnen. Je nach individueller Konstitution kommen inzwischen auch Rekonstruktionen mit Lipofilling in Betracht.12
Komplikationsspektrum bei Mammarekonstruktion
Frühe postoperative Komplikationen bei Brustimplantaten umfassen Serombildung, Hämatome und Infektionen.13 Antibiotische Therapien und Wundrevisionen bis hin zur Implantatexplantation können in der Folge notwendig sein. Besonders nach vorangegangener Strahlentherapie ist die Komplikationsrate erhöht. Langfristig kann es zu einer Kapselfibrose kommen, die Schmerzen, Verformungen oder Implantatrupturen verursachen kann,14 was häufig Revisionsoperationen nötig macht. Eine seltene Spätkomplikation ist das Auftreten eines Brustimplantat-assoziierten anaplastischen großzelligen Lymphoms (BIA-ALCL), das typischerweise durch das Entstehen eines Seroms mehrere Jahre nach Implantation auffällt.15
Ein spezifisches Komplikationsrisiko bei autologer Brustrekonstruktion ist die Lappennekrose durch unzureichende Durchblutung des transplantierten Gewebes.16 Spätkomplikationen umfassen Narbenbildung, Lipoatrophie und Volumenverlust des transplantierten Gewebes. Zudem können Hernien oder Muskelfunktionsverluste an der Spenderstelle auftreten.17
Daher ist für alle Methoden der Brustrekonstruktion die Wahl der für die individuelle Patientin passenden Methode nach entsprechender Risikoaufklärung von höchster Bedeutung.
Optionen der operativen Risikoreduktion
Ideal wäre, alle BRCA-Mutationsträgerinnen vor Auftreten einer Erkrankung zu identifizieren, um direkt primär prophylaktisch handeln zu können. Bei gesunden Mutationsträgerinnen besteht neben der Option der intensivierten Früherkennung18 die Option einer bilateralen risikoreduzierenden ME (BRRM). Durch diese Maßnahme kann eine Reduktion des Risikos für eine BC-Erkrankung um mehr als 95% erreicht werden.19 Bezüglich der Möglichkeiten der Brustrekonstruktion bestehen keine Unterschiede im Vergleich zu bereits erkrankten Mutationsträgerinnen.
Darüber hinaus sollten Betroffene hinsichtlich einer möglichen risikoreduzierenden bilateralen Oophorektomie (RR-BSO) beraten werden, da diese einen eindeutigen Überlebensvorteil und eine Reduktion des Risikos für ein OC um bis zu 96% bietet.20 Auch bei jung an BC erkrankten BRCA-Mutations-Trägerinnen zeigte sich ein signifikant positiver Einfluss auf das Gesamtüberleben.9 Hierbei ist zu bedenken, dass gerade bei jungen Frauen in der Prämenopause diese Maßnahme direkt Einfluss auf die Familienplanung und Lebensqualität hat.21 Nach aktuellen Empfehlungen sollte bei gesunden BRCA1-Trägerinnen die RR-BSO mit 35 Jahren, bei BRCA2-Trägerinnen mit 40–45 Jahren erfolgen.22
Literatur:
1 Schütz F, Thomssen C: www.ago-online.de/fileadmin/ago-online/downloads/_leitlinien/kommission_mamma/ 2023/Einzeldateien/AGO_2023D_02_Brustkrebsrisiko_Genetik_und_Praeven tion.pdf (01.05.2023) 2 Krebs in Deutschland für 2019/2020. 14. Ausgabe (2023); doi: 10.25646/11357 3 Engel C et al.: Int J Cancer 2020; 146: 999-1009 4 Kast K et al.: J Med Genet 2016; 53(7): 465-71 5 Liede A et al.: J Clin Oncol 2004; 22(4): 735-42 6 Wang C et al.: Breast Cancer 2022; 29(2): 314-23 7 Evans DGS et al.: Breast Cancer Res Treat 2013; 140(1): 135-42 8 Heemskerk-Gerritsen BAMA et al.: Int J Cancer 2015; 136(3): 668-77 9 Lambertini M et al.: SABCS 2024, Abstr. #SESS-1627 10 Patani N et al.: Surg Oncol 2008; 17: 97-105 11 Fritschen UVB et al.: Handchir Mikrochir Plast Chir 2020; 52: 58-66 12 Kümmel AS et al.: Breast Care (Basel) 2019; 14(3): 165-9 13 Meshkin DHJM et al.: Ann Transl Med 2023; 11(12): 416 14 Luvsannyam ED et al.: Cureus 2020; 12(9): e10341 15 Marra A et al.: Cancer Treat Rev 2020; 84: 101963 16 Bhullar H et al.: Aesthetic Plast Surg 2020; 44(5): 1454-61 17 Fisher MH et al.: J Plast Reconstr Aesthet Surg 2024; 90: 88-94 18 Schmutzler RK, Deutsches Konsortium Familiärer Brust- und Eierstockkrebs (2020): www.konsortium-familiaerer-brustkrebs.de/konsensusempfehlung 19 De Felice F, Marchetti C: Oncotarget 2015; 6(37): 39391-2 20 Xiao YL et al.: Clin Breast Cancer 2019; 19(1): e48-e65 21 Paluch-Shimon S et al.: Ann Oncol 2022; 33(11): 1097-118 22 S3-Leitlinie Diagnostik, Therapie und Nachsorge maligner Ovarialtumoren (2024): www.leitlinienprogramm-onkologie.de/leitlinien/ovarialkarzinom (Zugriff 13.02.2025)
Das könnte Sie auch interessieren:
Welche Risiken sind zu erwarten?
Die präventive Mastektomie wird vor allem bei genetischer Vorbelastung, z.B. bei BRCA1/2-Mutationen, erwogen. Der Eingriff kann das Brustkrebs-Erkrankungsrisiko deutlich reduzieren, aber ...
Die Rolle von HPV in der Genese kutaner Plattenepithelkarzinome
Einige humane Papillomaviren (HPV), sogennante High-Risk-HPV der Genus-Alpha-HPV, sind ursächlich an der Entstehung des Zervixkarzinoms und anderer anogenitaler und oraler Karzinome ...
AI in der Reproduktionsmedizin
Kein Thema bewegt derzeit die Menschen mehr als künstliche Intelligenz (AI – „artificial intelligence“). Wiewohl in der Behandlung des unerfüllten Kinderwunsches in den letzten ...