TNM-Staging nach NACT und Anforderungen im Rahmen klinischer Studien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Pathologie beeinflusst massgeblich das Management von Patient:innen mit Mammakarzinom nach NACT. Zudem sind die Kenntnis der initialen Tumorbiologie und die Korrelation mit dem klinisch und radiologisch definierten Tumoransprechen essenziell für die korrekte histologische Interpretation der Gewebeproben und die Festlegung der TNM-Kategorie. Dieses Ziel lässt sich nur mit enger multidisziplinärer Zusammenarbeit erreichen, idealerweise im Rahmen eines interdisziplinären Tumorboards. Ein gutes Verständnis der pathologischen Beurteilung und Vorgehensweise erleichtert die interdisziplinäre Kommunikation und ermöglicht dadurch optimale und individuell angepasste Therapiekonzepte.
Keypoints
-
Die pathologische Aufarbeitung und Berichterstattung von Mammapräparaten nach NACT sollte standardisiert und in Anlehnung an international gültige Empfehlungen erfolgen, die von der ICCR regelmässig aktualisiert werden.
-
Die pathologische Interpretation erfolgt in Zusammenschau mit essenziellen klinischen Informationen. Diese beinhalten unter anderem die ursprüngliche Tumorlokalisation und Grösse sowie das radiologische Tumoransprechen nach NACT.
-
Zu den Kernelementen im histologischen Bericht gehören der Durchmesser des grössten zusammenhängenden Tumorherdes (TNM-Grösse) sowie der RCB-Score (Gesamtausdehnung und Tumorzellularität).
-
Eine standardisierte histologische Aufarbeitung ist insbesondere im Rahmen multizentrischer Studien (VISION, TAXIS) entscheidend, damit die Daten reproduzierbar sind und sinnvoll ausgewertet werden können.
Systemische neoadjuvante Therapie (NACT) hat in den letzten Jahren zunehmend an Bedeutung gewonnen und wird heutzutage bei HER2-positivem und bei tripelnegativem Mammakarzinom standardmässig durchgeführt. Das komplette pathologische Ansprechen (pCR), im Sinne einer kompletten histologischen Remission des invasiven Karzinoms in der Mamma und in den Lymphknoten, gilt als wichtiger prognostischer Faktor bei allen Subtypen des Mammakarzinoms.1
Andererseits braucht es bei Patient:innen mit residuellem Karzinom ein massgeschneidertes adjuvantes Behandlungskonzept in Abhängigkeit vom jeweiligen histologischen Tumoransprechen auf die stattgefundene NACT. Die pathologische Beurteilung des Ansprechens auf NACT sollte deshalb präzise und standardisiert erfolgen, damit die Daten reproduzierbar sind und auch innerhalb von Studien angewandt und ausgewertet werden können.
Empfehlungen zur Aufarbeitung und Berichterstattung von Mammakarzinomen nach NACT werden unter Berücksichtigung neuester wissenschaftlicher Erkenntnisse regelmässig von der ICCR (International Collaboration on Cancer Reporting) herausgegeben und aktualisiert. Letztmalig wurde die Empfehlung zur Aufarbeitung von Mammapräparaten nach NACT Ende 2023 aktualisiert.2 Darin wird zwischen Kernelementen, die im Bericht zwingend erwähnt werden sollten, und fakultativ erwähnenswerten Angaben unterschieden. Die Empfehlungen der ICCR gelten als international gültige Richtlinien, sie sollten in jedem Pathologieinstitut bekannt sein und angewandt werden.
Im Folgenden werden die makroskopische und mikroskopische Aufarbeitung von Operationspräparaten nach NACT dargestellt.
Histologische Beurteilung des Tumoransprechens auf NACT
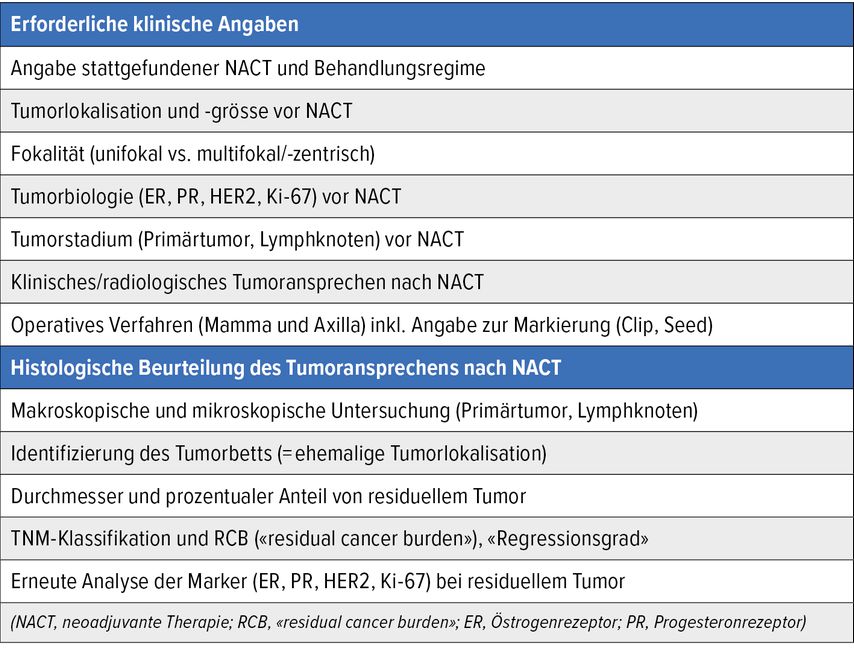
Die histologische Interpretation der Befunde erfolgt immer im Kontext der klinischen Information und erfordert eine enge multidisziplinäre Zusammenarbeit. Insbesondere die Korrelation mit radiologischen Befunden vor und nach der NACT ist massgebend für eine korrekte Interpretation der histologischen Befunde. Idealerweise kann der Informationsaustausch im Rahmen einer präoperativen Vorstellung am interdisziplinären Tumorboard stattfinden. Essenzielle klinische Angaben sollen jedoch auch auf dem Einsendeformular vermerkt werden (Abb.1).
Abb. 1: Essenzielle und erforderliche klinische Informationen auf dem Einsendeformular bzw. erforderliche Angaben nach histologischer Aufarbeitung
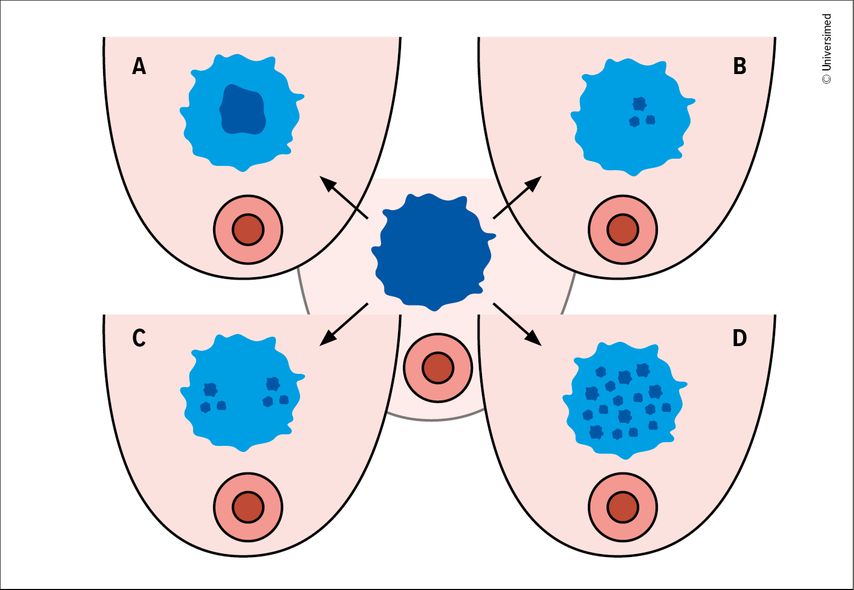
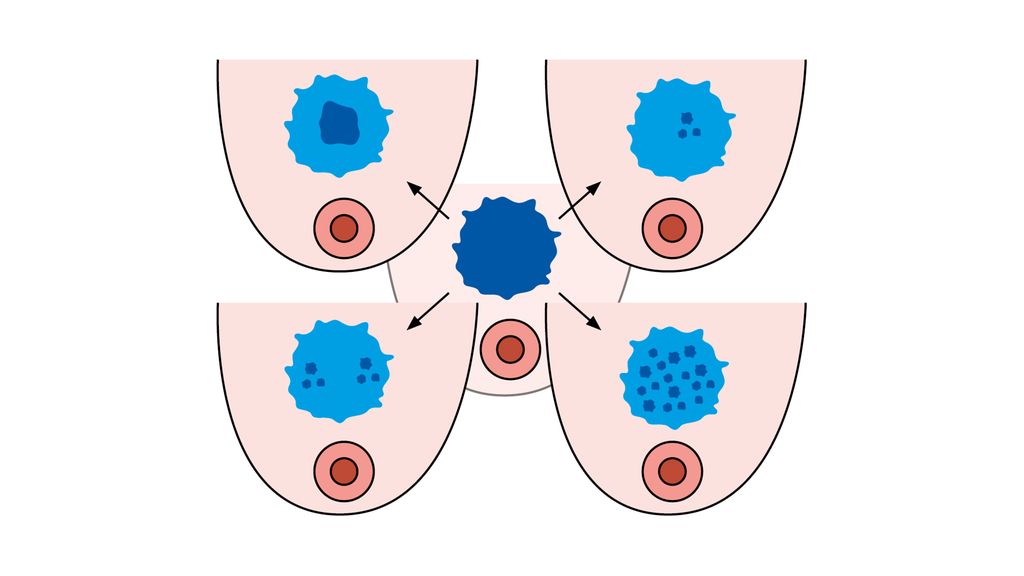
Die pathologische Befundung ist häufig komplex und aufwendig, da verschiedene Faktoren einen Einfluss auf das Tumorverhalten nach NACT haben. Residuelles Tumorgewebe kann sich in verschiedenen morphologischen Mustern präsentieren, die sich im Ausmass der Fibrose und der vitalen Tumorareale unterscheiden. Dabei kann sowohl die relative Menge an vitalem Tumor als auch dessen topografische Verteilung innerhalb des Tumorbetts stark variieren (Abb.2).
Abb. 2: Verschiedene Ansprechmuster bei residuellem Tumor nach neoadjuvanter Therapie (modifiziert nach Pastorello RG et al.)3
Das resultierende, morphologisch erkennbare Muster des Ansprechens wird durch tumorintrinsische Faktoren wie die Tumorbiologie und Multifokalität, aber auch extrinsische Faktoren wie das Behandlungsregime beeinflusst.
Makroskopische Beurteilung
Bei der initialen makroskopischen Beurteilung ist die korrekte Identifizierung des Tumorbetts (ehemalige Tumorlokalisation) entscheidend für die weitere histologische Aufarbeitung des Präparats. Dabei ist eine gezielte Untersuchung insbesondere bei grösseren Tumorektomie- oder Mastektomiepräparaten sinnvoller als eine komplette oder ausgedehnte «blinde» Einbettung von Gewebe, was lediglich in unnötig hohem Aufwand und Kosten resultiert.
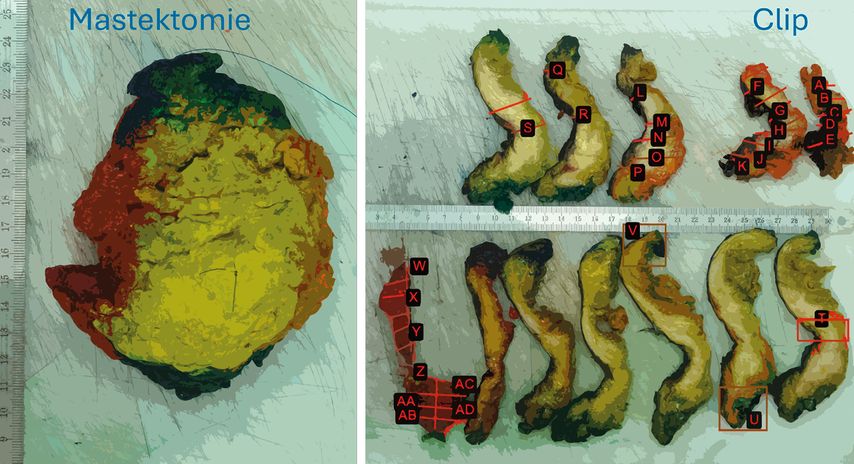
Das Tumorbett sollte jedoch in jedem Fall vollständig histologisch untersucht werden. Dies setzt die Kenntnis der genauen ursprünglichen Tumorlokalisation voraus, da bei komplettem Ansprechen eine Unterscheidung zwischen fibrosiertem Tumorbett und unspezifischer nichttumorassoziierter Fibrose makroskopisch schwierig sein kann. Deshalb ist es entscheidend, die genaue ehemalige Tumorlokalisation und allfällige weitere Tumorherde auf den Einsendeformularen zu vermerken. Das Vorhandensein (inkl. Anzahl) oder Fehlen einer Clip- oder Seedmarkierung vor Therapiebeginn sollte explizit angegeben werden. Eine Fotodokumetation/Skizze mit Markierung entnommener Areale ist sehr empfehlenswert und erleichtert die mikroskopische Beurteilung und Rekonstruktion der Grösse des Tumorbetts oder des residuellen Tumors (Abb.3).
Abb. 3: Makroskopische Aufarbeitung eines Mastektomiepräparates mit Sampling und kompletter Einbettung der Clip-markierten ehemaligen Tumorlokalisation
Mikroskopische Beurteilung
In den meisten Fällen nach NACT können Restanteile von vitalem Tumor erst histologisch nachgewiesen werden. Das mikroskopische Tumorbett lässt sich anhand typischer histologischer Veränderungen wie Fibrose, Entzündungsinfiltrat aus Lymphozyten und Plasmazellen sowie Makrophagen und Blutungsresiduen, teils auch Mikrokalk, identifizieren. Bei komplettem Ansprechen kann das Tumorbett manchmal lediglich als zellarme Fibrose imponieren und ist dann auch histologisch schwierig als solches zu erkennen. Die Korrelation mit der makroskopisch fotografierten Clip-/Seed-markierten ehemaligen Tumorlokalisation erlaubt jedoch die korrekte Interpretation.
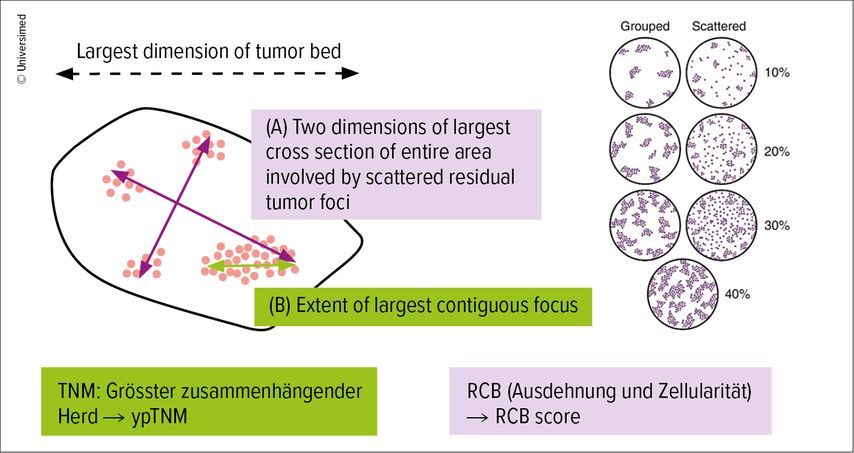
Massgebend für das weitere Management der Patient:innen ist nicht nur der Nachweis von vitalem Tumor, sondern auch die Bestimmung der Tumordimensionen, die nach der TNM-Klassifikation und RCB («residual cancer burden») angegeben werden (Abb.4).
Für das TNM-Staging wird der Durchmesser des grössten zusammenhängenden Tumorherdes ohne dazwischen liegende Fibrose gemessen. Dies kann sich bei heterogenem Tumoransprechen schwierig gestalten und sollte unter Kenntnis und Berücksichtigung des initialen Tumorwachstums erfolgen (z.B. diskontinuierlich wachsendes invasives lobuläres Karzinom).
Bei der Quantifizierung des residuellen Tumors nach RCB hingegen wird das gesamte Tumorareal (residuelles invasives Karzinom) unter Einbezug von Fibrose, Fettgewebe und normalem Mammagewebe in zwei Dimensionen gemessen. Anhand dieser «RCB-Flächendimension» und der abgeschätzten Tumorzellularität wird letztlich der RCB-Score mittels öffentlich zugänglichem «residual cancer burden calculator» berechnet.
Klinische Studien nach NACT: VISION und TAXIS
Zwei laufende Studien, die in Zusammenhang mit NACT durchgeführt werden, sind VISION und TAXIS.
VISION («Intelligent Vacuum assisted biopsy Immediately before Surgery as an Intra- or pre-Operative surrogate for patient response to Neoadjuvant chemotherapy for breast cancer») ist eine multizentrische prospektive Machbarkeitsstudie, die bei Patient:innen mit radiologischer Komplettremission (rCR) nach NACT durchgeführt wird.
Nach erfolgter NACT wird zuerst das Tumorbett mittels vakuumassistierter Biopsie (VAB) entfernt, gefolgt von der eigentlichen Operation (brusterhaltend oder Mastektomie). Der primäre Endpunkt der Studie ist die Untersuchung der Sensitivität der VAB zur Vorhersage der patholoschen Komplettremission (pCR) des Primärtumors in der Brust. Entscheidend ist, dass die histologische Untersuchung der VAB unbeeinflusst und vor der histologischen Untersuchung des Operationspräparates erfolgt.
Bei der TAXIS-Studie («tailored axillary surgery with or without axillary lymph node dissection followed by radiotherapy in patients with clinically node-positive breast cancer») handelt es sich um eine multizentrische randomisierte Phase-III-Studie, bei der eine gezielte axilläre Chirurgie («targeted axillary surgery», TAS) mit oder ohne axilläre Lymphknotendissektion vorgenommen wird mit anschliessender Radiotherapie.
In dieser Studie soll primär geklärt werden, ob die Kombination von TAS und Radiotherapie vergleichbar bzw. nicht schlechter ist im Vergleich zur axillären Lymphknotendissektion in Bezug auf das krankheitsfreie Überleben von Patient:innen mit nodal metastasiertem Mammakarzinom. Ein Einschlusskriterium ist eine histologisch gesicherte Lymphknotenmetastasierung.
Im Vordergrund steht hier eine ausführliche histologische Untersuchung der mittels TAS entnommenen Lymphknoten. Dabei muss jeder entnommene Lymphknoten vom chirurgischen Team spezifisch bezeichnet werden (z.B. «palpabler und Clip-markierter Sentinel-Lymphknoten», «Sentinel-Lymphknoten, palpabel, suspekt», «Sentinel-Lymphknoten, nicht palpabel», «Non-Sentinel-Lymphknoten, palpabel» etc.), damit die histologischen Veränderungen jeweils zugeordnet und korreliert werden können. Bei vorausgegangener NACT sollte histologisch die Frage nach vitalem Resttumor sowie nach Vorhandensein oder Fehlen von Regressionszeichen explizit beantwortet werden.
Langfristig haben beide Studien zum Ziel, den Umfang der operativen Eingriffe zu minimieren und dadurch zu einer Verbesserung der Lebensqualität beizutragen.
Literatur:
1 Yau C et al.: Residual cancer burden after neoadjuvant chemotherapy and long-term survival outcomes in breast cancer: a multicentre pooled analysis of 5161 patients. Lancet Oncol 2022; 23(1): 149-60 2 Bossuyt V et al.: A dedicated structured data set for reporting of invasive carcinoma of the breast in the setting of neoadjuvant therapy: recommendations from the International Collaboration on Cancer Reporting (ICCR). Histopathology 2024; 84(7): 1111-29 3 Pastorello RG et al.: Clinico-pathologic predictors of patterns of residual disease following neoadjuvant chemotherapy for breast cancer. Mod Pathol 2021; 34(5): 875-82 4 Bossuyt V et al.: Recommendations for standardized pathological characterization of residual disease for neoadjuvant clinical trials of breast cancer by the BIG-NABCG collaboration. Ann Oncol 2015; 26(7): 1280-91
Das könnte Sie auch interessieren:
Die Menopause aus evolutionärer Perspektive
Kann man die menopausale Transition überhaupt als pathologisches Geschehen interpretieren, wenn alle Frauen um das 50. Lebensjahr diese durchleben? Oder wurde das obligate irreversible ...
Sport und Krebserkrankungen
In den letzten Jahzehnten hat sich insgesamt ein Paradigmenwechsel in der Medizin vollzogen – von der körperlichen Schonung hin zur Aktivität und frühen Mobilisierung im Rahmen von ...
Hormonelle Gesundheit nach der Menopause
Frauen verbringen heute rund ein Drittel ihres Lebens in der Postmenopause. Diese Lebensphase ist mit einer hohen Symptomlast und langfristigen gesundheitlichen Risiken verbunden, was ...