Wann steht die Operation nicht an erster Stelle?
Autor:
Prof. Dr. med. Andreas Günthert
Leiter gyn-zentrum
Brustzentrum Hirslanden Klinik St. Anna und Brustzentrum Aarau Cham Zug
Leiter Gynäkologisches Tumorzentrum Hirslanden Klinik St. Anna, Luzern
E-Mail: andreas.guenthert@gyn-zentrum.ch
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Therapieentscheidung beim Mammakarzinom basiert immer stärker auf molekularbiologischen Faktoren. Multimodale Therapiekonzepte führen zunehmend zu einer Deeskalation der Chirurgie. Dieser Artikel gibt einen Überblick über diese Entwicklungen, erhebt aber keinen Anspruch auf Vollständigkeit, zumal das Thema immer komplexer wird.
Keypoints
-
Beim metastasierten Mammakarzinom bringt eine Operation keinen Überlebensvorteil.
-
Bei geriatrischen Patientinnen kann unter bestimmten Voraussetzungen auf eine Operation verzichtet werden.
-
Beim inflammatorischen Mammakarzinom ist die neoadjuvante Therapie Standard.
-
Beim TNBC ist die neoadjuvante Therapie Standard.
-
Bei HER2-überexprimierenden Mammakarzinomen ab 2cm ist die neoadjuvante Therapie Standard.
-
Die neoadjuvante Therapie ermöglicht meist eine Deeskalation der Chirurgie.
-
Die neoadjuvante In-vivo-Testung ist auch beim ERpos. Mammakarzinom zur Deeskalation der Chemotherapie geeignet.
William Stewart Halsted veröffentlichte im Jahr 1907 in den «Annals of Surgery» seine Arbeit zur radikalen Chirurgie des Mammakarzinoms, durch die annähernd 50% seiner Patientinnen als geheilt beschrieben wurden. Bereits einige Jahre zuvor postulierten Albert Schinzinger in Freiburg und Sir George Beatson in Glasgow die Ovarektomie als primäre Methode bei inoperablem Mammakarzinom, womit die endokrine und auch die neoadjuvante Therapie implementiert wurden. Spätestens mit Bernard Fisher, Pittsburgh, 1971, wurde die Systemtherapie als wesentlicher Bestandteil der Therapie des Mammakarzinoms endgültig etabliert. Insbesondere Studien zu neoadjuvanten Therapien führen seit etwa zwei Jahrzehnten dazu, dass wir einerseits eine In-vivo-Testung der Therapiekonzepte haben, andererseits aber auch die Radikalität der Lokaltherapie deeskalieren können. Mit Charles Perous Publikation in «Nature» im Jahr 2000 und seinem Modell der intrinsischen Subtypen hat ein differenziertes Umdenken stattgefunden, auch wenn dieses Modell natürlich längst weiterentwickelt wurde, sodass wir heute sehr detailliert die Molekularbiologie, die Genetik und auch das Immunsystem in die Therapieentscheidung mit einbeziehen. Bei Verdacht auf eine Mutation in den Genen BRCA 1 oder 2 hat der Gentest einen potenziellen Einfluss auf die Chirurgie, wobei wir heute erfreulicherweise das Testergebnis recht schnell erhalten und eine dadurch bedingte Therapieverzögerung kaum mehr eine Rolle spielen sollte.
Gründe, warum primär operiert werden sollte
Ein Grund kann sein, dass ein neoadjuvantes Konzept nichts an der Situation verbessert. Die Gruppe der Patientinnen, auf die dies zutrifft, wird allerdings immer kleiner, zumal bei HER2-überexprimierenden Tumoren und auch beim tripelnegativen Mammakarzinom (TNBC) die neoadjuvante Therapie nur in Ausnahmen nicht dem Standard entspricht. Es müssen aber auch die Aspekte der Patientin berücksichtigt werden. Sollte diese aus psychologischen Gründen eine Operation unbedingt an erster Stelle wünschen, dann kann es gerechtfertigt sein, nach entsprechender Aufklärung diesem Wunsch auch nachzukommen. Zudem gibt es auch Patientinnen, die jegliche weitere Therapieoption ablehnen, sodass eine alleinige Operation, zumindest nach Halsted-Doktrin, eine gewisse Chance auf Heilung bringen kann.
Gründe, warum nicht primär operiert werden sollte
Gründe, primär nicht zu operieren, können sein, dass es nicht möglich ist, dass es nichts bringt oder dass neoadjuvant zu therapieren besser ist. Es kann natürlich vorkommen, dass eine Patientin aktuell wegen Komorbiditäten nicht operiert werden kann oder eine Operation auch ablehnt. Insbesondere bei geriatrischen Patientinnen wird oft nicht primär operiert, insbesondere wenn die Lebenserwartung in keiner Relation zum Nutzen einer Operation des Mammakarzinoms steht. Hierfür gibt es entsprechende Möglichkeiten, dies gegeneinander abzuwägen, z.B. mit dem Charlson-Komorbiditäts-Index. Bei einem wenig aggressiven und hormonabhängigen Tumor ist oftmals die alleinige endokrine Therapie zunächst gerechtfertigt, wobei ein wesentlicher Teil der Patientinnen im Verlauf doch noch operiert wird.1
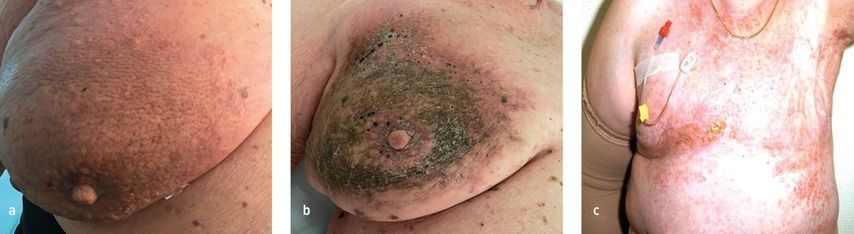
Es kann auch sein, dass eine Operation vermutlich nicht wesentlich etwas an der Prognose ändert, hier sind das primär metastasierte Mammakarzinom und auch das inflammatorische Mammakarzinom (IBR) zu nennen. Auch wenn bei Letzterem eine radikale Operation in Form der Mastektomie und der axillären Lymphadenektomie etablierter Therapiebestandteil des trimodalen Konzeptes ist, so fehlt bisher eine klare Evidenz, dass dies einen entscheidenden Einfluss auf das Überleben hat, wenn auch eine bessere lokale Kontrolle dadurch erzielt wird.2 Standard ist beim IBR jedoch unverändert die primäre Systemtherapie mit anschliessender radikaler Chirurgie, wobei hinsichtlich der Axilla eine Deeskalation bei klinischer Komplettremission gefolgt von der Radiotherapie vertretbar zu sein scheint. Beim metastasierten Mammakarzinom ist die Situation inzwischen recht gut untersucht und es gab diverse multizentrische randomisierte Studien (TATA, POSYTIVE, ECOG 2108, MF07-01), die untersuchten, ob die Tumorchirurgie in dieser Situation überhaupt einen Einfluss auf das Überleben hat. Fazit dieser Studien ist, dass die Operation keinen Einfluss auf das Überleben hat. Lediglich in der MF07-01-Studie aus der Türkei zeichnete sich ein positiver Effekt in der Subgruppe des rezeptorpositiven Mammakarzinoms mit ausschliesslich ossärer Metastasierung ab.3 Es kann auch eine vertretbare palliative Massnahme sein, eine lokale Kontrolle durch Chirurgie zu erzielen, wenn z.B. ein Befund ein Problem im Alltag darstellt oder auch um einen Cancer en cuirasse zu verhindern (Abb. 1). In der Regel ergibt sich dies aber im Verlauf, nicht primär. Auch wenn aktuell gilt, dass eine Operation beim metastasierten Mammakarzinom keinen Einfluss auf das Überleben hat, so muss dies fortlaufend durch Etablierung weiterer Therapien immer wieder neu überprüft werden; das metastasierte Mammakarzinom ist nicht mehr in jedem Fall unheilbar.
Abb. 1 a–c: a und b: palliative Situation unter Letrozol vor und nach 3 Monaten Therapie. c: Cancer en cuirasse
Wann ist die neoadjuvante Therapie besser?
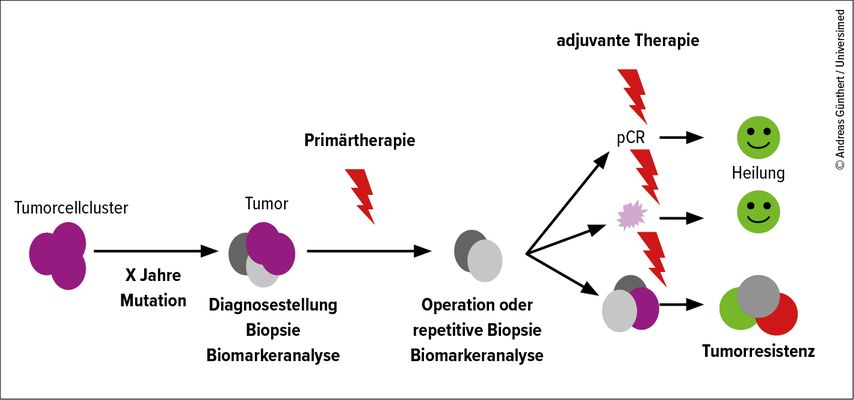
Die neoadjuvante Therapie ist in jedem Fall dann besser, wenn eine Deeskalation der Chirurgie und auch der Radiotherapie erzielt werden kann. Zudem hat die In-vivo-Testung einer Therapie einen immer höheren Stellenwert. Die Deeskalation der Chirurgie durch neoadjuvante Therapie ist eine noch recht junge Entwicklung der letzten 15 Jahre. Zunächst konnte durch Florian Fitzal im Jahr 2011 in einer Kohortenstudie gezeigt werden, dass durchaus in den neuen Tumorgrenzen nach neoadjuvanter Therapie bei gleicher Sicherheit operiert werden und vielen Patientinnen die Mastektomie erspart werden kann. Dies konnte durch die Datenbank der «German Breast Group» später anhand von 6134 Patientinnen bestätigt werden, sodass auch bei initial multizentrischen Befunden eine brusterhaltende Therapie möglich ist.4,5 Ein äusserst wichtiger etablierter prognostischer Faktor ist die pathologische Komplettremission nach neoadjuvanter Therapie (pCR). Lag die pathologische Komplettremission in den ersten neoadjuvanten Chemotherapie-Studien wie z.B. der NSABP-B27-Studie im Jahr 2008 noch bei 26%, so erreichte die NeoALTTO-Studie 2012 bereits eine pCR von 51%. In jüngeren Studien mit dualer Inhibition bei HER2 überexprimierenden Tumoren und auch mit Checkpoint-Inhibitoren beim TNBC werden noch deutlich höhere Raten erreicht. In der TRYPHAENA-Studie wurde beim HER2-überexprimierenden Mammakarzinom durch duale Antikörpertherapie in Kombination mit Chemotherapie eine pCR von 64% erreicht.6 Die KATHERINE-Studie zeigte wiederum, dass bei fehlender pCR eine Umstellung in der adjuvanten Situation auf T-DM1 einen Vorteil gegenüber der Therapie mit Trastuzumab hat.7 Eine vergleichbare Situation ergibt sich für das TNBC. In der KEYNOTE-522-Studie zeigte sich bei einer PD-L1-Expression eine pCR in über 70% der Fälle nach Therapie mit Pembrolizumab in Kombination mit Chemotherapie, wobei ein Vorteil der adjuvanten Therapie mit Pembrolizumab nur bei fehlender pCR gegeben war.8 Die In-vivo-Testung der neoadjuvanten Therapie hat also bereits einen signifikanten Einfluss auf die Operation und auch auf die weitere adjuvante Therapie. Auch beim rezeptorpositiven Mammakarzinom gibt es Entwicklungen, die auf eine Optimierung der Systemtherapie durch In-vivo-Testung im neoadjuvanten Setting zielen. Die ADAPT-Studien überprüfen sehr detailliert Biomarker unter neoadjuvanter Therapie in unterschiedlichen Ausgangssituationen, um so eine zielgerichtete Therapie durch In-vivo-Testung besser abzustimmen. Die Ergebnisse zur Deeskalation der adjuvanten Chemotherapie beim rezeptorpositiven Mammakarzinom durch repetitive Biomarkeranalyse mittels Oncotype DX nach neoadjuvanter endokriner Therapie sind äusserst vielversprechend.9 Insofern wird sich wohl in absehbarer Zeit die Frage stellen, bei welchen Patient*innen eine primäre Systemtherapie nicht erfolgen sollte (Abb. 2).
Abb. 2: Sehr vereinfachtes Modell der adaptierten Tumortherapie durch In-vivo-Testung. Von der Tumorzellentstehung bis zur Diagnosestellung eines Tumors vergeht ein gewisser Zeitraum, in dem sich der Tumor verändert und sich dann inhomogen präsentiert. Die Biomarkeranalyse führt zu einer primären Therapieentscheidung, die Wirksamkeit wird bildgebend und durch erneute Analyse nach neoadjuvanter Therapie überprüft. Nach dieser In-vivo-Testung ist für die weitere adjuvante Therapie entscheidend, ob eine pCR vorliegt. Die wesentlichen Nachteile einer adjuvanten Therapie liegen darin, dass unklar ist, ob diese überhaupt benötigt wird und ob die Patienten letztendlich darauf ansprechen
Es stellt sich zudem die Frage, ob wir überhaupt noch alle Patientinnen mit klinischer Komplettremission operieren müssen. Problematisch ist bisher die Verifizierung der klinischen Komplettremission als pCR ohne chirurgische Entfernung des Gewebes. Auch der Stellenwert der axillären Resektion der Lymphknoten vor und nach neoadjuvanter Therapie ist noch nicht geklärt. Nachdem bei cN0 die Sentinelnode-Biopsie nach abgeschlossener neoadjuvanter Therapie akzeptiert worden ist (Studien ACOSOG Z1071, SENTINA, SN FNAC und GANEA 2), setzt sich nun bei initial positivem Lymphknotenstatus zunehmend die «targeted axillary dissection» durch (TAD), die aktuell noch in multizentrischen Studien überprüft wird (TAXIS, AXSANA u.a.). Hierbei wird die Sentinelnode-Biopsie mit der Resektion von markierten positiven Lymphknoten und suspekten Lymphknoten kombiniert. Die Korrelation für ypN0 zu ypT0 liegt bei HER2pos und TNBC über 70%, eine axilläre «mixed response» findet sich dagegen bei ERpos/HER2neg in 75% der Fälle. Dies bedeutet, dass durch die neoadjuvante Therapie die chirurgische Radikalität in der Axilla erheblich reduziert werden kann, wenn auch die Langzeitdaten der o.a. Studien noch ausstehen. Der Stellenwert der adjuvanten Radiotherapie der Lymphabflusswege ist hier allerdings noch unklar, die Deeskalation der Chirurgie sollte aber wohl nicht mit einer Eskalation der Radiotherapie kompensiert werden.
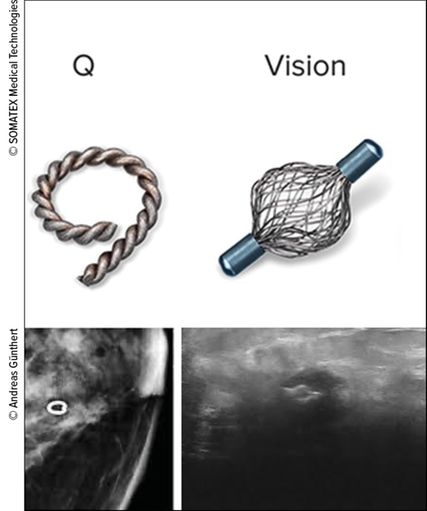
Abb. 3: Zwei repräsentative Clips, die in der SENTA-Registerstudie durch die höhere Detektionsrate positiv aufgefallen sind. Allerdings sind diese Clips problematisch für eine Vakuumbiopsie, da durch ihre Grösse das System bei der Biopsie blockiert werden kann
Noch viel Entwicklungspotenzial besteht bei der adäquaten Markierung der Befunde vor der Therapie und der Detektion zur Reevaluation respektive Operation. Traditionell werden hier Metallclips verwendet, die aber unterschiedlich gut detektierbar sind oder auch dislozieren können. In Evaluation befinden sich andere Systeme, wie radioaktive Seeds, magnetische Clips, Radarreflektoren und Radiofrequenzmarkierungen. Ausser zu den konventionellen Clips sind bisher nur wenige Daten zu den Systemen verfügbar. Durch die zunehmende Standardisierung der neoadjuvanten Therapie spielen diese Systeme aber eine bedeutende Rolle (Abb. 3). In der multizentrischen SENTA-Register-Studie konnte der Clip nach neoadjuvanter Therapie bei 78% der Fälle erfolgreich intraoperativ entfernt werden, meist durch zusätzliche präoperative Drahtmarkierung. Hier besteht also offensichtlich noch Verbesserungspotenzial. Auch die Verifizierung der pCR durch minimal invasive Techniken wird angestrebt. Es wurden bereits einige Studien zur Vakuumbiopsie nach neoadjuvanter Therapie publiziert, besonders hervorzuheben ist hierbei die RESPONDER-Studie, die eine Falsch-negativ-Rate von 17,8% hatte, was so zunächst noch nicht akzeptabel war. Allerdings waren die Biopsienadeln in der Studie nicht selten verhältnismässig klein und es besteht diesbezüglich noch eine Lernkurve.10 Dieses Konzept wird international weiterverfolgt, in der Schweiz läuft dazu die multizentrische VISION1-Studie. Es ist also absehbar, dass nicht wenige Patientinnen nach neoadjuvanter Therapie und Verdacht auf pCR in einigen Jahren keine Operation mehr benötigen werden.
Literatur:
1 Jauhari Y et al.: Surgical decisions in older women with early breast cancer: patient and disease factors. Br J Surg 2021; 108: 160-7 2 Adesoye T, Lucci A: Current surgical management of inflammatory breast Cancer. Ann Surg Oncol 2021; 28: 5461-7 3 Soran A et al.: Randomized trial comparing resection of primary tumor with no surgery in stage IV breast cancer at presentation: Protocol MF07-01. Ann Surg Oncol 2018; 25: 3141-9 4 Fitzal F et al.: Oncologic safety of breast conserving surgery after tumour downsizing by neoadjuvant therapy: a retrosprective single center cohort study. Breast Cancer Res Treat 2011; 127: 121-8 5 Ataseven B et al.: Impact of multifocal or multicentric disease on surgery and locoregional, distant and overall survival of 6’134 breast cancer patients treated with neoadjuvant chemotherapy. Ann Surg Oncol 2015; 22: 1118-27 6 Schneeweiss A et al.: Long-term efficacy analysis of the randomized, phase II TRYPHAENA cardiac safety study: Evaluating pertuzumab and trastuzumab plus standard neoadjuvant anthracycline-containing and anthracycline-free chemotherapy regimens in patients with HER2-positive early breast cancer. Eur J Cancer 2018; 89: 27-35 7 Von Minckwitz G et al.: Trastuzumab emtansine for residual invasive HER2-positive breast cancer. N Engl J Med 2019; 380: 617-28 8 Schmid P et al.: Pembrolizumab for early triple-negative breast cancer. N Engl J Med 2020; 382: 810-21 9 Nitz UA et al.: Endocrine therapy response and 21-gene expression assay for therapy guidance in HR+/HER2- early breast cancer. J Clin Oncol 2022; 40: 2557-67 10 Pfob A et al.: Intelligent vacuum-assisted biopsy to identify breast cancer patients with pathologic complete response (ypT0 and ypN0) after neoadjuvant systemic treatment for omission of breast and axillary surgery. J Clin Oncol 2022; 40: 1903-15
Das könnte Sie auch interessieren:
Welche Risiken sind zu erwarten?
Die präventive Mastektomie wird vor allem bei genetischer Vorbelastung, z.B. bei BRCA1/2-Mutationen, erwogen. Der Eingriff kann das Brustkrebs-Erkrankungsrisiko deutlich reduzieren, aber ...
Operative Therapie und Risikoreduktion bei BRCA-Mutations-Trägerinnen
Familiäre Krebserkrankungen, besonders durch pathogene Genveränderungen bedingt, sind vermehrt in den Fokus der Forschung gerückt. Dies zeigt sich vor allem bei Brustkrebs (BC). Das ...
AI in der Reproduktionsmedizin
Kein Thema bewegt derzeit die Menschen mehr als künstliche Intelligenz (AI – „artificial intelligence“). Wiewohl in der Behandlung des unerfüllten Kinderwunsches in den letzten ...