Kombinationstherapie mit plättchenreichem Plasma und Hyaluronsäure
Autor:innen:
Dr. Elisângela Wenzel1
Dr. rer. nat. Norbert Laube2
1 Privatpraxis Dr. Wenzel, Meerbusch
2 RegenLab GmbH, München
E-Mail: wenzel@praxis-drwenzel.de
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Hochwertiges autologes plättchenreiches Plasma (PRP) verfügt von Natur aus über einen komplex zusammengesetzten Cocktail aus zahlreichen bioaktiven Substanzen. Gegenüber dem Vollblut sind die im fraktionierten Plasma suspendierten Thrombozyten u.a. isoliert und moderat aufkonzentriert. Fachgerecht reinjiziert, kann PRP lokal die natürlichen Mechanismen der Wundheilungs- und Regenerations-prozesse unterstützen.
Keypoints
-
Autologes thrombozytenreiches Plasma (PRP) ist ein injizierbares Orthobiologikum. Diese reine Plasmafraktion wird schonend aus dem Vollblut des Patienten gewonnen und ist idealtypisch ausschließlich mit moderat aufkonzentrierten vitalen und viablen Thrombozyten angereichert.
-
PRP ist nicht nur für die Anwendung im Bereich der ästhetischen Medizin geeignet.
-
PRP adressiert das gesamte Indikationsspektrum lokaler Erkrankungen der Haut und fällt damit prinzipiell in die Bereiche der (klassischen) kurativen Dermatologie sowie der plastischen und ästhetischen Chirurgie mit ihren rekonstruktiven Aufgaben.
-
Nur ein definiert zusammengesetztes, biologisch hochpotentes PRP ist der Schlüssel zu einem nachhaltigen Therapieerfolg.
Autologes plättchenreiches Plasma (PRP) hat sich mittlerweile, nach zum Teil berechtigter Anfangsskepsis und trotz auch heute noch zu Recht geäußerter Kritik, in fast allen medizinischen Fachrichtungen als geeignete Therapieoption zur lokalen Unterstützung der Geweberegeneration durchgesetzt.1 In der Dermatologie gibt es zahlreiche Indikationen für PRP, auch jenseits eines Kosmetikums. Die klinische Evidenz steigt stetig und untermauert dabei das Konzept einer individualisierten regenerativen Medizin.
Rationale für den Einsatz von PRP
Die in einem PRP aufbereitete Kombination aus den im Plasma in hoher Konzentration vorkommenden zahlreichen bioaktiven Molekülen (u.a. Fibrinogen und andere Gerinnungsmoleküle sowie essenzielle Zellnährstoffe) und den von den Thrombozyten sezernierten Signalproteinen kann einen Reset und/oder Boost der an der Läsion gehemmten oder gestörten physiologischen Prozesse bewirken. Die proliferative Phase der Wundheilung wird unterstützt und gegebenenfalls (re)orchestriert, wodurch eine vollständige Reparation eingeleitet werden kann.
Aufgrund dieser anabol reparativen Wirkung werden PRP zur Behandlung verletzter Gewebe insbesondere mit niedrigem bzw. stark limitiertem intrinsischem Heilungspotenzial (z.B. atrophe Narben, Keloide) und bei Melasma, Alopecia, Striae cutis distensae, Lichen sclerosus, Belastungsinkontinenz oder weiblicher sexueller Funktionsstörung angewendet.
Besonders der Einsatz von sachgerecht aufbereiteten PRP mit einem biologisch sinnvoll definierten und anwenderunabhängig gleichbleibend reproduzierbaren Plasmazellprofil kann die Regenerationsprozesse nachhaltig unterstützen.
Exkurs
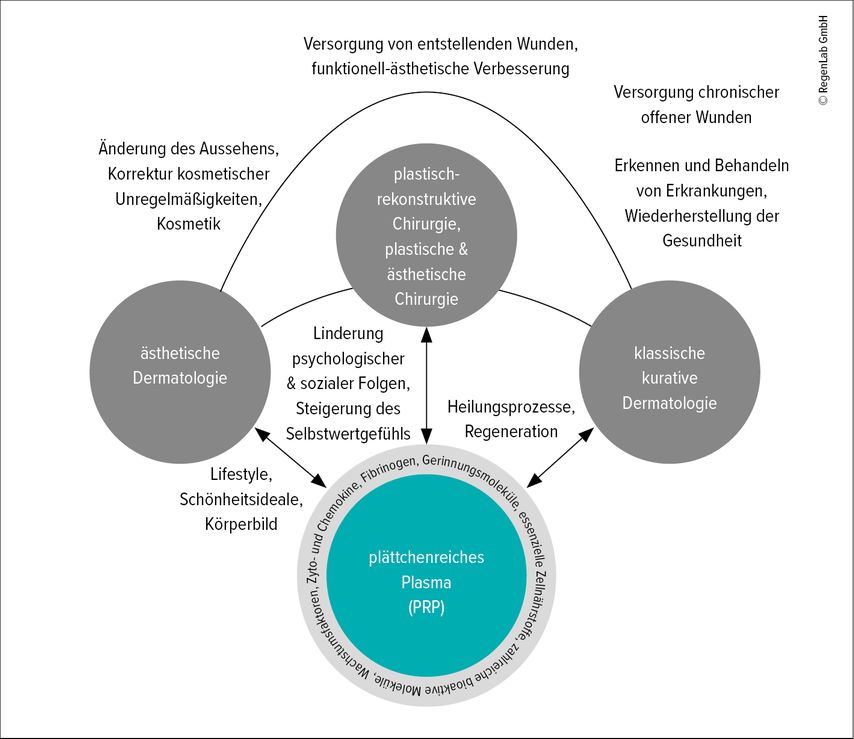
Trotz ihres unbestreitbaren biologischen Potenzials haben sich PRP-Anwendungen in den kurativen und operativen Teilgebieten der Dermatologie (Abb.1) jedoch nur zögerlich etabliert.
Abb. 1: Autologes plättchenreiches Plasma (PRP) hat Eingang in die Dermatologie über Applikationen im Bereich der ästhetischen Medizin gefunden (z.B. zur Faltenreduktion, Hautverjüngung und Narbenbehandlung) und dort einen festen Platz eingenommen.5 Mittlerweile werden PRP-Aufbereitungen, ihrer essenziellen Fähigkeit zur „Heilungsförderung“ entsprechend, in sämtlichen Teilgebieten der Dermatologie eingesetzt – denn aus der biologischen Rationale heraus ist ein PRP-Einsatz prinzipiell überall dort indiziert, wo akut oder chronisch gestörte Heilungsprozesse lokal initiiert, beschleunigt und stabilisiert werden sollen („There is only one biology“). Physiologisch hochwertige PRP, mit ihrem intrinsisch-regenerativen Potenzial, u.a. aus Plasmavitalstoffen und dem von den Thrombozyten sezernierten „molekularen Werkzeugkasten“, bestehend aus verschiedensten biologisch aktiven Substanzen, können dabei die nachhaltigsten Ergebnisse erzielen. Mittlerweile haben sich in der Dermatologie, wie auch in zahlreichen anderen medizinischen Fachrichtungen, PRP-Anwendungen klinisch evident bewährt und dabei zunehmend etabliert (modifiziert nach Pixley JN et al. 2023 und Manole CG et al. 2023)6,7
Die ersten ausgiebigen Anwendungen erfolgten im Umfeld der ästhetischen Dermatologie. Hier übernahm das PRP schnell die Rolle eines fantastischen Jungbrunnens, ein Versprechen, das verständlicherweise nicht gehalten werden konnte und kann. Vielleicht lag und liegt dies daran, dass dieses aggressiv umworbene Marktsegment besonders stark von unrealistischen Erwartungen und fragwürdigen Billigangeboten von Medizinprodukten für die PRP-Herstellung betroffen war (und immer noch ist). Diese oftmals ausschließlich über das Internet vertriebenen „Fake-Produkte“ verletzen z.T. sämtliche gesetzlichen Zulassungsrichtlinien und werden ohne die von der Medizinprodukte-Betreiberverordnung vor-geschriebene fachgerechte Einweisung an die Kunden ausgeliefert. Die Eigenschaften der damit aufbereiteten „Blutprodukte“ können als zweifelhaft, ihr Einsatz muss als Patientengefährdung bezeichnet werden.2
Objektive Ergebnislagen, wie sie für die Schaffung von klinischer Evidenz auf Basis placebokontrollierter, randomisierter und doppelblinder Studien unabdingbar sind, konnten und können so nicht erzielt werden. Dies hat zu einem Vertrauensverlust geführt, welcher bei allen berechtigten Zweifeln dem Ruf von PRP im Gesamtgebiet der Dermatologie für (zu) lange Zeit geschadet hat. Gründe für diese Zweifel sind u.a. uneinheitliche und herstellungsprozessbedingt mehrheitlich nicht reproduzierbare PRP-Zusammensetzungen, eine fehlende, nicht einheitliche oder gar falsche Nomenklatur bzw. unterschiedliche Applikationsschemata.
Die folgenden Anwendungsbeispiele aus unserer Praxis zeigen, dass PRP nicht nur ein Kosmetikum ist, sondern mit seinem autolog-biologischen Wirkstoffcocktail zu Recht als eine moderne konservative Therapiealternative in der Behandlung verschiedenster akuter und chronischer Hauterkrankungen gilt, wirksam u.a. bei Alopecia androgenetica, Alopecia areata, Melasma, Lichen sclerosus, Belastungsinkontinenz und weiblicher sexueller Funktionsstörung.3,4
Beispiele für die Anwendung von PRP in der Hautarztpraxis
PRP-Aufbereitung
In unserer Praxis kommen plättchenreiche Plasmen (RegenPRP™) und Kombinationstherapien mit RegenPRP™+Hyaluronsäure (HA) (hergestellt mit Cellular Matrix) zum Einsatz.
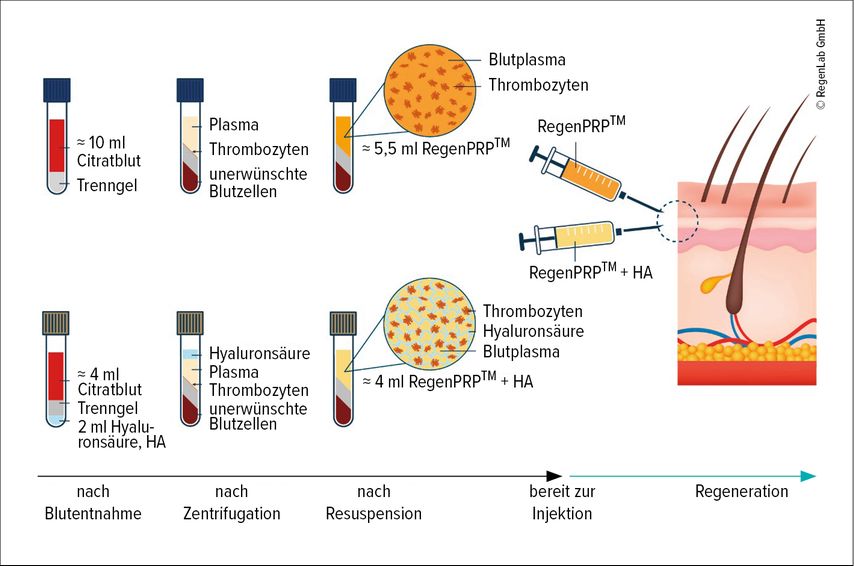
Die Herstellung dieser Blutprodukte ist durch die Einfachheit, die regulatorische Sicherheit und die anwenderunabhängige Wiederholbarkeit (wichtig im Praxisalltag mit wechselndem Personal) der Zusammensetzung des jeweils erhaltenen Plasmazellprofils gekennzeichnet (Abb. 2). Da hier die PRP-Separation und die HA-Beimischung verfahrenstechnisch auf einem physikalischen Zwangsprozess basieren, ist die wiederholbare stöchiometrische und zellbiologische Qualität der injektionsfertigen PRP-HA-Kombination sichergestellt. Diese Eigenschaft ermöglicht vor allem bei Mehrschritttherapien nachhaltige Erfolge.
Abb. 2: Die RegenLab®-Technologie (Schema) eröffnet über einen von einem thixotropen Trenngel vermittelten physikalischen Zwangsprozess die anwenderunabhängige und irreversible Aufbereitung eines sogenannten RegenPRP™ (oben), eines physiologisch günstig konzentrierten PRP (Faktor ≈1,65 gegenüber Vollblut)8,9 mit definiertem und reproduzierbarem Plasmazellprofil. Dieses Verfahren schließt auch die selektive dichtefraktionierte Trennung der Leukozyten ein: Während sich nach der PRP-Aufbereitung ein Großteil der immunologisch wirksamen Lymphozyten und Monozyten (= mononukleäre Zellen des peripheren Blutes; PBMC) im PRP befindet, sind die entzündungsfördernden neutrophilen Granulozyten, zusammen mit den Erythrozyten, mehrheitlich unterhalb des Trenngels irreversibel aus dem Überstand entfernt. Das Cellular-Matrix-Konzept kombiniert die Herstellung von RegenPRP™ mit gleichzeitiger Bereitstellung einer bereits im Medizinprodukt vorgelegten zweckoptimierten Hyaluronsäure (HA) (unten). Beide Blutpräparate, RegenPRP™ und RegenPRP™+HA, werden jeweils in einem „geschlossenen System“, durchgehend von der Blutentnahme bis nach der Überführung in die Applikationsspritze, regulatorisch einwandfrei hergestellt
Diätetische Prähabilitation – kein Nachteil in der Orthobiologie
Führt man sich vor Augen, dass die Blutzusammensetzung auch ohne Krankheitswert u.a. jahreszeitlichen und zirkadianen (stoffwechselphysiologischen/metabolischen) Schwankungen bezüglich der Konzentrationen der im Plasma gelösten Substanzen, der zellulären Bestandteile und der damit verknüpften Parameter des Gerinnungs- und fibrinolytischen Systems unterliegt,10–12 so scheint zumindest bei einigen Patienten eine frühzeitige zielgerichtete Aufklärung im Vorfeld einer geplanten PRP-Therapie sinnvoll.13 Das typischerweise gelblich klare Blutplasma kann aufgrund von zahlreichen Ursachen wie Ernährung, Trinkvolumen, Supplementen, Hormonhaushalt, Medikamenten, Stoffwechselerkrankungen, bakterieller Kontamination, Hämolyse etc. unterschiedliche Färbungen aufweisen. Daher ist empfehlenswert, bei einer besonders auffälligen PRP-Farbe den Grund abzuklären und diesen gegebenenfalls vor der nächsten Behandlung abzustellen. Ein lipämisches PRP (sog. „fatty PRP“) sollte immer verworfen werden.
Um dem Patienten die Möglichkeit zu eröffnen, das „bestmögliche“ PRP reinjiziert zu bekommen, ist es im Vorfeld der Maßnahme immer zweckmäßig (wenn nicht schon im Rahmen der Gesamtbehandlung geschehen), ihn über den Umstand aufzuklären, dass z.B. die Ernährungsweise einen negativen Einfluss auf die (Haut-)Gesundheit haben kann.14–17 Es ist bestimmt kein Nachteil, wenn der Patient (zumindest) jeweils für 1–2 Wochen vor und nach einer PRP-Injektion die Aufnahme stark säurebildender18 sowie entzündungsfördernder Nahrungsmittel einschränkt oder besser ganz vermeidet.
Ebenso gänzlich vermieden werden sollten aus dem Rahmen fallende tagesaktuelle/spontane Lebens- und Ernährungsweisen, welche die PRP-Qualität stark beeinflussen und damit den Therapieerfolg schmälern können. Extreme Diäten oder exzessive Partyaktivitäten am Vortag der Behandlung sind für das Erreichen eines Behandlungserfolgs eher hinderlich.
Wirkung der anabolen Faktoren des PRP
Die anabolen Faktoren eines PRP können die Heilung und Neubildung gesunden Gewebes nachhaltig stimulieren: Aus dem von neutrophilen Granulozyten konsequent befreiten RegenPRP™ (Abb.2) können die von den Thrombozyten freigesetzten Wachstumsfaktoren sowie Zytokine mit ihren verschiedenen anabolen, antiinflammatorischen und antibakteriellen19 Wirkungen besonders effektiv die Kontrolle über den Verlauf des proliferativen Stadiums übernehmen.
Dieses hohe Nettopotenzial der zellregenerativen Thrombozytenwirkung wird zusätzlich durch die im Blutplasma gelösten Nährstoffe (u.a. Elektrolyte, Hormone, Proteine, Wachstumsfaktoren, Vitamine), welche für das Zellüberleben wichtig sind, therapeutisch gewinnbringend unterstützt.
Dass die für die Koagulation und Fibrinpolymerisation verantwortlichen Plasmaproteine durch die Wechselwirkung mit den in der Interstitialflüssigkeit gelösten Ca2+-Ionen und dem an der Einstichstelle freigelegten Kollagen (re)aktiviert werden, führt zur Bildung eines moderat viskosen temporären Gel-Depots. Dadurch wird eine ungewollte Verteilung des RegenPRP™ vermieden und es werden, vermittelt durch die Gerüststruktur des Fibrins, u.a. eine Zelleinwanderung und Gewebeneubildung gefördert.20 Gleichzeitig bleiben die Thrombozyten, den Therapieerfolg begünstigend, über mehrere Tage hinweg biosynthetisch aktiv.
Hyaluronsäure
Die bewährten biologischen Effekte eines RegenPRP™ können durch geeignete Kombination mit einer passend funktionalisierten matrix- und feuchtigkeitsgebenden HA verstärkt bzw. synergistisch gesteigert werden („liquid tissue engineering“).21–31 Dadurch wird die zeitliche Verfügbarkeit des PRP am Injektionsort erhöht; es ergeben sich gleichzeitig eine die Gewebeneubildung ausrichtende permeable 3D-Struktur und auch immer eine intensive Hauthydratation sowie ein moderat anhaltender Auffülleffekt. Eigenschaften, die sowohl in der ästhetischen als auch z.B. in der gynäkologischen Dermatologiewichtige biologische Funktionen übernehmen.32–34
Basierend auf der bereits zur Herstellung von RegenPRP™ verwendeten Trenngeltechnologie erfolgt mit Cellular Matrix die stöchiometrisch sichere Aufbereitung einer injektionsfertigen homogenen Mischung aus RegenPRP™+HA in einem geschlossenen System mit einer bereits im Zentrifugenröhrchen vorgelegten und perfekt abgestimmten HA (Abb.2).
Anwendungs- und Injektionsprotokolle
Die Vorbereitung des Patienten beinhaltet u.a. die Reinigung des Behandlungsgebiets mit alkoholfreiem Desinfektionsmittel und ggf. eine topische geringdosierte Betäubung (z.B. Lidocain-/Prilocain-haltige Salbe). Die Injektion von RegenPRP™ und Cellular Matrix erfolgt intradermal, in kleinen Abständen (ca. 0,5–1cm) und gleichmäßig über das Behandlungsareal verteilt. Bei gynäkologischen Indikationen wie beispielsweise der Behandlung weiblicher sexueller Funktionsstörungen erfolgt die Applikation des PRP an drei unterschiedlichen anatomischen Injektionspunkten der Vagina in unterschiedlichen Tiefen.
Die nachhaltigen regenerativen Effekte der PRP- oder PRP+HA-Injektionen stellen sich meist nach zwei bis drei Behandlungen ein und behalten ihre Wirkung über bis zu vier Monate bei. Treten im Zusammenhang mit einer PRP-Anwendung Hautreaktionen wie Brennen, Jucken oder Rötung auf, handelt es sich dabei höchstwahrscheinlich um eine nachvollziehbare, natürliche, milde, passagere Reaktion der Haut auf die Injektionsverletzung, welche in der Regel gut toleriert wird und innerhalb kürzester Zeit abklingt. Schwere oder andauernde Nebenwirkungen sind extrem selten.
Praxistipp: Übung macht den Meister!
Um über die aktuellen Entwicklungen zu Themen rund um PRP – von Akne und Applikationstechniken bis hin zu Zoster-bedingten Schmerzen35 oder Zentrifugationsprotokollen – in der Klinik und Praxis informiert zu sein, besuchen Sie Schulungen und „Hands-on-Workshops“, die von erfahrenen Ärztinnen und Ärzten zahlreich angeboten werden.
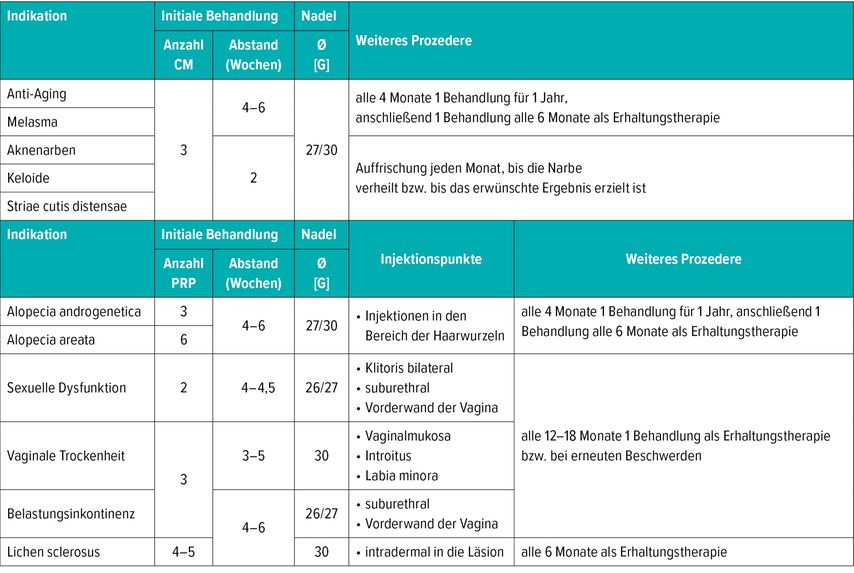
In der Tabelle 1 sind für verschiedene Indikationen die in unserer Praxis bewährten klinischen Vorgehensweisen bei Anti-Aging- und Alopecia-Behandlungen sowie bei der Therapie weiblicher sexueller Funktionsstörungen zusammengefasst.
Tab. 1:Typische kosmetologische und gynäko-dermatologische Indikationen und praxisnah empfohlene Anwendungsprotokolle für PRP (RegenPRP™) und eine Kombination aus PRP und Hyaluronsäure (RegenPRP™+HA; CM). Die Injektionen erfolgen immer intradermal. Bei topischen Anwendungen von RegenPRP™ können im Vorfeld konditionierende („hautöffnende“) Maßnahmen wie z.B. Laserbehandlung, Radiofrequenztherapie oder Microneedling eingesetzt werden
Conclusio
Sachgerecht zubereitet und fachgerecht angewendet, eröffnen autologes PRP und Mischungen aus PRP und HA konservative Behandlungsoptionen für ein breites Indikationsspektrum – in allen Bereichen der Dermatologie, wo natürliche regenerative Prozesse lokal regelgerecht angeregt werden sollen.
Literatur:
1 Gupta S et al.: Expert Review of Hematology 2020; 14(1): 97-108 2 Wenzel E et al.: Haut 2024: 3: 258-61 3 Rodriguez M et al.: Cureus 2024; 16(8): e68306 4 Vladulescu D et al.: Biomedicines 2023; 12(1): 7 5 Elghblawi E: J Cosmet Dermatol 2018; 17(3): 423-30 6 Pixley JN et al.: J Dermatolog Treat 2023; 34(1): 2142035 7 Manole CG et al.: Life (Basel) 2023; 14(1): 40 8Berndt S et al.: Tissue Eng Part A 2019; 25(21-22): 1550-639 Yoshida R et al.: J Orthop Res 2014; 32(2): 291-5 10 Budkowska M et al.: Thromb Res 2019; 182: 79-88 11 Pritchett D et al.: J Biol Rhythms 2015; 30(5): 374-88 12 Hartley PS: Platelets 2012; 23(2): 157-60 13 Platzer H et al.: Orthopadie (Heidelb) 2023; 52(11): 907-15 14 Ryguła I et al.: Nutrients 2024; 16(10): 1476 15 Katsimbri P et al.: Antioxidants (Basel) 2021; 10(2): 157 16 Keri JE et al.: J Clin Aesthet Dermatol 2008; 1(3): 22-6 17 Min M et al.: Life (Basel) 2024; 14(11): 1439 18 Remer T et al.: J Am Diet Assoc 1995; 95(7): 791-7 19 Cetinkaya RA et al.: Eur J Trauma Emerg Surg 2018; 44(6): 859-67 20 Berndt S et al.: Biomedicines 2021; 9(3): 251 21 Smith OJ et al.: Int Wound J 2019; 16(1): 275-85 22 Choi SY et al.: Dermatol Ther 2017; 30(6) 23 Iio K et al.: Asia Pac J Sports Med Arthrosc Rehabil Technol 2016; 4: 27-32 24 Chen WH et al.: Biomaterials 2014; 35(36): 9599-607 25 Taieb M et al.: J Cosmet Dermatol 2012; 11(2): 87-92 26 Succi IB et al.: Dermatol Surg 2012; 38(2): 192-8 27 Cervelli V et al.: Adv Skin Wound Care 2010; 23(6): 262-72 28 Smith JD et al.: Microvasc Res 2007; 73(2): 84-94 29 Wiest L et al.: J Dtsch Dermatol Ges 2008; 6(3): 176-80 30 Edwards PC et al.: Clin Interv Aging 2007; 2(4): 509-19 31 Anitua E et al.: Rheumatology (Oxford) 2007; 46(12): 1769-72 32 Hersant B et al.: Menopause 2018; 25(10): 1124-30 33 Aguilar P et al.: Springerplus 2016; 5(1): 1184 34 Zendell K et al.: JAMA Dermatol 2013; 149(10): 1199-202 35 Wang Y et al.: Front Pain Res (Lausanne) 2024; 5: 1485113
Das könnte Sie auch interessieren:
Management und neue Therapieoptionen: ein Update
Mosaikwarzen gehören zu den besonders hartnäckigen Warzenformen und sprechen oft nur unzureichend auf Standardtherapien an. Innovative Verfahren wie die Mikrowellentherapie, ...
Der Nutzen und die Limiten der Therapie mit mesenchymalen Stammzellen
Neue Perspektiven in der Transplantationsmedizin, speziell in der «vascularized composite allotransplantation»: Aus Fettgewebe isolierte Stammzellen könnten einen bedeutenden Beitrag zur ...
Die menschliche Haut in der modernen Kunst
Dr. Ralph Ubl, Professor für neuere Kunstgeschichte an der Universität Basel, stellte sich der schwierigen Herausforderung, einem Raum voller erwartungsvoller Dermatologen das Organ Haut ...