Die Haut in der Pubertät
Autorin:
Univ.-Prof. Dr. Doris Maria Gruber
Fachärztin für Gynäkologie & Geburtshilfe, Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Akne im Jugendalter ist eine der nichtkontrazeptiven Indikationen, wegen deren Pille & Co verschrieben werden – und das oft bevor die hormonelle Entwicklung abgeschlossen ist. Aber welche Auswirkungen haben Ovulationshemmer, wenn es noch keine Ovulation gibt, die zu hemmen wäre?
Keypoints
-
Hyperandrogenämie ist ein notwendiges – meist transientes – endokrinologisches Stadium in der Pubertät. Klinisch zeigen sich oft belastende Manifestationen an Haut und Haaren.
-
Die Jahre der Pubertät mit den hormonellen Schwankungen sollten genau beobachtet werden, um echte Pathologien von vorübergehenden hormonellen Anpassungen und Entwicklungsschritten rechtzeitig zu unterscheiden.
-
Starke hyperandrogenämische Manifestationen an der Haut sollten dermatologisch (topisch/systemisch) behandelt werden, um langfristige Narbenbildungen zu verhindern.
-
Hormonelle Ovulationshemmer stellen das weibliche Hormonsystem ruhig, wie ihr Name sagt. Diese „Ruhigstellung“ eines sich in Entwicklung befindlichen Hormonsystems kann in der Pubertät nachteilig für eine gesunde hormonelle Entwicklung sein.
-
Hormonelle Ovulationshemmer können nach individueller Abwägung der Vorteile und der möglichen langfristigen Nachteile zum Einsatz kommen, sobald sich ein ausgereiftes Menstruationsgeschehen etabliert hat.
Weibliche Gesundheit, Wohlbefinden und auch die Schönheit hängen eng mit dem perfekt orchestrierten Zusammenspiel der Hormone zusammen. Dieser Prozess der Orchestrierung beginnt mit der Pubertät, dauert im Durchschnitt 4 bis 6 Jahre und resultiert im fein aufeinander abgestimmten Wirken der beteiligten Organsysteme. Dazu gehören der Hypothalamus, die Hypophyse, die inneren weiblichen Geschlechtsorgane mit Ovarien und Uterus, das Brustgewebe sowie das Fettgewebe. Weiter gefasst könnte man sogar den Eindruck gewinnen, dass der gesamte weibliche Organismus daran beteiligt ist.
Als äußeres Zeichen des Funktionierens des weiblichen Endokriniums tritt eine regelmäßige Menstruationsblutung nach der Ovulation auf. Auch auf der Haut macht sich das „Eintreffen“ der Hormone bemerkbar, leider allerdings oft zum Missfallen der Betroffenen. Dann dominieren jahrelang die männlichen Hormone und diese bewirken Akne, Pustelbildung, vermehrte Talgdrüsenaktivitäten und rasch nachfettendes Haar. Bei ausgeprägter dermaler Manifestation, besonders in der Pubertät, hinterlassen vor allem die Einflüsse der männlichen Hormone oft unschöne Narben auf der Haut.
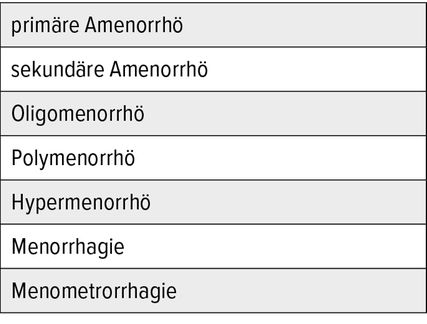
Der medizinische Alltag in der gynäkologischen und vor allem in der dermatologischen Ordination ist geprägt von diesbezüglichen Fragen von Frauen aller Altersgruppen. Meist sind es junge Mädchen in der Pubertät, aber auch perimenopausal häufen sich diese Beschwerdebilder. Vorgebracht werden – mit unterschiedlich großem Leidensdruck – Beschwerden über Akne, Hirsutismus und Effluvium sowie unangenehm stark ausgeprägte Körperbehaarung. Begleitet werden diese Beschwerden sehr häufig von Zyklusstörungen „aller Art“ (Tab. 1).
Mädchen in der Pubertät
Junge Frauen unter 18 Jahren stellen hormonell betrachtet eine sehr inhomogene Gruppe dar. Einige haben schon ein ausgereiftes Hormonsystem – und können somit auch schwanger werden –, andere aber haben dieses Stadium noch lange nicht erreicht. Vereinzelt hatten manche Mädchen mit 16 bis 18 Jahren noch nicht einmal die Menarche. In diesem Fall spricht man von primärer Amenorrhö. Klinisch entscheidend ist, die Anamnese diesbezüglich abzufragen und entsprechende Fragen zu stellen, etwa: Wie weit ist der Menstruationszyklus etabliert? Die Antworten sollten die weiteren diagnostischen und therapeutischen Schritte bestimmen.
Ist das Hormonsystem bei einem jungen Mädchen mit 14 bis 16 Jahren schon bis zum Eisprung entwickelt oder nicht? Wenn es vollständig ausgereift und der Zyklus regelmäßig ist, mit nachgewiesener Ovulation, so besteht selbstverständlich die Möglichkeit, schwanger zu werden. Dementsprechend ist – wenn sexuelle Aktivität angegeben wird – eine Verhütungsmethode angezeigt. Die junge Frau ist fruchtbar und kann mit „Pille & Co“ effizient verhüten. Die Verwendung einer hormonellen Kontrazeption bringt auch mit sich, dass der Zyklus „pillengesteuert“ regelmäßig und verlässlich eintritt, die menstruations-assoziierten Beschwerden meist vollständig behoben werden und Haut und Haare besonders schön imponieren. Diese sogenannten „nichtkontrazeptiven Effekte“ der hormonellen Verhütung werden voll ausgeschöpft. Die Beeinflussung des Körpergewichts durch die hormonelle Wirkung kann aber von Fall zu Fall unterschiedlich ausfallen und wird von den Betroffenen auch meist unterschiedlich wahrgenommen und den Ärzten berichtet.
Was passiert aber mit all jenen Mädchen, die diese hormonelle Entwicklung noch nicht vollständig abgeschlossen haben, bei denen das hormonelle Orchester noch nicht fein aufeinander abgestimmt ist? Bei denen die Menstruationsblutung unregelmäßig eintritt, und bei Eintritt dann womöglich von starken Schmerzen begleitet wird? Was kann man tun, wenn die Hyperandrogenämie der Haut so schwer zusetzt, aber es keinen Hinweis darauf gibt, dass sich der Zyklus parallel dazu reguliert? Diese Fragen sollten akribisch gestellt werden, denn ihre Beantwortung in die eine oder andere Richtung hat zukunftweisende und oft langfristige Folgen für die individuelle Gesundheit. Eine „Therapie“-Antwort zu den oben angeführten Beschwerden kann sofort gegeben werden: Sehr oft wird in diesen Fällen zur „Pille“ geraten. Die detaillierte Antwort mit individuellen Therapieangeboten bedarf allerdings eines genauen Studiums der jeweiligen endokrinologischen Situation.
Was kann die „Pille“?
Im historischen Beipacktext der „Pille“ wurde das Indikationsgebiet auch „temporäres Unfruchtbarmachen“ genannt. Dieser Satz trifft es sehr genau. Es impliziert, dass eine Fruchtbarkeit gegeben sein sollte, die die Frau für eine gewisse Zeitspanne ruhigstellen möchte. Alle hormonellen Verhütungsmittel sind darauf ausgerichtet und unterdrücken die Fruchtbarkeit für die Zeit der Einnahme. Es stellt sich nach Absetzen der hormonellen Methode auch wieder jenes hormonelle „Gleichgewicht“ ein, das vorher gegeben war.
Die zentrale Frage in diesem Zusammenhang ist nun: Was wird mit „Pille & Co“ unterdrückt, wenn bei jungen Mädchen ab 14 Jahren noch kein hormonelles Regelwerk etabliert ist, das „stillgelegt“ werden kann bzw. muss? Diese Frage muss im Sinne der Frauengesundheit gestellt werden. Häufig wird aus nichtkontrazeptiven Indikationen in dieser Altersgruppe ein hormonelles Verhütungsmittel verschrieben, etwa weil die Haut und die zugrunde liegende Hyperandrogenämie zu schaffen machen oder wenn Verhütungsnotwendigkeit besteht. Was wird aber nun gehemmt, wenn es noch keine Ovulation gibt, die vordergründig zu hemmen ist? Wird womöglich all das, was gerade im Entstehen, in Entwicklung, in Ausreifung ist, unterdrückt? Wir wissen dahin gehend leider zu wenig und auch Studien zu diesen entscheidenden Fragen sind rar. Aber: Wir wissen vieles aus der klinischen Praxis.
Ein kurzer Rückblick
Die Pille (= hormoneller Ovulationshemmer) ist seit dem Ersteinsatz im Jahr 1960 aus dem gynäkologischen Alltag nicht mehr wegzudenken. Ihre Entwicklung stellt eine Erfolgsgeschichte für die Gynäkologie dar. Die Datenlage für Studien zur hormonellen Kontrazeption ist bibliotheksfüllend und es gibt scheinbar kaum eine Fragestellung, die nicht untersucht wurde. Man weiß alles über Pille & Co. Aber wirklich alles?
Es gibt Informationslücken in der riesigen „Pillen-Studien-Bibliothek“, und diese Lücken betreffen vor allem Fragestellungen bei jungen Mädchen unter 18 Jahren. Die Mehrheit der Studien mit Ovulationshemmern betrifft ein Alter ab 18 Jahren und umfasst ein großes Kollektiv von jungen, gesunden (meist nicht rauchenden) und normalgewichtigen Frauen. Die Studienergebnisse sind detailliert, vielversprechend und bilden die Wirklichkeit unter idealen Bedingungen ab. Die Daten erfassen alle wichtigen Parameter des weiblichen Zyklus, Fragen zu Dysmenorrhö, Migräne und zur Gewichtszunahme werden diskutiert, ebenso die Auswirkungen auf Haut und Haare. Dass hormonelle Ovulationshemmer aller Art eine Schwangerschaft verhindern, ist selbstverständlich, was in umfangreichen Studienprogrammen sehr gewissenhaft nachgewiesen wurde. Der Pearl-Index ist niedrig. Die Pille wirkt! Demzufolge sieht die Welt für Frauen, die mit Pille & Co verhüten, sehr rosig aus. Es lag und liegt nahe, diese Medikamentengruppe auch unter 18-Jährigen zu verordnen – unter Rückgriff auf die umfassenden Daten –, ohne den guten wissenschaftlichen Gepflogenheiten zu folgen, wonach zuerst Studiendaten zu einem Medikament in einer entsprechenden Altersgruppe vorzuliegen haben, bevor mit der Verordnung begonnen wird.
Pro „Pille & Co“
Hormonelle Ovulationshemmer regulieren den Zyklus, verringern Dysmenorrhö, schwächen die Menstruationsblutung ab und lindern sehr effizient menstruationsassoziierte Beschwerden. Sie stellen die Hormonproduktion bei Endometrioseschmerzen ruhig und beseitigen PMS-Beschwerden. Sie unterdrücken die Androgene und verbessern dadurch die klinischen Auswirkungen der männlichen Hormone auf Haut mit Akne und/oder Seborrhö und Haarausfall. Die Indikationen für Pille & Co bei Zyklusstörung, Dysmenorrhö sowie Akne mit Hyperandrogenämie betreffen sehr häufig junge Frauen, weshalb ihr Einsatz auch rasch erfolgt. Zumal auch die sexuelle Aktivität – unabhängig davon, ob schon die volle Fruchtbarkeit eingesetzt hat – in der Pubertät zügig aufgenommen wird. Selbst dann, wenn sich die Frage nach Verhütung (noch) gar nicht stellt, wird aus den oben genannten Beschwerden und somit aus „therapeutischen Gründen“ zu Ovulationshemmern gegriffen. Man schöpft in vollem Umfang die benefiziellen nichtkontrazeptiven Effekte der hormonellen Kontrazeptiva aus.
Ovulationshemmer und Ovar
Die klinische Empirie aus den letzten Jahrzehnten legt die Vermutung nahe, dass die frühzeitige (pubertäre) Unterdrückung der Eierstockaktivität mithilfe von hormonellen Ovulationshemmern aller Art eine der Ursachen für das gehäufte Auftreten verschiedener Varianten des polyzystischen Ovar-Syndroms (PCOS) ist. So verständlich der Wunsch eines pubertierenden Mädchens nach einem schönen, ebenmäßigen Hautbild ist, so schlecht sind die Auswirkungen der Unterdrückung der männlichen Hormone (und in weiterer Folge der weiblichen) zu diesem Zeitpunkt für die Etablierung der hormonellen Achsen zwischen Hypothalamus, Hypophyse, Eierstock, Gebärmutter und Fettgewebe. Je nachdem, wo die hormonelle Entwicklung bei der jungen Frau gerade angekommen“ ist und durch die Gabe eines Ovulationshemmers (sic)unterbrochen wird, ergeben sich das eine oder andere – klinisch sehr vielschichtige – Bild des PCOS und vielleicht noch viele weitere feinste individuelle endokrin-pathologische Schattierungen.
Der Eierstock macht in der Pubertät physiologisch ein multifollikuläres Stadium durch – anders schafft er den Übergang aus der kindlichen Ruhephase in die Fertilität nicht. So unerfreulich die Auswirkung der männlichen Hormone für das Hautbild des jungen Mädchens sind, so wichtig ist deren Wirkung am Eierstock. Deshalb ist ihre Unterdrückung in diesem Zeitraum langfristig umso nachteiliger. Nicht nur dass der Eierstock in seiner Aktivität gestört wird, auch die Gebärmutter wird im Wachstum behindert, wenn Hormone zur Blockierung der Eierstockaktivität verabreicht werden. Auf Englisch würde man sagen: Es kommt zum „freezing“ oder es entsteht ein „screenshot“ (Ultraschall!), wenn Ovulationshemmer angewendet werden. Die Eierstöcke (und auch der Uterus) verharren bei hormoneller Ruhigstellung in dem Zustand, in dem sie gerade sind. Meist ist es eben das polyzystische bzw. multifollikuläre Stadium mitten in der Pubertät. Sie verbleiben dort so lange, bis die hormonelle Unterdrückung wieder wegfällt, und setzen dann ihre Aktivität fort ... oder auch nicht!
Wir kennen das klinische Phänomen der Post-Pillen-Amenorrhö sehr genau. Diese dauert oft desto länger, je früher mit der Pille begonnen und je länger sie eingenommen worden ist. Es kommt unter der Pilleneinnahme gewollt zur Unterdrückung eines funktionsfähigen Endometriums. Darauf folgt die sogenannte Entzugsblutung.
Fällt die Ruhigstellung durch das Absetzen der Pille nach Jahren weg, so fällt es den inneren Geschlechtsorganen oft schwer, von selbst wieder aktiv zu werden. Myometrium und Endometrium haben in der Zeit der Ruhigstellung pseudoatrophisiert und an Volumen deutlich verloren. Das Warten auf die Menstruationsblutung kann in dieser Situation länger dauern.
Hormonelle Kontrazeptiva haben einen Einfluss auf die übergeordneten Steuerungszentralen im Gehirn (Hypothalamus und Hypophyse) und auf die „Erfolgsorgane“ in der Peripherie. Aus der Wirkungsweise auf diesen beiden Ebenen sind sowohl die therapeutischen Erfolge (in erster Linie die kontrazeptive Wirkung) als auch die Nebenwirkungen und Langzeitfolgewirkungen zu erklären.
Hyperandrogenämie und klinische Bedeutung
Dass es in der Pubertät zu einer Ausschüttung an männlichen Hormonen kommt, ist für die meisten Pubertierenden stark registrierbar. Dieser metabolische Prozess ist aber unabdingbar, denn ohne Aktivierung der männlichen Steroidhormone aus Ovar und Nebennierenrinde ist eine hormonell geordnete Pubertät nicht möglich. Durch den Impuls aus dem Hyperthalamus werden zuerst GnRH und in weiterer Folge LH und FSH ausgeschüttet, welche direkt die Androgenproduktion in Gang setzen.1 Erst wenn die Androgene einen gewissen Schwellenwert erreicht haben, schaltet der Körper auf die Östrogenproduktion um.
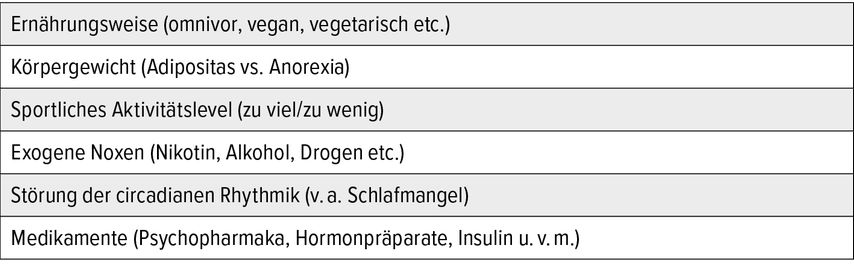
Klinisch macht sich das im Sistieren der dermatologischen Problematik bemerkbar und an der Stabilisierung des Menstruationszyklus. Das Ausbilden der komplexen Feedback-Schleifen zwischen Hypothalamus/Hypophyse und dem metabolischen Interagieren der Hormone mit ihren Erfolgsorganen nimmt Zeit in Anspruch und macht das System störanfällig. Faktoren, die diese Entwicklung exogen beeinflussen können, sind unter anderem Ernährung und Essgewohnheiten, sportliche Aktivität, aber auch Inaktivität, manche Medikamente und Noxen (Tab. 2).
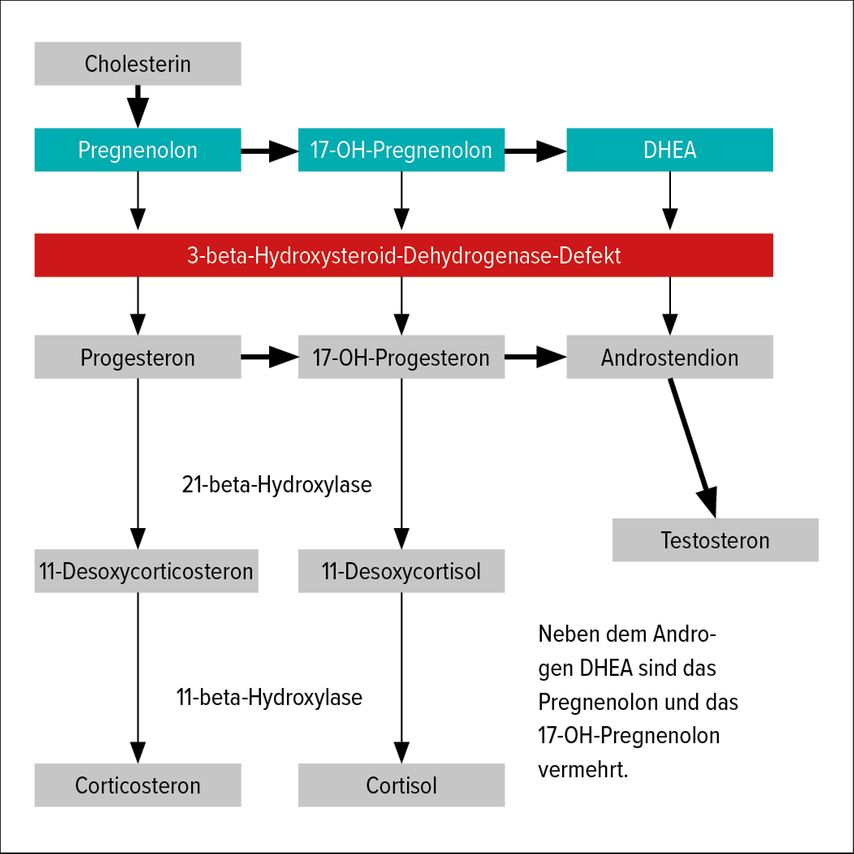
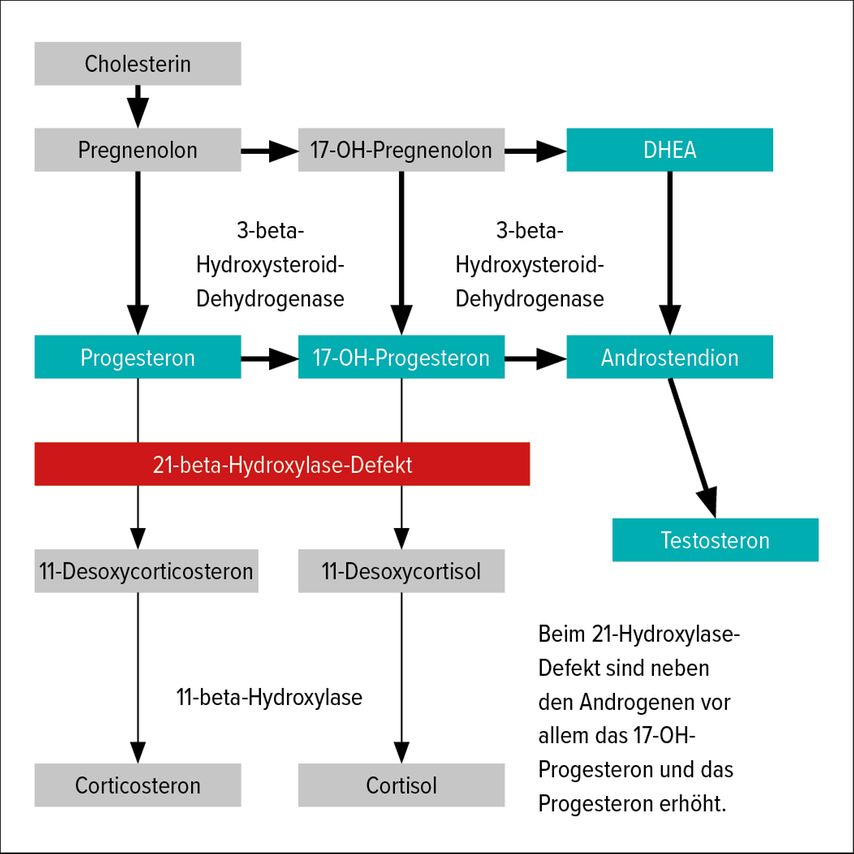
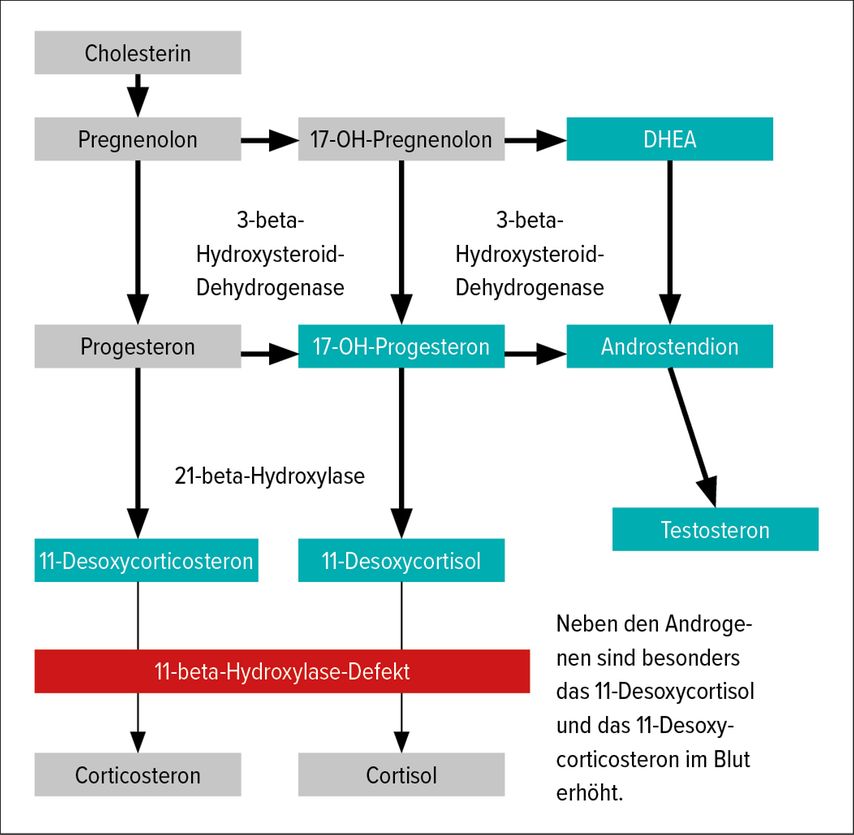
Die metabolischen Prozesse in Nebennierenrinde und Ovar sind äußerst komplex, sodass bis jetzt leider noch immer nicht alles bin ins kleinste Detail verstanden wird. Derzeit sind 3 wichtige (aber selten vorkommende) Enzymdefekte gut bekannt, die in einer Vermehrung der Androgene resultieren und klinisch relevante Auswirkungen haben (Abb. 1–3). Die Betroffenen leiden unter Akne, Hirsutismus, Gewichtsproblemen sowie Tempoanomalien und im unterschiedlichen Graden an Fertilitätsproblemen. Kausale Therapien sind bei diesen Enzymdefekten derzeit nicht bekannt. Symptomatisch wird je nach Erscheinungsbild mit Hormongaben, aber auch Antihormongaben, systemisch oder lokal, gearbeitet. Differenzialdiagnostisch sollte bei dem klinischen Bild einer Hyperandrogenämie an das Vorliegen eines anderen NNR-Prozesses gedacht werden (Cushing-Syndrom), an eine echte Hypertrichose, an das adrenogenitale Syndrom (auch „late onset“; siehe Abb. 1), an Diabetes mellitus, Galaktorrhö oder Akromegalie.
Wenn man nach den Ursachen für diese Veränderungen forscht, so ist weder die derzeit vorhandene Literatur ergiebig noch sind die bekannten Lehrbücher sehr aussagekräftig. Vereinzelt findet man diskrete Hinweise darauf, dass die beschriebenen individuellen Probleme epigenetischen Ursprungs sein könnten. Es gibt eine höchst interessante Publikation, die als eine der Ursachen für endokrine Funktionsstörungen mütterlichen Stress (in vielfachen Ausprägungen) auf das Ungeborene vermutet. Es scheint die übermäßige Cortisolproduktion der Mutter einen Einfluss auf die zukünftige Steroid- und Enzymkonstellation des Nachwuchses zu haben.2 Zumindest legen das Forschungsergebnisse im Mausmodell nahe. Wenn man bedenkt, welch vielfältigen und oft belastenden Lebenssituation manche Schwangere ausgesetzt ist, könnte dieser Mechanismus durchaus auch auf das Säugetier Mensch übertragen werden. Zumal eine Schwangerschaft ja wesentlich länger dauert als bei Mäusen. Somit ist auch der Zeitraum viel größer, in dem diese enzymatischen/metabolischen Veränderungen – getriggert über den mütterlichen Stress und die Placenta – bis zu embryonaler Nebennierenrinde und Ovar stattfinden können.
Therapiemöglichkeiten bei Hyperandrogenämie
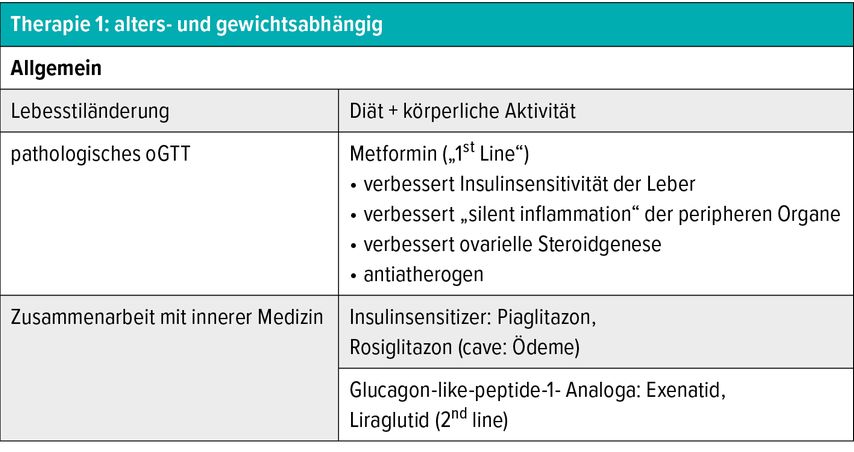
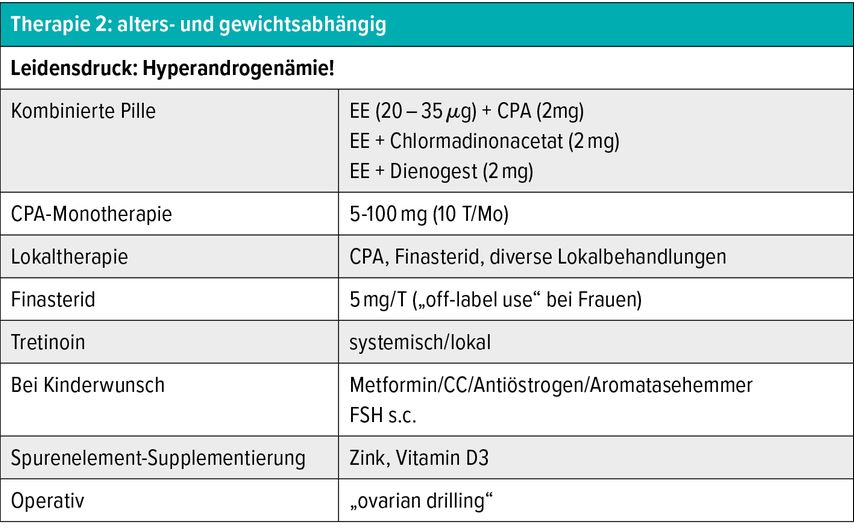
Nicht nur die klinischen Auswirkungen der vermehrten Androgenproduktion auf Haut und Haare sollten therapiert werden. Langfristig ist es auch notwendig, die negativen Folgen für das Gefäßsystem und den Glukosestoffwechsel so lange wie möglich zu verhindern.3 Außerdem bewirkt diese endokrine hyperandrogenämische Belastung für alle Gewebe eine chronische Inflammation, die langfristig negative Auswirkungen für den gesamten Organismus hat.4 Für die Linderung der dermatologischen Manifestation in der Pubertät sollten systemisch-hormonelle Therapien mit Zurückhaltung angeboten werden. Hingegen können die Antibiotikagabe und die Behandlung der Akne mittels Ciscutan® (Isotretinoin) sowie die lokalen Therapien ausgeschöpft werden. Die Behandlungskonzepte sollten alters- und gewichtsabhängig gestaltet werden und gemäß dem Sistieren oder dem Fortschreiten der Symptomatik alle 3 Monate evaluiert und gegebenenfalls angepasst werden (Tab. 3 und 4).
Zusammenfassung
Das klinische Bild der Hyperandrogenämie in der Pubertät sollte genauer unter die endokrinologische Lupe genommen werden, denn es können sich komplexe Störungen der hormonellen Verschaltung dahinter verbergen. Meist ist es ein „unangenehmes“ Übergangsstadium, das einerseits hormonell gesehen notwendig ist, andererseits auch klinisch sehr störend ist. Eine alleinige symptomatische Therapie der initial vorwiegend dermatologischen Manifestationen der Hyperandrogenämie bewirkt zwar die Linderung der Symptomatik, aber resultiert meist in keiner kausalen Behebung des Problems. Mit Geduld „wächst“ sich das klinische Bild meist immer aus und sistiert nach einer gewissen Zeitspanne vollständig. Die Gabe von hormonellen Ovulationshemmern, um die gesamte ovarielle Aktivität zu diesem Zeitpunkt zu unterdrücken, soll individuell und mit Augenmaß abgewogen werden, denn sie kann nachhaltige Folgen für die Gesundheit – vor allem für die Fertilität – haben. Um metabolisch-endokrinologische Langzeitfolgen bestmöglich zu verhindern, müssen frühzeitig die Stoffwechsellage und auch die hormonelle Situation untersucht sowie alters- und gewichtsbezogen interdisziplinär behandelt werden.
Literatur:
1 Delemarre EM et al.: Inducing puberty. Eur J Endocrinol 2008; 159: Suppl 1: 9-15 2 Barra R et al.: Maternal sympathetic stress impairs follicular development and puberty of the offspring. Reproduction 2014; 148(2): 137-45 3 Daghestani MH et al.: Adverse effects of selected markers on the metabolic and endocrine profiles of obese women with and without PCOS. Front Endocrinol (Lausanne). 2021; 12: 665446 4 Rostamtabar M et al.: Pathophysiological roles of chronic low-grade inflammation mediators in polycystic ovary syndrome. J Cell Physiol 2021; 236(2): 824-38
Das könnte Sie auch interessieren:
Rolle der Prophylaxe bei der Therapie des hereditären Angioödems
Im Management des hereditären Angioödems (HAE) ist eine kontinuierliche präventive Therapie unerlässlich, um zukünftige Schübe zu verhindern und die Erkrankung besser zu managen: die ...
Wege zur korrekten Diagnose
Patientinnen und Patienten mit verhärteter Haut können an sehr unterschiedlichen Erkrankungen leiden. Im Zentrum steht immer ein Fibroblast, eine mesenchymale Vorläuferzelle, die durch ...
Die menschliche Haut in der modernen Kunst
Dr. Ralph Ubl, Professor für neuere Kunstgeschichte an der Universität Basel, stellte sich der schwierigen Herausforderung, einem Raum voller erwartungsvoller Dermatologen das Organ Haut ...