Un diagnostic ciblé, un meilleur traitement: l’anamnèse approfondie comme base
Compte-rendu: Dre méd. Felicitas Witte
Contrôle professionnel:
Pr Dr méd. Peter Schmid-Grendelmeier
Senior Consultant Dermatologie/Allergologie
Hochgebirgsklinik Davos
Zuger Kantonsspital
Universitätsspital Zürich
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Que conseille-t-on aux parents de nouveau-né·es pour prévenir la dermatite atopique (DA) chez leur bébé? Quand un diagnostic allergologique basé sur les composants est-il pertinent? Comment une anamnèse approfondie permet-elle d’orienter vers un traitement ciblé? Le Pr Dr méd. Peter Schmid-Grendelmeier, de Zurich, a présenté un aperçu actualisé des facteurs de risque et de déclenchement de la DA, de la prévention primaire et du diagnostic ciblé lors des Journées zurichoises de formation continue en dermatologie.
Keypoints
-
Les tests diagnostiques modernes permettent de déterminer plus précisément la forme de la DA et les éventuels symptômes associés, et d’adapter le traitement en conséquence.
-
Dans les cas sévères, la DA peut être liée à une réaction auto-immune, avec des anticorps IgE dirigés contre des antigènes cutanés ou non cutanés.
-
Les soins de la peau sont essentiels, mais des soins excessifs peuvent également s’avérer nocifs.
-
La longue liste de comorbidités montre que la DA peut être une maladie systémique aux conséquences parfois importantes.
La dermatite atopique (DA) est un thème central dans tout cabinet de dermatologie et dans tout service d’allergologie. En 2023, la directive allemande de l’AWMF a été mise à jour et s’applique également en Suisse. Toutefois, dans la pratique quotidienne, il reste souvent peu de temps pour parcourir ces informations détaillées et se tenir au courant des nouveautés. Lors des Journées zurichoises de formation continue en dermatologie, le Pr Dr méd. Peter Schmid-Grendelmeier a proposé un aperçu complet de la prévention et du diagnostic de la DA. Ce dermatologue et allergologue a dirigé pendant 21 ans l’unité d’allergologie du service de dermatologie de l’Hôpital universitaire de Zurich et mène depuis des décennies des recherches intensives sur la DA.
Éviter les soins cutanés excessifs
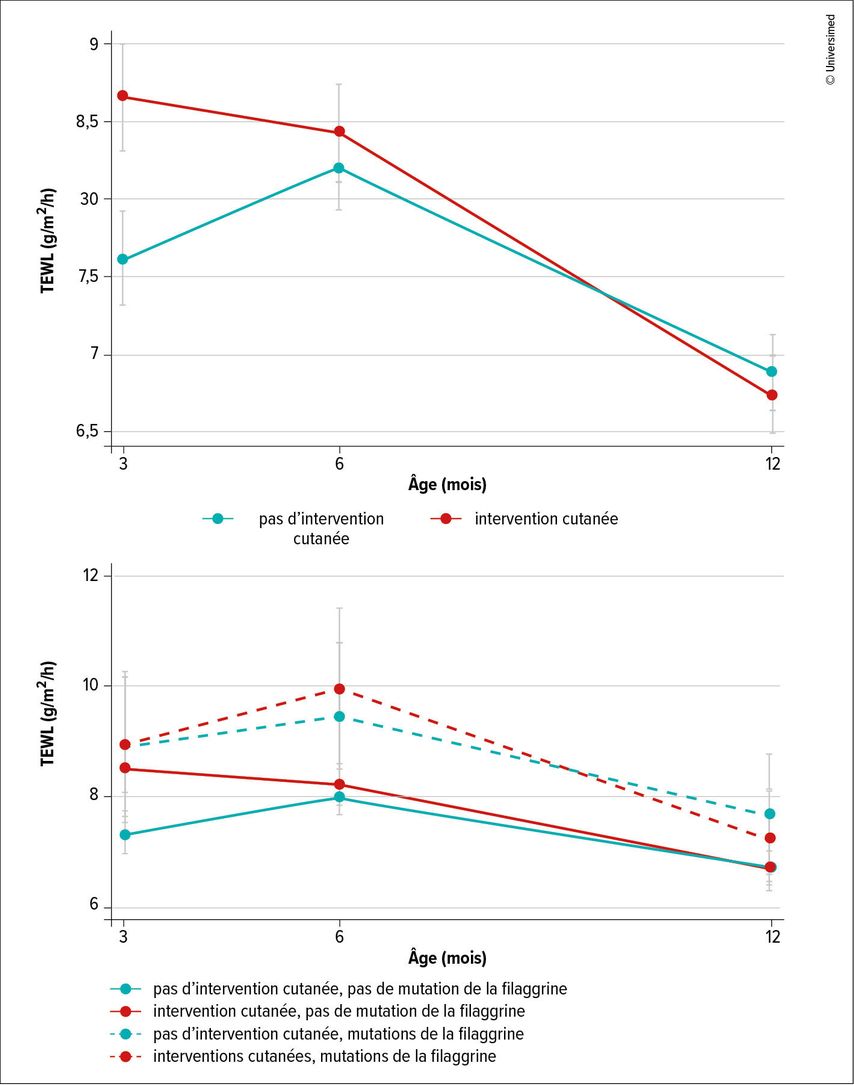
La prévention primaire de la DA est un sujet de plus en plus abordé dans la littérature spécialisée ces dernières années. «Il est important de transmettre le message suivant: les soins de la peau sont absolument essentiels», a déclaré le Dr P. Schmid-Grendelmeier. «Mais des soins cutanés excessifs, plusieurs fois par jour, peuvent non seulement être inutiles, mais aussi potentiellement délétères.» Dans l’étude PreventADALL1 portant sur 2153 nourrissons, des bains d’huile répétés plusieurs fois par semaine ont entraîné une altération de la barrière cutanée, principalement en raison d’une perte hydrique accrue par la peau au cours des trois premiers mois. Les enfants présentant des mutations de la filaggrine étaient particulièrement concerné·es (Fig.1,2). La protéine filaggrine joue un rôle clé dans la formation et le fonctionnement de la barrière cutanée. En cas de mutation du gène de la filaggrine avec «loss of function», la barrière cutanée est altérée et le risque de DA augmente. Entre 20% et 50% des patient·es atteint·es de DA présentent au moins une mutation du gène de la filaggrine, contre environ 10% de la population générale.2 Une application excessive de crème peut également avoir des effets négatifs: dans l’étude BEEP,3 1394 nouveau-né·es à haut risque de DA ont été enduit·es quotidiennement de crème, ou non. L’application de crème n’a pas protégé contre l’eczéma, et les enfants enduit·es de crème présentaient même un risque accru d’infections cutanées et possiblement d’allergies alimentaires. Il est possible que l’application de crème perturbe mécaniquement la barrière cutanée et que les bains d’huile modifient la composition lipidique, entraînant une perte hydrique accrue et un dessèchement cutané. Ces dernières années, il est apparu qu’il existe quatre endotypes et phénotypes distincts de la DA, différenciables notamment par la concentration de certains biomarqueurs, tels que des interleukines, cytokines et leucocytes TH2.4Jusqu’à présent, nous utilisons surtout ces types dans le cadre de la recherche», a déclaré le Dr P. Schmid-Grendelmeier. «Mais j’espère qu’ils nous permettront bientôt d’adapter plus finement les traitements et, par exemple, de réserver les nouveaux biomédicaments aux patient·es dont le profil de biomarqueurs prédit une réponse favorable.»
Fig.1 et 2: Perte d’eau transépidermique (TEWL) en g/m2/h (IC à 95%) chez 1683 nourrissons avec et sans mutations dans le gène de la filaggrine, avec et sans intervention cutanée (bains d’huile) (modifiées selon Rehbinder EM et al. 2024)1
Diagnostic allergologique basé sur les composants
Le diagnostic repose toujours en premier lieu sur l’examen clinique. Cependant, les tests modernes permettent aujourd’hui de caractériser plus précisément la forme de la DA et les éventuels symptômes associés, et d’adapter le traitement en conséquence. Selon les études, une sensibilisation IgE-médiée aux aéroallergènes et/ou aux allergènes alimentaires est détectable chez 50 à 80% des patient·es atteint·es de DA.5,6 Certains phénotypes sont associés à des allergènes spécifiques. Par exemple, chez les patient·es atteint·es de DA avec érythrodermie, on observe plus fréquemment des taux élevés d’anticorps IgE dirigés contre la caséine du lait de vache (Bos d 8).7 Ces nourrissons présentent un risque élevé de réaction allergique au lait de vache et de persistance d’une éventuelle allergie.8–12 «Si un enfant présentant une sensibilisation marquée à la caséine réagit effectivement de manière allergique au lait de vache, il doit éviter le lait et disposer en permanence d’un kit d’urgence», a précisé le Dr P. Schmid-Grendelmeier. «Le·la pédiatre expérimenté·e en allergologie contrôlera alors régulièrement les taux d’IgE dirigés contre la caséine (Bos d 8) au cours des années suivantes, car une tolérance spontanée peut se développer et permettre une réintroduction du lait.» La directive allemande AWMF5 recommande un diagnostic allergologique ciblé avec prick-tests et/ou dosage des IgE lorsque l’anamnèse de l’enfant ou ses symptômes suggèrent une allergie. «La pertinence clinique d’un taux élevé d’IgE doit ensuite être évaluée plus en détail», a ajouté le Dr P. Schmid-Grendelmeier. «Notamment en évitant les allergènes concernés pendant 4 à 6 semaines – lorsque cela est possible – et en observant si les symptômes disparaissent.» Une autre option consiste à réaliser un test de provocation sous surveillance médicale. Une élévation isolée des IgE sans corrélation clinique ne justifie toutefois pas une éviction de l’allergène, selon le Dr P. Schmid-Grendelmeier.
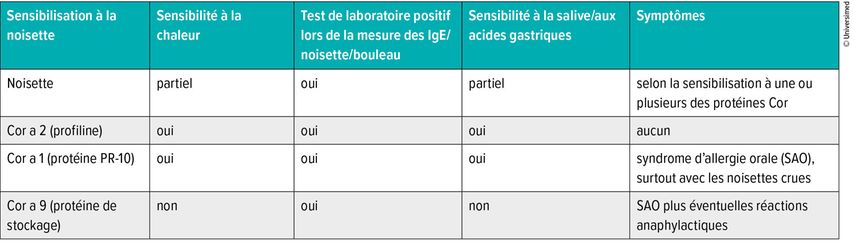
Mieux conseiller les patient·es grâce aux tests sur puce
Les kits de test sur puce modernes tels qu’ImmunoCAP ISAC® ou Alex® Allergy Explorer permettent de déterminer, en un seul test, les anticorpsIgE dirigés contre 113 ou 282 allergènes. «Sur la base du profil allergénique, nous pouvons estimer le phénotype clinique et la gravité potentielle, et adapter le traitement», a déclaré le Dr P. Schmid-Grendelmeier. Lors d’un entretien, ce dernier a illustré la pertinence pratique de ces tests en prenant l’exemple de la noisette (Tab.1). Si un·e patient·e est sensibilisé·e à la protéine profiline, appelée Cor a 2 dans la noisette, des anticorps IgE peuvent être détectés pour toutes les sources d’allergènes contenant de la profiline. Cela concerne pratiquement tous les pollens. Le·la patient·e ne présente toutefois pas de symptômes lors de d’inhalation de ces pollens. La situation est différente pour l’allergène principal du pollen de bouleau, appelé Bet v 1. Celui-ci se retrouve également sous forme homologue dans les fruits à noyau et à pépins; ils appartiennent tous à la famille des protéines PR-10. Le·la patient·e ne développe pas seulement une rhinite en présence de pollen de bouleau, mais peut également ressentir des picotements dans la bouche en raison de réactions croisées lorsqu’il·elle consomme certains aliments contenant des homologues de Bet v 1, comme la noisette (Cor a 1), la pomme, la pêche, le céleri ou la carotte. Ces allergènes sont toutefois thermolabiles. «C’est pourquoi les symptômes surviennent généralement uniquement lors de la consommation de noisettes crues ou d’aliments crus», a expliqué le Dr P. Schmid-Grendelmeier. La salive et le suc gastrique dénaturent les protéines, de sorte que les symptômes restent limités à la cavité buccale (symptôme d’allergie orale), sans réaction allergique systémique. En revanche, si un·e patient·e est sensibilisé·e à des protéines résistantes à la chaleur et aux sucs gastriques – dans le cas de la noisette, des protéines de stockage telles que Cor a 9 ou Cor a 14 – cela peut entraîner, en plus d’un syndrome d’allergie orale plus sévère, une anaphylaxie avec urticaire, des crises d’asthme, voire un choc allergique. «Ces protéines arrivent presque intactes dans l’intestin et y sont absorbées dans le sang.» Le diagnostic allergologique moléculaire permet d’identifier les patient·es présentant des réactions croisées associées au pollen, par exemple une réactivité à l’allergène Bet v 1 du pollen de bouleau ainsi qu’à Mal d 1 dans la pomme et Cor a 1 dans la noisette.6 «Cela nous aide à mieux conseiller les patient·es, par exemple en expliquant qu’une personne allergique au pollen de bouleau tolère nettement mieux les pommes cuites que crues.» Le diagnostic ciblé a toutefois un coût: les tests multi-puces s’élèvent à environ 340 et 350 francs par puce.
Tab.1: Exemple de sensibilisation à la noisette: une détermination ciblée des anticorps IgE contre les allergènes permet d’identifier si des aliments doivent être évités, et lesquels (d’après le Dr P. Schmid-Grendelmeier)
La DA comme réaction auto-immune
Dans les cas sévères, la DA peut être liée à une réaction auto-immune, avec des anticorps IgE dirigés contre des antigènes cutanés ou non cutanés. Le·la patient·e se sensibilise via des allergènes environnementaux tels que la cyclophiline (CYP) ou la manganèse superoxyde dismutase (MnSOD), et les anticorps IgE produits se dirigent ensuite contre des antigènes de l’organisme présentant des similitudes avec la CYP ou la MnSOD. Il existe encore divers autres allergènes environnementaux homologues à des protéines humaines. À ce jour, les recommandations ne préconisent pas encore la détermination systématique des anticorpsIgE dirigés contre ces antigènes, mais cela pourrait s’avérer pertinent. Le groupe de recherche du Pr Dr méd. Paolo Matricardi, de la Charité de Berlin, et spécialiste du diagnostic moléculaire des maladies allergiques, a développé dans une étude7 portant sur 3325 patient·es allergiques – dont 577 atteint·es de DA – un indice IgE basé sur la réactivité à cinq groupes d’allergènes exogènes homologues à l’humain: arginine kinases, énolases (ENO), CYP, lipocaline et MnSOD. Cet indice était positif chez 10,7% des patient·es allergiques sans DA. Chez les patient·es atteint·es de DA, l’indice fournissait une indication du degré de sévérité: il était positif chez 20% des patient·es en rémission, 39% de ceux·celles présentant une DA modérée et 54% des patient·es avec une DA sévère. «Cela suggère que les auto-anticorps IgE contribuent à la DA chez ces patient·es», a déclaré le Dr P. Schmid-Grendelmeier. Les IgE pourraient également permettre de prédire la réponse au traitement par dupilumab: les patient·es atteint·es de DA présentant des IgE dirigés contre ENO répondaient moins bien, tandis que ceux·celles ayant des IgE contre MnSOD et NPC-2 – une protéine intracellulaire de transport du cholestérol – présentaient une meilleure réponse.
Longue liste de comorbidités
Un autre élément clé du diagnostic consiste à interroger le·la patient·e sur les facteurs déclenchant les poussées de DA. Il existe par exemple des indications selon lesquelles des températures très élevées ou très basses, une faible humidité de l’air, les rayonnements UVB ou un chauffage accru dans la maison en hiver peuvent aggraver la maladie cutanée.13 Lorsque ces facteurs altèrent la barrière cutanée, les allergènes ou irritants peuvent pénétrer plus facilement dans la peau et déclencher une dermatite de contact.14 Il convient également de consacrer suffisamment de temps à la recherche d’éventuelles comorbidités, a souligne le Dr P. Schmid-Grendelmeier. «Parfois, ce n’est pas tant l’eczéma lui-même qui limite les patient·es, mais les maladies associées.» On parlait autrefois de «marche allergique», c’est-à-dire d’une succession typique de symptômes apparaissant dans un ordre caractéristique:15 d’abord des croûtes de lait chez le nourrisson, puis une dermatite atopique, suivie d’une allergie alimentaire et, plus tard, d’une rhinite allergique et d’un asthme allergique. Ce concept est toutefois de plus en plus remis en question, car cet séquence classique n’est observée que chez environ 7% des patient·es.16 Certain·es auteur·es proposent donc plutôt de parler de «cluster atopique».15
La liste des comorbidités est longue: outre l’asthme, la rhinite et les allergies alimentaires, les patient·es atteint·es de DA présentent plus fréquemment des infections virales, bactériennes ou fongiques, pouvant évoluer vers des complications graves telles que la septicémie ou l’endocardite. On observe également des troubles du sommeil ainsi que des maladies psychiatriques telles que la dépression, les troubles anxieux, le syndrome de déficit de l’attention/hyperactivité et les troubles du spectre de l’autisme.17 «Le large éventail de comorbidités montre que la DA peut être une maladie systémique aux conséquences parfois importantes», souligne le Dr P. Schmid-Grendelmeier. Jusqu’à présent, des études contradictoires ont évalué si la DA était également associée à un risque accru de maladies cardiovasculaires. Une équipe de chercheurs de Zurich, Davos et Augsbourg, à laquelle participait également le Dr P. Schmid-Grendelmeier, a récemment montré, dans une étude portant sur 677 patient·es atteint·es de DA et 79 patient·es témoins, que ce lien est plus complexe qu’on ne le pensait.18 Dans l’ensemble, aucune corrélation n’a été observée entre la DA et les maladies cardiovasculaires. Cependant, chez les patient·es atteint·es de DA sans comorbidités atopiques, une activité accrue de la maladie était associée à un risque plus élevé de maladies cardiovasculaires (Fig.3). «La sévérité de la DA semble influencer la probabilité de lésions cardiovasculaires, mais uniquement chez les patient·es atteint·es de DA «pure», c’est-à-dire sans comorbidités atopiques», conclut le Dr P. Schmid-Grendelmeier. L’équipe cherche actuellement à élucider les mécanismes sous-jacents. «Cela semble être lié à une augmentation de certaines cytokines.» Les conséquences pour la pratique ne sont pas encore claires. «Il est possible que nous devions dépister plus systématiquement les complications cardiovasculaires chez les patient·es atteint·es de DA pure.»
Fig.3: Dermatite atopique (DA) et risque accru de maladies cardiovasculaires. La sévérité de la DA semble influencer la probabilité de lésions cardiovasculaires, mais uniquement chez les patient·es atteint·es de DA sans comorbidités atopiques (modifiée selon Fehr D et al. 2025)18
Une autre comorbidité probablement encore sous-estimée est l’ostéoporose. Selon une méta-analyse de 2021 portant sur dix études totalisant plus de trois millions de participant·es, la DA est associée à un risque accru de diminution de la densité osseuse, d’ostéopénie, d’ostéoporose et de fractures associées.19 Ce lien est également clairement observé chez les enfants.20 «Il est possible que cela soit lié à la corticothérapie», a indiqué le Dr P. Schmid-Grendelmeier. Un traitement par médicaments biologiques pourrait avoir un effet positif sur l’os. Dans une étude21 publiée jusqu’à présent uniquement sous forme de résumé dans un numéro spécial du British Journal of Dermatology, les enfants atteint·es de DA traité·es par dupilumab présentaient des taux sériques plus élevés de phosphatase alcaline osseuse (BALP) que ceux·celles sous placebo. L’étude incluait 245 enfants âgé·es de 6 à 11 ans, dont 203 sans corticothérapie systémique préalable et 42 avec. L’effet du dupilumab était indépendant d’une prise préalable de glucocorticoïdes. «Le fait que le dupilumab augmente la BALP est compréhensible, car il permet généralement de réduire l’utilisation de stéroïdes, en particulier en administration systémique», a déclaré le Dr P. Schmid-Grendelmeier. «Mais cela n’avait encore jamais été démontré aussi clairement.» Des études supplémentaires sont nécessaires pour déterminer les implications thérapeutiques. «Il faut d’abord démontrer que l’augmentation des taux de BALP se traduit effectivement par une réduction du risque de fracture.»
Source:
Journées zurichoises de formation continue en dermatologie, conférence du Pr Dr méd. Peter Schmid-Grendelmeier, 21 juin 2025
Littérature:
1 Rehbinder EM et al.: Frequent oil baths and skin barrier during infancy in the PreventADALL study. Br J Dermatol 2024; 191(1): 49-57 2 Thyssen JP et al.: Evidence that loss-of-function filaggrin gene mutations evolved in Northern Europeans to favor intracutaneous vitamin D3 production. Evol Biol 2014; 41(3): 388-96 3 Bradshaw LE et al.: Emollient application from birth to prevent eczema in high-risk children: the BEEP RCT. Health Technol Assess 2024; 28(29): 1-1164 Bakker D et al.: Biomarkers in atopic dermatitis. J Allergy Clin Immunol 2023; 151(5): 1163-8 5 Werfel T et al.: S3 guideline atopic dermatitis: part 1 - general aspects, topical and non-drug therapies, special patient groups. J Dtsch Dermatol Ges 2024; 22(1): 137-53 6 Tokura Y, Hayano S: Subtypes of atopic dermatitis: from phenotype to endotype. Allergol Int 2022; 71(1): 14-24 7 Scala E et al.: A microarray-based IgE-molecular mimicry index (IgE-MMI): a biomarker for disease severity, clinical phenotypes, and therapeutic response in atopic dermatitis? Allergy 2024; 79(12): 3415-29 8 Matricardi PM et al.: The „allergic nose as a pollen detector“ concept: e-Diaries to predict pollen trends. Pediatr Allergy Immunol 2023; 34(6): e13966 9 Caubet JC et al.: Utility of casein-specific IgE levels in predicting reactivity to baked milk. J Allergy Clin Immunol 2013; 131(1): 222-4 10 Ito K et al.: The usefulness of casein-specific IgE and IgG4 antibodies in cow’s milk allergic children. Clin Mol Allergy 2012; 10(1): 1 11 Bartuzi Z et al.: Contribution of molecular allergen analysis in diagnosis of milk allergy. Curr Allergy Asthma Rep 2017; 17(7): 46 12 Kleine-Tebbe J, Jakob T: Molecular allergy diagnostics. Innovation for a better patient management. Springer 2017; 12(3): 291-304 13 Wang SP et al.: Impact of climate change on atopic dermatitis: a review by the international eczema council. Allergy 2024; 79(6): 1455-69 14 Engebretsen KA et al.: The effect of environmental humidity and temperature on skin barrier function and dermatitis. J Eur Acad Dermatol Venereol 2016; 30(2): 223-49 15 Belgrave DCM et al.: Developmental profiles of eczema, wheeze, and rhinitis: two population-based birth cohort studies. PLoS Med 2014; 11(10): e1001748 16 Paller AS et al.: The atopic march and atopic multimorbidity: many trajectories, many pathways. J Allergy Clin Immunol 2019; 143(1): 46-55 17 Brunner PM et al.: Increasing comorbidities suggest that atopic dermatitis is a systemic disorder. J Invest Dermatol 2017; 137(1): 18-25 18 Fehr D et al.: Deciphering the connection between atopic dermatitis and cardiovascular diseases: analysis of clinical associations and cardiometabolic proteins. Allergy 2025; 80(8): 2187-200 19 Wu D et al.: Bone mineral density, osteopenia, osteoporosis, and fracture risk in patients with atopic dermatitis: a systematic review and meta-analysis. Ann Transl Med 2021; 9(1): 40 20 Lee SW et al.: Fracture incidence in children after developing atopic dermatitis: a Korean nationwide birth cohort study. Allergy 2023; 78(3): 871-5 21 Irvine AD et al.: 676 - Dupilumab increases levels of bone growth biomarker irrespective of prior use of systemic corticosteroids in children with moderate-to-severe atopic dermatitis. Br J Dermatol 2024; 191(Supple_2): ljae266.050
Das könnte Sie auch interessieren:
Comorbidités de la dermatite atopique
La dermatite atopique (DA) est souvent associée à des comorbidités atopiques et non atopiques. L’apparition ou le risque de maladies concomitantes peut influencer la prise en charge des ...
Thérapie biologique: pipeline et clinique
Les médicaments biologiques offrent la possibilité d’intervenir de manière ciblée dans les processus immunitaires à l’origine de la dermatite atopique. Cette voie a d’abord été empruntée ...
Aspects centraux de la dermatite atopique
Au-delà du traitement médicamenteux, la prise en compte des facteurs environnementaux, l’assurance de l’adhérence et l’adaptation du traitement aux comorbidités ou aux changements de ...
%20et%20risque%20accru%20de%20maladies%20cardiovasculaires..jpg)