Rémission du VIH, transmission périnatale et nouvelle approche thérapeutique chez l’enfant
Compte-rendu:
Mag. Birgit Leichsenring
Journaliste scientifique
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
La Conference on Retroviruses and Opportunistic Infections (CROI) est considérée comme le point culminant annuel de la recherche sur le VIH. Bien que la CRIO ait été tenue en ligne pour la troisième fois, elle n’a rien perdu de son ambiance particulière.
Le cas présenté d’une autre rémission du VIH peut être considéré comme le point fort médiatique.1 Une femme américaine d’âge moyen, diagnostiquée séropositive au VIH en 2013 et sous traitement anti-VIH efficace a présenté de plus une leucémie myéloïde aiguë. En vue de la transplantation de cellules souches qui a suivi, on a utilisé pour la première fois du sang de cordon ombilical avec la délétion homozygote CCR5-Δ32. Cette mutation rare entraîne une modification du récepteur de surface CCR5 sur les cellules CD4, qui est généralement nécessaire pour la fusion et donc l’infection de la cellule par le VIH. Atteignant environ 1%, cette mutation de CCR5 affiche la prévalence la plus élevée en Europe du Nord. La patiente a bien toléré la transplantation et la chimiothérapie; en particulier, il n’y a pas eu de réaction du greffon contre l’hôte aiguë ou chronique.
37 mois après la transplantation, le traitement contre le VIH (traitement antirétroviral, TAR) a été arrêté. La patiente ne prend actuellement plus de TAR depuis près d’un an et demi et il n’y a pas eu de rebond viral. Aucun ADN du VIH-1 n’est détecté et la patiente est désormais séronégative.1 Il s’agit donc du troisième cas de guérison présumée publié. Jusqu’à présent, chez les patients dits de Berlin et de Londres, le TAR a également été arrêté après une transplantation de moelle osseuse incluant un donneur présentant une délétion CCR5-Δ32 et aucun rebond viral n’a été observé. La particularité du cas actuel n’est pas seulement le fait qu’il s’agisse pour la première fois d’une femme, mais aussi de l’origine ethnique mixte de cette patiente. Dans ce cas, trouver un donneur adéquat s’avère particulièrement difficile. L’approche consistant à recourir au sang de cordon ombilical pourrait donc ouvrir la voie à de futurs cas similaires.
Pas de transmission périnatale lors de l’amorce du TAR avant la grossesse
Le risque de transmission verticale du VIH de la mère à l’enfant est directement associé à la charge virale et au statut thérapeutique de la mère. Une étude française a montré de manière impressionnante l’effet d’un traitement antirétroviral chez les femmes enceintes sur le risque de transmission périnatale.2
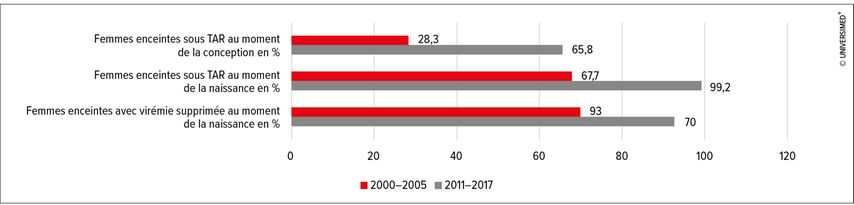
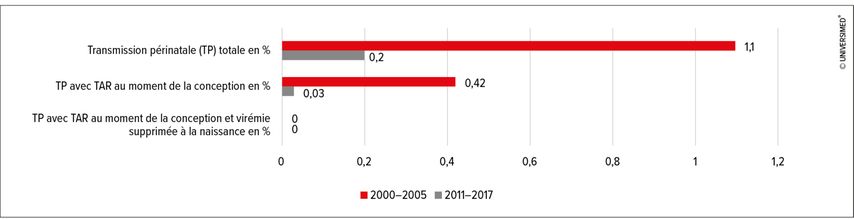
Les grossesses de 14630 femmes séropositives au VIH ont été analysées entre 2000 et 2017. La proportion de femmes déjà sous TAR au moment de la conception est passée de 28,3% à 65,8% au fil des années. De même, la proportion de femmes sous TAR au moment de l’accouchement est passée de 67,7% à 99,2%. Au début de la période d’observation, 70% des femmes avaient une virémie supprimée au moment de l’accouchement, contre 93% à la fin de l’observation (Fig. 1). L’effet du TAR sur les transmissions était nettement visible: dans l’ensemble, le taux de transmissions périnatales est passé de 1,1% à 0,2%. Dans le groupe des femmes qui prenaient déjà un TAR au moment de la conception, le taux de transmission périnatale est passé de 0,42% à 0,03%. Chez les 5482 femmes qui prenaient un TAR au moment de la conception et qui avaient une charge virale inférieure au seuil de détection au moment de l’accouchement, aucune transmission périnatale n’a été observée (Fig. 2).
Fig. 1: Augmentation du traitement antirétroviral (TAR) chez les femmes enceintes (modifié d’après Sibiude J et al. 2022)2
Il convient de noter que les femmes n’ont pas allaité et que, par conséquent, les transmissions potentielles pendant la période d’allaitement ne peuvent pas être évaluées. L’étude souligne toutefois que l’utilisation d’un TAR efficace dès le début de la grossesse permettrait d’exclure les transmissions périnatales.
Utilisation d’anticorps neutralisants à large spectre chez l’enfant
Pour la première fois, l’association de deux bNAb («broadly neutralising antibodies») a été étudiée comme une alternative au traitement conventionnel du VIH chez les enfants.3
L’étude TATELO menée au Botswana portait sur des enfants séropositifs ayant commencé un traitement contre le VIH au cours de la première semaine après la naissance et qui présentaient une charge virale supprimée. Les enfants, âgés de 2 à 6 ans et présentant un nombre moyen de cellules CD4 d’environ 1200/µl, ont d’abord reçu le TAR ainsi que les deux bNAb (VRC 01LS et 10-1074) sous forme de perfusion toutes les 4 semaines dans le cadre d’une phase de transition. Le TAR a ensuite été arrêté. 44% des enfants (11/25) présentaient toujours une charge virale inférieure au seuil de détection après 6 mois de traitement par bNAb uniquement. Le traitement a été bien toléré et, selon les auteurs, favorisé par les parents, car la perfusion mensuelle était plus simple qu’une prise quotidienne dans la vie quotidienne des enfants. Il faut toutefois souligner qu’il s’agit exclusivement d’une étude de validation de concept.
Avec le développement futur d’anticorps neutralisants à large spectre dans le traitement du VIH, une option pourrait toutefois s’ouvrir ici pour le traitement des enfants séropositifs.
Source:
29th Conference on Retroviruses and Opportunistic Infections, 13 au 24 février 2022
Littérature:
1Bryson Y et al.:HIV-1 remission with CCR5Δ32Δ32 haplo-cord transplant in a U.S. woman: Impaact P1107. CROI 2022, Abstract #65 2 Sibiude J et al.:Perinatal HIV-1 transmission in France: U=U for mothers on ART from conception. CROI 2022, Poster #P03 3Shapiro RL et al.:Treatment with broadly neutralizing antibodies in children with HIV in Botswana. CROI 2022, Abstract #32
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...