Approches immunothérapeutiques face aux tumeurs gastro-intestinales
Compte-rendu:
Dr Ine Schmale
Journaliste médicale
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Comme pour de nombreuses autres entités, la disponibilité des immunothérapies modifie le paysage des traitements des tumeurs gastro-intestinales. En particulier, la thérapie associée des inhibiteurs de points de contrôle avec des traitements établis ayant d’autres modes d’action donne des résultats prometteurs selon les études présentées au World Congress on Gastrointestinal Cancer (WCGC). De nouvelles approches thérapeutiques potentielles résultent également du perfectionnement de substances immunothérapeutiques. Tout au moins pour le carcinome du pancréas, une petite avancée pourrait également être démontrée avec un régime de chimiothérapie élargi.
Premiers résultats du pembrolizumab en cas de cancer de l’estomac HER2-positif
Pour le traitement de patients atteints d’adénocarcinome métastatique HER2-positif de l’estomac ou de la jonction gastro-œsophagienne, le pembrolizumab, le trastuzumab et la chimiothérapie ont été associés dans l’étude de phase III KEYNOTE-811. Dans l’essai contrôlé par placebo, 692 patients ont reçu du trastuzumab et une chimiothérapie (5-fluorouracil plus cisplatine ou CAPOX) avec ou sans pembrolizumab. Le double critère d’évaluation primaire consistait dans une prolongation de la survie globale (OS) et de la survie sans progression (PFS). Lors du WCGC, la première analyse intermédiaire planifiée pour les 264 premiers participants à l’étude avec une durée de suivi ≥8,5 mois a été présentée.1 La population de sécurité (≥1 dose du médicament à l’étude) était alors composée de 433 patients. La durée médiane du suivi était de 12,0 mois pour la population d’efficacité et de 9,9 mois pour la population de sécurité. L’âge médian des patients était de 61 à 63 ans et dans environ 80% des cas, il s’agissait d’hommes. Environ 85% des patients présentaient un Combined Positive Score (CPS) pour PD-L1 ≥1 et environ 80% présentaient une forte expression de HER2 (immunohistochimie: IHC 3+). Entre 86% et 88% des patients des deux bras de l’étude au sein des deux populations étudiées ont reçu le régime CAPOX comme chimiothérapie de choix.
Dans le bras pembrolizumab, 97% des patients ont présenté une rétraction tumorale et 32% une rétraction tumorale ≥80%. Dans le bras placebo, une configuration afférente a été observée chez 90% et 15% des patients, respectivement. Le taux de réponse (ORR) était de 74,4% contre 51,9% (p<0,0001) dans les bras expérimental et témoin, respectivement. Une rémission complète a été obtenue chez 11% des patients du bras pembrolizumab et chez 3% des patients du bras témoin. Le bénéfice en termes d’ORR pour le traitement contenant du pembrolizumab a été observé pour tous les sous-groupes étudiés. La durée médiane de la réponse était de 10,6 mois contre 9,5 mois. Le profil de sécurité était comparable dans les deux bras de l’étude.
Les auteurs ont conclu que le pembrolizumab associé au trastuzumab et à la chimiothérapie est un régime potentiel de première intention pour les patients atteints d’adénocarcinome HER2-positif localement avancé, non résécable ou métastatique de l’estomac ou de la jonction gastro-œsophagienne.
Nouvel inhibiteur de PD-1 en cas de carcinome hépatocellulaire prétraité
Les résultats d’une étude mondiale de phase II mettent en évidence une activité clinique prometteuse et soutenue pour le tislelizumab, un anticorps ciblant le PD-1, chez des patients atteints d’un carcinome hépatocellulaire avancé prétraité.2 Le tislelizumab est un nouvel inhibiteur du point de contrôle PD-1 qui présente une affinité et une spécificité élevées pour le récepteur PD-1 des cellules T, mais qui se lie de façon minime au récepteur FcyR des macrophages, empêchant ainsi la phagocytose dépendante des anticorps. Ce dernier élément est un mécanisme de clairance des cellules T et un mécanisme de résistance potentiel au traitement par PD-1. Au total, 249 patients ont été recrutés dans l’étude à un seul bras, parmi lesquels 138 patients avaient reçu un traitement antérieur et 111 patients avaient reçu ≥2 intentions de traitement. L’âge médian des patients était de 62 ans, avec une fourchette allant de 28 à 90 ans. Un statut PD-L1 positif a été détecté chez 6,0% des patients, 57,4% des patients n’avaient aucune expression de PD-L1 et le statut PD-L1 était inconnu chez 36,5% des patients. 80,3% des patients présentaient des lésions extrahépatiques.
Une réponse globale a été observée chez 13,3% des patients, avec un pourcentage comparable de 13,8% en deuxième intention de traitement et 12,6% avec ≥2 intentions de traitement antérieures. En outre, une maladie stable a été observée chez 39% des patients. 79,2% des patients ayant répondu ont présenté des rémissions durables sur une durée ≥12 mois. La survie médiane des patients était de 13,2 mois (IC à 95%: 10,8–15,0). Le taux d’OS à 6 mois était de 77,2% et le taux d’OS à 12 mois était de 54,3%. La PFS médiane était de 2,7 mois. Des effets secondaires de grade ≥3 ont été rapportés chez 48,6% des patients et des effets secondaires de grade ≥3 associés au traitement chez 14,5%. 10,4% des patients ont interrompu le traitement en raison d’effets secondaires et 4,8% en raison d’effets secondaires associés au traitement. Les effets secondaires les plus fréquents ont été l’augmentation des taux d’AST et d’ALT (12,9 et 9,2%, respectivement), l’asthénie (7,6%), l’hypothyroïdie (7,6%), l’élévation de la bilirubine sanguine (6,8%) et le prurit (6,8%).
Inhibition de PD-1 en deuxième intention dans le carcinome épidermoïde de l’œsophage
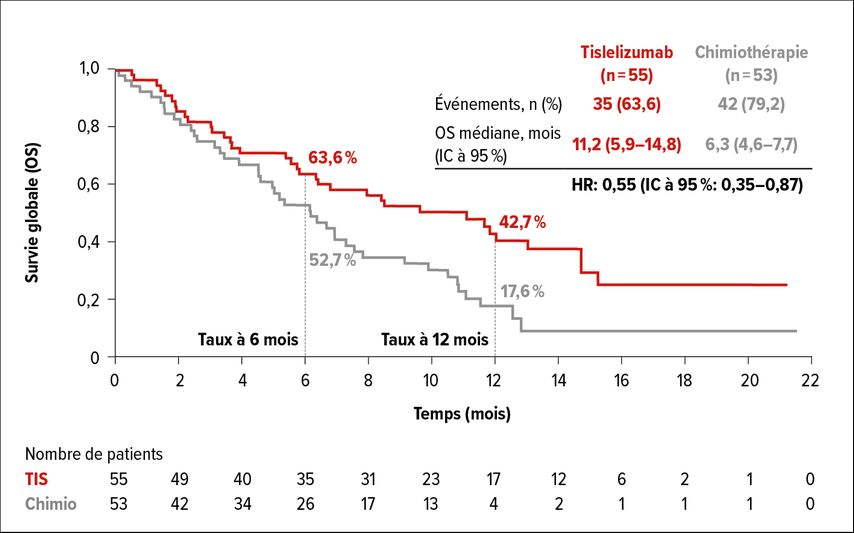
Le tislelizumab a également été étudié pour le traitement du carcinome épidermoïde avancé ou métastatique de l’œsophage. Dans l’essai de phase III RATIONALE 302, un total de 512 patients présentant une progression pendant ou après un traitement de première intention ont reçu du tislelizumab (200mg, q3w) ou une chimiothérapie au choix de l’investigateur (paclitaxel, docétaxel ou irinotécan). 108 patients avaient été recrutés en Europe ou en Amérique du Nord. Pour le WCGC, les résultats de ce sous-groupe géographique ont été analysés.3 La survie globale a été significativement prolongée, passant d’une médiane de 6,3 mois avec la chimiothérapie à 8,6 mois avec le tislelizumab pour l’ensemble de la population étudiée dans l’essai RATIONALE 302 (critère d’évaluation primaire) (HR: 0,70; IC à 95%: 0,57–0,85; p=0,0001). Le taux d’OS à 6 mois était de 62,3 contre 51,8% et le taux d’OS à 12 mois était de 37,4 contre 23,7%. Pour les participants à l’étude venus d’Europe ou d’Amérique du Nord, le risque de décès a été réduit de 45% (HR: 0,55; IC à 95%: 0,35–0,87) et la survie globale médiane a été prolongée de 6,3 à 11,2 mois (Fig. 1). Après 6 mois, 63,6 contre 52,7% et après 12 mois, 42,7 contre 17,6% des patients européens et nord-américains étaient en vie. Aucune différence dans la PFS n’a été observée entre les deux groupes d’étude dans la population européenne et nord-américaine (HR: 0,97; IC à 95%: 0,64–1,47). Il y a eu une réponse de 20,0% au tislelizumab contre 11,3% à la chimiothérapie dans les populations européenne et nord-américaine. La durée médiane de la réponse était de 5,1 mois contre 2,1 mois. Après 6 mois, 42,4 contre 20,0% des patients répondants étaient toujours en rémission et après 12 mois, 28,3 contre 0% des patients répondants étaient toujours en rémission. Une maladie stable a été observée chez 30,9 contre 37,7% des patients.
Fig. 1: Survie globale sous tislelizumab par rapport à la chimiothérapie dans le sous-groupe des participants européens et nord-américains à l’étude (d’après Ajani J et al.)3
19,2% contre 26,7% des patients des deux bras de l’étude ont interrompu le traitement en raison d’effets secondaires. Les effets secondaires les plus fréquents étaient l’anémie (11,0 contre 34,6%), la diminution de l’appétit (6,3 contre 31,3%), la diarrhée (5,5 contre 27,5%) et les nausées (2,7 contre 27,5%). D’après les résultats de l’essai RATIONALE 302, le tislelizumab est un traitement potentiel de deuxième intention pour les patients atteints d’un carcinome épidermoïde avancé ou métastatique de l’œsophage, ont conclu les auteurs.
Traitement préopératoire par avélumab pour le cancer du rectum avancé
Dans l’étude italienne de phase II AVANA, l’inhibiteur PD-L1 avélumab a été utilisé en préopératoire en plus de la chimioradiothérapie pour le cancer du rectum localement avancé.4 Le critère d’évaluation principal de l’étude était le taux de rémissions complètes pathologiques (RCP). Suite à l’opération, une chimiothérapie adjuvante avec 6 cycles de XELOX ou de capécitabine a été ajoutée en fonction du résultat pathologique. 101 patients d’un âge médian de 63 ans ont pu être recrutés. Plus de 90% des patients ont reçu la dose complète de radiothérapie, de capécitabine et/ou d’avélumab. Une RCP a été observée chez 23% des patients et une bonne réponse pathologique chez 60% d’entre eux. Le statut des microsatellites était disponible pour 62 patients, dont 2 seulement présentaient une instabilité microsatellitaire élevée. Le traitement était bien gérable avec des effets secondaires de grade ≥3 chez 8% des patients. Les auteurs suggèrent que cette approche prometteuse devrait être poursuivie.
Prolongation de la survie grâce à un traitement adjuvant en cas de cancer du pancréas
L’essai multicentrique, ouvert et randomisé de phase III APACT a comparé l’administration adjuvante de nab-paclitaxel plus gemcitabine par rapport à la gemcitabine seule chez un total de 866 patients atteints d’un cancer du pancréas résécable. L’essai n’a pas atteint le critère d’évaluation primaire de prolongation de la survie sans maladie (DFS) vérifiée indépendamment (HR: 0,88; IC à 95%: 0,729–1,063), mais a fait ressortir un avantage pour le traitement associé dans l’évaluation DFS des investigateurs (HR: 0,82; IC à 95%: 0,694–0,965). Il a également été démontré que l’administration supplémentaire de nab-paclitaxel présentait un avantage en termes d’OS (HR: 0,82; IC à 95%: 0,680–0,996). Lors du WCGC, les données sur la SG à 5 ans ont été présentées, indiquant un avantage potentiel du nab-paclitaxel.5
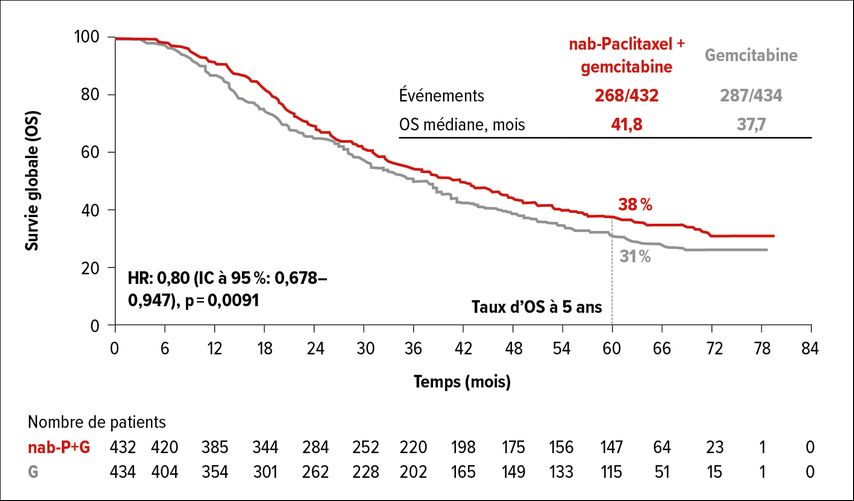
La durée médiane de suivi pour l’analyse actuelle de l’OS était de 63,2 mois et un total de 555 événements étaient survenus. Avec une médiane de 41,8 mois pour le traitement par nab-paclitaxel plus gemcitabine contre 37,7 mois pour le traitement par gemcitabine seule, le nab-paclitaxel a révélé une réduction de 20% du risque de décès (HR: 0,80; IC à 95%: 0,678–0,947; p=0,0091). Après 62 mois, 38 contre 31% des patients étaient en vie (Fig. 2).
Ces résultats suggèrent que même si l’essai n’a pas atteint son critère d’évaluation primaire, les patients peuvent bénéficier de l’ajout du nab-paclitaxel, ont conclu les auteurs.
Source:
World Congress on Gastrointestinal Cancer (WCGC), 30 juin au 3 juillet 2021
Littérature:
1 Janjigian YY et al.: Pembrolizumab plus trastuzumab and chemotherapy for HER2+ metastatic gastric or gastroesophageal junction cancer: initial findings of the global phase 3 KEYNOTE-811 study. WCGC 2021, Abstr. #LBA-4 2 Ducreux M et al.: Results from a global phase 2 study of tislelizumab, an investigational PD-1 antibody, in patients with previously treated advanced hepatocellular carcinoma. WCGC 2021, Abstr. #O-1 3 Ajani J et al.: Randomized, phase 3 study of second-line tislelizumab vs chemotherapy in advanced or metastatic esophageal squamous cell carcinoma (RATIONALE 302) in the overall population and the Europe/North America subgroup. WCGC 2021, Abstr. #O-15 4 Salvatore L et al.: Phase II study of preoperative chemoradiotherapy plus avelumab in patients with locally advanced rectal cancer – the AVANA study. WCGC 2021, Abstr. #O-12 5 Tempero MA et al.: Phase 3 APACT trial of adjuvant nab-paclitaxel plus gemcitabine vs gemcitabine alone in patients with resected pancreatic cancer: updated 5-year overall survival. WCGC 2021, Abstr. #LBA-1
Das könnte Sie auch interessieren:
BPCO: identification de patients non diagnostiqués
De nombreuses personnes atteintes de BPCO et/ou d’asthme n’ont jamais été diagnostiquées et ne sont donc pas traitées. Plusieurs études publiées ces derniers mois se penchent sur ce ...
Diarrhée chronique: déroulement de l’examen
La diarrhée chronique est le symptôme de différentes maladies. Le Pr Alain Schoepfer a expliqué comment rechercher au mieux le facteur déclenchant dans son exposé lors du congrès annuel ...
Réduction, voire arrêt des corticoïdes grâce à la biothérapie?
Les corticoïdes oraux constituent le traitement de référence des exacerbations de l’asthme et sont également utilisés pour celles de la BPCO. Cette norme s’appuie toutefois sur des ...