ANCA-assoziierte Vaskulitiden
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Als ANCA-assoziierte Vaskulitiden wird eine Gruppe von nekrotisierenden Entzündungen der kleinen Gefäße bezeichnet, die ein hohes Risiko von Organversagen mit sich bringen können. In der Therapie werden Glukokortikoide und Immunsuppression eingesetzt. Mit Avacopan steht auch ein innovatives Medikament zur Verfügung, das in die für die ANCA-assoziierten Vaskulitiden typische Komplementaktivierung eingreift.
Definition und Klassifikation der ANCA-assoziierten Vaskulitiden (AAV)
Charakteristisch für die ANCA-assoziierten Vaskulitiden (AAV) ist das Auftreten von antineutrophilen zytoplasmatischen Antikörpern (ANCA) mit den Zielantigenen Myeloperoxidase und Proteinase 3. Gemäß der Chapel-Hill-Nomenklatur von 2012 werden die Granulomatose mit Polyangiitis (GPA – früher als Morbus Wegener bezeichnet), die eosinophile Granulomatose mit Polyangiitis (EGPA – früher als Morbus Churg-Strauss bezeichnet) und die mikroskopische Polyangiitis (MPA) als ANCA-assoziierte Vaskulitiden bezeichnet.1 „Es handelt sich dabei um Systemerkrankungen, da kleine Gefäße überall im Körper zu finden sind. Häufig sind Nieren und Lunge betroffen“, sagt dazu Prof. Dr. Benjamin Terrier von der Abteilung für Innere Medizin am Hôpital Cochin in Paris. Die unterschiedlichen ANCA-Vaskulitiden befallen die verschiedenen Organsysteme mit unterschiedlicher Häufigkeit.2
Epidemiologie
ANCA-Vaskulitis kann sowohl jüngere als auch ältere Menschen betreffen, ist jedoch bei Kindern und Jugendlichen selten. Die Inzidenz steigt mit dem Alter, die jährliche Gesamtinzidenzrate in Europa beträgt ungefähr 13–20 Fälle pro 1 Million Einwohner. Die Prävalenz hat in den letzten 20 Jahren zugenommen und beträgt derzeit etwa 46–184 Fälle pro 1 Million Einwohner. GPA und MPA sind die häufigsten klinischen Subtypen der AAV.3–5
Pathophysiologie
Eine wichtige Rolle in der Pathophysiologie der ANCA-Vaskulitiden spielt das Komplementsystem, das infolge der Interaktion zwischen Granulozyten und Antikörpern über den alternativen Pathway aktiviert wird. Dabei aktiviert der Faktor C3 die C5-Konvertase, die den Komplementfaktor C5 in C5a und C5b spaltet. In der Folge kommt es zur Aktivierung des C5a-Rezeptors auf neutrophilen Granulozyten, die zur Degranulation und Freisetzung von Zytokinen und reaktiven Sauerstoffspezies führt. Diese setzen einen Entzündungsprozess mit Influx inflammatorischer Zellen in Gang, was schließlich in Vernarbung und Gefäßschädigung resultiert.6 Als therapeutische Optionen stehen Glukokortikoide, Cyclophosphamid, Rituximab, Plasmapherese sowie seit einigen Jahren der C5a-Rezeptor-Blocker Avacopan zur Verfügung, erläutert Terrier.
Therapeutisches Management
Im praktischen Management der Erkrankungen stellen sich fünf Fragen, so Terrier: Welches Glukokortikoid-Regime soll zum Einsatz kommen? Welche Immunsuppressiva sollen verwendet werden? Wann soll Plasmapherese eingesetzt werden? Welchen Stellenwert hat Avacopan? Wie kann ich Remission erhalten?
Glukokortikoide
Zum Einsatz von Glukokortikoiden (GC) geben die unterschiedlichen Guidelines leicht divergierende Empfehlungen. Das American College of Rheumatology (ACR) empfiehlt bei aktiver, schwerer GPA/MPA entweder hoch dosierte orale GC oder eine intravenöse Pulstherapie.7 Die European Alliance of Associations for Rheumatology (EULAR) empfiehlt orale GC mit einer Startdosis von 50–75mg am Tag.8 Laut Kidney Disease: Improving Global Outcomes (KDIGO) sollen GC bereits initial mit Cyclophosphamid oder Rituximab kombiniert werden.9
Wichtige Informationen zum Management der ANCA-Vaskulitis lieferte vor wenigen Jahren die PEXIVAS-Studie, die die Wirksamkeit und Sicherheit zweier GC-Regime sowie von Plasmapherese untersuchte. Die etwas über 700 schwer erkrankten Patient:innen hatten als Induktionstherapie entweder Cyclophosphamid oder Rituximab erhalten. Die GC-Therapie wurde mit 1–3 intravenösen Pulsen begonnen, gefolgt von einer oralen Therapie entweder mit Standard- oder reduzierter Dosis, beide beginnend mit 50–75mg, abhängig vom Körpergewicht. Der Unterschied zwischen den Gruppen lag in einer schnelleren Dosisreduktion in einem der beiden Arme. In den ersten sechs Monaten hatten die Patient:innen im Arm mit reduzierter Dosis weniger als 60% der Gesamtdosis des Standard-Arms erhalten. Endpunkt war die Inzidenz von Tod oder Nierenversagen. Im Hinblick auf diesen Endpunkt zeigte sich kein Unterschied zwischen den beiden Armen. Sehr wohl waren jedoch schwere Infektionen im Behandlungsarm mit der niedrigeren kumulativen Steroiddosis seltener.10
Noch weiter reduziert wurde die Steroiddosis in der japanischen LoVAS-Studie, die ebenfalls Non-Inferiority für die niedrigere GC-Dosis zeigte. Terrier betont allerdings, dass die angepeilten Dosierungen in dieser Studie so niedrig waren, dass sie bei rund 60% der Patient:innen nicht erreicht werden konnten und Schemata individualisiert werden mussten, wobei die kumulative Dosis dennoch niedriger war als im Standard-Arm. Es sei also durchaus sinnvoll, sich ambitionierte Ziele zu setzen.11 Auf Basis dieser Daten geben mittlerweile auch die Guidelines der reduzierten GC-Dosis den Vorzug.7–9 Allerdings mahnen neuere Daten zur Vorsicht, zumal in PEXIVAS die große Mehrheit der Patient:innen eine Induktionstherapie mit Cyclophosphamid erhalten hatte. Der Frage, ob dies auch mit dem heute gebräuchlicheren Rituximab zu erwarten sei, wurde in einer Real-World-Studie mit mehr als 300 Patient:innen nachgegangen, für die auch der primäre Endpunkt erweitert wurde. Zusätzlich zu Tod und Nierenversagen enthielt dieser nun auch Progression der ANCA-Vaskulitis vor Remission oder Rezidiv innerhalb von 12 Monaten nach der Induktion. Im Hinblick auf diesen Endpunkt erwies sich die reduzierte GC-Dosis als schlechtere Option, wobei Tod und Nierenversagen mit reduzierter Steroidtherapie nicht häufiger eintraten. Dies war jedoch bei Patient:innen, die eine Induktion mit Rituximab erhalten hatten oder deren Serum-Kreatinin über 300μmol/L lag, sehr wohl der Fall.12 Daher sei Vorsicht geboten, wenn die reduzierte GC-Therapie bei Patient:innen mit schwerer Nierenerkrankung oder in Verbindung mit einer Rituximab-Induktion zum Einsatz kommen soll, erläutert Terrier. Wenn möglich soll jedoch der niedrigeren Steroidexposition der Vorzug gegeben werden. Dies entspricht auch der aktuellen Position der Guidelines.
Hinsichtlich der initialen Pulstherapie hält Terrier fest, dass sich diese gewissermaßen zum Standard of Care entwickelt habe, obwohl dazu nur Evidenz aus indirekten Vergleichen von Studien vorliegt und Beobachtungsstudien sogar ungünstige Effekte im Sinne eines höheren Infektionsrisikos zeigen. Daher sollte Pulstherapie nur eingesetzt werden, wenn die akute Gefahr schwerer Organschäden besteht.
Cyclophosphamid und Plasmapherese nur einsetzen, wenn unbedingt notwendig
Hinsichtlich der Wahl der Immunsuppression empfehlen die KDIGO-Leitlinien in den meisten Fällen Rituximab. Cyclophosphamid ist lediglich bei schwerer Nierenbeteiligung der Vorzug zu geben oder wenn Rituximab nicht verfügbar ist. Rituximab und Cyclophosphamid können auch kombiniert werden.9
Zur Rolle der Plasmapherese zeigen die verfügbaren Studien widersprüchliche Ergebnisse. In PEXIVAS brachte Plasmapherese keinen Vorteil. Dieses Ergebnis war durch alle Subgruppen kohärent.10 Eine Metaanalyse aller verfügbaren Studien zeigt jedoch Vorteile für die Plasmapherese in definierten Patient:innenpopulationen. Dies jedoch um den Preis eines erhöhten Infektionsrisikos.13 Dementsprechend empfehlen die Leitlinien die Plasmapherese für ausgewählte Gruppen von Patient:innen mit GPA oder MPA, insbesondere bei schwerer Nierenbeteiligung und Gefahr von Nierenversagen. Eine Nierenbiopsie kann bei der Entscheidung helfen, da sich damit Fälle von besonders ausgeprägter proliferativer Glomerulonephritis identifizieren lassen.8,9 Terrier betont auch, dass die Entscheidung für eine Plasmapherese nach ausreichender Aufklärung mit den Patient:innen besprochen werden muss.
Avacopan: direkter Eingriff in die Komplementaktivierung
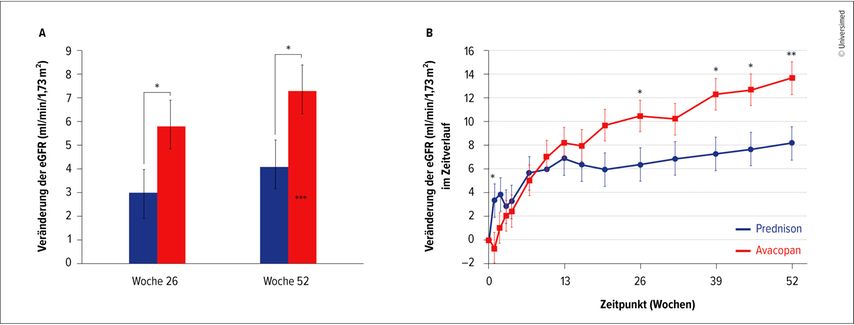
Mit der Zulassung des C5a-Rezeptor-Blockers Avacopan besteht seit einigen Jahren auch die Möglichkeit, in die für die ANCA-Vaskulitiden typische pathologische Komplementaktivierung einzugreifen. Diese Zulassung beruht auf der randomisierten, kontrollierten multizentrischen Phase-III-Studie ADVOCATE, die (zusätzlich zu Cyclophosphamid/Azathioprin oder Rituximab) Avacopan 30mg mit Prednison verglich. In die Studie eingeschlossen waren Patienten mit entweder neu diagnostizierter oder rezidivierender Erkrankung, von denen 81% eine Nierenbeteiligung aufwiesen. Primärer Endpunkt war das Erreichen von Remission (BVAS 0) zu Woche 26 ohne Glukokortikoideinnahme in den vier Wochen davor. Zweiter primärer Endpunkt war Remission zu Woche 26 und 52. ADVOCATE war eine Non-Inferiority-Studie. Die Ergebnisse zeigen, dass Avacopan im Vergleich zu oralen Glukokortikoiden (Prednison 2x30mg mit Tapering-Schema) eine mindestens gleichwertige effektive Remissionsinduktion bewirkte (zu Woche 26) und darüber hinaus einen überlegenen Remissionserhalt (Woche 52) im Sinne eines geringeren absoluten Rezidivrisikos zeigte (Abb.1).14 Avacopan war auch mit einer signifikanten Verbesserung der Nierenfunktion über ein Jahr assoziiert, wovon insbesondere Patient:innen mit schlechter Nierenfunktion profitierten.15 Die Glukokortikoidexposition war in der Avacopan-Gruppe signifikant geringer, was auch in weniger Glukokortikoidtoxizität (insbesondere betreffend BMI, Glukosetoleranz, Lipidmetabolismus und Hauttoxizität) resultierte. Die Leitlinien geben daher eine schwache Empfehlung für Avacopan als Teil einer Strategie zur Reduktion der Steroidexposition, wobei KDIGO anführt, dass Patient:innen mit ausgeprägter Niereninsuffizienz am deutlichsten profitieren.8,9 Terrier betont, dass Glukokortikoide nach Beginn einer Therapie mit Avacopan innerhalb von vier Wochen ausgeschlichen werden und keinesfalls unkritisch weitergeführt werden sollten: „Der Sinn von Avacopan liegt darin, das Glukokortikoid loszuwerden.“
Abb. 1: ADVOCATE: Entwicklung der geschätzten glomerulären Filtrationsrate (eGFR) im Zeitverlauf; * = signifikant, ** = hochsignifikant (modifiziert nach Jayne DRW et al. 2021)14
In der Erhaltung der Remission ist Rituximab Standard, wobei unterschiedliche Regime empfohlen werden. KDIGO empfiehlt mit 24 bis 48 Wochen die längste Therapie, die auch verlängert werden kann, wenn hohes Rezidivrisiko besteht.9 Studiendaten zeigen, dass die Chancen auf Erhalt der Remission am höchsten sind, wenn Rituximab in einem festen Dosisschema von 500mg alle sechs Monate über 18 oder 36 Monate gegeben wird. Bei einem individualisierten Schema über 18 Monate steigt das Rezidivrisiko. Am höchsten ist das Risiko jedoch, wenn Azathioprin zur Erhaltungstherapie eingesetzt wird.16
Sonderfall EGPA: Indikation für Anti-IL-5/IL-5-R-Antikörper
Terrier weist auch darauf hin, dass sich die EGPA in mehrfacher Hinsicht von den übrigen ANCA-assoziierten Vaskulitiden unterscheidet und in separaten Studien untersucht wurde. So sind Patient:innen mit EGPA unabhängig vom ANCA-Titer von Asthma und Nasenpolypen betroffen. Darüber hinaus stellt sich die Frage nach dem Stellenwert der ACPA bei dieser Erkrankung. Terrier gibt zu bedenken, dass ACPA-positive EGPA-Patient:innen mit hohem Risiko von Glomerulonephritis, Mononeuritis multiplex und Purpura mehr von B-Zell-Depletion profitieren könnten, während für ANCA-negative Patient:innen gegen die Eosinophilie gerichtete Therapien besser geeignet sein könnten. Allerdings mangle es derzeit noch an qualitativ hochwertiger Evidenz für eine unterschiedliche Behandlung dieser zwei Formen der EGPA.
Factbox
Wichtige Informationen zum Management der ANCA-Vaskulitis lieferte vor wenigen Jahren die PEXIVAS-Studie, die die Wirksamkeit und Sicherheit zweier GC-Regime sowie von Plasmapherese untersuchte.
Aktuell empfehlen die Leitlinien zur Induktion von Remission die Kombination von hoch dosierten GC und Cyclophosphamid. Hoch dosierte GC und Rituximab werden als Alternative angeführt. Zur Erhaltung der Remission können Methotrexat, Azathioprin, Mepolizumab (bzw. mittlerweile auch Benralizumab) oder Rituximab eingesetzt werden, wobei bei Patient:innen ohne lebensbedrohliche Organbeteiligung Mepolizumab oder Benralizumab der Vorzug gegeben werden soll.8,17 Die Empfehlung dieser Anti-IL-5/IL-5-R-Antikörper geht allerdings auf Studien zurück, in die keine Patient:innen mit schwerer EGPA oder nach kürzlich erfolgter EGPA-Diagnose eingeschlossen waren.18,19
Quelle:
HOT (How to Treat) Session „ANCA Vasculitis and EGPA“ im Rahmen des EULAR 2025, Barcelona
Literatur:
1 Jennette JC et al.: 2012 revised International Chapel Hill Consensus Conference Nomenclature of Vasculitides. Arthritis Rheum 2013; 65(1): 1-11 2 Kitching AR et al.: ANCA-associated vasculitis. Nat Rev Dis Primers 2020; 6(1): 71 3 Watts RA et al.: Classification, epidemiology and clinical subgrouping of antineutrophil cytoplasmic antibody (ANCA)-associated vasculitis. Nephrol Dial Transplant 2015; 30(Suppl_1) 4 Watts RA et al.: Epidemiology of systemic vasculitis: a ten-year study in the United Kingdom. Arthritis Rheum 2000; 43(2): 414-9 5 Omerod AS, Cook MC: Epidemiology of primary systemic vasculitis in the Australian Capital Territory and south-eastern New South Wales. Intern Med J 2008; 38(11): 816-23 6 Zipfel PF et al.: Complement catalyzing glomerular diseases. Cell Tissue Res 2021; 385(2): 355-70 7 Chung SA et al.: 2021 American College of Rheumatology/Vasculitis Foundation Guideline for the management of antineutrophil cytoplasmic antibody-associated vasculitis. Arthritis Rheumatol 2021; 73(8): 1366-83 8 Hellmich B et al.: EULAR recommendations for the management of ANCA-associated vasculitis: 2022 update. Ann Rheum Dis 2024; 83(1): 30-47 9 Kidney Disease: Improving Global Outcomes (KDIGO) ANCA Vasculitis Work Group: KDIGO 2024 Clinical Practice Guideline for the management of antineutrophil cytoplasmic antibody (ANCA)-associated vasculitis. Kidney Int 2024; 105(3S): 71-116 10 Walsh M et al.: Plasma exchange and glucocorticoids in severe ANCA-associated vasculitis. N Engl J Med 2020; 382(7): 622-31 11 Furuta S et al.: Effect of reduced-dose vs high-dose glucocorticoids added to rituximab on remission induction in ANCA-associated vasculitis: a randomized clinical trial. JAMA 2021; 325(21): 2178-87 12 Nagle S et al.: Real-life use of the PEXIVAS reduced-dose glucocorticoid regimen in granulomatosis with polyangiitis and microscopic polyangiitis. Ann Rheum Dis 2025; 84(2): 319-28 13 Walsh M et al.: The effects of plasma exchange in patients with ANCA-associated vasculitis: an updated systematic review and meta-analysis. BMJ 2022; 376: e064604 14 Jayne DRW et al.: Avacopan for the treatment of ANCA-associated vasculitis. N Engl J Med 2021; 384(7): 599-609 15 Cortazar FB et al.: Renal recovery for patients with ANCA-associated vasculitis and low eGFR in the ADVOCATE trial of avacopan. Kidney Int Rep 2023; 8(4): 860-70 16 Delestre F et al.: Rituximab as maintenance therapy for ANCA-associated vasculitides: pooled analysis and long-term outcome of 277 patients included in the MAINRITSAN trials. Ann Rheum Dis 2024; 83(2): 233-41 17 Emmi G et al.: Evidence-based guideline for the diagnosis and management of eosinophilic granulomatosis with polyangiitis. Nat Rev Rheumatol 2023; 19(6): 378-93 18 Wechsler ME et al.: Mepolizumab or placebo for eosinophilic granulomatosis with polyangiitis. N Engl J Med 2017; 376(20): 1921-32 19 Wechsler ME et al.: Benralizumab versus mepolizumab for eosinophilic granulomatosis with polyangiitis. N Engl J Med 2024; 390(10): 911-21
Das könnte Sie auch interessieren:
Schwierig zu behandelnde oder therapierefraktäre SpA
Die Behandlungsmöglichkeiten bei Spondyloarthritis haben sich mit Einführung der Biologika dramatisch verbessert. Das bedeutet allerdings nicht, dass alle Patient:innen in ausreichendem ...
Biologikatherapien in der Schwangerschaft
„Biologika sind in der Schwangerschaft in Ordnung“ – mit dieser klaren Aussage fasste Prof.Dr. Ian Giles, University College London, im Rahmen der RheumaPreg-2025- Konferenz in Wien die ...
Riesenzellarteriitis: Ultraschall ist erste Wahl in der Diagnostik
Bei der Riesenzellarteriitis ist, insbesondere wenn sie die Arteria temporalis betrifft, rasches Handeln erforderlich. Die Diagnose kann mittels Sonografie und Labor schnell gestellt ...