Zeitnahe Integration von Palliative Care: Theorie und Praxis
Autor:innen:
OÄ Priv.-Doz. Dr. Gudrun Kreye, MBA1
Manuela Wasl, MSc1
Univ.-Doz. Dr. Ansgar Weltermann2
1 Klinische Abteilung für Innere Medizin 2, Universitätsklinikum Krems
2 Zentrum für Tumorerkrankungen, Ordensklinikum Linz
Korrespondenz:
E-Mail: gudrun.kreye@krems.lknoe.at
Die zeitnahe und systematische Integration der Palliativversorgung (PC) in die onkologische Standardversorgung ist von entscheidender Bedeutung. Sie verbessert nachweislich die Lebensqualität, reduziert die Symptomlast und erhöht die Zufriedenheit der Patient:innen.1,2
Keypoints
-
Die zeitgerechte und systematische Integration der Palliativversorgung (PC) in die onkologische Behandlung verbessert die Lebensqualität und reduziert die Symptomlast.1
-
Trotz klarer Empfehlungen wird die spezialisierte PC in der klinischen Praxis oft zu spät oder gar nicht konsultiert; eine retrospektive Analyse zeigte eine mediane Zeitspanne von nur 17,2 Tagen zwischen der Erstkonsultation und dem Tod.5
-
Die zeitgerechte PC erfordert einen systematischen Ansatz, der vier Schlüsselelemente umfasst: routinemäßiges Screening der PC-Bedürfnisse, proaktive Versorgungsplanung (ACP), routinemäßiges Symptom-Monitoring und die frühzeitige Einbeziehung des Spezialisierten Palliativteams.6
-
Wesentliche Barrieren für die Integration sind die Überschätzung der Prognose durch Kliniker:innen,7 die Angst, den Patient:innen die Hoffnung zu nehmen,8 sowie systemische Mängel in der Kommunikation und der Dokumentation in der elektronischen Patientenakte (EMR).6
Trotz internationaler Leitlinien wie der Empfehlungen der American Society of Clinical Oncology (ASCO)3 und der European Society for Medical Oncology (ESMO),4 die eine frühe Integration befürworten, zeigen Analysen der klinischen Praxis, dass die Überweisung an spezialisierte Palliativteams (SPCT) weiterhin stark verzögert erfolgt.5 Um die Versorgung zu optimieren, muss die theoretische Forderung nach zeitgerechter PC in die praktische Realität des Versorgungsmodells umgesetzt werden.
Theoretische Grundlagen und nachgewiesener Nutzen
Die PC wird von der Weltgesundheitsorganisation (WHO) als ein aktiver, ganzheitlicher Ansatz zur Verbesserung der Lebensqualität bei lebensbedrohlichen Erkrankungen definiert. Dies umfasst die Prävention und Linderung von Leiden durch frühzeitiges Erkennen sowie die tadellose Behandlung körperlicher, psychosozialer und spiritueller Probleme.6
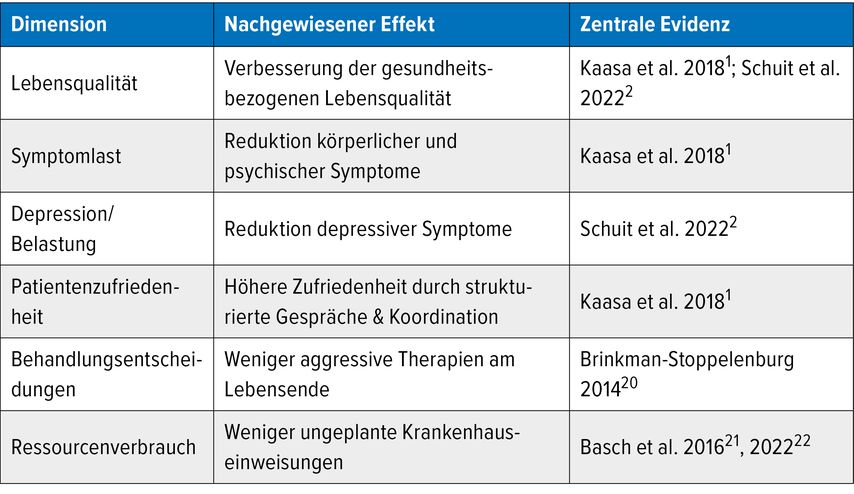
Die ASCO empfiehlt die Integration der Palliativversorgung in die Standardversorgung innerhalb von acht Wochen nach der Diagnose einer fortgeschrittenen Krebserkrankung.3 Zahlreiche Studien (Tab.1) belegen den klinischen Nutzen einer frühen Integration, darunter das Verbessern der Lebensqualität und Verringern depressiver Symptome und der Symptombelastung.1,2
Das Generalisten-Spezialisten-Modell
Ein weitverbreitetes Modell zur Bereitstellung der PC ist das allgemeinistisch-spezialistische Modell.7 Hierbei erbringen Onkolog:innen und onkologisches Pflegepersonal die grundlegende (generalistische) PC (z.B. Basis-Symptommanagement und „Goals of Care“-Gespräche). Das Spezialisierte Palliativteam (SPCT) wird bei komplexen Symptomen, multidimensionalen Belastungen oder auf Wunsch der Patient:innen unterstützend hinzugezogen.7,8
Basierend auf einer Delphi-Studie wurden vier Schlüsselelemente für die zeitnahe Integration der PC in die onkologische Krankenhausversorgung identifiziert:
-
routinemäßiges Screening der PC-Bedürfnisse,
-
„Advance Care Planning“ (ACP),
-
routinemäßiges Symptom-Monitoring und
-
Einbeziehen des SPCT.8
Die Herausforderung der späten Überweisung („reality check“)
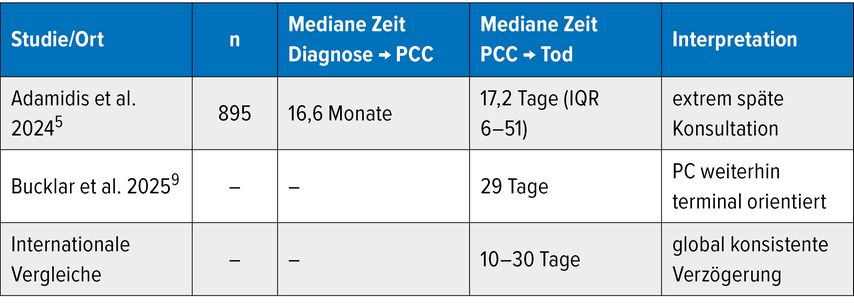
Die tatsächliche klinische Praxis steht oft im Widerspruch zu den Empfehlungen. Retrospektive Analysen zeigen, dass die spezialisierte PC in der Akutversorgung häufig sehr spät hinzugezogen wird (Tab.2).
Späte Konsultationszeiten
Eine retrospektive Analyse von 895 Palliativkonsilen (PCC) an der Wiener Universitätsklinik ergab, dass die mediane Zeit von der Erstdiagnose bis zur ersten PCC 16,6 Monate betrug.5 Die mediane Zeit von der ersten PCC bis zum Tod betrug lediglich 17,2 Tage (Interquartilbereich [IQR]: 6,1–50,7 Tage).5 Rund 50% der Patient:innen verstarben im Zeitraum zwischen 5 und 47 Tagen nach der ersten Konsultation.5 Auch in einer Analyse aus einem Schweizer Universitätsspital lag die mediane Überlebenszeit nach der Konsultation bei nur 29 Tagen.9 Diese Befunde verdeutlichen die Diskrepanz, dass PC in der klinischen Wahrnehmung häufig immer noch der terminalen Phase zugeordnet wird.5
Barrieren in der Praxis
Die späte Integration ist auf multiple Barrieren zurückzuführen (Tab.3):7,10
-
Kliniker:innenebene: Ärzt:innen konzentrieren sich stark auf die kurative Therapie11 und überschätzen häufig die Prognose der Patient:innen.12 Zudem besteht die Sorge, durch das Ansprechen von PC den Betroffenen die Hoffnung zu nehmen.10,13
-
Patient:innenebene: Patient:innen assoziieren PC oft fälschlicherweise mit dem unmittelbaren Sterben,8 was eine frühzeitige Diskussion erschwert. Sie können zudem schockiert reagieren, wenn das Thema zu früh oder unsensibel angesprochen wird.8
-
Hämatoonkologie: Bei hämatologischen Malignomen stellt der unvorhersehbare Krankheitsverlauf eine besondere Hürde dar.14,15 Dies kann dazu führen, dass kurative Optionen gegenüber palliativen Behandlungen priorisiert werden, obwohl eine frühzeitige, integrierte Versorgung möglich wäre.16
-
Systemische Barrieren: Organisatorische Mängel, wie Zeitmangel, fehlendes Wissen und unzureichende Dokumentation von Ergebnissen des Symptom-Monitorings in der elektronischen Patient:innenakte (EMR), verhindern eine systematische Umsetzung der PC.8,17
Strategien zur Förderung derzeitnahen Integration
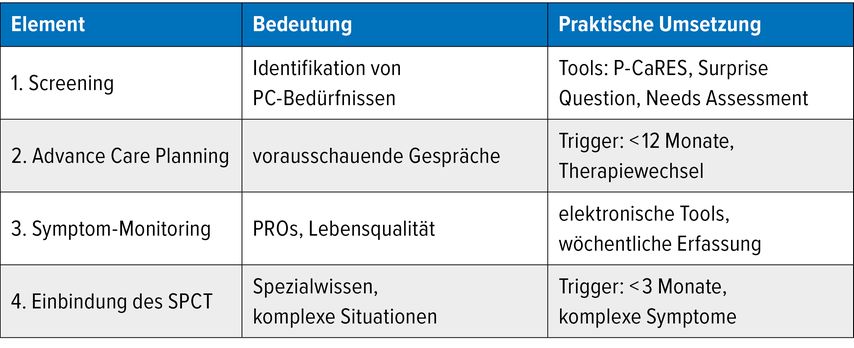
Die zeitnahe Integration erfordert sowohl standardisierte Prozesse als auch die Wahrnehmung des richtigen individuellen Zeitpunkts (Tab.4).18
Proaktive Versorgungsplanung (ACP)
ACP sollte allen Patient:innen mit unheilbarem Krebs angeboten werden.19 Es führt zu besseren Ergebnissen am Lebensende, wie Reduktion von nicht sinnvollenlebensverlängernden Maßnahmen.20
ACP als dynamischer Prozess: ACP sollte nicht als einmaliges Ausfüllen einer Checkliste betrachtet werden, sondern als ein kontinuierlicher, gradueller Prozess.8 Diskussionen sollten durch prognostische Trigger ausgelöst werden, etwa eine erwartete Lebensdauer von <12 Monaten (ermittelt mit „surprise question“: „Wäre ich überrascht, wenn diese:r Patient:in innerhalb von 12 Monaten sterben würde?“) oder einen Wechsel der Behandlungslinie.8
Routinemäßiges Symptom-Monitoring
Das routinemäßige Erfassen der Symptomlast verbessert nachweislich die Kommunikation und die gesundheitsbezogene Lebensqualität der Patient:innen.21,22 Das Monitoring sollte alle vier Dimensionen der Lebensqualität abdecken: körperlich, psychologisch, sozial und spirituell.8,23
In einer Machbarkeitsstudie berichteten Patient:innen, bei denen Probleme auf der sozialen Dimension überwacht wurden, eine signifikant höhere allgemeine Zufriedenheit mit der Pflege.8 Es ist jedoch eine Herausforderung, die Ergebnisse des Symptom-Monitorings standardisiert und adäquat in der EMR zu dokumentieren.8
Zeitnahes Einbinden des Spezialisierten Palliativteams (SPCT)
Das Hinzuziehen des SPCT ist besonders bei komplexer, multidimensionaler Symptomlast oder auf Wunsch der Patient:innen indiziert.8,24 Es sollte eine routinemäßige Konsultation angeboten werden, wenn eine erwartete Lebensdauer von <3 Monaten (ermittelt mit angepasster „surprise question“) vorliegt.8 Es besteht Konsens, dass sowohl die behandelnden Ärzt:innen (90% Konsens) als auch spezialisierte Pflegekräfte (86% Konsens) Patient:innen über das SPCT informieren sollten.6
Kommunikation als Schlüsselkompetenz
Um die Akzeptanz von PC zu erhöhen, ist eine proaktive, sensitive und graduelle Kommunikation essenziell.8 Kliniker:innen sollten in der Lage sein, ernste Nachrichten zu übermitteln und über Behandlungsziele zu sprechen.25 Patient:innen empfinden es als hilfreich, wenn Ärzt:innen die Dinge beim Namen nennen (z.B. „Tod“ oder „Sterben“)8 und die Worte sorgfältig wählen, da die Formulierung die Reaktion der Patient:innen beeinflusst.8 Kommunikationsstrategien können erlernt werden. Kommunikationsseminare sollten daher verpflichtend für alle sein, die mit unheilbar krebserkrankten Menschen arbeiten.
Literatur:
1 Kaasa S et al.: Integration of oncology and palliative care: a Lancet Oncology Commission. Lancet Oncol 2018; 19(11): e588-e653 2 Schuit AS et al.: Efficacy of the eHealth application Oncokompas, facilitating incurably ill cancer patients to self-manage their palliative care needs: a randomized controlled trial. Lancet Reg Health Eur 2022; 18: 100390 3 Ferrell BR et al.: Integration of palliative care into standard oncology care: American Society of Clinical Oncology Clinical Practice Guideline Update. J Clin Oncol 2017; 35(1): 96-112 4 Blum D et al.: Patterns of integrating palliative care into standard oncology in an early ESMO designated center: a 10-year experience. ESMO open 2021; 6(3): 100147 5 Adamidis F et al.: Timely integration of palliative care. the reality check. A retrospective analysis. Support Care Cancer 2024; 32(8): 518 6 Sepúlveda C et al.: Palliative care: the World Health Organization’s global perspective. J Pain Symptom Manage 2002; 24(2): 91-6 7 Quill TE, Abernethy AP: Generalist plus specialist palliative care-creating a more sustainable model. N Engl J Med 2013; 368(13): 1173-5 8 Heipon CS et al.: Characteristics of timely integration of palliative care into oncology hospital care for patients with incurable cancer: results of a Delphi Study. Support Care Cancer 2024; 32(5): 324 9 Bucklar N et al.: Early integration or last consultation: in-house palliative care involvement for hospitalized patients in tertiary medicine—a retrospective analysis. Support Care Cancer 2025; 33(4): 251 10 Guccione L et al.: Why is advance care planning underused in oncology settings? A systematic overview of reviews to identify the benefits, barriers, enablers, and interventions to improve uptake. Front Oncol 2023; 13: 1040589 11 Horlait M et al.: What are the barriers faced by medical oncologists in initiating discussion of palliative care? A qualitative study in Flanders, Belgium. Support Care Cancer 2016; 24(9): 3873-81 12 Ingersoll LT et al.: The contagion of optimism: the relationship between patient optimism and palliative care clinician overestimation of survival among hospitalized patients with advanced cancer. Psychooncology 2019; 28(6): 1286-92 13 van den Berg BM et al.: Clinicians’ experiences, perspectives, barriers, and facilitators of integrating palliative care into haematological cancer care: a qualitative interview study. Support Care Cancer 2025; 33(8): 697 14 El-Jawahri A et al.: Palliative and end-of-life care for patients with hematologic malignancies. J Clin Oncol 2020; 38(9): 944-53 15 Wedding U: Palliative care of patients with haematological malignancies: strategies to overcome difficulties via integrated care. Lancet Healthy Longev 2021; 2(11): e746-53 16 An A, Hui D: Immunotherapy versus hospice: treatment decision-making in the modern era of novel cancer therapies. Curr Oncol Rep 2022; 24(3): 285-94 17 Franzoi MA et al.: Implementation of a remote symptom monitoring pathway in oncology care: analysis of real-world experience across 33 cancer centres in France and Belgium. Lancet Reg Health Eur 2024; 44 18 Hui D et al.: Timely palliative care: personalizing the process of referral. Cancers 2022; 14(4): 1047 19 Rietjens JAC et al.: Definition and recommendations for advance care planning: an international consensus supported by the European Association for Palliative Care. Lancet Oncol 2017; 18(9): e543-51 20 Brinkman-Stoppelenburg A et al.: The effects of advance care planning on end-of-life care: a systematic review. Palliat Med 2014; 28(8): 1000-25 21 Basch E et al.: Symptom monitoring with patient-reported outcomes during routine cancer treatment: a randomized controlled trial. J Clin Oncol 2016; 34(6): 557-65 22 Basch E et al.: Effect of electronic symptom monitoring on patient-reported outcomes among patients with metastatic cancer: arandomized clinical trial. JAMA 2022; 327(24): 2413-22 23 Raijmakers NJH et al.: Health-related quality of life among cancer patients in their last year of life: results from the PROFILES registry. Support Care Cancer 2018; 26(10): 3397-404 24 Grant M et al.: A systematic review of classifications systems to determine complexity of patient care needs in palliative care. Palliat Med 2021; 35(4): 636-50 25 Crowley F et al.: American Society of Clinical Oncology guideline update on palliative care for patients with cancer: addressing the reality gap. Cancer 2025; 131(1): e35656
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...