Therapiestandard der CLL 2021 – hat die Chemotherapie noch einen Platz?
Autor:
FA Dr. Manuel Orlinger
Interne I: Internistische Onkologie und Hämatologie
Ordensklinikum Linz Barmherzige Schwestern
Die Therapie der chronischen lymphatischen Leukämie (CLL) hat sich in den letzten Jahren deutlich verändert und zielgerichtete Therapien können fast ohne Rücksicht auf Alter oder Fitnessgrad eingesetzt werden. Die Schwierigkeit besteht in der Auswahl der optimalen Therapie für den einzelnen Patienten und auch die Chemotherapie kann theoretisch noch eine Rolle spielen.
Keypoints
-
Zur Erstlinientherapie der CLL stehen mit den zugelassenen BTK-Inhibitoren sowie mit Venetoclax in Kombination mit Obinutuzumab mehrere zielgerichtete Therapieoptionen zur Verfügung, welche unabhängig von Alter und Fitness eingesetzt werden können.
-
Die Therapieauswahl muss anhand bestehender Komorbiditäten sowie unter Rücksichtnahme auf mögliche Nebenwirkungen, potenzielle Medikamenteninteraktionen und Patientenpräferenz erfolgen.
-
Die Chemotherapie mit FCR kann bei jungen Patienten mit IGHV-Hypermutation und ohne sonstige Risikofaktoren noch zum Einsatz kommen, um ein längeres therapiefreies Intervall zu ermöglichen.
Die CLL ist als häufigste Leukämie des Erwachsenenalters durch ein heterogenes Krankheitsbild geprägt, wobei einerseits jahrelange Phasen der Observanz möglich sind, während andererseits Fälle mit aggressiverem Verlauf zu beobachten sind.
Die Abschätzung der Prognose gelingt anhand definierter biologischer Risikofaktoren (IGHV-Mutationsstatus, TP53-Mutation, del(17p13), komplexer Karyotyp), wovon einige auch Eingang in etablierte Risiko-Scores (CLL-IPI)1 gefunden haben. Trotz des Wissens um biologische Risikofaktoren wird die Indikation zur Therapieeinleitung weiterhin anhand klinischer Faktoren (Binet-Stadium, massive oder symptomatische Splenomegalie bzw. Lymphadenopathie, Lymphozytenverdoppelungszeit, refraktäre Immunzytopenie, B-Symptomatik)2 gestellt. Die molekularbiologische Diagnostik sollte spätestens vor Therapieeinleitung erfolgen, da die Therapieauswahl unter Umständen davon beeinflusst wird.
An therapeutischen Optionen stehen aktuell mehrere Optionen zielgerichteter Therapien zur Verfügung (BCL-2-Inhibition, Hemmung des B-Zell-Rezeptor-Signalwegs, Kombination mit monoklonalen Anti-CD20-Antikörpern), die Kombination aus Chemotherapie und Anti-CD20-Antikörpern kommt noch selten zum Einsatz.
Hemmung des B-Zell-Rezeptor-Signalwegs
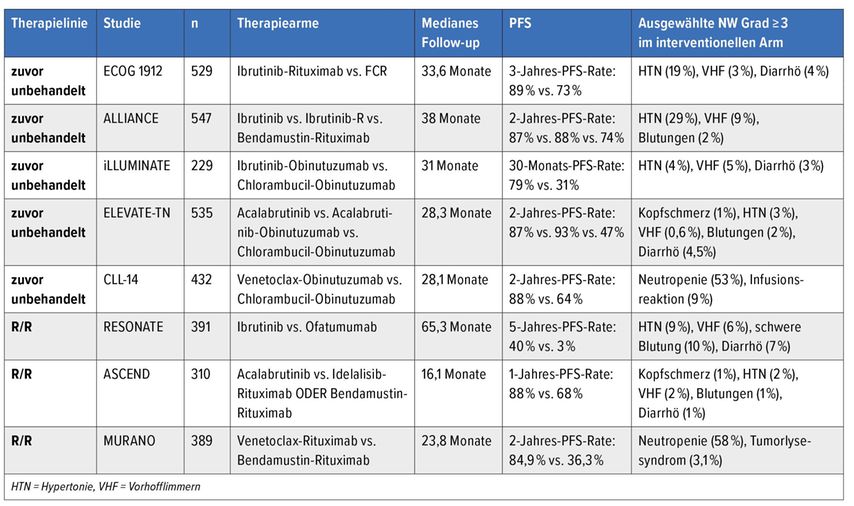
Die Zulassung von Inhibitoren der Bruton-Tyrosinkinase (BTK) hat die Therapie der CLL wesentlich verändert. Im Rahmen der ECOG-1912-Studie wurden ein verlängertes progressionsfreies Überleben (PFS) und Gesamtüberleben (OS) beim Einsatz von Ibrutinib in Kombination mit Rituximab im Vergleich zur Chemo-Immuntherapie mit FCR (Fludarabin, Cyclophosphamid, Rituximab) bei jüngeren, fitten, unbehandelten Patienten ohne Nachweis einer TP53-Mutation oder del(17p) gezeigt, wobei kein signifikanter Unterschied bzgl. PFS und OS bei Patienten mit IGHV-Hypermutation nachgewiesen werden konnte.3
Auf ähnliche Weise wurde im Rahmen der ALLIANCE-202-Erstlinien-Studie bei älteren Patienten (inkl. Patienten mit TP53-Mutation und del[17p]) eine Verlängerung des PFS durch den Einsatz von Ibrutinib (mit oder ohne Rituximab) im Vergleich zur Therapie mit Bendamustin-Rituximab nachgewiesen, wobei kein signifikanter Unterschied zwischen den Ibrutinib-Armen mit bzw. ohne Rituximab gezeigt werden konnte.4
Schließlich konnte im Rahmen der iLLUMINATE-Studie auch die verbesserte Effektivität und Machbarkeit einer Therapie mit Ibrutinib in Kombination mit Obinutuzumab bei älteren, unfitten Patienten im Vergleich zu Obinutuzumab-Chlorambucil gezeigt werden.5
Als alternativer zugelassener BTK-Inhibitor steht seit Kurzem Acalabrutinib zur Verfügung, dieser führte im Zuge der ELEVATE-TN-Studie als Monotherapie oder in Kombination mit Obinutuzumab zu einer deutlichen Verlängerung des PFS im Vergleich zur Therapie mit Chlorambucil-Obinutuzumab.6
Auch in späteren Therapielinien konnte die Effektivität der genannten BTK-Inhibitoren gezeigt werden, wobei Ibrutinib im Rahmen von RESONATE-1 mit Ofatumumab verglichen wurde, Acalabrutinib im Rahmen von ASCEND mit Bendamustin-Rituximab oder Idelalisib-Rituximab.7,8
Neben einer Inhibition der Bruton-Tyrosinkinase greift auch eine Hemmung von PI3K in den B-Zell-Rezeptor-Singalweg ein, eine zugelassene Therapieoption stellt der PI3K-Inhibitor Idelalisib in Kombination mit Rituximab dar, wobei diese Kombination ab der zweiten Therapielinie oder bei Hochrisikopatienten mit Vorliegen von Kontraindikationen für eine andere Therapie zugelassen ist.9 Beim Einsatz von Idelalisib sind eine Prophylaxe gegen eine Pneumocystis-jirovecii-Pneumonie (PjP) sowie ein laufendes Screening bezüglich Zytomegalievirus-Infektion unbedingt erforderlich.2
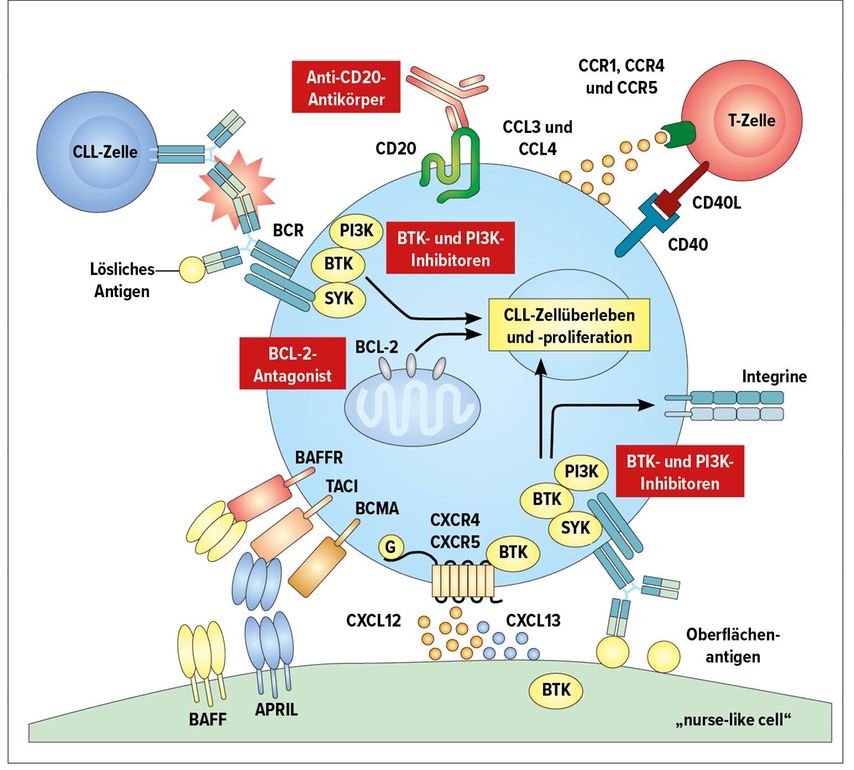
Abb. 1: Faktoren in der Mikroumgebung der CLL-Zelle aktivieren Wachstums- und Überlebenspfade, die mit neuartigen Therapeutika angegangen werden können (adaptiert nach: Burger JA & O’Brien S)13
Hemmung von BCL-2
BCL-2 und die gleichnamige BCL-2-Proteinfamilie spielen bei der Regulation der Apoptose eine entscheidende Rolle, eine Hemmung von BCL-2 durch Venetoclax führt daher zu proapoptotischen Effekten. Neben den BTK-Inhibitoren steht damit eine zweite zielgerichtete Therapieoption zur Verfügung, wobei der Einsatz in der Regel in Kombination mit einem Anti-CD20-Antikörper erfolgt und im Gegensatz zur BTK-Inhibitor-Therapie (welche als Dauertherapie angelegt ist) eine begrenzte Therapiedauer möglich ist.
Im Rahmen der CLL-14-Erstlinienstudie wurde die Effektivität einer auf 12 Monate begrenzten Therapie mit Venetoclax-Obinutuzumab im Vergleich zur Therapie mit Obinutuzumab-Chlorambucil bei älteren Patienten mit Begleiterkrankungen untersucht, wobei eine deutliche Verlängerung des PFS erreicht werden konnte und im Venetoclax-Arm eine hohe Rate an Negativität bzgl. einer minimalen Resterkrankung (MRD) gezeigt wurde.10 Dies führte zur Zulassung dieser Kombination für alle Patienten mit CLL und Therapieindikation, unabhängig vom Alter oder von Komorbiditäten.
Die Effektivität in späteren Therapielinien konnte im Rahmen der MURANO-Studie gezeigt werden, wobei die Kombination von Venetoclax mit Rituximab zu einer deutlichen Verlängerung von PFS und OS im Vergleich zu Bendamustin-Rituximab führte. In diesem Fall war die Therapiedauer im Venetoclax-Arm auf 24 Monate begrenzt.11
Rolle der Chemotherapie
Aufgrund der Entwicklungen auf dem Gebiet der zielgerichteten Therapien hat die klassische Chemotherapie in Kombination mit Anti-CD20-Antikörpern deutlich an Stellenwert verloren. Die Patientengruppe, welche am ehesten von einer Chemoimmuntherapie profitiert, ist die der jungen, fitten Patienten mit IGHV-Mutation und ohne Risikofaktoren. In diesem Kollektiv kann mit einer relativ kurzen Therapie mit FCR häufig ein langes progressions- und therapiefreies Intervall erreicht werden. Die potenziellen Nebenwirkungen dieser Therapie müssen im Vergleich zu anderen Alternativen mit den betroffenen Patienten besprochen werden und eine sorgfältige Abwägung sollte erfolgen.
Andere chemotherapeutische Optionen (Bendamustin, Chlorambucil) können in Einzelfällen noch zum Einsatz kommen, stellen jedoch für den Großteil der Patienten keinen Therapiestandard mehr dar.
Therapiewahl anhand von Komorbiditäten, Nebenwirkungen und Patientenpräferenz
Somit stehen aktuell verschiedene Therapieoptionen zur Verfügung, welche (mit Ausnahme der Chemoimmuntherapie mit FCR) relativ unabhängig von Alter oder Fitness angewandt werden können, sich jedoch durch potenzielle Nebenwirkungen unterscheiden.
Als relevante Nebenwirkungen der BTK-Inhibitor-Therapie sollen vor allem Herzrhythmusstörungen (am häufigsten Vorhofflimmern) sowie Blutungskomplikationen erwähnt werden, sodass der Einsatz von BTK-Inhibitoren bei Notwendigkeit einer Antikoagulation bzw. Einnahme von Thrombozytenaggregationshemmern nur nach sorgfältiger Abwägung erfolgen sollte. Als typische Nebenwirkung von Acalabrutinib wurden Kopfschmerzen beschrieben, diese sprechen gut auf eine Therapie mit Koffein an.
Beim Einsatz des BCL-2 Inhibitors Venetoclax ist eine langsame Dosissteigerung zu Beginn der Therapie erforderlich, um das Auftreten eines Tumorlyse-Syndroms zu verhindern, zudem treten gehäuft Zytopenien auf, welche den Einsatz von Wachstumsfaktoren oder Dosisreduktionen erforderlich machen können.12
Neben den potenziellen Nebenwirkungen unterscheiden sich die zielgerichteten Therapien auch durch die Therapiedauer (Dauertherapie bei BTK-Inhibitoren, begrenzte Therapiedauer bei Venetoclax-Therapie), dem gegenüberzustellen ist die einfachere Applikation der BTK-Inhibitoren zu Beginn der Therapie.
Zukünftig wird möglicherweise die Kombination aller genannten zielgerichteten Optionen (BTK-Inhibition, BCL-2-Inhibition, Anti-CD20-Antikörper) einen neuen Standard darstellen, auf Ergebnisse laufender Phase-III-Studien muss jedoch zum aktuellen Zeitpunkt noch gewartet werden. Ebenso wird derzeit die Therapie mit weiterentwickelten BTK-Inhibitoren sowie CAR-T-Zellen im Rahmen von Studien untersucht.
Literatur:
1 International CLL-IPI Working Group: An international prognostic index for patients with chronic lymphocytic leukaemia (CLL-IPI): a meta-analysis of individual patient data. Lancet Oncol 2016; 17(6): 779-90 2 Onkopedia: Leitlinie CLL. Online unter: https://www.onkopedia.com/de/onkopedia/guidelines/chronische-lymphatische-leukaemie-cll/@@guideline/html/index.html 3 Shanafelt TD et al.: Ibrutinib–rituximab or chemoimmunotherapy for chronic lymphocytic leukemia. N Engl J Med 2019; 381(5): 432-43 4Woyach JA et al.: Ibrutinib regimens versus chemoimmunotherapy in older patients with untreated CLL. N Engl J Med 2018; 379(26): 2517-28 5 Moreno C et al.: Ibrutinib plus obinutuzumab versus chlorambucil plus obinutuzumab in first-line treatment of chronic lymphocytic leukaemia (iLLUMINATE): a multicentre, randomised, open-label, phase 3 trial. Lancet Oncol 2019; 20(1): 43-56 6Sharman JP et al.: ELEVATE TN: Phase 3 study of acalabrutinib combined with obinutuzumab (O) or alone vs O plus chlorambucil (Clb) in patients (Pts) with treatment-naive chronic lymphocytic leukemia (CLL). Blood 2019; 134 (Suppl 1): 31 7 Byrd JC et al.: Ibrutinib versus ofatumumab in previously treated chronic lymphoid leukemia. N Engl J Med 2014; 371(3): 213-23 8 Ghia P et al.: ASCEND: phase III, randomized trial of acalabrutinib versus idelalisib plus rituximab or bendamustine plus rituximab in relapsed or refractory chronic lymphocytic leukemia. J Clin Oncol 2020; 38(25): 2849-61 9 Furman RR et al.: Idelalisib and rituximab in relapsed chronic lymphocytic leukemia. NEngl J Med 2014; 370(11): 997-1007 10 Al-Sawaf O et al.: Venetoclax plus obinutuzumab versus chlorambucil plus obinutuzumab for previously untreated chronic lymphocytic leukaemia (CLL14): follow-up results from a multicentre, open-label, randomised, phase 3 trial. Lancet Oncol 2020; 21(9): 1188-200 11 Seymour JF et al.: Venetoclax plus rituximab is superior to bendamustine plus rituximab in patients with relapsed/refractory chronic lymphocytic leukemia — results from pre-planned interim analysis of the randomized phase 3 murano study. Blood 2017; 130(suppl. 1): LBA-2 12 Awan FT et al.: Current perspectives on therapy for chronic lymphocytic leukemia. Am Soc Clin Oncol Educ Book Actions 2020; 40: 320-29 13Burger JA, O‘Brien S: Evolution of CLL treatment — from chemoimmunotherapy to targeted and individualized therapy. Nat Rev Clin Oncol. 2018; 15(8): 510-27 14 Fakhri B, Andreadis C: The role of acalabrutinib in adults with chronic lymphocytic leukemia. Ther Adv Hematol 2021; 12: 2040620721990553.
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...