„Science from the Heart of Europe“ – innovative Studienstarts der ABCSG
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Neben der Planung und Durchführung von klinischen Studien ist die Weitergabe wissenschaftlicher Erkenntnisse ein zentrales Anliegen der Austrian Breast & Colorectal Cancer Study Group (ABCSG): die Veröffentlichung von Studienergebnissen in führenden internationalen Fachmagazinen sowie die kontinuierliche Fortbildung medizinischen Fachpersonals. Auch 2026 verantwortet die ABCSG mehrere Forschungsprojekte und ist an weiteren maßgeblich beteiligt. Vier neue Studien mit laufendem Patient:inneneinschluss werden im Folgenden vorgestellt.
ABCSG 61/TEODOR
-
Neoadjuvant TrEatment Optimization driven by ctDNA and endocrine Responsiveness
-
Studienstart: Q3/2025
-
Coordinating Investigators: Michael Gnant, Wien; Daniel Egle, Innsbruck
-
Stichprobenumfang: 256 (national)
-
Sponsor: ABCSG
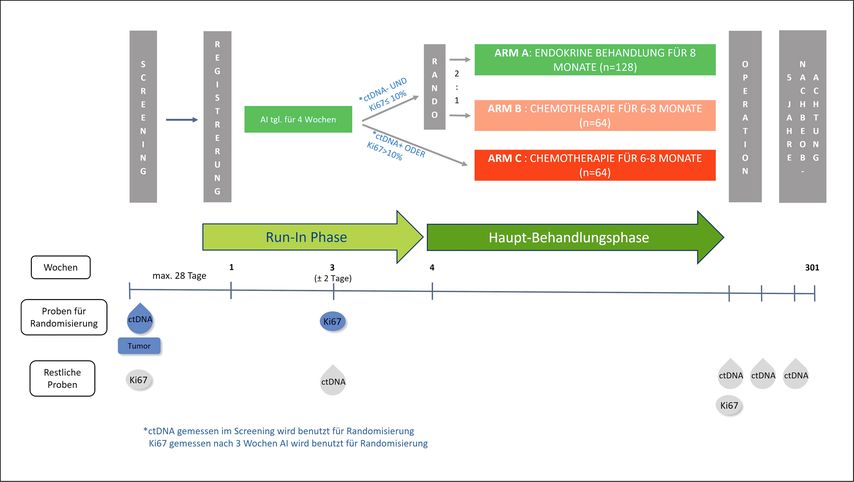
TEODOR ist eine prospektive, randomisierte, offene, multizentrische Phase-II-Studie, die bei Hormonrezeptor-positiven (HR+), HER2-negativen (HER2–), ctDNA-negativen und endokrin sensitiven Patient:innen mit frühem und lokal fortgeschrittenem Brustkrebs eine neoadjuvante endokrine Therapie im Vergleich zu einer Chemotherapie untersucht.
Im Juli 2025 startete die Rekrutierung in die Studie ABCSG 61/TEODOR. Die erste Teilnehmerin wurde im August 2025 an der Univ.-Klinik für Frauenheilkunde der Medizinischen Universität Innsbruck (MUI) registriert. Insgesamt nehmen 14 Zentren in Österreich an der Studie teil.
TEODOR beschäftigt sich mit dem Vergleich von neoadjuvanter endokriner Therapie mit neoadjuvanter Chemotherapie, beides gemäß Standard of Care, in der Behandlung von ER-positiven (ER+), HER2– Patient:innen ohne detektierbare ctDNA, die endokrin responsiv sind.
Der primären Studienhypothese nach ist die Effektivität endokriner Therapie in diesem Patient:innenkollektiv zumindest vergleichbar mit jener einer neoadjuvanten Chemotherapie, was anhand des „Preoperative Endocrine Prognostic Index“(PEPI)-Scores gemessen wird, bei gleichzeitig vorteilhafterem Verträglichkeitsprofil und höherer Lebensqualität der endokrin behandelten Patient:innen.
An der nationalen Phase-II-Studie nehmen insgesamt 14 österreichische Zentren teil. Geplant ist die Einbringung von 256 Patient:innen. Nach Abschluss der etwa acht- bis zehnmonatigen Therapiephase ist eine Nachbeobachtungszeit von fünf Jahren vorgesehen. Koordiniert wird die Studie von Univ.-Prof. Dr. Michael Gnant, Medizinische Universität Wien (MUW), und LOA Dr. Daniel Egle, MUI.
Im translationalen Programm der Studie wird die ctDNA im Blut der Studienteilnehmer:innen zu mehreren Zeitpunkten zwischen Behandlungsstart und fünfähriger Nachbeobachtungsphase mittels SignateraTM-Test monitiert, was u.a. Aufschluss über den Zusammenhang von ctDNA-Detektion und Behandlungs-Outcome liefern soll.
ABCSG 63/ERIKA
-
Elacestrant and RIbociclib in Ki67-tested endocrine responsive breAst cancer
-
Studienstart: Q3/2025
-
Coordinating Investigators: Christian Singer, Wien; Michael Gnant, Wien
-
Stichprobenumfang: 120 (Österreich, Deutschland)
-
Sponsor: ABCSG
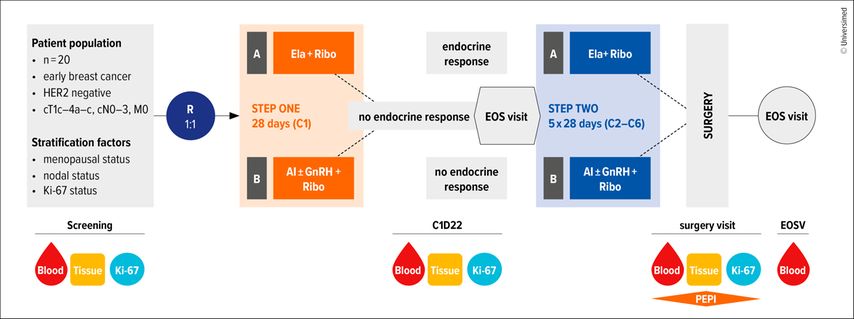
ERIKA ist eine offene, zweiarmige, randomisierte Phase-II-Studie mit Elacestrant plus Ribociclib vs. Aromataseinhibitor (plus GnRH-Agonist bei prä- und perimenopausalen Frauen und Männern) plus Ribociclib als neoadjuvante Therapie für endokrin responsiven HER2– Brustkrebs im Frühstadium.
In der Studie ABCSG 63/ERIKA konnte das erste Prüfzentrum im August 2025 für die Zentrumsfreischaltung aktiviert werden. Die erste Patientin wurde im September 2025 an der Medizinischen Universität Graz (Gynäkologie) eingeschlossen.
In die vorliegende Studie werden Patient:innen mit ER+, HER2– frühem Brustkrebs eingeschlossen. Das therapeutische Potenzial und die Sicherheit einer Kombination aus dem oral verfügbaren SERD Elacestrant und dem CDK4/6-Inhibitor Ribociclib werden evaluiert, wobei die Patient:innen im Arm A Elacestrant und Ribociclib und im Arm B einen Aromataseinhibitor und Ribociclib erhalten. Der primäre Studienendpunkt ist als der Anteil des PEPI-Scores von 0 zum Zeitpunkt der Operation definiert.
In Summe sollen 120 Patient:innen an 18 Zentren (10 in Österreich, 8 in Deutschland) in die ABCSG-63/ERIKA-Studie eingeschlossen werden, die Rekrutierungsdauer ist für etwa ein Jahr angesetzt.
ABCSG 65/DEFINITIVE
-
Diagnostic HER2DX-guided treatment For patIeNts wIth early-stage HER2-posiTIVE breast cancer
-
Studienstart: 11/2024 (global), 07/2025 (national)
-
Coordinating Investigator AT: Apl. Prof. Priv.-Doz. Dr. Simon Gampenrieder, Salzburg
-
Stichprobenumfang: 315 (global), 70 (national)
-
Sponsor: FRCB-IDIBAPS
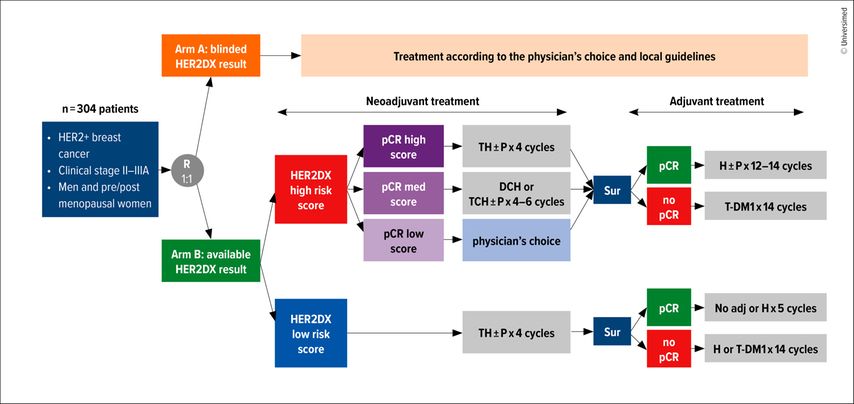
DEFINITIVE ist eine internationale, multizentrische, prospektive, zweiarmige, randomisierte, offene Phase-III-Studie, die nachweisen soll, dass personalisierte Behandlungsentscheidungen bei HER2+ Brustkrebs im Frühstadium mithilfe des HER2DX®-Diagnosetests die Lebensqualität verbessern, ohne die Ergebnisse und Überlebensraten zu beeinträchtigen.
Die DEFINITIVE-Studie wird von der Europäischen Kommission unterstützt. Sie zielt darauf ab, 315 Patient:innen mit frühem HER2+ Brustkrebs in sieben Ländern einzuschließen. Österreich beteiligt sich mit insgesamt neun Zentren an dieser wichtigen klinischen Studie.
Die globale Koordination liegt bei der spanischen Studiengruppe SOLTI, die ABCSG ist für die Durchführung in Österreich verantwortlich. Hier ist die Einbringung von 61 Patient:innen geplant. Nationaler Studienleiter ist Apl. Prof. Priv.-Doz. Dr. Simon Gampenrieder, Salzburg.
DEFINITIVE untersucht, ob der innovative Diagnosetest HER2DX®, entwickelt von Reveal Genomics®, eine präzisere und personalisierte Behandlung von Patient:innen mit frühem HER2+ Brustkrebs ermöglicht. Der Test basiert auf künstlicher Intelligenz und nutzt sowohl biologische als auch klinische Informationen des Tumors. Das Ziel der Studie ist es, zu untersuchen, ob eine auf HER2DX® basierende, personalisierte Therapie die gesundheitsbezogene Lebensqualität (HRQoL) der Patient:innen verbessern kann – bei gleichbleibender Sicherheit, Wirksamkeit und ohne negative Auswirkungen auf das Überleben.
Ein bedeutender Meilenstein in der globalen Studie wurde im August 2025 erreicht, als das das Ordensklinikum Linz GmbH BHS als erstes Zentrum in Österreich aktiviert wurde.
NIS ABCSG 67N/CAROLEEN
-
A non-interventional study for riboCiclib in combination with an Aromatase inhibitor for adjuvant treatment in patients with HR+/HER2- eaRly breast cancer at high risk of recurrence tO evaLuate rEal-world EffectiveNess, safety profile, patient compliance and quality of life
-
Studienstart: Q1/2025 (global), Q4/2025 (national)
-
Coordinating Investigator AT: Christian Singer, Österreich
-
Stichprobenumfang: 3250 (Österreich, Deutschland)
-
Sponsor: Novartis
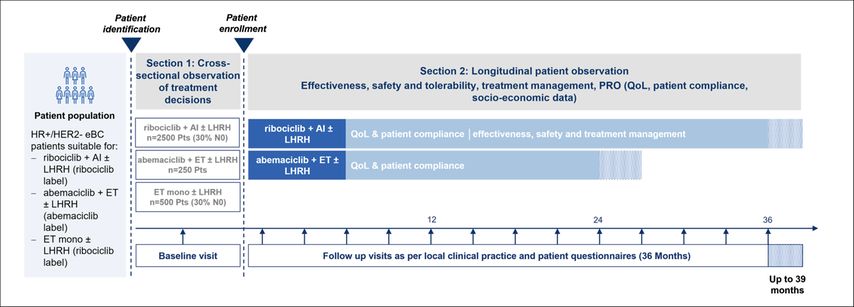
CAROLEEN ist eine nichtinterventionelle Studie zu Ribociclib in Kombination mit einem Aromatasehemmer zur adjuvanten Behandlung von Patient:innen mit HR+/HER2– frühem Mammakarzinom mit hohem Rezidivrisiko zur Bewertung der Wirksamkeit, des Sicherheitsprofils, der Therapie-Compliance und der Lebensqualität.
Die Studie wird in Österreich und in Deutschland von Novartis als Sponsor durchgeführt und von der ABCSG in Österreich koordiniert. In Deutschland startete CAROLEEN bereits mit Q1/2025 und die Einbringungsdauer ist laut Protokoll mit zwei Jahren angesetzt (voraussichtlich bis Q1/2027).
Die NIS wird in Österreich unter der Leitung von PI Univ.-Prof. Dr. Christian Singer (Universitätsklinik Wien) durchgeführt. Es ist geplant, dass in Österreich 16 Prüfzentren teilnehmen, die in Summe 300 Patient:innen einbringen sollen. Mit dem Sanatorium Hera, Wien, wurde im September 2025 das erste Zentrum initiiert und mittlerweile auch für die Einbringung aktiviert.
ABCSG-Präsident Univ.-Prof. Dr. Michael Gnant zu den aktuellen Studien der ABCSG
„Gerade in einem so dynamischen Umfeld wie der modernen Brustkrebstherapie können nur gut geplante, randomisierte Studien verlässliche Evidenz schaffen. Deshalb starteten letzten Herbst die Studien ABCSG 61/TEODOR, ABCSG 63/ERIKA, ABCSG 65/DEFINITIVE und NIS ABCSG 67N/CAROLEEN, und 2026 werden dann die Studie ABCSG 64/neoGRACE sowie mehrere weitere Forschungsprojekte der ABCSG starten – von Biomarker-gesteuerten Ansätzen über Deeskalationskonzepte bis hin zu Assay-gestützten Protokollen –, um den zentralen Herausforderungen von heute und morgen zu begegnen. [...] Diese nun praktisch zeitgleich initiierten Studienprojekte unterstreichen den Innovationsgeist, die wissenschaftliche Exzellenz und das unermüdliche Engagement der ABCSG, die Versorgung von Brustkrebspatient:innen auch weiter nachhaltig zu verbessern.“
Über die ABCSG
Die ABCSG (Austrian Breast & Colorectal Cancer Study Group) ist Österreichs größte und bekannteste akademische Forschungsorganisation, die international erfolgreich klinische Studien zu Brust- und Darmkrebs durchführt – seit 2013 auch Projekte zu Bauchspeicheldrüsenkrebs. Ziel der ABCSG ist es, wissenschaftlich fundierte Fortschritte in der Diagnostik, Therapie und Nachsorge zu erzielen und so die Lebensqualität und die Überlebenschancen von Patient:innen langfristig zu verbessern. Seit der Gründung im Jahr 1984 haben knapp 30000 Patient:innen weltweit an ABCSG-Studien teilgenommen.
Ein zentrales Anliegen der ABCSG ist die Weitergabe wissenschaftlicher Erkenntnisse: Die Veröffentlichung von Studienergebnissen in führenden internationalen Fachmagazinen sowie die kontinuierliche Fortbildung medizinischen Fachpersonals zählen zu den festen Säulen unserer Arbeit.
Dafür organisiert die ABCSG regelmäßig eigene Formate wie etwa die große Jahrestagung mit jährlich rund 300 Teilnehmer:innen, den „Interdisziplinären Mamma Diskurs“, „Science & Cases“, die „Experts on Tour“-Reihe, das Format „abcsg in touch“ der Task Force „Future Now“ speziell für den medizinischen Nachwuchs
sowie Online-Angebote wie Webinare und E-Learnings. Onkologisch tätige Ärzt:innen profitieren vom interdisziplinären Wissenstransfer und dem direkten Zugang zu neuesten Studiendaten und praxisrelevanten Empfehlungen. Weitere Informationen finden Sie unter: www.abcsg.org
Abkürzungen:
adj, adjuvant; AI, Aromase-Inhibitor; ctDNA, zirkulierende Tumor-DNA; DHC ± P, Docetaxel/Carboplatin/Trastuzumab ± Pertuzumab; eBC, früher Brustkrebs; Ela, Elacestrant; ET, endokrine Therapie; EOS, „end of study“; GnRH, „Gonadotropin-releasing hormone“; H ± P, Trastuzumab ± Pertuzumab; LHRH, “luteinizing hormone-releasing hormone”; P, Pertuzumab; pCR, pathologische Komplettremission; PEPI, „preoperative endocrine prognostic index“; QoL, Lebensqualität; Ribo, Ribociclib; Sur, Operation; TCH ± P, Paclitaxel/Carboplatin/Trastuzumab ± Pertuzumab; TH ± P, Paclitaxel/Trastuzumab ± Pertuzumab
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...