Onkologisches Outcome der Resektion von Lebermetastasen
Autoren:
Priv.-Doz. Dr. Andreas Lambertz
Univ.-Prof. Dr. med. Ulf P. Neumann
Klinik für Allgemein-, Viszeral- und Transplantationschirurgie
Uniklinik RWTH Aachen
E-Mail: uneumann@ukaachen.de
Resektable kolorektale Lebermetastasen sollten primär operiert werden. Dies gilt auch bei limitiertem extrahepatischem Tumorbefall. Bei initialer Irresektabilität kann die Zahl derPatienten mit sekundär resektablenMetastasen durch die Anwendung multimodaler Therapiekonzepte mit einer hochaktiven Induktionschemotherapie signifikant erhöht werden. Auch bei Rezidivmetastasen sollte die Entscheidung für eine Resektion unter den gleichen Aspekten wie bei der primären Metastasierung getroffen werden, weil sich nach erneuter vollständiger Resektion weiterhin gute onkologische Ergebnisse erzielen lassen. Dies begründet den Trend zur Anwendung parenchymsparender Resektionsverfahren in der kolorektalen Lebermetastasenchirurgie.
Keypoints
-
Patienten mit primär resektablen kolorektalen Lebermetastasen haben nach R0-Resektion mit einem medianen 5-Jahres-Überleben von über 50% eine günstige onkologische Prognose. Dies gilt auch bei limitiertem extrahepatischem Tumorbefall.
-
Insbesondere grenzwertig resektable Patienten sollten in einem spezialisierten Zentrum behandelt werden, damit optimale onkologische Ergebnisse erzielt werden können.
-
Auch bei Rezidivmetastasen sollte die Entscheidung für die Resektion unter den gleichen Aspekten wie bei der primären Metastasierung getroffen werden, weil sich nach erneuter vollständiger Resektion weiterhin gute onkologische Ergebnisse erzielen lassen.
-
Bei initialer Irresektabilität kann die Zahl sekundär resektabler Patienten durch die Anwendung multimodaler Therapiekonzepte mit einer hochaktiven Induktionschemotherapie signifikant erhöht werden.
Zum Zeitpunkt der Erstdiagnose eines kolorektalen Karzinoms haben ca. 20% der Patienten bereits hepatische Metastasen. Grundsätzlich ist eine Unterscheidung zwischen primär resektablen und primär nicht resektablen Lebermetastasen für die Festlegung des weiteren onkologischen Konzeptes von entscheidender Bedeutung. Diese Einteilung sollte initial in einer interdisziplinären Tumorkonferenz unter Beteiligung eines erfahrenen Leberchirurgen erfolgen.
Bei den primär resektablen Lebermetastasen hat das operative Vorgehen nach wie vor oberste Priorität. Mit einem 5-Jahres-Überleben von im Median mehr als 50% haben die betroffenen Patienten eine günstige onkologische Prognose.1 Die entscheidende Voraussetzung hierfür ist, dass eine vollständige Tumorentfernung erreicht werden kann. Dies gilt auch bei limitiertem extrahepatischem Tumorbefall. Hier konnte für Patienten mit Lungenmetastasen mit einem medianen Überleben von 45 Monaten die günstigste Prognose gezeigt werden. Bei peritonealem oder paraaortalem Lymphknotenbefall reduzieren sich die medianen Überlebensraten auf 29 bzw. 26 Monate.2
Leberfunktion prä- und postoperativ
Im Gegensatz zu früheren Überzeugungen sind heute also extrahepatische Tumormanifestationen im oligometastasierten Stadium sowie hepatische Metastasenanzahl und -größe nicht mehr als Kontraindikationen zum operativen Vorgehen zu werten. Der entscheidende limitierende Faktor ist jedoch die postoperativ zu erwartende (Rest-)Leberfunktion, sodass diese präoperativ ausführlich evaluiert werden muss. Hierzu stehen neben laborchemischen auch bildgebende und apparative Verfahren wie der LiMAx-Test zur Verfügung.3,4 In der Regel sollten Volumen- mit Funktionsmessungen kombiniert werden. Während im gesunden Lebergewebe Resektionen von bis zu 80% des Lebervolumens komplikationsarm möglich sind, werden die operativen Möglichkeiten durch eine Reduktion der Leberfunktion erheblich eingeschränkt. Auch bei eingeschränkter Leberfunktion sind Resektionen aber selbst bei Patienten im Child-Stadium B in limitiertem Ausmaß möglich. Insbesondere Leberverfettungen über 60% scheinen dabei mit einer deutlichen Erhöhung der Morbidität nach Leberresektionen vergesellschaftet zu sein, schließen ein operatives Vorgehen jedoch nicht grundsätzlich aus.5 Auch Faktoren wie eine präoperativ vorhandene Cholestase bei zentraler Tumorlokalisation oder durchgeführte Chemotherapien führen zu einer Reduktion der postoperativen Leberregeneration und zu erhöhten postoperativen Komplikationsraten.6 Wenn also präoperativ die Suffizienz des postoperativ verbleibenden Lebervolumens oder dessen Funktion unklar ist, sollten beide Faktoren möglichst optimiert werden. Neben der Beseitigung einer bestehenden Cholestase stehen zur Induktion einer Leberhypertrophie neben der interventionellen Option der Pfortaderembolisation (PVE)7 auch mehrzeitige operative Verfahren wie der In-situ-Split („associating liver partition with portal vein ligation for staged hepatectomy“, ALPPS) zur Verfügung.8 Hierbei wird die Pfortader des tumortragenden Leberanteils operativ unterbunden, während die arterielle Versorgung erhalten bleibt. Da beide Leberanteile nach Parenchymdissektion anschließend in situ verbleiben, kann auch der tumortragende Anteil weiterhin zur Leberfunktion beitragen. Während die Pfortaderembolisation zur Induktion einer Leberhypertrophie heute in Zentren fest etabliert ist, kommt der In-situ-Split bei technisch nicht durchführbarer PVE, bei Ausbleiben einer erforderlichen Leberhypertrophie nach PVE, aber auch als primärer Ansatz zum Einsatz. Insofern sollten insbesondere Patienten mit grenzwertig resektablen Metastasenin einem spezialisierten Zentrum behandelt werden, damit optimale onkologische Ergebnisse erzielt werden können.
Behandlung der Rezidivmetastasen nach Resektion
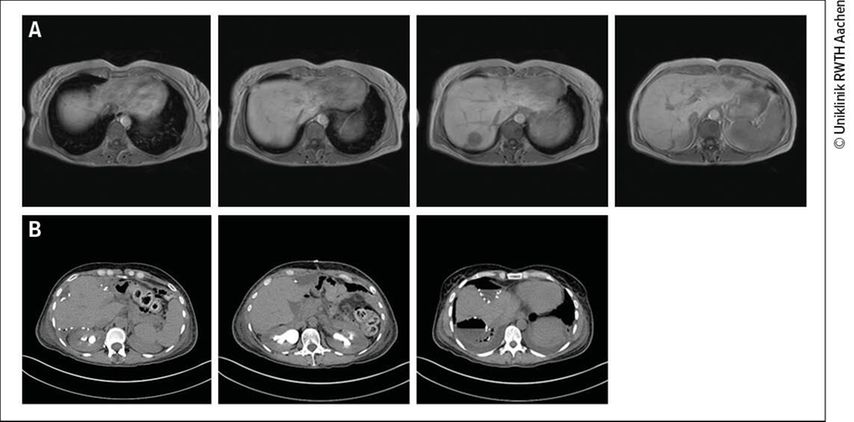
Nach einer kurativen Resektion treten bei ca. einem Drittel der Patienten im Verlauf wieder isolierte hepatische Rezidivmetastasen auf. Nach erneuter vollständiger Resektion zeigen sich in retrospektiven Analysen 3-Jahres-Überlebensraten von über 60% und 5-Jahres-Überlebensraten von über 40% bei Raten an „Major“-Komplikationen von 5% und gleichwertigen onkologischen Ergebnissen.9 Insofern sollte die Entscheidung für die Resektion beim Rezidiv unter den gleichen Aspekten wie bei der primären Metastasierung getroffen werden. Aus diesem Grund ist in der modernen Chirurgie kolorektaler Lebermetastasen eine Entwicklung zu parenchymsparenden, atypischen oder anatomischen Resektionen mit der Extremform des sogenannten „berry picking“ zu beobachten (Abb. 1). Durch den Verzicht auf „Major“-Resektionen bleiben so im Falle späterer Rezidive weitere operative Optionen erhalten. Des Weiteren nimmt die Anzahl laparoskopischer Leberresektionen in letzten Jahren stetig zu. Dies liegt neben der generellen Zunahme der Zahl minimalinvasiver Resektionen in der Viszeralchirurgie insbesondere an einer permanenten Verbesserung der Dissektionstechniken, sodass heute selbst anspruchsvolle Resektionen in entsprechenden Zentren laparoskopisch durchführbar sind. Neben den bekannten Vorteilen der laparoskopischen Chirurgie – verkürzter Krankenhausaufenthalt, geringere postoperative Schmerzen, weniger Transfusionsbedarf und besseres kosmetisches Ergebnis– konnte eine Gleichwertigkeit der onkologischen Ergebnisse gezeigt werden.10
Abb. 1: Patient, 39 Jahre; hep./pulm. metastasiertes Sigmakarzinom. Sigmaresektion und Hemikolektomie li.; vor drei Wochen letzte Chemotherapie mit Cetuximab/FOLFOX, Calciumfolinat, Oxaliplatin. (A) Z.n. atypischer Lungenteilresektion UL, OL (B) 4x atypische Leberteilresektion
Neoadjuvante Systemtherapie bei initial nicht resektablen Befunden
Während es nach einer R0-Resektion primär resektabler kolorektaler Metastasen bei fehlendem Wirkungsnachweis zurzeit keine Empfehlung der Durchführung einer perioperativen oder einer adjuvanten Therapie gibt, ist eine neoadjuvante Systemtherapie zum Downsizing bei initial nicht resektablen Befunden von entscheidender Bedeutung. Es werden hochaktive Schemata mit zwei (FOLFIRI) oder drei Substanzen(FOLFOXIRI) mit Antikörpertherapien kombiniert. Zur Therapieentscheidung tragen neben dem RAS-Mutationsstatus des Patienten auch die Lokalisation des Primärtumors bei. Wenn anschließend eine sekundäre Resektabilität erreicht werden kann, ist die Prognose der Patienten nur marginal schlechter als nach primärer Resektabilität.11 Aufgrund der zu erwartenden Lebertoxizität der Systemtherapie sollte allerdings die Resektabilität regelmäßig überprüft werden, damit die Resektion zum frühestmöglichen Zeitpunkt erfolgen kann. Ein maximales Tumoransprechen ist in der Regel nach 3–4 Monaten zu erwarten. Im Intervall zwischen Systemtherapie und Resektion sind prognoserelevante Rückschlüsse auf das tumorbiologische Verhalten möglich. Bei Progress in diesem Intervall ist die Prognose der Patienten entsprechend schlecht.
Lokal ablative Verfahren
Insbesondere bei nicht vollständig resektablen Befunden gewinnen lokal ablative Verfahren wie die Radiofrequenzablation (RFA) und die Mikrowellenablation (MWA) sowie transarterielle Verfahren wie die transarterielle Chemoembolisation (TACE) und die selektive intraarterielle Radiotherapie (SIRT), aber auch die stereotaktische Bestrahlung zunehmend an Bedeutung. In Kombination mit Systemtherapien und Resektionen sind diese Verfahren mittlerweile feste Bestandteile des multimodalen Therapiekonzeptes. Dies verdeutlicht, dass neben der ausschließlichen Betrachtung des Gesamtüberlebens mittlerweile auch Faktoren wie das krankheitsfreie Überleben oder das chemo- sowie therapiefreie Zeitintervall entscheidende Parameter für die Bewertung moderner onkologischer Therapieverfahren geworden sind.
Literatur:
1 Van CE et al.: ESMO consensus guidelines for the management of patients with metastatic colorectal cancer. Ann Oncol 2016; 27(8): 1386-422 2 Hwang M et al.: Systematic review of outcomes of patients undergoing resection for colorectal liver metastases in the setting of extra hepatic disease. Eur J Cancer 2014; 50(10): 1747-57 3 Schoening WN et al.: [Preoperative imaging/operation planning for liver surgery]. Chirurg 2015; 86(12): 1167-79 4 Stockmann M et al.: The LiMAx test: a new liver function test for predicting postoperative outcome in liver surgery. HPB (Oxford) 2010; 12(2): 139-46 5 McCormack L et al.: Hepatic steatosis is a risk factor for postoperative complications after major hepatectomy: a matched case-control study. Ann Surg 2007; 245(6): 923-30 6 Nakano H et al.: Sinusoidal injury increases morbidity after major hepatectomy in patients with colorectal liver metastases receiving preoperative chemotherapy. Ann Surg. 2008; 247(1): 118-24 7 Geisel D et al.: Improved hypertrophy of future remnant liver after portal vein embolization with plugs, coils and particles. Cardiovasc Intervent Radiol 2014; 37(5): 1251-8 8 Schadde E et al.: Prediction of mortality after ALPPS stage-1: An analysis of 320 patients from the international ALPPS registry. Ann Surg 2015; 262(5): 780-5 9 Heise D et al.: Long-term outcome and quality of life after initial and repeat resection of colorectal liver metastasis: A retrospective analysis. Int J Surg 2017; 48: 281-5 10 Allard MA et al.: Early and long-term oncological outcomes after laparoscopic resection for colorectal liver metastases: a propensity score-based analysis. Ann Surg 2015; 262(5): 794-802 11 Tomlinson JS et al.: Actual 10-year survival after resection of colorectal liver metastases defines cure. J Clin Oncol 2007; 25(29): 4575-80
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...