Neue zielgerichtete Therapiestrategien beim Lungenkarzinom
Autor:
OA Dr. Maximilian J. Hochmair
Leiter der pneumo-onkologischen
Ambulanz + Tagesklinik
Abteilung für Innere Medizin und Pneumologie
Karl-Landsteiner-Institut für Lungenforschung und pneumologische Onkologie
Klinik Floridsdorf, Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Das nicht kleinzellige Lungenkarzinom (NSCLC) ist eine heterogene Erkrankung, die oft durch Treibermutationen ausgelöst wird. Es gibt eine Reihe von verfügbaren zielgerichteten Therapien zur Behandlung von NSCLC mit Treibermutationen (wie EGFR-, ALK-, ROS1-, RET- oder BRAF-gerichtete Therapien). Für andere Treibermutationen gibt es bisher noch keine zugelassenen Therapien, aber eine Reihe von vielversprechenden Daten. In diesem Bericht liegt der Schwerpunkt auf KRAS-Mutationen, „uncommon“ EGFR-Mutationen und Antikörper-Wirkstoff-Konjugaten gegen HER2, HER3 und TROP2.
KRAS-Mutationen
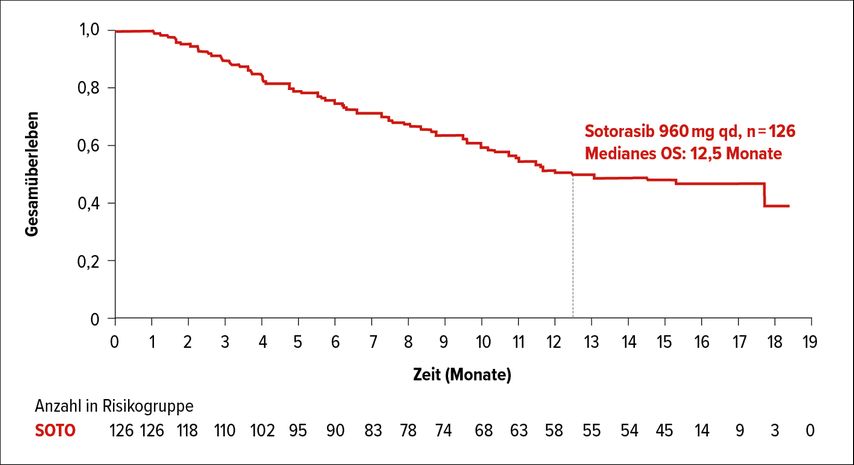
Die KRASG12C-Mutation wird bei etwa 13% der Patienten mit einem Adenokarzinom der Lunge identifiziert. Sotorasib ist der erste irreversible und selektive KRASG12C-Inhibitor, dessen Einsatz in der einarmigen Phase-II-Studie CodeBreaK1001 bei 126 vorbehandelten Patienten mit lokal fortgeschrittenem bzw. metastasiertem NSCLC untersucht wird. Bei der Jahrestagung der American Society of Clinical Oncology (ASCO) wurde dieses Jahr ein Update der Studie präsentiert. Unter Sotorasib zeigten mehr als 80% der Patienten eine Krankheitskontrolle. Bei 3,5% der Patienten wurde ein komplettes und bei 33,9% ein partielles Ansprechen mit einer medianen Dauer von 11,1 Monaten beobachtet. Eine Krankheitsstabilisierung wurde bei 43,5% der Patienten erreicht. Das progressionsfreie Überleben (PFS) betrug im Median 6,8 Monate (95% CI: 5,1–8,2) und das Gesamtüberleben (OS) median 12,5 Monate (95% CI: 10,0 bis nicht erreicht) (Abb. 1).
Ein Ansprechen auf die Therapie mit Sotorasib konnte bei allen untersuchten Subgruppen beobachtet werden. Besonders Patienten, die eine Anti-PD-(L)1-Therapie, aber keine Chemotherapie erhalten hatten, scheinen von Sotorasib zu profitieren. Die Ansprechrate betrug bei dieser kleinen Gruppe von Patienten (n=13) 69,2% und das mediane OS 17,7 Monate. In einer explorativen Analyse molekular definierter Subgruppen wurde eine Ansprechrate von 40 bzw. 42% bei Patienten mit hoher bzw. niedriger Tumormutationslast festgestellt. Eine Effektivität wurde auch bei Subgruppen mit Indikatoren für einen suboptimalen Therapieerfolg unter Standardtherapien, wie beispielsweise den Mutationen in STK11 oder, in geringerem Maße, KEAP1 gesehen.
Die therapieassoziierten Nebenwirkungen waren generell gut handhabbar. Am häufigsten wurden Diarrhö (alle Grade: 31,7%; Grad 3: 4,0%), Übelkeit (19,0%; 0%) und erhöhte ALT- und AST-Werte (jeweils 15,1%; Grad 3: 6,3 bzw. 5,6%) berichtet.
Antikörper-Wirkstoff-Konjugate
Antikörper-Wirkstoff-Konjugate (ADC) sind ein innovativer Therapieansatz, bei dem die Spezifität der zielgerichteten Antikörpertherapien mit zytotoxischen Wirkstoffen kombiniert werden. Dieses Jahr gab es mehrere Studien, die Daten mit dieser Art von Wirkstoffen untersuchten.
Trastuzumab-Deruxtecan
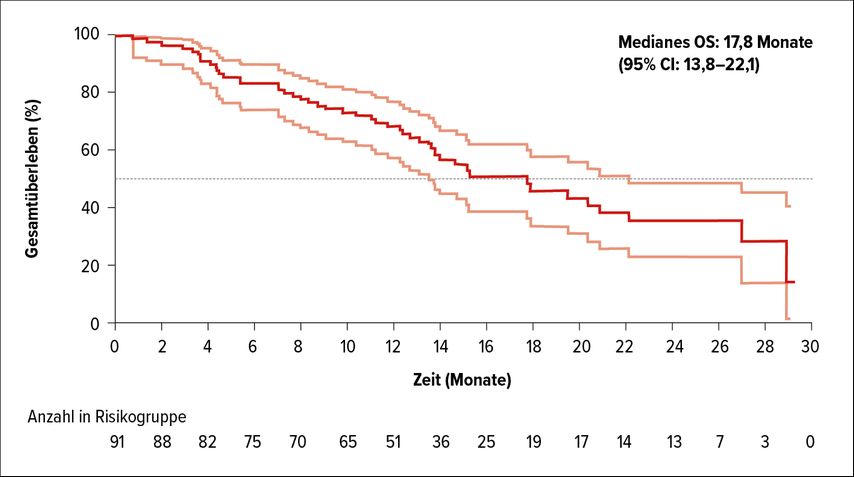
Etwa 3% der NSCLC, die histologisch keine Plattenepithelkarzinome sind, weisen HER2-Mutationen auf und sind mit einem etwas jüngeren Alter, weiblichem Geschlecht, Nichtraucher-Historie, einer schlechten Prognose und einer erhöhten Inzidenz von Hirnmetastasen assoziiert. Bis jetzt haben es HER2-gerichtete Therapie für NSCLC-Patienten noch nicht zur Zulassung geschafft. Trastuzumab-Deruxtecan (T-DXd) ist ein HER2-Antikörper-Wirkstoff-Konjugat, das bereits zur Behandlung von HER2-positiven Mammakarzinomen von der EMA eine Zulassung erhalten hat. In der DESTINY-Lung01-Studie2 wurden nun die Wirksamkeit und die Sicherheit von T-DXd bei relapsierten/refraktären HER2-mutierten NSCLC-Patienten untersucht. Am ESMO-Kongress wurden Daten von 91 in die Studie eingeschlossenen Patienten präsentiert. Die Patienten waren im Median 60,0 Jahre alt, 65,9% waren weiblich und hatten im Median 2 vorangegangene Therapien erhalten. Die Gesamtansprechrate belief sich unter T-DXd auf 54,9%, die Krankheitskontrollrate betrug 92,3%. Es konnte ein medianes PFS von 8,2 Monaten (95% CI: 6,0–11,9) und ein medianes Gesamtüberleben von 17,8 Monaten (13,8–22,1) beobachtet werden (Abb. 2).
Das Sicherheitsprofil war mit vorangegangenen Studien vergleichbar. 24 Patienten erlitten interstitielle Lungenerkrankungen (ILD) oder Pneumonitis, die in 4 Fällen vom Grad 3, in 2 Fällen vom Grad 5 war.
Datapotamab-Deruxtecan
TROP2 wird bei NSCLC hochexprimiert und ist mit einer schlechten Prognose assoziiert. Das Antikörper-Wirkstoff-Konjugat Datapotamab-Deruxtecan (Dato-DXd) besteht aus einem monoklonalen Anti-TROP2-Antikörper sowie einem potenten Topoisomerase-1-Inhibitor. Damit können sowohl Zieltumorzellen als auch die umgebenden Zellen eliminiert werden. Bei der World Conference on Lung Cancer (WCLC) wurde dieses Jahr ein Update zur Phase-I-Studie TROPION-PanTumor013 präsentiert, die die NSCLC-Kohorte umfasste. In diese Kohorte wurden 180 Patienten mit fortgeschrittenem oder metastasiertem NSCLC unabhängig von der Expression von TROP2 eingeschlossen: 50 Patienten erhielten 4mg/kg Dato-DXd, 50 Patienten 6mg/kg und 80 Patienten 8mg/kg. Die Patienten hatten zuvor bereits ≥3 vorangegangene Therapien erhalten, davon 74–88% Immuntherapie und 96–98% eine Platinum-basierte Chemotherapie.
Generell zeigte die Substanz eine gute Verträglichkeit. Die große Mehrheit der Patienten profitieren von der Therapie mit Dato-DXd. Die Gesamtansprechraten betrugen je nach Dosierung zwischen 24 und 28%.
Bei der Jahrestagung der European Society for Medical Oncology (ESMO) wurde kurz darauf die Auswertung einer Subgruppe von 34 Patienten mit therapierbaren genetischen Alterationen präsentiert.4 Von diesen 34 Patienten wiesen 85% eine EGFR-Mutation, 9% eine ALK-Fusion, 3% eine ROS-Fusion und 3% eine RET-Fusion auf. Die Gesamtansprechrate in dieser Subpopulation betrug 35%.
Patritumab-Deruxtecan
EGFR-Tyrosinkinase-Inhibitoren (TKI) sind für Patienten mit EGFR-mutiertem NSCLC eine etablierte Erstlinientherapie, obwohl sich langfristig Resistenzen entwickeln. Im Zusammenhang mit der Resistenz gegenüber EGFR-TKI wurde eine Vielzahl von genomischen Alterationen identifiziert. HER3 wird in 83% der NSCLC-Tumoren exprimiert. Bisher sind HER3-Alterationen nicht als Mechanismus für Resistenzen gegen EGFR-TKI bei EGFR-mutierten NSCLC bekannt.
Das Antikörper-Wirkstoff-Konjugat Patritumab-Deruxtecan (HER3-DXd) bindet an HER3 und wurde in einer Phase-I-Dosiseskalations-Studie bei Patienten mit lokal fortgeschrittenem oder metastasiertem NSCLC nach Versagen von Osimertinib getestet.5 Der primäre Endpunkt der Studie war die ORR nach RECIST 1.1, sekundäre Endpunkte umfassten die Dauer des Ansprechens (DOR), PFS und Sicherheit. Der Großteil der eingeschlossenen Patienten war auf die Gabe von Osimertinib progredient, die übrigen Patienten hatten zuvor andere TKI erhalten. Die Ansprechrate betrug sowohl unter Vortherapie mit Osimertinib als auch unter Vortherapie mit anderen TKI 39%. Das mediane PFS lag jeweils bei 8,2 Monaten und die DOR bei 7,0 Monaten unter Osimertinib-Vorbehandlung bzw. 6,9 Monaten unter Vorbehandlung mit anderen TKI. Die Substanzkombination zeigte unabhängig vom Resistenzmechanismus und auch bei Vorliegen von Hirnmetastasen Wirkung. Das Nebenwirkungsprofil mit vorrangig Thrombozytopenie, Neutropenie und Fatigue ist bereits bekannt. Die Ergebnisse der Phase-II-Studien werden mit Spannung erwartet.
„Uncommon“ EGFR-Mutationen
Exon-20-Insertionen zählen zu den „uncommon EGFR mutations“ und machen etwa 5–12% der EGFR-Mutationen aus. Wie in einer Studie von Chouaid et al. am ASCO-Kongress gezeigt wurde, sind EGFR-Exon-20-Insertionen mit einem schlechteren Outcome assoziiert.6 In diesem Jahr gab es Updates zu Studien mit Mobocertinib und Amivantamab.
Mobocertinib
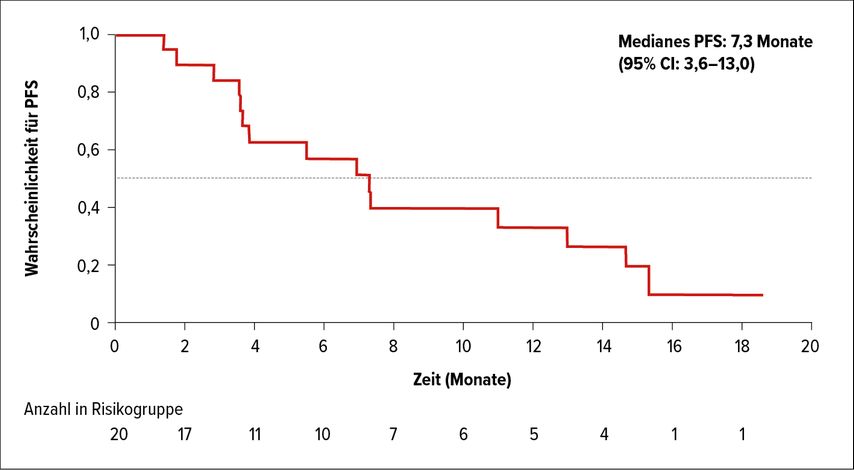
Mobocertinib (TAK 788) ist ein EGFR-TKI, der spezifisch zur Behandlung von NSCLC-Patienten mit EGFR-Exon-20-Insertionen entwickelt wurde. Dieses Jahr gab es am WCLC und am ESMO-Kongress ein Update zu der Phase-I/II-Studie, die den Einsatz von Mobocertinib bei NSCLC-Patienten untersuchte.7 Ausgewertet wurden Patienten mit EGFR-Exon-20-Insertionen der Kohorte 5, die nach einem Ansprechen oder stabiler Erkrankung für ≥6 Monate auf EGFR-TKI-Therapie (Poziotinib, Osimertinib, Afatinib oder Erlotinib) refraktär waren. Von den 20 in die Studie eingeschlossenen Patienten wiesen 8 (40%) eine partielle Remission auf und bei 10 Patienten konnte eine Erkrankungsstabilisierung beobachtet werden. Die Krankheitskontrollrate betrug 90%, die mediane Ansprechdauer belief sich auf 13 Monate. Es wurde ein medianes PFS von 7,3 Monaten beobachtet (95% CI: 3,6–13,0). Mobocertinib beweist somit auch nach vorangegangener Gabe anderer TKI Wirksamkeit.
Das Sicherheitsprofil war gut handhabbar. Am häufigsten traten Diarrhö (90%), Übelkeit (35%), Pruritus (30%), Rash (25%) und Anämien (25% auf).
Amivantamab
Bereits auf der WCLC 2020 wurden in der CHRYSALIS-Studie vielversprechende Ergebnisse mit Amivantamab, einem bispezifischen monoklonalen Antikörper gegen EGFR und MET, gezeigt.8 Es wurden Ansprechraten von 40% und eine mediane Dauer des Ansprechens von 11,1 Monaten berichtet.
Beim ASCO-Kongress 2021 wurde eine Analyse präsentiert, die die CHRYSALIS-Studiendaten von 81 Patienten mit einem gepoolten unbehandelten Real-World-Datenset von 125 Patienten verglich.9 Die Patienten aus dem Real-World-Datenset mussten die relevanten Einschlusskriterien der CHRYSALIS-Studie erfüllen. Die Analyse ergab unter Amivantamab eine deutliche Reduktion des Risikos für einen Progress (–53%) sowie eine Verlängerung der Zeit bis zur nächsten Behandlung (–60%) oder bis zum Tod Tod (–51%).
In der CHRYSALIS-Studie gibt es zusätzlich zum Monotherapie-Arm mit Amivantamab einen Kombinationsarm mit Avimantamab plus Lazertinib.10 Bei Lazertinib handelt es sich um einen Tyrosinkinase-Inhibitor der dritten Generation. Man geht davon aus, dass diese Wirkstoffkombination nach Versagen von Osimertinib besonders wirksam ist: Hier kommt es zu verschiedenen Resistenzen, bei denen sowohl EGFR als auch MET eine entscheidende Rolle spielen. In die Studie eingeschlossen waren 45 Patienten mit metastasiertem bzw. nicht resezierbarem NSCLC und EGFR-Exon-19-Deletion oder L858R-Mutation, die nach Gabe von Osimertinib progredient waren. Das mediane PFS betrug 4,9 Monate und Gesamtansprechrate 36%, wobei die mediane Dauer des Ansprechens bei 9,6 Monaten lag. Bei jenen Patienten, bei denen eine EGFR-/MET-basierte Resistenz identifiziert werden konnte, lag die Ansprechrate etwas höher. Die Testung auf MET spielt dabei eine besondere Rolle: Bei einer MET-basierten Resistenz lag die Ansprechrate bei 75%. Möglicherweise lässt sich die Suszeptibilität mittels immunhistochemischer Färbung festmachen. In der Studie sprachen neun von zehn Patienten, die immunhistochemisch positiv für eine EGFR/MET-Expression waren, auf die Kombinationstherapie an.
Literatur:
1 Skoulidis F et al.: Overall survival and exploratory subgroup analyses from the phase 2 CodeBreaK 100 trial evaluating sotorasib in pretreated KRAS p.G12C mutated non-small cell lung cancer. ASCO 2021, Abstr. #9003 2 Li BT et al.: Primary data from DESTINY-Lung01: a phase 2 trial of trastuzumab deruxtecan (T-DXd) in patients (Pts) with HER2-mutated (HER2m) metastatic non-small cell lung cancer (NSCLC). ESMO 2021, Abstr. #LBA45 3 Garon EB et al.: TROPION-PanTumor01: updated results from the NSCLC cohort of the phase 1 study of datopotamab deruxtecan in solid tumors. WCLC 2021, Abstr. #MA03.02 4 Garon E et al.: Efficacy of datopotamab deruxtecan (Dato-DXd) in patients (pts) with advanced/metastatic (adv/met) non-small cell lung cancer (NSCLC) and actionable genomic alterations (AGAs): Preliminary results from the phase I TROPION-PanTumor01 study. ESMO 2021, Abstr. #LBA49 5 Janne PA et al.: Efficacy and safety of patritumab deruxtecan (HER3-DXd) in EGFR inhibitor-resistant, EGFR-mutated (EGFRm) non-small cell lung cancer (NSCLC). ASCO 2021, Abstr. #9007 6 Chouaid C et al.: EGFR Exon 20 insertion: Prognostic and predictive values in advanced non-small cell lung cancer, a real-world study. ASCO 2021, Abstr. 9062 7 Spira A et al.: Mobocertinib in EGFR exon 20 insertion positive metastatic NSCLC patients with disease control on prior EGFR TKI therapy. WCLC 2021, Abstr. #OA15.01 8 Sabari JK et al.: Amivantamab in Post-platinum EGFR Exon 20 Insertion Mutant Non-small Cell Lung Cancer. WCLC 2020, Abstr. # OA04.04 9 Michom A et al.: Amivantamab compared with real-world therapies in patients with NSCLC with EGFR Exon 20 insertion mutations who have progressed after platinum doublet chemotherapy. ASCO 2021, Abstr. #9052 10 Bauml J et al.: Amivantamab in combination with lazertinib for the treatment of osimertinib-relapsed, chemotherapy-naïve EGFR mutant (EGFRm) non-small cell lung cancer (NSCLC) and potential biomarkers for response. ASCO 2021, Abstr. #9006
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...