Neue Therapieoptionen für Patienten mit schwer behandelbaren Tumoren
Bericht: Dr. Ine Schmale
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Unter den gastrointestinalen Tumoren befinden sich einige der auch heutzutage noch schwer behandelbaren Entitäten. Patienten mit Leberzell-, Pankreas- und Rektumkarzinom haben – bei begrenzten Therapiemöglichkeiten – häufig eine schlechte Prognose. Beim Gastrointestinal Cancers Symposium der American Society of Clinical Oncology (ASCO GI) 2022 wurden vielversprechende Studienergebnisse präsentiert, die auf eine mögliche Verbesserung der Therapie für spezifische Patientenpopulationen hinweisen.
Mit Lenvatinib wurde im Vergleich zu Sorafenib in der Erstlinienbehandlung des fortgeschrittenen Leberzellkarzinoms ein nicht unterlegenes Gesamtüberleben (OS; median 13,6 vs. 12,3 Monate; HR: 0,92) bei Verlängerung des progressionsfreien Überlebens (PFS; median 7,4 vs. 3,7 Monate; HR: 0,66) sowie höheren Ansprechraten (24,1 vs. 9,2%) erreicht.1 In der chinesischen Studie LAUNCH wurde nun mit der Kombination von Lenvatinib und einer transarteriellen Chemoembolisation (TACE) eine weitere Effektivitätssteigerung gesehen.2 338 Patienten mit zuvor nicht systemisch behandeltem fortgeschrittenem Leberzellkarzinom erhielten in der Studie randomisiert TACE plus Lenvatinib oder alleiniges Lenvatinib. Primärer Studienendpunkt war das OS.
Die Patienten waren median 54–56 Jahre alt mit mehrheitlich multiplen intrahepatischen Läsionen sowie Metastasen bei über der Hälfte der Patienten. Bei etwa der Hälfte der Patienten lag der durchschnittliche AFP(Alpha-Fetoprotein)-Wert bei ≥400ng/ml. Mit einer Ansprechrate von 45,9 versus 20,8% laut RECIST-1.1-Kriterien bzw. 54,1 versus 25,0% laut mRECIST-Kriterien profitierten Patienten häufiger von Lenvatinib plus TACE als von der alleinigen Lenvatinib-Therapie. Das OS wurde durch die Kombination mit TACE von median 11,5 auf 17,8 Monate verlängert, das mediane PFS von 6,4 auf 10,6 Monate. Die Risikoreduktion bezüglich des OS betrug 55% (HR: 0,45; 95% CI: 0,33–0,61; p<0,001) und bezüglich des PFS 57% (HR: 0,43; 95% CI: 0,34–0,55; p<0,001). Ein Überlebensvorteil durch TACE wurde für alle untersuchten Subgruppen gezeigt. 15,3% der Patienten im Lenvantinib/TACE-Arm, aber nur 1,8% im Lenvantinib-Arm konnten aufgrund der Tumorschrumpfung einer Resektion mit kurativer Intention unterzogen werden. Die meisten Patienten erhielten nach Versagen der Studienmedikation eine PD-1(„Programmed cell death protein 1“)-gerichtete Immuntherapie.
Die Therapiedauer betrug 8,2 Monate für die Kombinationstherapie und 5,1 Monate für die Lenvatinib-Monotherapie. Die Dosierung von Lenvatinib wurde bei 53 versus 45% der Patienten in den Studienarmen mit oder ohne TACE reduziert, bei 45 versus 40% unterbrochen und von 9 versus 8% der Patienten abgebrochen.
Tremelimumab plus Durvalumab beim Leberzellkarzinom
Auch mit der kombinierten Checkpoint-Blockade von „Cytotoxic T-lymphocyte-associated protein 4“ (CTLA4) und PD-L1 wurden in der HIMALAYA-Studie verbesserte Gesamtüberlebensraten im Vergleich zu Sorafenib erzielt.3 In der offenen, multizentrischen Phase-III-Studie erhielten 393 Patienten das STRIDE(T300+D)-Regime, bestehend aus einer Dosis Tremelimumab (300mg) sowie Durvalumab (1500mg, q4w) bis Tumorprogress, 389 Patienten eine Durvalumab-Monotherapie und weitere 389 Patienten Sorafenib (400mg, bid). Ein vierter Arm mit Durvalumab plus 4 Dosen Tremelimumab wurde frühzeitig geschlossen. Laut Einschlusskriterien wiesen die Patienten ein bestätigtes nicht resektables Leberzellkarzinom in den BCLC-Stadien B und C auf, verfügten über eine gute Leberfunktion (Child-Pugh A) und hatten noch keine systemische Therapie erhalten.
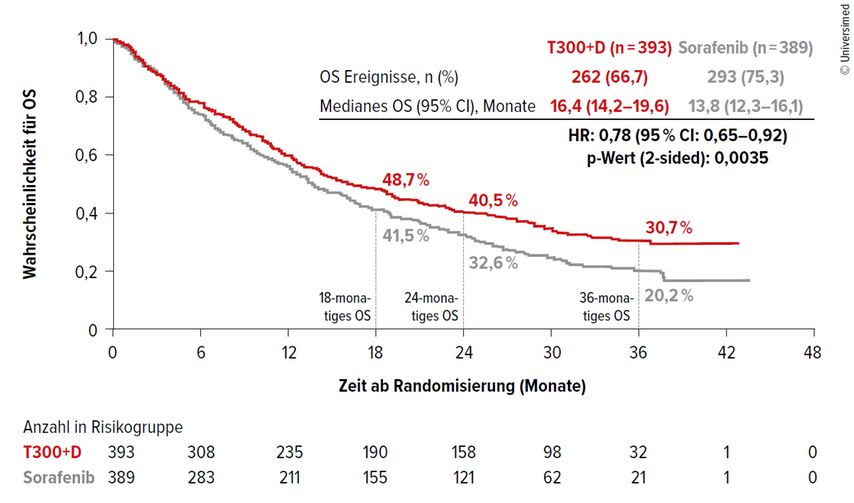
Die Studie erreichte ihren primären Endpunkt, eine signifikante OS-Verlängerung im Vergleich von T300+D versus Sorafenib. Im Median lebten die Patienten der beiden Studienarme 16,4 versus 13,8 Monate (HR: 0,78; 95% CI: 0,65–0,92; p=0,0035), nach 24 Monaten betrug die OS-Rate 40,5 versus 32,6% und nach 36 Monaten 30,7 versus 20,2% (Abb. 1). Mit der Durvalumab-Monotherapie wurde eine Verlängerung des OS auf median 16,6 Monate beobachtet, der Unterschied der Kaplan-Meier-Kurven erreichte den Nachweis der Nichtunterlegenheit von Durvalumab, aber keine signifikante Überlegenheit gegenüber Sorafenib (HR: 0,86; 95% CI: 0,73–1,03). Nach 24 Monaten lebten 39,6% und nach 36 Monaten 24,7% der Patienten im Durvalumab-Monotherapie-Arm. Das mediane PFS war zwischen den Studienarmen mit 3,78 (T300+D), 3,65 (Durvalumab) und 4,07 Monaten (Sorafenib) vergleichbar. Ein Ansprechen wurde aber häufiger unter T300+D (20,1%) und Durvalumab (17,0%) im Vergleich zu Sorafenib (5,1%) beobachtet. Die Krankheitskontrollrate betrug 60,1 vs. 54,8 vs. 60,7%, die mediane Dauer des Ansprechens (DOR) 22,34 vs. 16,82 vs. 18,43 Monate.
Therapieassoziierte Nebenwirkungen wurden bei 75,8 vs. 52,1 vs. 84,8% der Patienten berichtet, von Grad 3/4 in 25,8 vs. 12,9 vs. 36,9% der Fälle. Klinisch relevante therapieassoziierte Nebenwirkungen traten bei 17,5 vs. 8,2 vs. 9,4% der Patienten auf. Bei 8,2 vs. 4,1 vs. 11,0% der Patienten führten die therapieassoziierten Nebenwirkungen zum Therapieabbruch. Es kam in den Immuntherapie-Armen nicht zu einer relevanten Erhöhung der Lebertoxizität oder des Blutungsrisikos.
Die Autoren der Studien schlossen aus den Ergebnissen, dass Durvalumab sowohl mit einer initialen Tremelimumab-Dosis als auch als Monotherapie eine neue Option für Patienten mit nicht resezierbarem Leberzellkarzinom sein könnte.
Dostarlimab bei Patienten mit MMR-defizientem Rektumkarzinom
Die Immuntherapie eröffnet auch für die adjuvante Behandlung von Patienten mit lokal fortgeschrittenem Rektumkarzinom möglicherweise neue Optionen. Die Standardbehandlung für diese Patientenklientel besteht aus neoadjuvantem FOLFOX/CAPOX sowie einer Chemo(radio)therapie. Nach dem Re-Staging wird dann ein nichtoperatives Management bei Patienten mit Komplettremission oder eine totale mesorektale Exzision bei residualer Erkrankung angeschlossen.
Eine amerikanische Phase-II-Studie untersucht für die 5–10% der Patienten mit Mismatch-Reparatur-defizienten (MMRd) Tumoren die PD-1-Blockade mit Dostarlimab als neoadjuvante Monotherapie.4 In die Studie eingeschlossen wurden bisher 16 von 30 geplanten Patienten mit MMRd-Rektumkarzinom im klinischen Stadium II und III. Die Patienten erhielten 9 Zyklen Dostarlimab (500mg, d1, q3w), im Fall von residualer Erkrankung gefolgt von einer Chemoradiotherapie und Resektion bei weiter bestehender residualer Erkrankung. Bei klinischer Komplettremission (cCR; definiert als endoskopisches plus radiologisches komplettes Ansprechen) werden die Patienten nach Dostarlimab und auch nach Chemoradiotherapie nichtoperativ weiterbehandelt. 11 Patienten komplettierten bisher die PD-1-gerichtete Therapie. Die cCR-Rate für diese 11 Patienten beträgt 100%.
Adagrasib bei Patienten mit KRASG12C-mutiertem Pankreaskarzinom
Etwa 90% aller Pankreaskarzinome weisen eine KRAS-Mutation auf, bei ca. 2% von diesen handelt es sich um eine G12C-Punktmutation. Die Phase-I/II-Studie KRYSTAL-1 untersuchte den KRASG12C-Inhibitor Adagrasib bei Patienten mit nicht resektablen oder metastasierten soliden Tumoren mit KRASG12C-Mutation, darunter 10 auswertbare Patienten mit Pankreaskarzinom sowie 17 auswertbare Patienten mit anderen gastrointestinalen Tumoren.5 Insgesamt waren die Patienten median 65,5 Jahre alt und hatten median 2 sowie in der Spanne 1–5 vorangegangene Therapielinien erhalten.
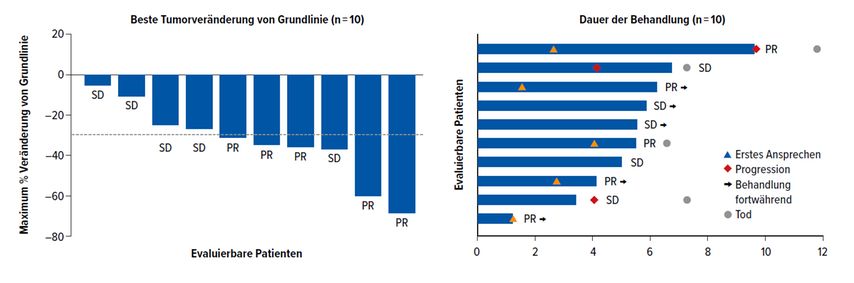
Patienten mit Pankreaskarzinom zeigten ein Ansprechen in 50% der Fälle (alles partielle Remissionen), bei weiteren 50% der Patienten stabilisierte sich die Erkrankung, sodass die Krankheitskontrollrate bei 100% lag (Abb. 2). Die mediane Zeit bis zum Ansprechen betrug 2,80 Monate und die mediane DOR 6,97 Monate. Im Median lebten die Patienten 6,60 Monate ohne Progress (95% CI: 1,0–9,7). Die Hälfte der Pankreaskarzinompatienten befand sich zum Zeitpunkt der Auswertung noch unter Therapie.
Abb. 2: Beste Tumorreduktion ab Therapiebeginn (links) und Dauer der Therapie (rechts) bei Pankreaskarzinompatienten unter Adagrasib. (Modifiziert nach 5)
Bei Patienten mit anderen GI-Tumoren wurde ein partielles Ansprechen bei 35% als bestes Ansprechen beobachtet und eine stabile Erkrankung bei 65% der Patienten. Somit lag auch bei diesen Patienten die Krankheitskontrollrate bei 100%. Die mediane Zeit bis zum Ansprechen betrug 1,3 Monate, die mediane DOR 7,85 Monate. Im Median betrug das PFS 7,85 Monate (95% CI: 6,90–11,30).
Die Nebenwirkungen der Adagrasib-Monotherapie waren in der Regel kontrollierbar mit Grad-3-Nebenwirkungen bei 27% der Patienten. In der laufenden KRYSTAL-1-Studie und in einem neu initiierten Early-Access-Programm (NCT05162443) ist Adagrasib für Patienten mit soliden Tumoren und KRASG12C-Mutation verfügbar.
Quelle:
Gastrointestinal Cancers Symposium (ASCO GI) 2022, 20.–22. Januar 2022, San Francisco und online
Literatur:
1 Kudo M et al.: Lenvatinib versus sorafenib in first-line treatment of patients with unresectable hepatocellular carcinoma: a randomised phase 3 non-inferiority trial. Lancet 2018; 391: 1163-73 2 Peng Z et al.: Lenvatinib combined with transarterial chemoembolization as first-line treatment of advanced hepatocellular carcinoma: a phase 3, multicenter, randomized controlled trial. ASCO GI 2022; Abstr. #380 3 Abou-Alfa GK et al.: Phase 3 randomized, open-label, multicenter study of tremelimumab and durvalumab as first-line therapy in patients with unresectable hepatocellular carcinoma: HIMALAYA. ASCO GI 2022;Abstr. #379 4 Lumish MA et al.: PD-1 blockade alone for mismatch repair deficient (dMMR) locally advanced rectal cancer. ASCO GI 2022; Abstr. #16 5 Bekaii-Saab TS et al.: KRYSTAL-1: updated activity and safety of adagrasib (MRTX849) in patients with unresectable or metastatic pancreatic cancer (PDAC) and other gastrointestinal tumors harboring a KRAS G12C mutation. ASCO GI 2022; Abstr. #519
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...