Neoadjuvante Radiochemotherapie versus perioperative Chemotherapie
Autor:
OA Dr. Ercan Müldür
Facharzt für Innere Medizin
Onkologie und Hämatologie
Zentrum für Onkologie, Hämatologie und Palliativmedizin
Wilhelminenspital der Stadt Wien
E-Mail: ercan.muelduer@wienkav.at
Das Ösophaguskarzinom und das Karzinom des gastroösophagealen Übergangs (EAC) sind Tumoren, die häufig bereits bei Diagnosestellung in fortgeschrittenen Stadien angetroffen werden. Um das bestmögliche onkologische Ergebnis für dieses Patient:innenkollektiv zu erzielen, bedarf es daher einer optimalen interdisziplinären Zusammenarbeit zwischen der Chirurgie, der Strahlentherapie und der Onkologie.
Beim Plattenepithelkarzinom des Ösophagus kann ab dem Stadium cT2 eine präoperative Radiochemotherapie angeboten werden. Ab cT3 ist eine neoadjuvante Radiochemotherapie mit anschließender Operation die Therapie der Wahl, alternativ kann hier auch eine definitive Radiochemotherapie erfolgen. Bei Plattenepithelkarzinomen im oberen Drittel des Ösophagus ist die definitive Radiochemotherapie ohne Operation unabhängig vom cT-Stadium die oft bevorzugte Option.
Bei Adenokarzinomen des Ösophagus und des gastroösophagealen Übergangs ist ab dem Stadium cT2 eine neoadjuvante Radiochemotherapie oder eine perioperative Chemotherapie indiziert, da dadurch das Gesamtüberleben der Patient:innen im Vergleich zur alleinigen Operation signifikant verlängert wird.
Der aktuelle Therapiestandard basiert auf der 2012 publizierten niederländischen CROSS-Studie und der 2019 veröffentlichten FLOT4-AIO-Studie. Erstere verfolgte einen multimodalen Therapieansatz, bestehend aus einer neoadjuvanten Chemotherapie mit Carboplatin und Paclitaxel plus Strahlentherapie gefolgt von Operation. Letztere setzte eine perioperative Chemotherapie, bestehend aus Chemotherapie vor und nach Operation, ein.
Die CROSS-Studie
In der CROSS-Studie (CROSS: „chemoradiotherapy for oesophageal cancer followed by Surgery Study Group“) wurden 368 Patient:innen mit resektablen Karzinomen des Ösophagus und des gastroösophagealen Übergangs randomisiert. Eine Gruppe erhielt eine präoperative Radiochemotherapie bis 41,4Gy in 23 Fraktionen von 1,8Gy, fünf Tage/Woche mit wöchentlicher Gabe von Carboplatin/Paclitaxel gefolgt von der Operation. Die andere Gruppe wurde allein chirurgisch behandelt. Bei 75% der Tumoren handelte es sich um Adenokarzinome. Bei vergleichbaren postoperativen Komplikationsraten war das mediane Gesamtüberleben in der Gruppe mit Radiochemotherapie und anschließender Operation mit 49,4 Monaten signifikant länger als in der allein chirurgisch behandelten Gruppe mit 24 Monaten.
Auch die Langzeitdaten der CROSS-Studie ergaben einen signifikanten Vorteil bezüglich des Gesamtüberlebens mit 48,6 Monaten in der Gruppe mit präoperativer Radiochemotherapie vs. 24,0 Monate in der nur operativ behandelten Gruppe.
Besonders stark haben Patient:innen mit Plattenepithelkarzinomhistologie (PEC) von der Radiochemotherapie profitiert (81,6 Monate vs. 21,1 Monate). Aber auch bei Patient:innen mit Adenokarzinomen war das mediane Gesamtüberleben durch die präoperative Radiochemotherapie und anschließende Operation signifikant länger als bei alleiniger chirurgischer Behandlung (43,2 Monate vs. 27,1 Monate).1
Die FLOT4-AIO-Studie
Die von Al-Batran et al. publizierte FLOT4-Studie zeigte einen signifikanten Überlebensvorteil einer perioperativen Chemotherapie bei Adenokarzinomen des Magens sowie des gastroösophagealen Übergangs. Es konnte gezeigt werden, dass vier Gaben FLOT (Fluorouracil/Leukovorin/Oxaliplatin/Docetaxel) im Abstand von 14 Tagen gefolgt von Operation und anschließend von vier weiteren Gaben von FLOT postoperativ dem bisherigen Standard (prä- und postoperative Gabe von jeweils drei Zyklen ECF bzw. ECX [Epirubicin, Cisplatin, Fluorouracil bzw. Capecitabin]) deutlich überlegen ist. Durch das FLOT-Regime wurde die Rate an R0-Resektionen (84% vs. 77%) erhöht, das progressionsfreie Überleben (PFS; 30 Monate vs. 18 Monate) und das Gesamtüberleben (OS; 50 Monate vs. 35 Monate) wurden signifikant verlängert.2
Die beiden Regime im direkten Vergleich
Beim Kongress ASCO-GI 2023 wurde die multizentrische, kontrollierte klinische Neo-AEGIS-Studie vorgestellt. Sie untersuchte erstmals randomisiert, ob Patient:innen mit lokal fortgeschrittenen Adenokarzinomen des Ösophagus und des gastroösophagealen Übergangs mehr von einem neoadjuvanten CROSS-Schema oder einer perioperativen modifizierten MAGIC/FLOT-Therapie profitieren.
Das modifizierte MAGIC-Schema mit drei Zyklen Chemotherapie vor und drei Zyklen nach Operation umfasste Epirubicin, Cisplatin oder Oxaliplatin und Fluorouracil oder Capecitabin.
Von 362 Patient:innen erhielten 178 CROSS und 184 MAGIC/FLOT (157/27), 90% waren männlich, 84% hatten Tumoren im Stadium cT3 und 58% hatten cN1.
Von 2013 bis 2018 erfolgte die Chemotherapie mit dem modifizierten MAGIC-Schema, und von 2019 bis 2020 erhielten die Patient:innen MAGIC oder FLOT (15% erhielten FLOT).
Hervorzuheben ist die Wahl des Chemotherapiearmes des MAGIC-Protokolls (85%), der nach der Veröffentlichung der FLOT-Daten nicht mehr als Standard gilt.
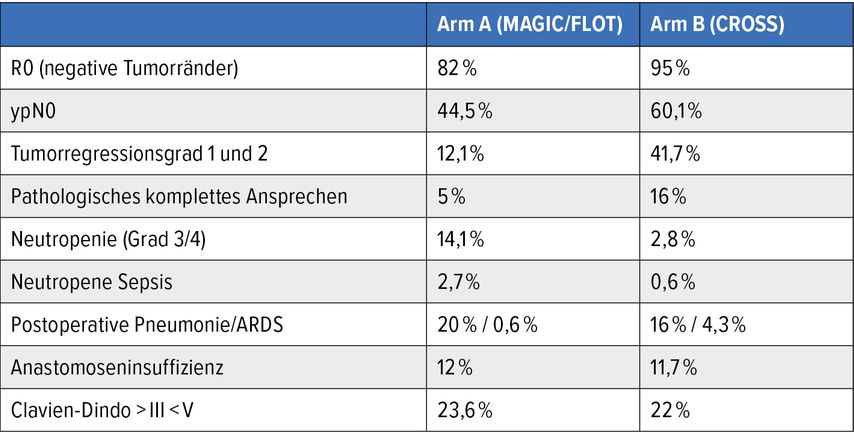
Beispielsweise lag in der FLOT-Studie die Rate an pathologischen Komplettremissionen (pCR) des FLOT-Arms bei 16%, während diese im EOX-Arm der Neo-AEGIS-Studie mit nur 5% angegeben wird. Das deutet darauf hin, dass die lokale Krankheitskontrolle im Chemotherapiearm (überwiegend EOX) der Neo-AEGIS-Studie der derzeit angewandten Standardbehandlung (FLOT) deutlich unterlegen ist.
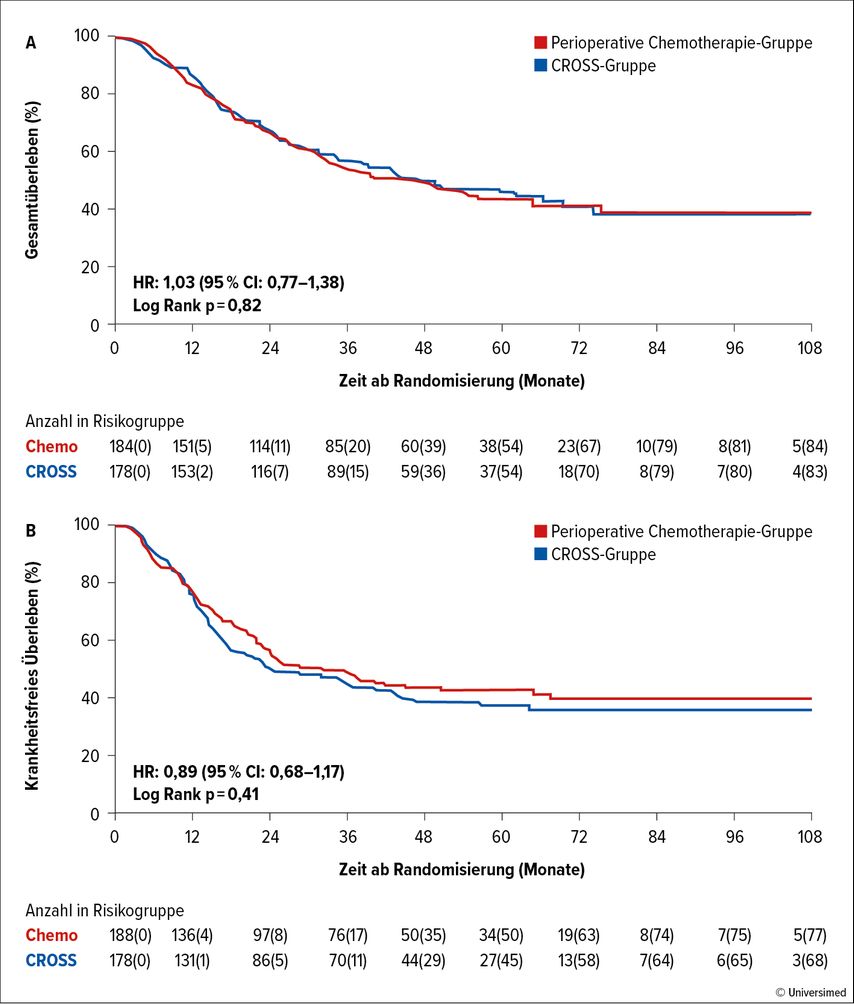
Mit einer 3-Jahres-OS-Rate von 55% im perioperativen Chemotherapiearm versus 57% mit CROSS-Schema brachte die Studie einen Gleichstand. Die Überlebenskurven überschnitten sich während der gesamten Nachbeobachtungszeit von 34,2 Monaten (Abb.1). Bei den Rezidivraten und Lokalisationen der Rezidive gab es ebenfalls keine Unterschiede zwischen den beiden Therapieschemata.
Trotz der ähnlichen OS-Rate waren die Raten für ein komplett pathologisches Ansprechen, tiefes pathologisches Ansprechen, R0-Resektion sowie Downstaging der Lymphknotenmetastasen unter dem CROSS-Schema höher. Interessant ist aber, dass die Verbesserung dieser wichtigen pathologischen Endpunkte sich nicht in einen Überlebensvorteil übersetzen lässt.
Tab. 1: Tumoransprechen und Toxizitätsprofil der Therapieregime (modifiziert nach Reynolds JV et al.)3
Erwähnenswert wäre auch noch, dass nur 40% der Patient:innen im perioperativen Chemotherapiearm die postoperative Chemotherapie erhielten, und noch weniger erhielten alle geplanten Dosen der postoperativen Chemotherapie.
Die beiden Gruppen unterschieden sich nicht in Bezug auf die Häufigkeit oder den Schweregrad operativer Komplikationen oder die postoperative Mortalität. Toxizität und unerwünschte Ereignisse des Grades 3 oder 4 traten jedoch häufiger unter der perioperativen Chemotherapie auf, vor allem Neutropenie, Durchfall und Erbrechen. Bis dato wurden noch keine Lebensqualitätsdaten zur Neo-AEGIS-Studie veröffentlicht.3
Jedenfalls brachte die Neo-AEGIS-Studie keinen Beweis dafür, dass die perioperative Chemotherapie der multimodalen Therapie mit CROSS inakzeptabel unterlegen ist.
Trotz der Daten der Neo-AEGIS-Studie ist nach wie vor nicht klar belegt, ob bei der Behandlung lokalisierter Adenokarzinome des Ösophagus sowie des gastroösophagealen Übergangs die neoadjuvante Radiochemotherapie der perioperativen Chemotherapie überlegen ist. Möglicherweise wird die laufende ESOPEC-Studie in den nächsten Jahren mehr klinisch relevante Daten liefern, um in dieser Fragestellung endlich Licht ins Dunkel zu bringen. Diese Studie hat nämlich ein ähnliches Design wie die Neo-AEGIS-Studie, jedoch mit dem FLOT-Schema als Chemotherapiearm.
Literatur:
1 Van Hagen P et al.: Neoadjuvant chemoradiotherapy plus surgery versus surgery alone for oesophageal or junctional cancer (CROSS). N Engl J Med 2012; 366(22): 2074-84 2 Al-Batran SE et al.: Perioperative chemotherapy with fluorouracil plus leucovorin, oxaliplatin, and docetaxel versus fluorouracil or capecitabine plus cisplatin and epirubicin for locally advanced, resectable gastric or gastro-oesophageal junction adenocarcinoma (FLOT4): a randomised, phase 2/3 trial. Lancet 2019; 393(10184): 1948-57 3 Reynolds JV et al.: Trimodality therapy versus perioperative chemotherapy in the management of locally advanced adenocarcinoma of the oesophagus and oesophagogastric junction (Neo-AEGIS): an open-label, randomised, phase 3 trial. Lancet Gastroenterol Hepatol 2023; 8(11): 1015-10
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...