Multiples Myelom und Magentumoren
Bericht:
Dr. Corina Ringsell
In der Februar-Sitzung der ASCO-Plenary-Serie wurde eine Studie zur Behandlung des rezidivierten/refraktären multiplen Myeloms vorgestellt, die zu einer Änderung der Therapiestandards führen könnte. Ausserdem wurde eine Option bei fortgeschrittenen Karzinomen des Magens und des ösophagogastralen Übergangs gezeigt.
Triplett-Therapie bei rezidiviertem/refraktärem MM
Prof. Dr. med. Maria-Victoria Mateos, von derUniversitätsklinik Salamanca, Spanien, stellte die Studie DREAMM-7 (NCT04246047) mit dem BCMA(«B-cell maturation antigen»)-gerichteten Antikörper-Wirkstoff-Konjugat Belamaf vor. Aufgenommen wurden 494 Patient:innen mit rezidiviertem/refraktärem multiplem Myelom (MM). Alle hatten zuvor mindestens eine Therapielinie erhalten. Sie wurden in zwei Gruppen randomisiert. Gruppe1 (n=243) erhielt die Triplett-Therapie aus Belantamab-Mafodotin (Belamaf), Bortezomib, Dexamethason (BVd), Gruppe2 (n=251) die Standardkombination Daratumumab, Bortezomib, Dexamethason (DVd).
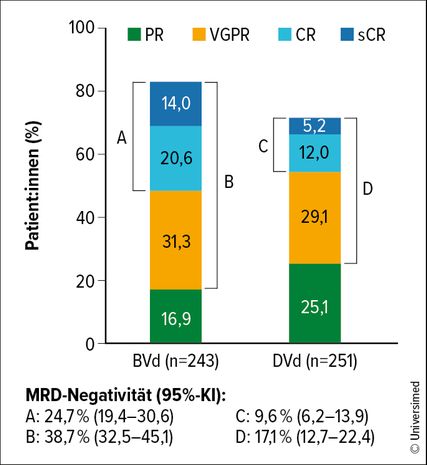
Abb. 1: DREAMM-7-Studie: höhere Raten an MRD-Negativität unter BVd im Vergleich zu DVd (modifiziert nach Mateos MV et al., ASCO Plenary Session)
Nach einem Follow-up von rund 28 Monaten betrug das mediane progressionsfreie Überleben (PFS) in der BVd-Gruppe 36,6 Monate, in der DVd-Gruppe 13,4 Monate (p<0,00001). Die mediane Dauer des Ansprechens (DOR) lag in der BVd-Gruppe bei 35,6 Monaten, in der DVd-Gruppe bei 17,8 Monaten. Erwähnenswert ist die Rate an minimaler Resterkrankung (MRD) in beiden Gruppen: Unter BVd war sie mehr als doppelt so hoch wie unter DVd (Abb. 1). Allerdings traten in der BVd-Gruppe auch mehr schwere Nebenwirkungen auf (50% vs. 37%). Studienleiterin Mateos betonte jedoch, diese seien handhabbar gewesen. Aufgrund dieser Resultate betrachtet sie BVd als potenziellen neuen Therapiestandard bei rezidiviertem/refraktärem MM.
Dr. med. Rachid Baz, Moffitt Cancer Center, Tampa, USA, bestätigte in seiner Diskussion der Studie die guten Ergebnisse und wies auf einen Vorteil der Kombination hin: Im Gegensatz zu anderen Therapieoptionen muss BVd nicht in einem spezialisierten Zentrum oder einer Klinik verabreicht werden. Einschränkend sei die hohe Abbruchrate in der BVd-Gruppe, so Baz.
Karzinome des Magens und des ösophagogastralen Übergangs
Prof. Dr. med. Rui-Hua Xu, Sun Yat-Sen University Cancer Center, Guangzhou, China, trug die Ergebnisse der FRUTIGA-Studie vor. Diese in China durchgeführte Phase-III-Studie evaluierte die Wirksamkeit und Sicherheit von Fruquintinib plus Paclitaxel im Vergleich zu Placebo plus Paclitaxel bei fortgeschrittenen Karzinomen des Magens und des ösophagogastralen Übergangs, die in der Erstlinientherapie unter Fluoropyrimidin- oder Platin-haltiger Chemotherapie progredient gewesen waren. Der duale primäre Endpunkt bestand aus PFS und Gesamtüberleben (OS). Fruquintinib ist ein oral zu verabreichender Inhibitor der «Vascular endothelial growth factor»-(VEGF)-Rezeptoren 1, 2 und 3. Der Wirkstoff hemmt so die Neoangiogenese bei Tumoren. In die Studie wurden 703 Patient:innen aufgenommen und im Verhältnis 1:1 randomisiert. Nach einem medianen Follow-up von rund 32 Monaten zeigte sich beim PFS ein statistisch signifikanter Vorteil für Fruquintinib (5,6 Monate vs. 2,7 Monate, p<0,0001). Der Unterschied beim OS von 9,6 Monaten vs. 8,4 Monate zugunsten von Fruquintinib war statistisch nicht signifikant. Die häufigsten Nebenwirkungen Grad 3 oder höher waren Neutropenie (60% vs. 36,4%), Leukopenie (42,9% vs. 23,5%) und Anämie (11,7% vs. 10,6%). Im weiteren Verlauf erhielten 52,7% in der Fruquintinib-Gruppe und 72,2% in der Placebogruppe weitere Antitumortherapien.
Prof. Dr. med. Florian Lordick, Universitäres Krebszentrum Leipzig, stellte in seiner Diskussion die Stärken und Schwächen der Studie heraus. Sie sei gut gepowert gewesen für die Analyse des PFS/OS und die Charakteristika der Teilnehmenden beider Gruppen seien gut ausbalanciert. Die Studie habe vielversprechende PFS-Ergebnisse gezeigt und eine interessante Steigerung der Ansprechrate. Als Schwächen nannte Lordick das negative OS-Resultat und fehlende Daten zur Lebensqualität und Symptomkontrolle. Er stellte die Frage nach den grossen Unterschieden hinsichtlich der nachfolgenden Therapien und warum keine Subgruppenanalysen gemacht wurden, um herauszufinden, wer von Fruquintinib profitiert. Als neuen Standard der Zweitlinientherapie bei Karzinomen des Magens und des ösophagogastralen Übergangs sieht Lordick den Wirkstoff derzeit nicht.
Quelle:
ASCO Plenary Series, 6. Februar 2024.Online unter https://meetings.asco.org/asco-plenary-series/15950?presentation=230741#230741
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...