Mammakarzinom
Bericht: Dr. Corina Ringsell
Im Juni drehte sich beim Cancer Update des CCC Vienna alles um das Thema Brustkrebs. Die Gastgeber:innen, Assoc. Prof. PD Dr. Ruth Exner, Universitätsklinik für Allgemeinchirurgie, und Univ.-Prof. Dr. Christian Singer, MPH, Universitätsklinik für Frauenheilkunde der MedUni Wien/AKH Wien, konnten hochkarätige Referent:innen aus unterschiedlichen Fachbereichen der MedUni Wien/des AKH Wien begrüßen, die einen Einblick in die Forschung und die Praxis zum Mammakarzinom gaben.
Männliches Mammakarzinom – State of the Art
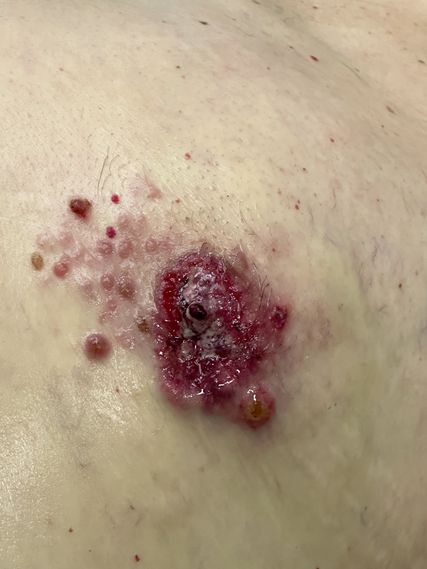
Prof. Exner befasste sich mit einem bei Ärzt:innen, Männern und der Bevölkerung allgemein noch immer wenig präsenten Thema: dem Brustkrebs beim Mann. Etwa 0,5–1% der Mammakarzinome betreffen Männer. Risikofaktoren sind vor allem höheres Alter, Rauchen, Alkoholabusus, Adipositas und eine genetische Disposition (v.a. BRCA1/2-Mutationen).1 Aufgrund des geringen Bewusstseins für die Krankheit erfolge die Diagnose meist erst spät (Abb.1). Zu diesem Zeitpunkt lägen in 30–40% der Fälle bereits Lymphknotenmetastasen vor, erklärte Exner. Diagnostik, Therapie und Nachsorge entsprechen den Maßnahmen bei postmenopausalen Frauen.1,2 Doch es gibt auch Unterschiede. So liegt beim Mann häufiger eine genetische Disposition vor und das Risiko für Zweitmalignome ist bis zu 20% höher als bei der Frau.1 Mehr als 90% der Männer hätten ein ER-positives, invasiv-duktales Karzinom,1 das sich meist als derber Tumor hinter der Brustwarze zeige (Abb.2), sagte Exner. Allerdings kämen auch andere Tumoren vor, etwa Sarkome.
Abb. 1: Wie bei diesem Patienten wird ein Mammakarzinom bei Männern meist erst in einem fortgeschrittenen Stadium diagnostiziert
Beim Brustkrebs des Mannes sei meist eine Mastektomie nötig, erklärte sie. Bei peripherer Lage sei allerdings auch eine brusterhaltende Operation mit adjuvanter Bestrahlung möglich.1,3 Für die endokrine Therapie ist Tamoxifen derzeit Standard, bei hohem Risiko auch ein GnRH-Analogon plus Aromatase-Inhibitor (AI).1–3 Dabei sei besonders auf die negativen Auswirkungen auf die Sexualfunktion zu achten, betonte Exner.
Behandlungsstrategien bei Knochenmetastasen
Assoc. Prof. PD Dr. Georg Pfeiler, Universitätsklinik für Frauenheilkunde, MedUni Wien/AKH Wien, zeigte, worauf bei Knochenmetastasen zu achten ist. Er wies darauf hin, dass der Knochenstoffwechsel ein sehr dynamischer Prozess ist, der bei Krebs durch verschiedene Faktoren beeinträchtigt werden kann: einerseits durch die Behandlung, etwa bei einer antihormonellen Therapie, andererseits durch Tumormetastasen.4 So fänden sich in 60–80% der Mamma- und Prostatakarzinome Knochenmetastasen,4 erklärte Pfeiler. Durchschnittlich 12% der Mammakarzinome würden ausschließlich in den Knochen metastasieren, sagte er. Knochenmetastasen können nicht nur das Frakturrisiko steigern, sondern auch zu Verletzungen des Rückenmarks infolge von Wirbelkörperfrakturen und zu einer Hyperkalzämie durch den Knochenabbau führen.4 Diese Komplikationen gelte es zu verhindern, sagte Pfeiler und betonte, dass die Therapie immer interdisziplinär erfolgen sollte.
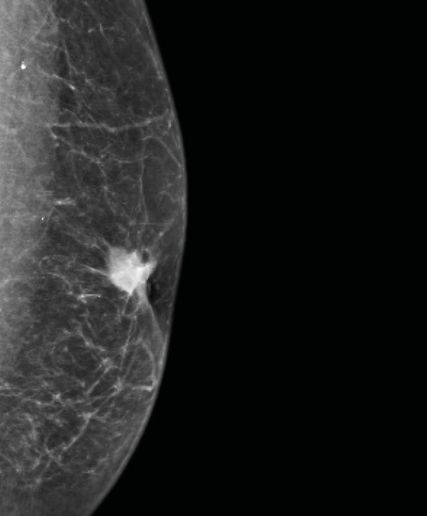
Abb. 2: Bei Männern zeigt sich ein Mammakarzinom, so wie in dieser Mammografie, meist als derber Knoten hinter der Brustwarze
Therapeutisch stehen verschiedene Optionen zur Verfügung. So kann bei Schmerzen aufgrund von Knochenmetastasen eine Radiotherapie rasche Linderung bringen.1,4 Um Frakturen zu verhindern, ist eine antiresorptive Behandlung mit Bisphosphonaten, bevorzugt Zoledronsäure, oder dem monoklonalen Antikörper Denosumab angezeigt. Diese Substanzen sind aus der Osteoporosetherapie bekannt, allerdings in geringerer Dosierung. Im direkten Vergleich war Denosumab der Zoledronsäure überlegen und ging zudem mit weniger unerwünschten Wirkungen einher. Zu beachten sei aber, dass es unter der höheren Dosierung des Antikörpers zu einer Hypokalzämie kommen könne, sagte Pfeiler. Daher sollte immer Kalzium substituiert werden. Zoledronsäure wird im ersten Jahr alle vier Wochen verabreicht, danach kann das Intervall auf zwölf Wochen verlängert werden. Für Denosumab fehlt diesbezüglich die Evidenz.1,4
Systemische Therapieoptionen beim fortgeschrittenen Brustkrebs
Dr. Sabine Danzinger, Universitätsklinik für Frauenheilkunde, MedUni Wien/AKH Wien, gab einen Überblick über die Therapie des Hormonrezeptor(HR)-positiven, HER2-negativen, metastasierten Mammakarzinoms. Die aktuellen AGO-Leitlinien empfehlen für die Erstlinientherapie CDK4/6-Inhibitoren in Kombination mit einem AI oder Fulvestrant.5 Hier sind alle drei Wirkstoffe (Palbociclib, Ribociclib, Abemaciclib) für das lokal fortgeschrittene und metastasierte Stadium zugelassen.6–8 Wichtig sei, vor Therapiebeginn ein großes Blutbild zu erstellen, die Leberfunktion zu überprüfen und, vor allem bei Ribociclib, ein EKG vorzunehmen.6–8 Diese Untersuchungen müssten während der Behandlung regelmäßg wiederholt werden, betonte Danzinger. Sollte es zu Nebenwirkungen kommen, gebe es in den jeweiligen Fachinformationen genaue Hinweise, wie vorzugehen ist und ab wann eine Dosisreduktion angezeigt ist.6–8 Wichtig sei es, die Patientin/den Patienten über mögliche Nebenwirkungen aufzuklären und dies auch für die Hausärztin/den Hausarzt zu verschriftlichen, erklärte sie. Müsse die Dosierung aufgrund von Nebenwirkungen reduziert werden, so habe dies keine negativen Auswirkungen auf das progressionsfreie Überleben (PFS).9
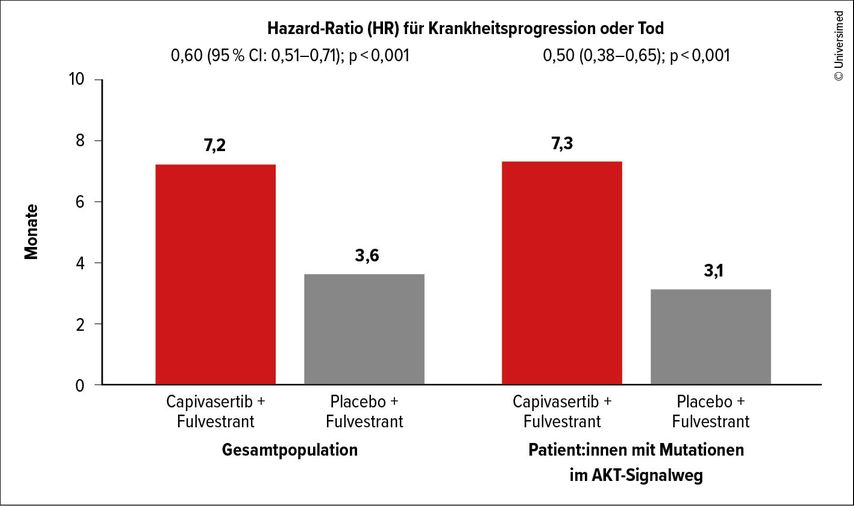
Für die Zweitlinientherapie stehen zahlreiche Wirkstoffe und Kombinationen zur Verfügung, zum Beispiel beim rezidivierten, ESR1-mutierten Mammakarzinom.5 Hier konnte der orale selektive Östrogenrezeptor-Degrader (SERD) Elacestrant in der EMERALD-Studie im Vergleich zur Standardbehandlung (endokrine Monotherapie) das PFS in der Gesamtpopulation und bei ESR1-Mutation signifikant verlängern.10,11 Bei Veränderungen im PI3K/AKT/mTOR-Signalweg, die in rund der Hälfte der ER-positiven fortgeschrittenen Mammakarzinome auftreten, sind zugelassen: Everolimus (mTOR-Inhibitor), Alpelisib (PIK3CA-Inhibitor) und Capivasertib (Pan-AKT-Inhibitor).12,13 Letzteres hemmt alle drei AKT-Isoformen und wurde in der Studie CAPItello-291 in Kombination mit Fulvestrant gegen Fulvestrant/Placebo getestet. Im Vergleich zur Placebogruppe verlängerte die Kombination das PFS nicht nur bei Mutationen im AKT-Signalweg signifikant, sondern auch in der Gesamtpopulation (Abb.3). Im Gesamtüberleben (OS) zeigte sich ebenfalls ein deutlicher Vorteil: 74 vs. 65% zu Monat 18. Hauptnebenwirkungen waren Durchfall und Hautausschläge.12
Eine recht neue Substanzklasse, die Antikörper-Wirkstoff-Konjugate (ADC), ist auch für HER2-positive Tumoren zugelassen. Danzinger stellte Trastuzumab deruxtecan (T-DXd) vor, das als Monotherapie in der Zweit- oder einer höheren Linie bei HER2-positivem, HER2-low und -ultralow Mammakarzinom zugelassen ist.14 In den DESTINY-Breast-Studien zeigte T-DXd objektive Responseraten (ORR) von bis zu 79% und ein medianes PFS von 29 Monaten.15 Dabei dürfe aber nicht außer Acht gelassen werden, dass bei rund 15% der Patient:innen eine nichtinfektiöse interstitielle Pneumonitis (ILD) auftrat,15 betonte Danzinger. Bei Symptomen wie trockenem Husten und Atembeschwerden im Zusammenhang mit T-DXd sollte man daher eine Thorax-CT veranlassen, sagte sie. Die ILD-Therapie besteht aus hoch dosiertem Kortison.
Abb. 3: Im Vergleich zu Fulvestrant plus Placebo verlängerte die Kombination von Capivasertib plus Fulvestrant das mediane PFS signifikant (modifiziert nach Turner NC et al.)12
Ein anderes ADC ist Sacituzumab govitecan, das in höheren Therapielinien beim HR-positiven, HER2-negativen metastasierten sowie beim metastasierten triple-negativen Mammakarzinom eingesetzt wird. Die häufigsten Nebenwirkungen sind Blutbildveränderungen und gastrointestinale Beschwerden.16
Welche tumorbiologischen Parameter brauchen Kliniker:innen?
Um bei der Vielzahl an Therapieoptionen die jeweils optimale auszuwählen, braucht es verlässliche pathologische Befunde. Welche dies sind, erklärte Assoc. Prof. PD Dr. Zsuzsanna Bago-Horvath, Klinisches Institut für Pathologie, MedUni Wien/AKH Wien. Das Mammakarzinom ist sehr heterogen mit unterschiedlichen Subtypen, aber auch intratumoraler Heterogenität. Bago-Horvath zeigte ein histologisches Bild eines Mammakarzinoms mit teils lobulärer, teils duktaler Differenzierung. Sie wies auch darauf hin, dass die Tumoren sich während der Therapie verändern. Dennoch gibt es Marker, die bei der Einordnung helfen.
Einer der ältesten prognostischen Parameter ist der Hormonrezeptorstatus.17 Dieser sollte in jedem Krankheitsstadium und für jede Metastase automatisch bestimmt werden, betonte Bago-Horvath. Zur Beurteilung wird am häufigsten der Allred-Score eingesetzt, der sich aus der Anzahl der HR-positiven Zellen und der Färbeintensität zusammensetzt. Er reicht von 0 (negativ) bis 8 (positiv), wobei nur Tumoren mit einem Score von 7 und 8 als hormonsensitiv gelten.17
Der zweite bereits seit Langem etablierte Marker ist HER2.18 Aufgrund neuer Medikamente wie T-DXd seien die Richtlinien zur HER2-Bestimmung überarbeitet worden. Zwar bleibe die Messung mittels Immunhistochemie (IHC) und In-situ-Hybridisierung (ISH) gleich; in den neuen Leitlinien werde aber die Angabe der Prozentzahl positiver Zellen empfohlen, da zum Beispiel T-DXd auch bei HER2-low- und -ultralow-Tumoren eingesetzt werden könne,19 so Bago-Horvath.
Der wichtigste Biomarker bei lokal fortgeschrittenem oder metastasiertem triple-negativem Mammakarzinom ist PD-L1, um die Indikation für einen PD-L1-Inhibitor zu stellen. Dabei sei darauf zu achten, dass es unterschiedliche Methoden für Pembrolizumab und Atezolizumab gibt, sagte Bago-Horvath. Der Combined Positivity Score (CPS) für Pembrolizumab könne ab 100 vitalen Tumorzellen bestimmt werden, während für den Immunzellscore (IC) für Atezolizumab nur 50 Zellen nötig seien. Auch die Gewebeart spielt eine Rolle. So dürfe der IC nicht auf zytologischem Material oder Knochenmetastasen bestimmt werden, betonte sie.
Da nicht immer eine Biopsie entnommen werden könne, sei es inzwischen auch möglich, alle therapeutisch wichtigen Biomarker aus einer Liquid Biopsy zu bestimmen. Bei der quantitativen Bestimmung von Biomarkern wie PD-L1, HER2 oder Ki67 helfen computerbasierte Systeme, die nicht nur präziser seien und mehr Zellen auszählen könnten als ein Mensch, sondern auch die Verteilung der positiven Zellen im Gewebe darstellten. Leider seien sie in den Laboren noch nicht Standard, so Bago-Horvath. Die neueste Entwicklung sei der Einsatz künstlicher Intelligenz. Es gebe bereits Systeme, die auf Basis der Histomorphologie Aussagen zum Therapieansprechen und zur Prognose treffen könnten, schloss sie.
Literatur:
1 S3-Leitlinie „Früherkennung, Diagnose, Therapie und Nachsorge des Mammakarzinoms“, Version 4.4, 2021, AWMF-Registernummer: 032-045OL 2 Loibl S et al.: Ann Oncol 2024; 35(2): 159-82 3 Lin AP: Br J Surg 2021; 108(9): 1034-42 4 Coleman R et al.: Ann Oncol 2020; 31(12): 1650-63 5 www.ago-online.de/fileadmin/ago-online/downloads/_leitlinien/kommission_mamma/2025/D_PDF/AGO_2025D_18_Endokrine_und_zielger_Therapie_met.pdf 6FI Ibrance 7 FI Verzenios 8 FI Kisqali 9 Rugo HS et al.: Oncologist 2021; 26(1): e53-65 10 Bidard FC et al.: JClin Oncol 2022; 40(28): 3246-56 11 Bardia A et al.: Clin Cancer Res 2024; 30(19): 4299-309 12 Turner NC et al.: N Engl J Med 2023; 388(22): 2058-70 13 Browne IM, Okines AFC: Cancers (Basel) 2024; 16(12): 2259 14 https://ec.europa.eu/health/documents/community-register/2025/20250324165432/anx_165432_de.pdf 15 Martín M et al.: Crit Rev Oncol Hematol 2024; 198: 104355 16 Spring LM et al.: Oncologist 2021; 26(10): 827-34 17 Choudhury KR et al.: J Histochem Cytochem 2010; 58(2): 95-107 18 Wolff AC et al.: Arch Pathol Lab Med 2018; 142(11): 1364-82 19 Wolff AC et al.: J Clin Oncol 2023; 41(22): 3867-72
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...