Infekte in der Hämatoonkologie
Bericht:
Dr. Norbert Hasenöhrl
Grundsätzlich unterscheidet sich die Therapie von Infektionen in derHämatoonkologie nicht von der sonstigen infektiologischen Behandlung. Infektionen sind bei immunsupprimierten und -kompromittierten Patient:innen jedoch häufiger und gefährlicher. Der renommierte Infektiologe Univ.-Prof. Dr. Florian Thalhammer, MedUni Wien, gibt einen Überblick überverschiedenste aktuelle Aspekte, von der Diphtherie bis zu Lieferengpässen von Antibiotika.
Keypoints
-
Die Kolonisation mit bestimmten Erregern erhöht das Risiko für Infektionen durch diese Erreger.
-
In den neuen CDI-Guidelines tritt Metronidazol in den Hintergrund.
-
Impfpräventable Erkrankungen wie Masern oder Diphtherie gibt es leider immer noch.
-
Neue Substanzen wie Delafloxacin, Eravacyclin, Oritavancin und Rezafungin bereichern das therapeutische Armamentarium.
-
Es gibt Möglichkeiten, auf Lieferengpässe von Antibiotika zu reagieren.
-
Bei BL/BLI-Kombinationen müssen Lücken im Spektrum beachtet werden. Therapie nur nach Antibiogramm!
-
Das neue „I“ der EUCAST bedeutet wirksam (bzw. empfindlich) bei höherer Dosierung.
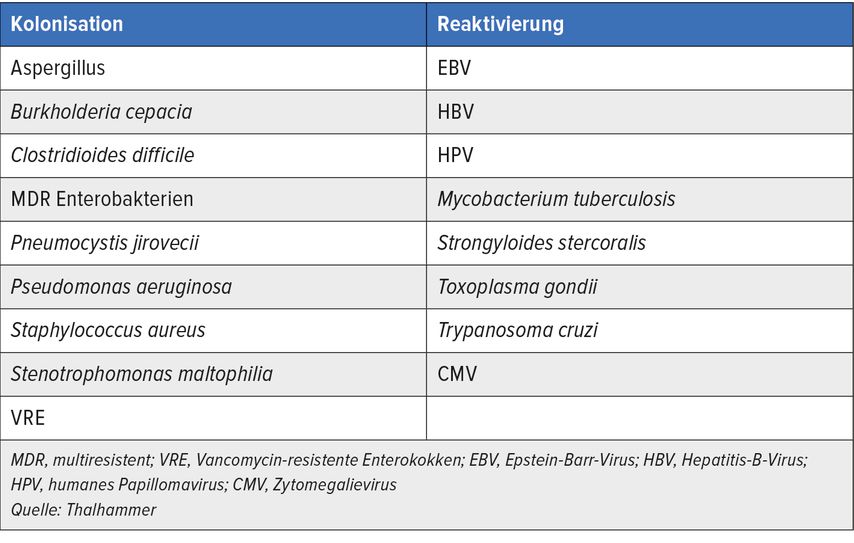
Infektionen sind durch die fast allgegenwärtige Immunsuppression gerade im Bereich der Hämatoonkologie ein großes Thema. Eine wirkliche Abschirmung ist im Krankenhausalltag nicht möglich. Deshalb sollte zunächst eine gezielte Anamnese zur Risikoerfassung bzw. -beurteilung durchgeführt werden. Dabei sind zwei Aspekte zu beachten: eine mögliche Kolonisation (viele Möglichkeiten von Aspergillus bis zu Vancomycin-resistenten Enterokokken) sowie eine Reaktivierung bestimmter Erreger (EBV, Hepatitis B, M. tuberculosis, CMV u.a.).
Die Kolonisation mit bestimmten Erregern kann das Infektionsrisiko durch ebendiese Erreger erhöhen, wie das z.B. für MRGN („multiresistente Gramnegative“) nachgewiesen ist. Deshalb ist eine aktive Surveillance gerade im hämatoonkologischen Umfeld eine sinnvolle Maßnahme. Aber auch darüber hinaus müssen gewisse Vorsichtsmaßnahmen getroffen werden, etwa die Untersuchung auf latente Tuberkulose vor Beginn einer Biologikatherapie. Zu Kolonisation und Reaktivierung siehe auch Tabelle 1.
Clostridium difficile
Die Infektion mit C. difficile (CDI) ist und bleibt eine der großen Herausforderungen im Bereich der nosokomialen Infektionen.
Sowohl die Guidelines der IDSA/SHEA (Infectious Diseases Society of America/Society for Healthcare Epidemiology of America) als auch jene der ESCMID (Europäische Gesellschaft für klinische Mikrobiologie und Infektionskrankheiten) haben hier Fidaxomicin als Erstlinientherapie für die Erstepisode in den Vordergrund gestellt, sowohl bei schwerem als auch bei leichterem Verlauf.
Vancomycin bleibt akzeptabel, während Metronidazol sehr in den Hintergrund gedrängt wurde. Letzteres wird jedoch von Infektiolog:innen durchaus kontrovers gesehen. Weitere Optionen sind Teicoplanin oral sowie die Kombination aus Fidaxomicin und Tigecyclin. Bezlotoxumab dient der Prävention weiterer Episoden, nicht aber der Therapie. Die Rolle der Stuhltransplantation (FMT) nach dem zweiten CDI-Rezidiv ist heute klarer, aber Timing und Modus erfordern noch weitere Studien.
Alt, aber nicht verschwunden
Es gibt Erkrankungen, an die man nur noch selten denkt, die aber nach wie vor eine Gefahr darstellen, insbesondere für immunsupprimierte Patient:innen. Zwei Beispiele, die leider eine gewisse traurige Aktualität aufweisen, sind die Masern und die Diphtherie.
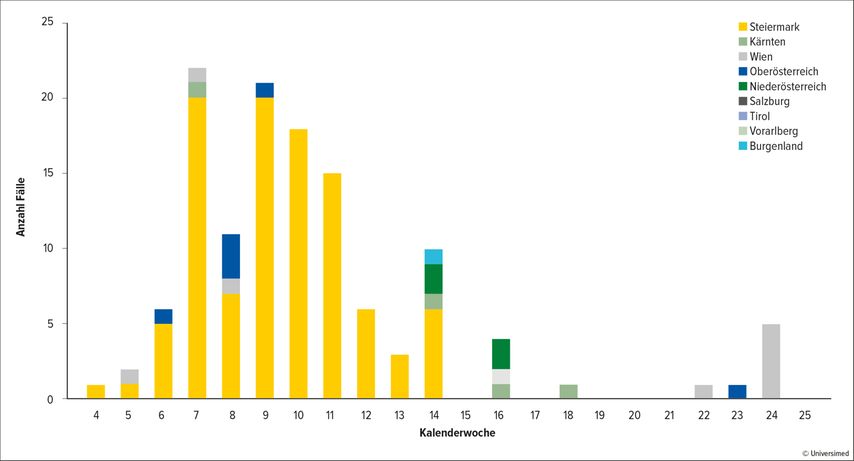
So gab es heuer, ausgehend von einer Hochzeit in Graz, einen großen Masernausbruch in der Steiermark, der sich vereinzelt auch auf andere Bundesländer ausgebreitet hat (Abb. 1).
Abb. 1: Masernausbruch in Österreich. Modifiziert nach der Agentur für Gesundheit und Ernährungssicherheit (AGES)
Die für eine Unterbrechung der Transmission notwendige Durchimpfungsrate von 95% ist in Österreich leider nicht verwirklicht. Bekannt ist, dass eine Maserninfektion im Gegensatz zur Impfung zu einem Verlust immunologischer Gedächtniszellen und daher zu einer über längere Zeit anhaltenden Immunsuppression führt. Die subakute sklerosierende Panenzephalitis ist eine gefürchtete Spätkomplikation der Masern, gegen die es keine Therapie gibt und die immer tödlich verläuft.
Auch die Diphtherie ist eine impfpräventable Erkrankung. Hier gibt es vor allem im Erwachsenenalter Impflücken, weil die Notwendigkeit einer Auffrischungsimpfung alle zehn und ab dem 65. Lebensjahr alle fünf Jahre zu häufig vergessen wird. Leider ist erst vor nicht allzu langer Zeit ein junger Asylwerber in Österreich trotz adäquater Therapie an Diphtherie gestorben.
Neue Substanzen
Delafloxacin ist ein neues gegen MRSA wirksames Fluorchinolon, das sich unter anderem durch eine Aktivitätszunahme im sauren Milieu auszeichnet. Dies ist z.B. für die Therapie von Abszessen wichtig, in die Delafloxacin gut penetriert. Es weist auch keine Phototoxizität und keine Verlängerung der QTc-Zeit auf, weiters wirkt es auch gegen Ciprofloxacin-resistente P.aeruginosa (hier ist jedoch ein Antibiogramm erforderlich). Generell ist zu Chinolonen zu sagen, dass sie zwar bei Bagatellinfektionen kontraindiziert sind, es jedoch keinen Grund gibt, sie nicht mehr zu verwenden, weil sie – neben den Betalaktamen – immer noch die wirksamste orale Antibiotikaklasse darstellen.
Eravacyclin ist ein fluoriertes Tetrazyklin mit einem breiten Aktivitätsspektrum, allerdings ohne Wirksamkeit gegen Pseudomonaden. Es wirkt jedoch gegen die meisten Betalaktamasen der Ambler-Klassen A, B und D und auch gegen A. baumannii und S. maltophilia. Eravacyclin weist eine höhere Aktivität als Tigecyclin auf und verursacht weniger Nebenwirkungen als dieses. Es kann u.a. gegen Carbapenem-resistente Enterobakterien, gegen A. baumannii, bei CDI und auch gegen atypische Mykobakterien eingesetzt werden. Eine mögliche höhere Dosierung wird zu diskutieren sein.
Enterokokken sind häufig Kolonisationskeime bzw. „Trittbrettfahrer“ und müssen in solchen Fällen auch nicht behandelt werden. Invasive Infektionen durch Enterokokken sind eher selten. Treten sie jedoch auf, so kann das Lipoglykopeptid Oritavancin eine sinnvolle Option sein. Es sollte jedoch bei Bakteriämie bzw. Sepsis und Endokarditis durch Enterokokken oder bei Vancomycin-resistenten Enterokokken (VRE) in Kombination mit einem zweiten Antibiotikum eingesetzt werden. Vorteile sind die lange Halbwertszeit – Oritavancin muss nur alle zwei Wochen in einer Dosis von 1,2g gegeben werden (und ist daher auch für eine ambulante parenterale Antibiotikatherapie, kurz APAT, geeignet) – und die Tatsache, dass es alle VRE erfasst.
Rezafungin ist ein Antimykotikum aus der Klasse der Echinocandine. Sein Wirkspektrum umfasst Candida albicans, auris, krusei und tropicalis, verschiedene Aspergillusspezies und nicht zuletzt auch Pneumocystisspezies.
Lieferengpässe
Welche Ausweichoptionen gibt es angesichts der auch Antibiotika betreffenden Lieferengpässe? Zunächst sollte die Indikation korrekt und streng gestellt werden: keine Antibiotika bei Verdacht auf und bei großer Wahrscheinlichkeit für virale Erreger. Der nächste Schritt wäre eine kurze Therapiedauer: Z.B. genügt für viele chirurgische Prophylaxen ein „single shot“.
Um Antibiotika zu sparen, wäre es prinzipiell eine Idee, den Patient:innen nur eine genau für sie passende, abgezählte Menge von Tabletten mitzugeben, was allerdings juristische Probleme verursachen könnte. Ein Ausweichen auf eine andere Dosierung desselben Antibiotikums kann evtl. auch erfolgen, also etwa statt 3x 1g eben 3x 2 Tabletten zu 500mg.
Eine andere Möglichkeit sind orale Alternativantibiotika, was bei Aminopenicillinen und Cephalosporinen jedoch schwierig ist. Ein Saft mit gleichem Inhaltsstoff wäre auch eine Alternative, aber oft sind gerade auch Kindersäfte nicht verfügbar. Schließlich ist noch die APAT zu erwähnen, die als intravenöse Kurzinfusion mit lang wirksamen Substanzen gegeben werden kann.
Neue BL/BLI-Kombinationen und ihre Schwächen
Neue BL/BLI-Kombinationen wie Ceftazidim/Avibactam, Ceftolozan/Tazobactam, Meropenem/Vaborbactam und Imipenem/Cilastatin/Relebactam sind hilfreich in der Therapie von gramnegativen Erregern, weisen jedoch Lücken auf, etwa was Produzenten von Metallobetalaktamasen (MBL) oder Klasse-D-Carbapenemasen wie OXA-48 angeht. Auch wirken sie nicht gegen A. baumannii oder S. maltophilia.
Nützlich ist hier das erste Siderophor-Cephalosporin Cefiderocol, das auch gegen MBL wirkt, weiters umfasst sein Spektrum auch P. aeruginosa, A. baumannii und S. maltophilia. Bei Carbapenem-resistentem Acinetobacter baumannii (CRAB) stellt es eine Alternative zu Colistin dar.
Kombinationstherapien können Synergismen bringen, etwa die Kombination von Betalaktam(BL)/Betalaktamaseinhibitor(BLI)-Kombinationen mit Fosfomycin (z.B. gegen multiresistenten P. aeruginosa) oder mit Aztreonam (z.B. gegen MBL-produzierende Klebsiella pneumoniae). Die Zugabe von Fosfomycin führt bei K. pneumoniae zu einem Abfall der MHK und zwar sowohl bei Verwendung einer BL/BLI-Kombination als auch bei Verwendung von Meropenem alleine.
Die Verwendung der erwähnten Substanzen ist insgesamt nur dann sinnvoll, wenn bekannte Lücken im Wirkspektrum beachtet und darüber hinaus konsequent Empfindlichkeitstestungen durchgeführt werden.
Dosierungsfehler vermeiden
Ein praktisches und eminent wichtiges Thema sind mögliche Dosierungsfehler, die bei BL/BLI-Kombinationen vorkommen können.
Beispiel Produkt Vaborem®: Diese Kombination aus Meropenem und Vaborbactam wird in Durchstichflaschen zu 1g/1g geliefert. Die Vorschreibung in der Praxis wird aber oft so vorgenommen, dass die Dosierungen beider Wirkstoffe zusammengezählt werden, und würde etwa lauten: „Vaborem® 4g 1–1–1. Hier müssten also pro Gabe je zwei Durchstichflaschen à 1g/1g verabreicht werden. Ähnliches gilt für andere BL/BLI-Kombinationen.
Anders beim Produkt Recarbrio®: Dieses besteht aus 500mg Imipenem, 500mg Cilastatin und 250mg Relebactam. Da Cilastatin aber selbst keine antibakterielle Wirkung besitzt, sondern nur die zu rasche Metabolisierung von Imipenem verhindert, wird Recarbrio® in der Regel als „750mg“ (also die Summe von 500mg Imipenem und 250mg Relebactam) vorgeschrieben.
„I“ heißt wirksam
Die EUCAST (Netzwerk unter der Schirmherrschaft der European Society of Clinical Microbiology and Infectious Diseases und des Europäischen Zentrums für die Prävention und die Kontrolle von Krankheiten) hat eine Definition ihrer Kategorie „I“ (wie „intermediär“ empfindlich) herausgegeben.
„I“ bedeutet nun: „empfindlich bei höherer Antibiotikaexposition“. Dies entspricht einer Hochdosistherapie im Gegensatz zu einer Standarddosierung. Hingegen bedeutet „S“ empfindlich bei Standarddosierung. Welche Dosierungen Standard bzw. Hochdosis sind, wird ebenfalls in EUCAST-Dokumenten festgehalten.
Das bedeutet nun konkret für Pseudomonas aeruginosa, dass dieser Erreger nach der neuen Definition bei praktisch keinem Antibiotikum (mit Ausnahme von Meropenem) unter die „S“-Kategorie fällt, weil er mit allen anderen Substanzen nur in höherer Dosierung behandelt werden kann. Das „I“ im Antibiogramm muss also neu verstanden und bewertet werden.
Quelle:
„Infektionen“, Vortrag von Univ.-Prof. Dr. Florian Thalhammer, MedUni Wien, im Rahmen des XXI. Hämatologiekurses der ONCONOVUM.academy, 5. Mai 2023, Jugendstilhörsaal, MedUni Wien
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...