Fokus auf Mutationen beim NSCLC
Zahlreiche Präsentationen beim ersten virtuellen Jahreskongress der AACR drehten sich um die Therapie des Lungenkarzinoms. Viele Arbeitsgruppen hatten sich mit dem Einfluss bestimmter Genmutationen auf die Therapie befasst; auch die Auswirkung des Raucherstatus wurde berichtet. So wurden unter anderem aktuelle Daten der Studien PACIFIC, RELAY und KEYNOTE-042 vorgestellt.
Keypoints
-
In einer kleinen Subgruppenanalyse der PACIFIC-Studie zeigten Raucher ein schlechteres Therapie-Outcome als Nichtraucher.
-
Das Vorliegen bestimmter EGFR-Mutationen verschlechtert die Prognose von NSCLCPatienten.
-
Der PD-L1-Inhibitor Pembrolizumab wirkt unabhängig vom Vorliegen von STK11- und KEAP1-Mutationen.
PACIFIC: Rauchen beeinflusst Immuntherapie
Die Phase-III-Studie PACIFIC hat den PD-L1-Inhibitor Durvalumab als Therapiestandard für Patienten mit lokal fortgeschrittenem und inoperablem nichtkleinzelligem Lungenkarzinom (NSCLC), die nach kombinierter Radiochemotherapie nicht progredient sind, etabliert.1 Dr. David Planchard vom Institut Gustave Roussy in Villejuif, Frankreich, befasste sich in seinem Vortrag mit dem Einfluss des Raucherstatus auf die Therapie mit Durvalumab.2
Von den 713 an PACIFIC teilnehmenden Patienten hatten 64 (9%) niemals geraucht. In dieser Subgruppe waren anteilig mehr Frauen und Asiaten als in der Raucherpopulation. Zudem wiesen die Nichtraucher histologisch häufiger ein nichtsquamöses NSCLC auf. Im Vergleich der beiden Therapiearme waren mehr Nichtraucher im Placeboarm im NSCLC-Stadium IIIB (52% vs. 40%) und mehr von ihnen hatten eine Chemotherapieinduktion erhalten (33% vs. 21%).2
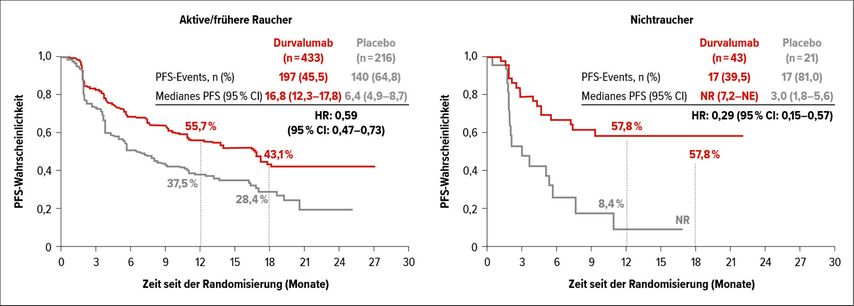
Sowohl bei den Rauchern wie auch bei den Nichtrauchern verbesserte Durvalumab im Vergleich zu Placebo das progressionsfreie (PFS) und Gesamtüberleben (OS). So betrug das mediane PFS unter Durvalumab bei den Rauchern rund 17 Monate (vs. Placebo 6,4 Monate). Bei den Nichtrauchern wurde der Median unter Durvalumab nicht erreicht (vs. Placebo 3 Monate) (Abb. 1). Der Median des OS wurde unter Durvalumab in der Rauchergruppe nicht erreicht (vs. Placebo 29 Monate); bei den Nichtrauchern lag das mediane OS bei rund 35 Monaten versus 19 Monate.2
In beiden Therapiearmen war die Rate an Nebenwirkungen Grad 3/4 bei Rauchern höher als bei Nichtrauchern. Dagegen traten in beiden Armen Pneumonien/Strahlenpneumonien jeglichen Grades häufiger bei Nichtrauchern auf. Planchard betonte, dass diese Unterschiede aufgrund der kleinen Subgruppe und der nicht ausgeglichenen Ausgangskriterien nicht geeignet seien, um daraus definitive Rückschlüsse auf die Outcomes bei Rauchern und Nichtrauchern zu ziehen.2
RELAY: Ergebnisse des Next Generation Sequencing
Die RELAY-Studie hatte bei nicht vorbehandelten Patienten mit fortgeschrittenem, EGFR-mutiertem NSCLC ein überlegenes PFS für die Kombination aus Ramucirumab plus Erlotinib (Ram/Erl) versus Placebo plus Erlotinib (Pbo/Erl) gezeigt (19,4 vs. 12,4 Mon.; p<0,0001). Eingeschlossen waren Patienten mit den EGFR-Mutationen Exon 19del oder Exon 21.L858R, ECOG-Performance-Status 0 oder 1 ohne Hirnmetastasen. Vor Therapiebeginn, zu Zyklus 4 sowie nach Therapieende wurden Flüssigbiopsien entnommen.3
Prof. Edward Garon vom UCLA Medical Center, Santa Monica, USA, und Kollegen untersuchten die nachgewiesenen Genmutationen mittels NextGenerationSequencing (NGS) auf potenzielle Biomarker und therapiebedingte Veränderungen, die für die Wahl von Folgetherapien relevant sein könnten. Bei der Ausgangsanalyse wurden 69 veränderte Gene gefunden, darunter ALK, MET und TP53, wobei ALK und MET das PFS und die Ansprechdauer (DOR) nicht beeinflussten. Dagegen waren TP53-Veränderungen mit einer schlechteren Prognose verbunden (p<0,001), zeigten aber auch einen Trend hin zu einer besseren Ram-Wirkung. Weitere prognostische Marker für ein kürzeres PFS waren PIK3CA (p=0,017) und EGFR „andere“ (p=0,04).4
Genveränderungen, die unter der Therapie entstanden waren, fanden sich in beiden Studienarmen mit ähnlicher Häufigkeit. Garon wies allerdings darauf hin, dass die Anzahl der ausgewerteten Proben gering war und möglicherweise einem Bias unterlag. Er hofft, dass zum Zeitpunkt der finalen OS-Auswertung klarere Daten zum Auftreten von Genveränderungen unter der Therapie vorliegen werden.4
KEYNOTE 042: Einfluss von KEAP1- und STK11-Mutationen auf Outcome
Prof. Byoung Chul Cho, Yonsei University, Seoul, Korea, präsentierte die Ergebnisse seiner explorativen Analyse der Studie KEYNOTE-042, in der er die Prävalenz der Genmutationen STK11 und KEAP1 sowie deren Einfluss auf die Therapie untersuchte. Beide Mutationen gehen mit Chemotherapieresistenz sowie schlechter Prognose bei Patienten mit NSCLC einher und werden häufiger bei PD-L1-negativen Tumoren mit hoher Mutationslast (TMB) gefunden. Cho und Kollegen bestimmten den Mutationsstatus und die TMB mittels Gesamt-Exom-Sequenzierung (WES) im Tumorgewebe und in normaler DNA. Zudem ermittelten sie den PD-L1-Status.5
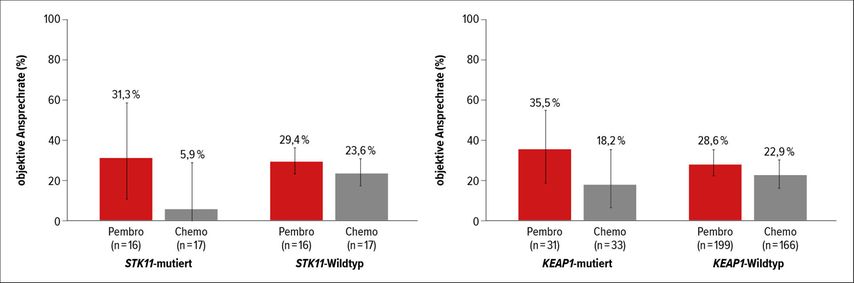
In KEYNOTE-042 wurde bei nicht vorbehandelten Patienten mit PD-L1-positivem, fortgeschrittenem NSCLC die Monotherapie mit Pembrolizumab mit einer Chemotherapie nach Wahl des Arztes verglichen. Die Pembrolizumabgabe resultierte in einem überlegenen OS in allen „Tumor Proportion Score“(TPS)-Gruppen.6 Von 429 der mehr als 1200 Studienteilnehmer lagen auswertbare WES-Daten vor. Davon wiesen 33 (8%) eine STK11- und 64 (15%) eine KEAP1-Mutation auf. Bei 12 (3%) Patienten wurden beide Mutationen gefunden. Patienten mit STK11-Mutation hatten tendenziell einen niedrigeren PD-L1-TPS als Patienten ohne diese Mutation (15 vs. 40%). Bei KEAP1 wurde kein Unterschied beobachtet: Patienten mit und ohne diese Mutation hatten einen TPS von 40%. Der TMB-Score war jeweils bei Patienten mit Mutationen höher als bei solchen ohne (STK11: 191 vs. 146; KEAP1 183 vs. 142).5 Die Mutationen hatten jedoch keinen Einfluss auf die Wirksamkeit von Pembrolizumab: PFS, OS und objektive Ansprechrate (ORR, Abb. 2) waren jeweils vergleichbar. Dagegen war die Wirksamkeit der Chemotherapie bei Patienten mit STK11-Mutation herabgesetzt. Die Autoren empfehlen daher Pembrolizumab – unabhängig vom STK11- und KEAP1-Status – als Standard in der Erstlinientherapie bei Patienten mit fortgeschrittenem, PD-L1-positivem NSCLC.5
Bericht:
Dr. Corina Ringsell
Quelle:
AACR Virtual Annual Meeting I, 27.–28. April 2020
Literatur:
1 Produktinformation Imfinzi® der Europäischen Arzneimittel-Agentur (www.ema.europa.eu) 2 Planchard D et al.: Impact of smoking on outcomes with durvalumab following chemoradiotherapy in unresectable Stage III NSCLC (PACIFIC). AACR Virtual Meeting 2020, Poster CT213 3 Nakagawa K et al.: Ramucirumab plus erlotinib in patients with untreated, EGFR-mutated, advanced non-small-cell lung cancer (RELAY): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet Oncol 2019; 20: 1655-69 4 Garon EB et al.: RELAY, ramucirumab plus erlotinib (RAM+ERL) versus placebo plus erlotinib (PBO+ERL) in previously untreated EGFR mutation-positive metastatic NSCLC: Next generation sequencing (NGS) results. AACR Virtual Meeting 2020, Poster CT215 5 Cho BC et al.: Relationship between STK11 and KEAP1 mutational status and efficacy in KEYNOTE-042: pembrolizumab monotherapy versus platinum-based chemotherapy as first-line therapy for PD-L1-positive advanced NSCLC. AACR Virtual Meeting 2020, Abstr. CT084 6 Mok TSK et al.: Pembrolizumab versus chemotherapy for previously untreated, PD-L1-expressing, locally advanced or metastatic non-small-cell lung cancer (KEYNOTE-042): a randomised, open-label, controlled, phase 3 trial. Lancet 2019; 393: 1819-30
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...