Eine Symphonie des Fortschritts
Bericht:
Dr. Kassandra Settele
Review von:
OA Dr. Maximilian J. Hochmair
Leiter der pneumo-onkologischen
Ambulanz und Tagesklinik
Abteilung für Innere Medizin und Pneumologie
Karl Landsteiner Institut für Lungenforschung
und pneumologische Onkologie
Krankenhaus Nord – Klinik Floridsdorf, Wien
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Aufgrund der Covid-19-Pandemie konnte die 2020 World Conference on Lung Cancer (WCLC) erst im Jänner 2021 stattfinden – und dies erstmalig als virtuelle Tagung. Wiegehabt bot die Konferenz eine höchst informative Plattform zur Fortbildung auf dem Gebiet des Lungenkrebses. Durch das virtuelle Format konnte eine noch größere Zielgruppe erreicht werden, auch wenn der persönliche Faktor etwas zu kurz kam.
NSCLC: Präzisionsmedizin
ITACA-Studie
Platin-basierte Chemotherapien bieten im Frühstadium von nicht kleinzelligen Lungenkarzinomen (NSCLC) nur einen geringen Überlebensvorteil von 5%. Daher besteht die Notwendigkeit, diejenigen Patienten zu identifizieren, die von ihnen profitieren können, und jene anderen, die keinen Vorteil daraus ziehen, nicht mit den toxischen Nebenwirkungen (AE) zu belasten. Die finalen Ergebnisse der von Dezember 2008 bis August 2014 zu dieser Fragestellung durchgeführten ITACA-Studie wurden bei der WCLC 2020 mit größter Spannung erwartet.
Eine Möglichkeit der Patientenselektion besteht in der Analyse der mRNA-Expressionslevel bestimmter molekularer Marker. Potenzial hierfür wurde in den Markern Excision Repair Cross Complementation 1 (ERCC1) und Thymidylatsynthase (TS) gesehen: In Berichten war eine hohe Expression von ERCC1 mit Resistenzen gegen Platin-basierte Therapien verbunden. Überdies konnte eine geringe Expression von TS mit einer höheren Wirksamkeit von Cisplatin plus Permetrexed bei Lungenadenomkarzinomen (und einer geringeren Wirksamkeit bei kleinzelligen Lungenkarzinomen [SCLC]) assoziiert werden.
Die Autoren untersuchten daher in dieser offenen, randomisierten Phase-III-Studie, ob ERCC1 und TS in der adjuvanten Therapie des NSCLC einen prädiktiven Wert haben. 773 Patienten wurden 6–12 Wochen nach Komplettresektion eines NSCLC im Stadium II–III in die Studie eingeschlossen und ihnen operativ entnommene Gewebeproben wurden genetisch untersucht. Anhand des genomischen Profils wurden die Patienten in vier Gruppen aufgeteilt und dann pro Gruppe zu einer für das jeweilige Profil „maßgeschneiderten“ Therapie vs. Standardtherapie bzw. Therapie nach Wahl des Behandlers randomisiert.
Insgesamt konnte kein Vorteil der Gabe einer „maßgeschneiderten“ adjuvanten Platin-basierten Chemotherapie für das Gesamtüberleben (OS) gezeigt werden, sodass sich das Studiendesign in der „realen Welt“ wohl nicht etablieren wird. Das Nebenwirkungsprofil konnte dennoch durch die individualisierte Therapie verbessert werden. Um die adjuvante Chemotherapie an die Patienten individuell anpassen zu können, wird es daher andere, differenziertere und effizientere Techniken brauchen.1
REFRACT-Studie
Diese retrospektive Analyse untersuchte den Einfluss von Radiotherapie, Tyrosinkinase-Inhibitoren (TKI) und Chemotherapie auf den Therapieerfolg bei nicht resezierbarem, lokal fortgeschrittenem NSCLC mit „Epidermal growth factor receptor“(EGFR)-Mutationen. Zur Frage nach dem Nutzen von TKI im Stadium IIIA/B gibt es bislang nur unzureichend Daten.
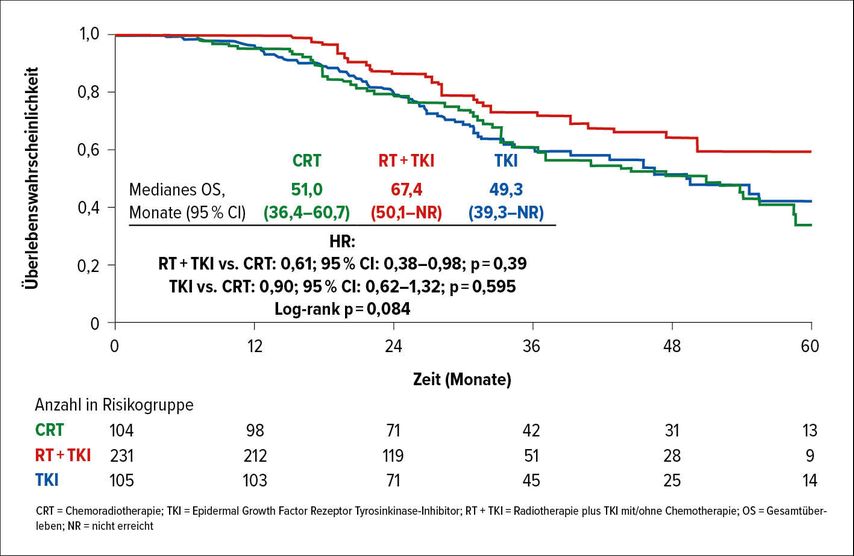
Von 2137 Patienten, die ein lokal fortgeschrittenes NSCLC hatten und zwischen 2012 und 2019 auf EGFR-Mutationen genotypisiert wurden, konnten bei 516 (24,1%) EGFR-Mutationen nachgewiesen werden. Bei 440 Patienten gab es genug Daten zum Einschluss in die Wirksamkeitsanalyse. Sie wurden nach Therapieart in drei Gruppen geteilt: kombinierte Radiotherapie mit EGFR-TKI mit/ohne Chemotherapie (TKI+RT; n=105), Chemoradiotherapie (CRT; n = 104) oder alleinige Therapie mit EGFR-TKI (TKI; n=231).
Bezüglich des OS zeigte sich ein klarer Vorteil für die Kombination TKI+RT mit einem medianen OS von 67,4 Monaten (CRT: 51,0 Monate; TKI: 49,3 Monate; Abb.1). Auch das progressionsfreie Überleben (PFS) war unter TKI+RT verlängert mit 26,2 Monaten (CRT 12,4 Monate; TKI 16,2 Monate). Das verbesserte Outcome könnte durch eine effektive Kontrolle von sowohl lokoregionalem als auch peripherem Krankheitsgeschehen erklärt werden.
Die Kombination von EGFR-TKI und Radiotherapie im Sinne der Präzisionsmedizin ist den Studiendaten zufolge die beste Behandlungsstrategie ohne eine relevante Erhöhung der AE. Weitere randomisierte, prospektive Daten sind jedoch vonnöten.2
Biomarker für Therapieentscheidung
Eine weitere retrospektive Analyse beschäftigte sich mit der Eignung von KRAS- und TP53-Mutationen als Biomarker in der Entscheidung über die Immuntherapie bei NSCLC-Patienten ohne EGFR- oder ALK-Mutation. Es zeigte sich, dass mit einer Immuntherapie bei Vorliegen beider Mutationen ein klar längeres PFS erzielt werden konnte, als wenn nur eine oder keine Mutation vorlag. Im Zweifelsfall könnte der Mutationsstatus also in die Entscheidung betreffend Immuntherapie miteinbezogen werden.3
NSCLC: zielgerichtete Therapien
Mobocertinib
Hochinteressant war eine Studie zu Mobocertinib, einem Antikörper, der bei Patienten mit einer EGFR-Exon-20-Insertion wirksam ist. Diese Mutation liegt zwar bei 2% aller NSCLC vor, doch bisher existiert keine spezifische Therapie.
Bei der WCLC wurden erste Daten der Phase-I/II-Kohorte der mit Platin-basierten Therapien vorbehandelten Patienten (PPP) und der EXCLAIM-Extension-Kohorte vorgestellt. Die Patienten befanden sich bereits in der zweiten oder dritten Therapielinie und erhielten 160mg Mobocertinib einmal täglich p.o. Nahezu alle profitierten von der Therapie: Bei 82% (PPP) bzw. 80% (EXCLAIM) konnte eine Reduktion des Durchmessers der Zielläsion erreicht werden. Die Rate an allgemeinem Ansprechen (ORR) lag in der PPP-Kohorte bei 30% und in der EXCLAIM-Kohorte bei 22%. Das mediane PFS betrug in beiden Gruppen 7,3 Monate, während sich die mediane Ansprechdauer (DOR) in der PPP-Kohorte auf 17,5 Monate belief und in der EXCLAIM-Kohorte noch nicht abschätzbar war. Bei einem Großteil der Patienten konnte in beiden Gruppen eine DOR >6 Monate beobachtet werden (78% PPP; 84% EXCLAIM). Zum Zeitpunkt des Data-Cut-offs wiesen über 50% ein andauerndes Ansprechen auf.
Die Substanz ist gut verträglich, mit den von „2nd Generation“-TKI bekannten AE wie z.B. Diarrhö, Übelkeit, Hautausschlag oder Paronychie. AE ≥Grad 3 traten bei 46% der PPP- bzw. 41% der EXCLAIM-Patienten auf. Ein Patient starb aufgrund von behandlungsbedingtem Herzversagen.
Gespannt werden die Daten der Phase-III-Studie zu Mobocertinib erwartet.4
Nivolumab ± Ipilimumab
Da eine Monotherapie mit einem PD-1-Inhibitor bei NSCLC mit EGFR-Mutation nur eine geringe Wirksamkeit hat, wurde in dieser Studie die Wirksamkeit der Kombination aus zwei Checkpoint-Inhibitoren überprüft: Ipilimumab als Verstärker der T-Zell-Funktion sollte dabei die Wirksamkeit von Nivolumab verbessern.
Die Studie hatte zwar mit nur 31 eingeschlossenen Patienten eine kleine Studienpopulation, jedoch kristallisierte sich eine klare Botschaft heraus: Eine alleinige Immuntherapie war bei einem Großteil der Patienten nicht wirksam und durch die Zugabe von Ipilimumab konnte kein klinischer Vorteil erzielt werden. Das mediane PFS betrug 1,31 Monate für Nivolumab alleine und 1,22 Monate für die Kombinationstherapie. Ein Patient in der Kombinationsgruppe erreichte ein partielles Ansprechen (PR) – allerdings ist unklar, welche Faktoren eine Wirksamkeit ermöglicht haben könnten.5
KEYNOTE-598
Hierbei handelt es sich um eine weitere negative Studie, die dennoch nicht unerwähnt bleiben soll. Patienten mit metastasiertem NSCLC mit PD-L1-Tumor-Proportion-Score (TPS) ≥50% und ohne angreifbare EGFR- oder „Anaplastische Lymphomkinase“(ALK)-Veränderungen wurden 1:1 randomisiert zu Pembrolizumab plus Ipilimumab (Pembro-Ipi) oder plus Placebo (Pembro-Pla). Das OS für Pembro-Ipi vs. Pembro-Pla war mit einer HR von 1,08 (95% CI: 0,85–1,37; p=0,74) und das PFS mit einer HR von 1,06 (95% CI: 0,86–1,30; p=0,72) ähnlich. Die ORR war mit 45,4% in beiden Armen gleich.
Insgesamt zeigte sich durch die Kombinationstherapie kein Vorteil, während die AE zunahmen (76,2% vs. 68,3%). Die Studie wurde daher auf Empfehlung des externen Datenbeobachtungskomitees abgebrochen.6
Patritumab Deruxtecan
Patritumab Deruxtecan ist ein HER3-gerichtetes Antikörper-Konjugat, dessen Sicherheit und Wirksamkeit bei Patienten mit fortgeschrittenem EGFR-mutiertem NSCLC nach Versagen von TKI und Platin-basierter Chemotherapie in dieser Phase-I-Studie untersucht wurde.
Die Patienten erhielten 5,6mg/kg der Substanz i.v. q3w. Unabhängig vom Resistenzmechanismus konnte eine Wirksamkeit gezeigt werden. Die ORR betrug 25%, eine Krankheitskontrolle konnte in 70% erzielt werden. Die mediane DOR belief sich auf 7 Monate. Als häufigste Nebenwirkungen ≥Grad 3 wurden Thrombozytopenie und Neutropenie beschrieben.7
NSCLC: Stadium IV
Beeindruckende Ansprechraten
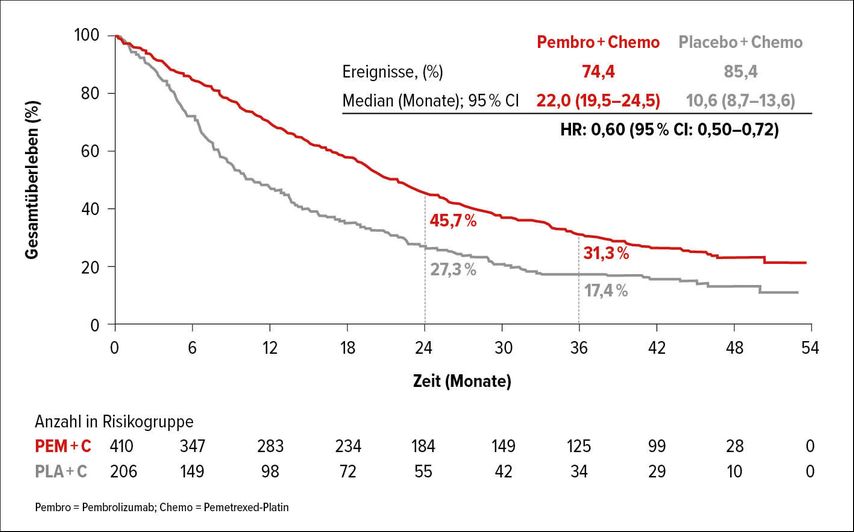
Als Featured Poster wurde das 4-Jahres-Follow-up der KEYNOTE-189-Studie präsentiert. In dieser Phase-III-Studie wurde das Ansprechen auf Pemetrexed-Platin in Kombination mit Pembrolizumab (n = 410) vs. Placebo (n = 206) als Erhaltungstherapie (über zwei Jahre oder bis zum bildmorphologischen Progress/bis zu inakzeptabler Toxizität) verglichen. Dabei zeigte sich, dass die Chemo-Immuntherapie der alleinigen Chemotherapie auch im 4-Jahres-Follow-up klar überlegen war.
Es konnten geradezu beeindruckende Ansprechraten gezeigt werden: Das mediane OS betrug unter der Kombinationstherapie 22,0 Monate vs. 10,6 Monate unter alleiniger Chemotherapie (HR: 0,60; 95% CI: 0,50–0,72). Die Rate des 3-Jahres-Überlebens betrug 31,3% vs. 17,4% (Abb.2). Auch das PFS war bemerkenswert im Vorteil mit 9,0 Monaten vs. 4,9 Monaten (HR: 0,50; 95% CI: 0,41–0,59). AE ≥Grad 3 traten bei 72,1% vs. 67,3% auf.
Bei 87,5% der 56 Patienten, die die Erhaltungstherapie mit Pembrolizumab erhalten zwei Jahre lang hatten, konnte ein objektives Ansprechen gezeigt werden: Ein komplettes Ansprechen (CR) erzielten sechs Patienten, ein PR 43 Patienten. Darüber hinaus erreichten sieben Patienten eine Krankheitsstabilisierung (SD). Zum Zeitpunkt des Cut-offs waren 45 Patienten (80,4%) noch am Leben, von ihnen 28 Patienten ohne PD.
Auch in Bezug auf das progressionsfreie Überleben unter der ersten Folgetherapie (PFS2) zeigte sich die Kombination vorteilhaft: Nach 3 Jahren betrug das PFS2 27,8% vs. 10,6%.
Unabhängig von einer PD-L1-Expression zeigte sich die Chemo-Immuntherapie vorteilhaft. Diese Therapie ist der Goldstandard für das neu diagnostizierte, metastasierte NSCLC. Auch für einen neoadjuvanten Ansatz könnte sie interessant sein.8
Nab-Paclitaxel vs. Docetaxel
Recht spannend war die Phase-III-Studie zum Vergleich von Nanopartikel-Albumin-gebundenem(nab) Paclitaxel (n-P) mit Docetaxel (D) bei Patienten mit vorbehandeltem NSCLC. Beide Therapien haben unterschiedliche Schwächen: Die Verträglichkeit von D ist schlechter, aber n-P muss einmal wöchentlich verabreicht werden.
503 japanische Patienten wurden 1:1 randomisiert. In Bezug auf das OS konnte die Gleichwertigkeit von n-P (16,2 Monate) zu D (13,6 Monate) bestätigt werden. Eine Überlegenheit konnte statistisch allerdings nicht nachgewiesen werden. Hinsichtlich des medianen PFS zeigte sich dennoch ein signifikanter Vorteil von n-P mit 4,2 Monaten vs. 3,4 Monate. Auch die ORR war unter n-P signifikant verbessert mit 29,9% vs. 15,4%, dies zeigte sich unabhängig von der Tumor-Histologie. Das Nebenwirkungsprofil der beiden Substanzen ist unterschiedlich – hämatologische AE waren unter n-P seltener. Eine febrile Neutropenie ≥Grad 3 trat bei 22% der D-Patienten auf, jedoch nur bei 2% der Patienten in der n-P-Gruppe. Eine periphere sensorische Neuropathie trat hingegen unter n-P häufiger auf mit 55,5% vs. 20,1%.9
Kleinzelliges Lungenkarzinom
Lurbinectedin
Beim SCLC handelt es sich bekanntermaßen um eine aggressive Krebserkrankung mit schlechter Prognose: Die 5-Jahres-Überlebens-Rate liegt bei nur 7%. Es besteht ein „unmet medical need“, da derzeit keine befriedigende Therapieoption vorhanden ist.
Lurbinectedin ist ein neuer Wirkstoff, der über die Inhibition der transaktivierten Transkription und Modulation der Tumor-Mikroumgebung wirkt. Im Juni 2020 ermöglichte die FDA in den USA eine beschleunigte Zulassung für Lurbinectedin als Therapie des metastasierten SCLC nach PD unter Platintherapie.
In präklinischen Studien wurde bereits ein synergistischer Effekt von Lurbinectedin mit Irinotecan berichtet. Die spanisch-amerikanische Forschungsgruppe unter Ponce-Aix evaluierte in dieser Phase-I/II-Studie Wirksamkeit und Sicherheit der Kombinationstherapie. 21 Patienten, die zuvor maximal zwei Therapielinien erhalten hatten und einen Eastern Cooperative Oncology Group (ECOG) Performance Status Score von 0–1 hatten, wurden in die Studie aufgenommen. Die vorgeschlagene Dosierung betrug 2mg/m2 Lurbinectedin an Tag 1 plus 75 mg/m2 Irinotecan an Tag 1 und 8 q3w plus die prophylaktische Gabe von Granulozyten-Kolonie stimulierendem Faktor (G-CSF).
Im Median erhielten die Patienten 7 Zyklen der Kombinationstherapie. Die ORR betrug 62%, eine Krankheitskontrolle (PR/SD) konnte in 90% erzielt werden. Die mediane DOR belief sich auf 5,7 Monate und das mediane PFS auf 6,2 Monate.
Bei sechs Patienten (28,6%) trat eine Grad-4-Neutropenie auf, bei zwei Patienten eine febrile Neutropenie (9,5%). Es kam zu keiner Anämie oder Thrombozytopenie von Grad 4. Nichthämatologische Toxizitäten traten lediglich ≤Grad 3 auf. Keinen fatalen AE oder Therapieabbrüche aufgrund einer toxischen Arzneimittelwirkung wurden berichtet. Das Nebenwirkungsprofil war insgesamt vorübergehend und gut handhabbar.
Die Kombinationstherapie mit Lurbinectedin und Irinotecan konnte somit ihre Wirksamkeit nach einer Erstlinientherapie beweisen. Sogar bei Patienten mit einer resistenten Erkrankung (Chemotherapie-freies Intervall < 90 Tage) konnte eine bemerkenswerte Aktivität erzielt werden.10
Atezolizumab
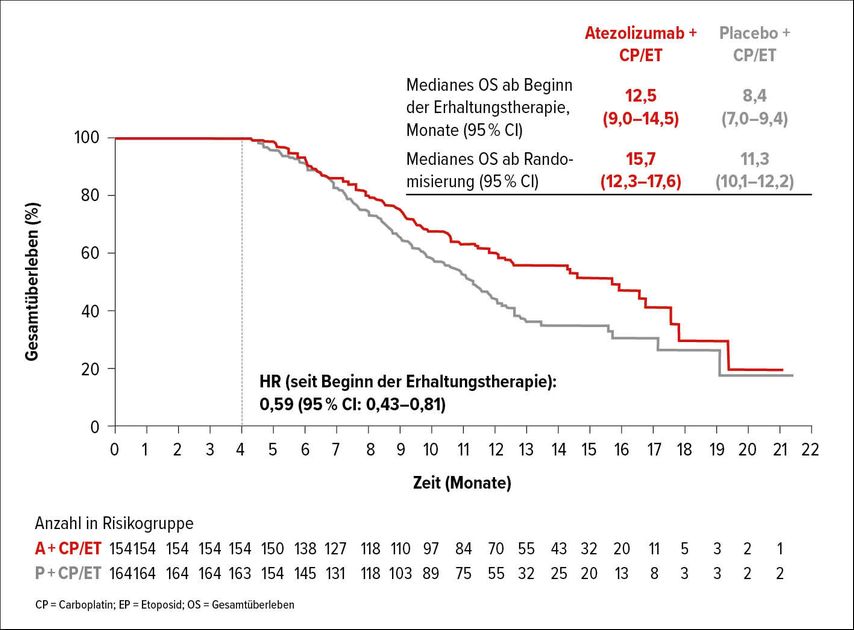
Beim fortgeschrittenen SCLC werden derzeit verschiedene Immuntherapien untersucht. Bisher konnte jedoch keine Studie ein verlängertes Überleben unter einer Erhaltungsimmuntherapie zeigen. In der IMpower133-Studie wurde im Erstliniensetting die Zugabe von und Erhaltungstherapie mit dem Anti-PD-L1-Antikörper Atezolizumab zur Carboplatin+Etoposid-Therapie untersucht. 403 nicht vorbehandelte Patienten mit fortgeschrittenem SCLC wurden 1:1 randomisiert zu vier Zyklen Carboplatin plus Etoposid mit 1200mg i.v. Atezolizumab oder mit Placebo. Die Erhaltungstherapie mit Atezolizumab/Placebo wurde bis zum Auftreten inakzeptabler Toxizität, PD oder bis zum klinischem Wirksamkeitsverlust durchgeführt. Zum Zeitpunkt des Data-Cut-offs betrug die mediane Zeit bis zum Follow-up 13,9 Monate. Der Zusatz von Atezolizumab führte zu einem signifikant längeren OS und PFS im Vergleich mit Placebo: Das mediane OS belief sich auf 15,7 Monate im Atezolizumab-Arm und 11,3 Monate im Placebo-Arm (HR: 0,67; 95% CI: 0,49–0,90; p=0,008; Abb. 3). Das mediane PFS betrug 5,5 bzw. 4,5 Monate (HR: 0,73; 95% CI: 0,57–0,92; p=0,008). Es wurden keine neuen Sicherheitssignale identifiziert. Die Erhaltungstherapie scheint zum Überlebensvorteil von Atezolizumab in der IMpower133-Studie beizutragen.11
Mesotheliom
CheckMate 743
Die CheckMate-743-Studie konnte sich als bahnbrechend erweisen und wird voraussichtlich einen neuen Goldstandard in der Erstlinientherapie des Mesothelioms schaffen, weshalb sie bereits beim Presidential Symposium im August vorgestellt wurde.
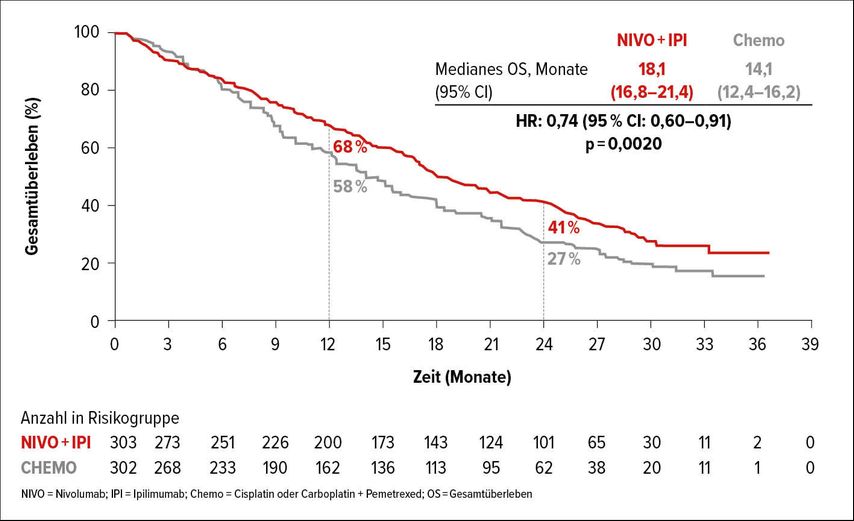
605 Patienten mit einem nicht resezierbaren pleuralen Mesotheliom, die bisher keine systemische Therapie erhalten hatten und einen ECOG Performance Status von 0–1 aufwiesen, wurden 1:1 randomisiert. Die Prüfgruppe erhielt 3mg/kg Nivolumab i.v. alle zwei Wochen plus 1 mg/kg Ipilimumab i.v. alle sechs Wochen für zwei Jahre oder bis eine Toxizität/ein PD auftrat. Die Kontrollgruppe erhielt sechs Zyklen Cisplatin oder Carboplatin plus Pemetrexed. Nach einer medianen Follow-up-Zeit von 29,7 Monaten kristallisierte sich ein klarer statistischer Vorteil der Immuntherapie in Bezug auf das OS heraus mit einer HR von 0,74 (96,6% CI: 0,60–0,91; p=0,0020; Abb. 4). Dabei hatte keine der untersuchten Subgruppen einen Nachteil durch die Therapie mit Nivolumab/Ipilimumab. Jedoch profitierten jene Patienten, die an einem nicht epithelioiden Mesotheliom erkrankt waren, besonders stark von der Therapie, mit einer HR von 0,46 (95% CI: 0,31–0,68).12
CONFIRM-Studie
Bei der CONFIRM-Studie handelt es sich um eine Phase-III-Studie, in der Nivolumab mit Placebo beim rezidivierten Mesotheliom verglichen wurde. Bisher konnte in keiner randomisierten Phase-III-Studie ein verlängertes Gesamtüberleben im rezidivierten Setting erwirkt werden.
Die hier eingeschlossenen Patienten hatten in der Erstlinie eine Chemotherapie erhalten. Das mediane OS betrug unter Nivolumab 9,2 Monate, unter Placebo 6,6 Monate. Das geschätzte Gesamtüberleben nach 12 Monaten beträgt in der Nivolumab-Kohorte 39,5% und 26,9% in der Placebo-Kohorte. Nivolumab kann demzufolge als eine Therapieoption in der Zweitlinie betrachtet werden.13
Quelle:
2020 World Conference on Lung Cancer, 28.–31. Jänner 2021
Literatur:
1 Novello S et al.: WCLC 2020; Abstr. #PS01.04 2 Bi N et al.: WCLC 2020; Abstr. #OA02.06 3 Li L et al.: WCLC 2020; Abstr. #OA07.06 4 Zhou C et al.: WCLC 2020; Abstr. #OA04.03 5 Lai G et al.: WCLC 2020; Abstr. #OA01.06 6Boyer M et al.: WCLC 2020; Abstr. #PS01.09 7 Yu H et al.: WCLC 2020; Abstr. #OA03.04 8 Gray J et al.: WCLC 2020; Abstr. #FP13.02 9 Nakamura A et al.: WCLC 2020; Abstr. #OA03.05 10 Ponce-Aix S et al.: WCLC 2020; Abstr. #OA11.04 11 Reck M et al.: WCLC 2020; Abstr. #OA11.06 12Baas P et al.: Lancet 2021; 397(10272): 375-86 13 Fennell D et al.: WCLC 2020; Abstr. #PS01.1
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...