Die wichtigsten Daten vom ASCO 2020 aus der Dermatoonkologie
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Auf der virtuellen Jahrestagung der ASCO wurden viele Studienupdates zu Melanomtherapien präsentiert. Aber auch Präsentationen zu experimentellen neuen Therapien und Biomarkeranalysen fanden ihren Platz. Im Folgenden ein Überblick über die spannendsten Ergebnisse.
(Neo)adjuvante Therapie des Melanoms
EORTC 1325/KEYNOTE-054
Hier wurden die Daten des medianen 3-Jahres-Follow-ups der Phase-III-Studie EORTC1325/Keynote-054 (Pembrolizumab vs. Placebo nach kompletter Resektion von Stadium-III-Melanomen) präsentiert.1 In der Studie erhielten Melanompatienten im Stadium IIIA, IIIB und IIIC (AJCC-Klassifikation, 7. Edition) mit mehr als 1-mm-Metastase in Sentinellymphknoten 1:1-randomisiert entweder Pembrolizumab 200mg alle 2 Wochen oder Placebo für 1 Jahr. Im Falle einer Progression gab es die Möglichkeit eines Cross-overs für jene Patienten, die im Placeboarm waren oder ein Rezidiv >6 Monate im Pembrolizumab-Arm hatten. Im Follow-up von median 3 Jahren waren 63,7% der Patienten im Pembrolizumab-Arm lebend und tumorfrei im Vergleich zu 44,1% im Placeboarm, dies ergab eine Hazard-Ratio (HR) von 0,56 (Abb. 1). PD-L1-positive Patienten waren im Therapiearm mit 65,3% rückfallfrei im Vergleich zu 56,9% bei PD-L1-negativen Patienten (vs. 52,2 und 33,3 respektive im Placeboarm). Der Unterschied im rezidivfreien Überleben (RFS) wurde in allen Stadien beobachtet (Stadium IIIA: HR von 0,50; Stadium IIIB: HR von 0,56; Stadium IIIC: HR von 0,57). Es zeigte sich kein Unterschied im RFS in Bezug auf den BRAF-Mutationsstatusim Therapiearm. Dort zeigten sich in 37,7% immunvermittelte Nebenwirkungen; ≥Grad III bei 7,7%. Vorherrschend waren gastrointestinale Symptomatiken als auch endokrine Symptomatiken. Das RFS vonBRAF-mutierten Patienten war ähnlich zu dem in der COMBI-AD-Studie. Patienten, die eine autoimmune Nebenwirkung aufwiesen, waren im Pembrolizumab-Arm mit längerem RFS vergesellschaftet, nicht jedoch im Placeboarm.
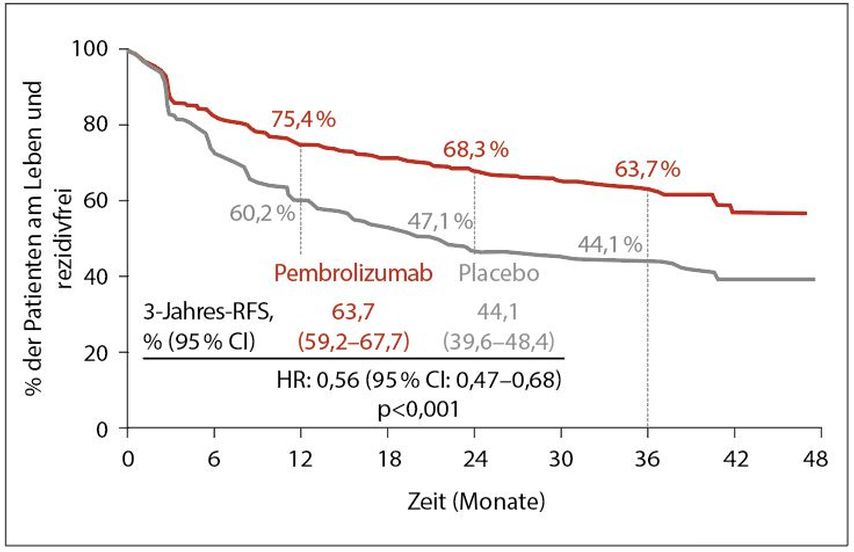
Abb. 1: Rezidivfreies Überleben in der Studie EORTC 1325/KEYNOTE-054 (nach Eggermont AM et al.)1
COMBI-AD
Als zweite Studie wurde die 5-Jahres-Auswertung der COMBI-AD-Studie präsentiert. Auch diese Studie hatte ähnliche Einschlusskriterien.2 Einzig eine BRAF-Mutation (V600E oder V600K) war Voraussetzung. Nach 1:1-Randomisierung erfolgte die Zuteilung zu Dabrafenib und Trametinib in den zugelassenen Dosierungen versus 2 gematchte Placebos. Die nunmehrige Analyse bezog sich auf das RFSwie auch das Fernmetastasen-freie Überleben mit einem medianen Follow-up von 60 Monaten. Im Vergleich zu den 4-Jahres-Daten (RFS von 55%) zeigte sich nach 5 Jahren nun ein rezidivfreies Überleben von 52% im Therapiearm, im Placeboarm (RFS nach 4 Jahren: 38%) von 36% (Abb. 2). Der Vorteil im Therapiearm zog sich durch sämtliche Subgruppen unabhängig von Geschlecht, Alter, Mikro- vs. Makrometastase und Anzahl der Lymphknotenmetastasen. Im Stadium IIIA betrug das RFS 65% im Therapiearm vs. 58% im Placeboarm,im Stadium IIIB 55% vs. 34% und im Stadium IIIC 45% vs. 29%. Bei der Umklassifizierung auf die 8. Edition AJCC zeigte sich ein anderes Bild. Das RFS betrug im Stadium IIIA 70% im Therapiearm vs. 71% im Placeboarm, bei einer geringen Patientenzahl, im Stadium IIIB 57% vs. 38%, im Stadium IIIC 47% vs. 30% und im Stadium IIID 43% vs. 18%. Das Fernmetastasen-freie Überleben (Fernmetastasen als erste Lokalisation des Rezidivs) war 65% vs. 54%.
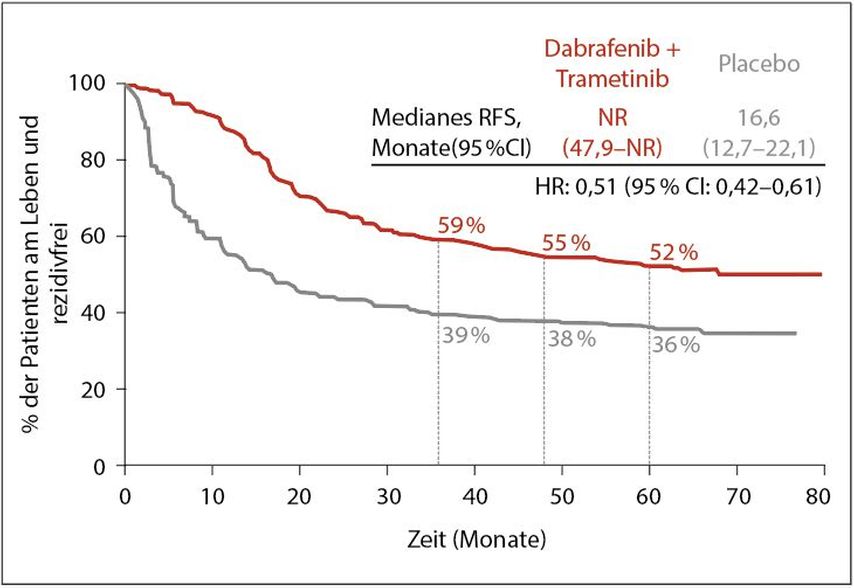
Abb. 2: Rezidivfreies Überleben in der Studie COMBI-AD (nach HauschildA et al.)2
PRADO
Im neoadjuvanten Bereich wurden Sicherheits- und Wirksamkeitsdaten der PRADO-Studie präsentiert.3 Dabei handelt es sich um eine Phase-II-Studie, die den neoadjuvanten Einsatz von Ipilimumab plus Nivolumab untersucht. In der Studie erhielten Patienten mit resezierbarem Melanom im Stadium IIIB, IIIC Ipilimumab 1mg/kg und Nivolumab 3mg/kg insgesamt zwei Zyklen nach vorheriger Markierung eines sogenannten Index-Lymphknotens. Dieser Index-Lymphknoten wurde nach den zwei Zyklen Ipilimumab + Nivolumab entfernt. Zeigte der Lymphknoten eine komplette pathologische Remission oder eine beinahe pathologische Remission, wurde keine Lymphadenektomie durchgeführt und der Patient entsprechend den vorgegebenen Studienleitlinien nachgesorgt. Zeigte der Patient ein partielles Ansprechen im Lymphknoten, und zwar über 10% und unter 50% lebendes Tumorgewebe, erfolgte eine Lymphadenektomie mit anschließenden Follow-up-Untersuchungen. Die dritte Gruppe waren die Patienten, die keine pathologische Remission zeigten (mehr als 50% lebende Tumorzellen). Bei diesen Patienten wurde eine Lymphknotendissektion angeschlossen und sie erhielten entweder Nivolumab alle 4 Wochen oder bei Nachweis einer BRAF-Mutation Dabrafenib und Trametinib für 1 Jahr. Die Kohorte umfasste 99 Patienten und zeigte in 50% der Fälle eine pathologische Komplettremission, in 11% eine beinahe pathologische Komplettremission, in 10% eine partielle pathologische Remission und in 21% kein Ansprechen. Das radiologische Ansprechen unterschätzte das pathologische Ansprechen, war jedoch wertvoll beim Identifizieren von Patienten, die vor der Entfernung des Index-Lymphknotens zu Stadium IV progredient waren (7%). Eine komplette Lymphknotendissektion wurde bei 60% der Patienten eingespart – dies zeigte sich auch in der Morbidität des chirurgischen Eingriffes, der in der Patientengruppe mit der kompletten Lymphadenektomie deutlich erhöht war (unerwünschte Ereignisse bezogen auf den Eingriff: 81% vs. 41%).
Palliative Therapie des metastasierten Melanoms mit Real-Life-Daten und -Studien
In der palliativen Therapie des metastasierten Melanoms gibt es gut etablierte Therapieschemata sowohl mit Anti-PD-1-Antikörpern allein oder in Kombination mit Anti-CTLA-4-Antikörpern als auch mit drei Kombinationen einer zielgerichteten Therapie bei BRAF-mutierten Patienten. Explorative Studien gingen der Frage einer geänderten Dosierung von Ipilimumab und Nivolumab nach und auch der Kombination von Anti-PD-1- mit Anti-CTLA-4-Antikörpern nach Versagen einer PD-1-Monotherapie.
Dosierung von Ipilimumab und Nivolumab
Präsentiert wurden Ergebnisse von einer Phase-II-Studie mit mehr als zwei Dosen Ipilimumab und Nivolumab bei Patienten mit unresezierbarem Stadium-III/IV-Melanom.4 Das Studiendesign war so aufgebaut, dass es am Anfang zwei Dosen Ipilimumab (3mg/kg) in Kombination mit Nivolumab (1mg/kg) gab und bereits nach 6 Wochen eine Durchuntersuchung. Zeigte sich keine Tumorlastvergrößerung, wurde bereits nach zwei Zyklen auf Nivolumab-Monotherapie als Maintenance umgestellt. Zeigte sich ein Tumorwachstum von über 4%, wurden zwei zusätzliche Gaben von Ipilimumab und Nivolumab verabreicht. Die nächste Evaluierung der Therapie erfolgte in Woche 12. Die primäre Fragestellung der Studie war die objektive Ansprechrate nach Woche 12. Sekundäre Studienendpunkte umfassten das Ansprechen nach Woche 6 und die beste Gesamtansprechrate. Insgesamt wurden 60 Patienten ausgewertet, der Großteil davon Patienten mit kutanem Melanom, aber auch zu einem Viertel Schleimhautmelanompatienten, einschließlich 16% Patienten mit Hirnmetastasen. 68% der Patienten zeigten eine Tumorverkleinerung in Woche 6 nach zwei Dosen Ipilimumab/Nivolumab. 32% zeigten ein Tumorwachstum.Von diesen Patienten wies anschließend kein Patient ein Ansprechen entsprechend den Recist-Kriterien auf. 18% erhielten eine Dosis Ipilimumab/Nivolumab, 58% zwei Dosen, 12% drei Dosen, 10% vier Dosen und 1 Patient (2%) sechs Dosen. In Woche 12 zeigten sich drei komplette Remissionen (CR), 26 partielle Remissionen (PR) und 11 stabile Erkrankungen (SD). CR und PR betrugen 48%. Bei allen Patienten wurden Nebenwirkungen berichtet, davon 57% von Grad III bis IV, was von der Kombination Ipilimumab und Nivolumab aus früheren Studien bekannt ist. Drei Patienten starben an der Toxizität, ein Patient plötzlich nach Nebennierenrindeninsuffizienz und Armvenenthrombose und zwei Patienten an einer Myokarditis. In Woche 3 und 6 war ein deutlicher Anstieg an KI-67-positiven CD8-Zellen und ICOS-positiven CD8-Zellen nachweisbar.
Kombination von Anti-PD-1- mit Anti-CTLA-4-Antikörpern nach Versagen einer PD-1-Monotherapie
Zwei weitere präsentierte Studien stellten sich der Frage einer Folgetherapie nach Progression unter einer Anti-PD-1-Antikörpertherapie. Bereits beim ASCO 2019 wurde von einer deutschen Gruppe Ansprechen auf Folgetherapien nach Progression unter PD-1 gezeigt, wobei die besten Erfolge mit Ipilimumab und Nivolumab als auch mit zielgerichteter Therapie mit einem BRAF- und MEK-Inhibitor gezeigt werden konnte. In einer präsentierten australischen Studie wurden 355 Stadium-III- und -IV-Melanompatienten eingeschlossen, die unter einer PD-1-Monotherapie adjuvant oder im metastasierten Setting einen Relaps oder eine Progression gezeigt hatten.5 Diese wurden randomisiert zu Ipilimumab oder Ipilimumab und Anti-PD-1-Antikörper. 12% der Patienten hatten einen Relaps nach adjuvanter Therapie und 88% waren metastasierte Patienten, von denen 74% eine primäre Resistenz und 26% eine sekundäre Resistenz zeigten. Im Therapiearm Ipilimumab + Anti-PD-1-Antikörper (IPI + PD-1-AK) zeigte sich eine objektive Ansprechrate von 32%, im Ipilimumab-Monotherapie-Arm (IPI) von 13%. Das progressionsfreie Überleben betrug nach 18 Monaten 22% unter IPI + PD-1-AK im Vergleich zu 18% unter IPI (Abb. 3). Die Gesamtüberlebensrate war 53% im Kombinationsarm und 25% im Monotherapiearm. Die höhergradigen unerwünschten Ereignisse (≥Grad III) waren in etwa gleich verteilt mit Ausnahme der Diarrhö/Kolitis, die häufiger im Ipilimumab-Monotherapiearm auftraten. Bei BRAF-mutierten Melanompatienten war das Ansprechen im Kombinationsarm und im Monotherapiearm ungefähr gleich. Bei BRAF-Wildtyp-Patienten gab es jedoch einen statistisch signifikanten Unterschied mit Ansprechraten von 37% im Kombinationsarm versus 10% im Monotherapiearm. Bei den Patienten unter adjuvanter Therapie betrug das Ansprechen im Kombinationsarm 36% und im Monotherapiearm 13%. Indikatoren für das Gesamtüberleben waren der ECOG-Status, das Vorhandensein von Knochenmetastasen und das erhöhte LDH. Weiters spielte das Geschlecht eine Rolle, die Zeitspanne bis zur Progression mit Anti-PD-1-Antikörpern (über 3 Monate) und die Art der Behandlung.
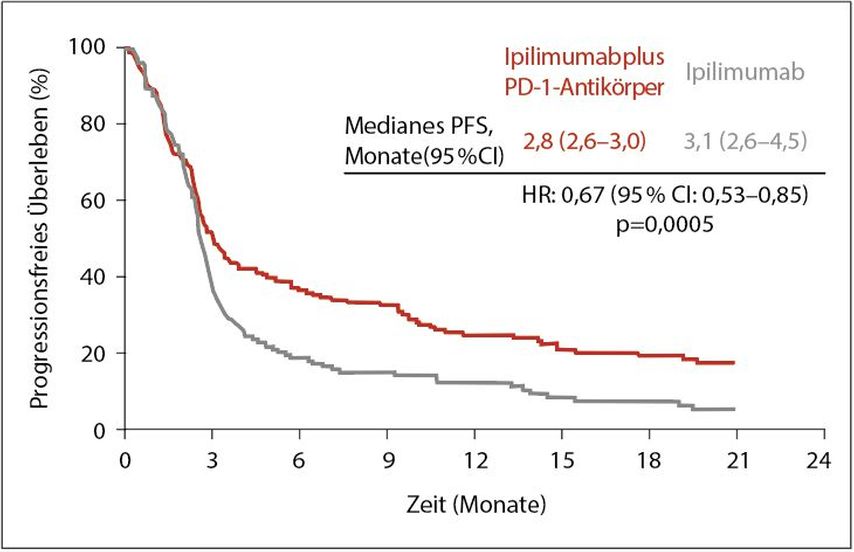
Abb. 3: Progressionsfreies Überleben unter Ipilimumab oder Ipilimumab plus Anti-PD-1-Antikörper (nach Da Silva IP et al.)5
Eine amerikanische Studie widmete sich der Fragestellung zu Pembrolizumab mit niedrig dosiertem Ipilimumab nach PD-1-Therapieversagen im adjuvanten oder palliativen Setting. Hierbei wurde Pembrolizumab 200mg alle 3 Wochen mit Ipilimumab 1mg/kg alle 3 Wochen in insgesamt vier Dosen verabreicht. In dieser Studiengruppe waren 89% kutane Melanome, 10% akrale Melanome und nur 1% Schleimhautmelanome. Die Einschlusskriterien waren eine Progression unter einer palliativen Anti-PD-1-Antikörpertherapie oder innerhalb von 6 Monaten nach einer adjuvanten Anti-PD-1-Antikörpertherapie. 71% der Patienten waren BRAF-Wildtyp und 10% hatten Hirnmetastasen. Von 70 Patienten waren 61 hinsichtlich des Ansprechens auswertbar und hierbei zeigten sich 5 komplette Remissionen, 14 partielle Remissionen und 11 stabile Erkrankungen. Die Ansprechrate betrug 27%. Das mediane PFS war 5 Monate, das mediane OS 24,7 Monate. Grad-3/4-Toxizitäten traten bei 27% der Patienten auf und betrafen hauptsächlich Kolitis, Leberenzymerhöhungen, Hautausschläge und Übelkeit. In einer Subgruppenanalyse zeigte sich bei 30% der Patienten ein Ansprechen bei Leber- oder Hirnmetastasen. Bei Patienten mit Progression nach adjuvanter Therapie zeigte sich in 15% der Fälle ein Ansprechen, bei Patienten mit nicht kutanem Melanom in 14% und bei erhöhter LDH in 42%. Auch hier zeigten BRAF-Wildtyp-Patienten ein besseres Ansprechen mit 31% vs. 26% bei den mutierten. PD-L1-negative Patienten zeigten in 38% der Fälle ein Ansprechenvs. 17% der PD-L1-positiven Patienten. Bei primär refraktären Patienten zeigte sich große Effektivität in nicht T-Zell-inflammierten Gen-Expressionsprofilen.
COLUMBUS
Als Poster wurden die 4-Jahres-Daten zum Gesamtüberleben in der COLUMBUS-Studie präsentiert.6 Im Teil 1 der Studie gab es eine 1:1:1-Randomisierung von Patienten mit metastasiertem Melanom und BRAF-Mutation (V600E oder V600K) in drei Arme. In Arm1 gab es eine Kombination von Encorafenib (450mg 1x täglich) und Binimetinib (45mg 2x täglich), in Arm 2 Vemurafenib in der Standarddosierung (960mg 2x täglich) und in Arm 3 Encorafenib (300mg 1x täglich). Auf dem Poster wurden das Gesamtüberleben und die 4-Jahres-Landmark-Analyse der Kombination vs. Vemurafenib präsentiert. Zur Erinnerung: Die 3-Jahres-Daten ergaben für die Kombination eine OS-Rate von 47%, unter Vemurafenib 31%. Die am ASCO präsentierte 4-Jahres-OS-Rate war unter der Kombination 39% und unter Vemurafenib 26%. Die 4-Jahres-PFS-Rate betrug 26% im Kombinationsarm und 12% im Vemurafenib-Arm. Die Sicherheitsdaten entsprachen dem bekannten Profil der Kombination, es gab keine neuen Sicherheitsbedenken.
Biomarker
Eine deutsche Gruppe hat eine Studie zu Autoantikörpern als Prädiktoren für das Gesamtüberleben und immunvermittelte Nebenwirkungen bei Checkpoint-Inhibitor-Therapien präsentiert.7 In der Studie wurden Blutproben von 333 Stadium-IV-Melanompatienten vor der Therapie mit Checkpoint-Inhibitoren untersucht. Insgesamt wurden 832 Antigene mit einer Luminex-Multiplex-Technologie analysiert. 30% der Patienten erhielten Ipilimumab, 45% Patienten Pembrolizumab, 6% Nivolumab und 19% Ipilimumab plus Nivolumab. Die multivariate Datenanalyse von allen Autoantikörpern zeigte eine Assoziation zwischen dem Auftreten von immunvermittelten Nebenwirkungen und besserem klinischem Outcome. Anti-MIF-Antikörper waren assoziiert mit Krankheitsprogression und einem niedrigeren Risiko für immunvermittelte Nebenwirkungen unter Pembrolizumab. Auch Anti-FGFR-1-Antikörper waren assoziiert mit Progression, kürzerem Überleben und einer niedrigen Rate von immunvermittelten Nebenwirkungen unter Ipilimumab. Hingegen waren Anti-MAGEB4-Antikörper assoziiert mit längerem Überleben und einer höheren Rate von immunvermittelten Nebenwirkungen unter Ipilimumab. Anti-MITF-Autoantikörper waren assoziiert mit Kolitis. Die Konklusion war, dass einige Autoantikörper mit klinischem Outcome und mit immunvermittelten Nebenwirkungen assoziiert sind. Autoantikörperpanels könnten nützlich sein, um sowohl das klinische Outcome als auch das Auftreten von immunvermittelten Nebenwirkungen vorherzusagen. Ziel weiterführender Studien sollte die Entwicklung prädiktiver diagnostischer Assays sein, die dann in weiteren Studien evaluiert werden könnten.
Experimentelle Therapien
Lifileucel
Bei den experimentellen Therapien wurde ein Langzeit-Follow-up von Lifileucel, einer kryopräservierten autologen Therapie mit tumorinfiltrierenden Lymphozyten (TIL), präsentiert.8 Patienten konnten in die Studie eingeschlossen werden, wenn sie unter einer Checkpoint-Inhibitor-Therapie und einer BRAF-/MEK-Inhibitor-Therapie (bei Nachweis einer BRAF-Mutation) progredient waren. Lifileucel wurde zentral hergestellt und kryopräserviert. Insgesamt wurden 66 Patienten präsentiert (aus der Kohorte 2). Der Studienablauf war folgender: Nach einer chirurgischen Resektion wurde das Präparat in 22 Tagen aufbereitet. Der Patient erhielt währenddessen eine nicht myeloablative Lymphodepletion mit Cyclophosphamid gefolgt von Fludarabin. Danach wurde dem Patienten die TIL-Infusion als einmalige Infusion verabreicht. Anschließend an Lifileucel erhielt der Patient einen kurzen Zyklus mit bis zu 6 Dosen von Interleukin-2-Infusionen, um die Antitumoraktivität zu steigern. Grad-3/4-Nebenwirkungen der Therapie zeigten sich bei 97% der Patienten, wobei in erster Linie Thrombozytopenien, Anämien, febrile Neutropenien, Neutropenien, Hypophosphatämien, Leukopenien und Lymphopenien im Vordergrund standen. Die objektive Ansprechrate betrug 36,4%. Komplette Remissionen waren bei 3%, bei 33% partielle Remissionen, bei knapp 44% stabile Erkrankungen zu beobachten. Das Ansprechen war unabhängig vom BRAF-Mutationsstatus; es war unabhängig vom PD-L1-Expressionslevel und auch bei jenen Patientennachweisbar, die Läsionen in der Leber und/oder dem Gehirn hatten.
Toripalimab
Die Ergebnisse einer Studie zum Gesamtüberleben und eine Biomarkeranalyse einer Phase-Ib-Studie mit Toripalimab, einem Anti-PD-1-Antikörper, mit Axitinib bei Patienten mit metastasiertem Schleimhautmelanom wurden am ASCO präsentiert.9 Insgesamt wurden 33 Patienten ausgewertet, alle aus dem asiatischen Raum. Die Ansprechrate betrug 48,5%, die Krankheitskontrollrate 84,8%. Es gab eine komplette Remission und 15 partielle Remissionen. Die Nebenwirkungen aller Grade betrugen 97%, Nebenwirkungen vom Grad3–5beliefen sich auf knapp 40%. Vorherrschend unter diesen Nebenwirkungen waren Proteinurie, Hypertension, Leberwerterhöhung, Gewichtsverlust und Neutropenie. Als Biomarker-Evaluation wurden PD-L1-positive Expression und Tumormutationslast (TMB) mit der Gesamtansprechrate korreliert. PFS und OS waren länger bei Patienten mit PD-L1-positivem Status.
Kutanes Plattenepithelkarzinom (PECA)
Beim ASCO20 Virtual wurden interessante Studien zum Einsatz von Cemiplimab beim kutanen Plattenepithelkarzinom präsentiert. In der EMPOWER-CSCC-1-Studie wurden Patienten in drei Gruppen aufgeteilt: Gruppe 1 waren erwachsene Patienten mit metastasiertem PECA, Gruppe 2 waren lokal fortgeschrittene PECA-Patienten und Gruppe 3 ebenfalls erwachsene Patienten mit metastasiertem PECA.10 Gruppe 1 und 2 erhielten Cemiplimab 3mg/kg alle 2 Wochen i.v. bis zu 96 Wochen mit einer Tumor-CT-Kontrolle alle 8 Wochen. Die Gruppe 3 erhielt Cemiplimab 350mg alle 3 Wochen als Fixdosis bis zu 54 Wochen. Hier erfolgte die Tumorevaluierung alle 9 Wochen. Präsentiert wurden die 3-Jahres-Follow-up-Daten nach einem medianen Follow-up von 15,7 Monaten. Insgesamt wurden 193 Patienten in die Studie eingebracht (59 in Gruppe 1, 78 in Gruppe 2 und 56 in Gruppe 3). Die Gesamtansprechrate bei einem zentralen Review war 46,1%; 50,8% für Gruppe 1, 44,9% für Gruppe 2 und 42,9% für Gruppe 3. Bei Patienten, die keine vorhergehende Systemtherapie erhalten hatten, betrug die Ansprechrate 48,4%, bei Patienten, die eine vorhergegangene Therapie erhalten hatten, 41,5%. Die mediane Dauer des Ansprechens war zum Zeitpunkt des Cut-offs nicht erreicht. Beinahe alle Patienten hatten Nebenwirkungen, wobei die Rate an Grad-3/4-Nebenwirkungen 48,7% betrug. Am häufigsten unter den schweren Nebenwirkungen fanden sich Anämie, Fatigue und Übelkeit. 7,3% der Patienten mussten die Behandlung abbrechen. Therapieassoziierte Nebenwirkungen ≥Grad 3 wurden bei 17% der Patienten beobachtet, am häufigsten Pneumonitis, Autoimmunhepatitis, Anämie, Kolitis und Durchfälle. Im Gesamten war die komplette Ansprechrate 16,1% und die mediane Dauer bis zum kompletten Ansprechen betrug 11,2 Monate.
Aus dieser Studie wurden auch Quality-of-Life-Daten präsentiert.11 Hierbei zeigte sich eine deutliche Reduktion des Schmerzes, noch vor dem Zyklus 3 mit Aufrechterhalten dieses Effektes über den Zyklus 12. Auch der Gesundheitsstatus verbesserte sich deutlich. Mit dem Zyklus 6 hatte die Mehrzahl der Patienten eine deutliche Verbesserung des gesamtheitlichen Gesundheitsstatus.
Ein weiteres Poster zum lokal fortgeschrittenen Plattenepithelkarzinom mit Therapie mit Cemiplimab ergab bei der Untersuchung von 36 Patienten zu 72% eine komplette und partielle Remission und zu 19% eine stabile Erkrankung. Bei knapp 31% der Patienten wurden unerwünschte Ereignisse beobachtet, Nebenwirkungen von Grad 3/4 waren nur beiknapp 9% zu sehen.
Zum lokal fortgeschrittenen oder metastasierten Plattenepithelkarzinom gab es ein weiteres spannendes Poster mit Nivolumab (3mg/kg) mit einer Therapiedauer von einem Jahr oder bis zu inakzeptabler Toxizität.12 24 Patienten wurden ausgewertet. Hierbei zeigte sich kein komplettes Ansprechen, bei 54,5% ein partielles Ansprechen und bei 22,7% eine stabile Erkrankung. Somit ergab sich eine Krankheitskontrollrate von 77%, bei Progression von 22,7%.
Literatur:
1 Eggermont AM et al.: Pembrolizumab versus placebo after complete resection of high-risk stage III melanoma: New recurrence-free survival results from the EORTC 1325-MG/Keynote 054 double-blinded phase III trial at three-year median follow-up. ASCO 2020, Abstr. #10000 2 Hauschild A et al.: Long-term benefit of adjuvant dabrafenib + trametinib (D+T) in patients (pts) with resected stage III BRAF V600–mutant melanoma: Five-year analysis of COMBI-AD. ASCO 2020, Abstr. #10001 3 Blank CU et al.: First safety and efficacy results of PRADO: A phase II study of personalized response-driven surgery and adjuvant therapy after neoadjuvant ipilimumab (IPI) and nivolumab (NIVO) in resectable stage III melanoma. ASCO 2020, Abstr. #10002 4 Postow MA et al.: A phase II study to evaluate the need for > two doses of nivolumab + ipilimumab combination (combo) immunotherapy. ASCO 2020, Abstr. #10003 5 Da Silva IP et al.: Ipilimumab (IPI) alone or in combination with anti-PD-1 (IPI+PD1) in patients (pts) with metastatic melanoma (MM) resistant to PD1 monotherapy. ASCO 2020, Abstr. #10005 6 Gigas H et al.: Update on overall survival in COLUMBUS: A randomized phase III trial of encorafenib (ENCO) plus binimetinib (BINI) versus vemurafenib (VEM) or ENCO in patients with BRAF V600-mutant melanoma. ASCO 2020, Abstr. #10012 7 Hassel JC et al.: Autoantibodies as predictors for survival and immune-related adverse events in checkpoint inhibition therapy of metastasized melanoma. ASCO 2020, Abstr. #10011 8 Sarnaik A et al.: Long-term follow up of lifileucel (LN-144) cryopreserved autologous tumor infiltrating lymphocyte therapy in patients with advanced melanoma progressed on multiple prior therapies. ASCO 2020, Abstr. #10006 9 Sheng X et al.: Overall survival and biomarker analysis of a phase Ib combination study of toripalimab, a humanized IgG4 mAb against programmed death-1 (PD-1) with axitinib in patients with metastatic mucosal melanoma. ASCO 2020, Abstr. #10007 10 Rischin D et al.: Phase II study of cemiplimab in patients (pts) with advanced cutaneous squamous cell carcinoma (CSCC): Longer follow-up. ASCO 2020, Abstr. #10018 11 Migden MR et al.: Health-related quality of life (HRQL) in patients with advanced cutaneous squamous cell carcinoma (CSCC) treated with cemiplimab: Post hoc exploratory analyses of a phase II clinical trial. ASCO 2020, Abstr. # 10033 12 Munhoz RR et al.: CA209-9JC: A phase II study of first-line nivolumab (NIVO) in patients (pts) with locally advanced or metastatic cutaneous squamous cell carcinoma. ASCO 2020, Abstr. #10044
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...


