ctDNA: Monitoring unter Immuntherapie
Autor:innen:
Felicitas Höfermann
OA Dr. Julian Kött
Klinik und Poliklinik für Dermatologie, Universitätsklinikum Hamburg-Eppendorf, Hamburg, Deutschland
Fleur Hiege-Centrum für Hautkrebsforschung, Universitätsklinikum Hamburg-Eppendorf, Hamburg, Deutschland
Korrespondenz:
E-Mail: j.koett@uke.de
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Immuncheckpoint-Inhibitoren haben die Prognose von Patient:innen mit malignem Melanom grundlegend verbessert, doch nicht alle sprechen dauerhaft auf die Therapie an. Die Analyse zirkulierender Tumor-DNA (ctDNA) eröffnet neue Möglichkeiten, das Ansprechen zu überwachen und Rückfälle frühzeitig zu erkennen.
Keypoints
-
ctDNA ist ein vielversprechender Biomarker, um Therapieansprechen, Krankheitsprogression und minimale Resterkrankung (MRD) beim malignen Melanom zu überwachen.
-
Tumoragnostische ctDNA-Analysen zeigen insbesondere bei klarer Mutations-lage, wie z.B. BRAF-mutierten kutanen Melanomen oder beim Uveamelanom, großes Potenzial.
-
„Tumor-informed“, ultrasensitive ctDNA-Messungen sind für das Monitoring des kutanen Melanoms besonders vielversprechend.
-
Der klinische Nutzen von ctDNA muss in randomisiert-kontrollierten Studien und Metaanalysen belegt werden, bevor ein Einsatz als Routine-Biomarker erfolgen kann.
In den letzten Jahren haben zielgerichtete Therapien (TT) und Immuntherapien die Behandlung des malignen Melanoms grundlegend verändert. Nach Jahrzehnten ohne wirksame Therapieoptionen führten die Zulassungen von BRAF- und MEK-Inhibitoren sowie von Immuncheckpoint-Inhibitoren (ICI) gegen PD-1 und CTLA-4 zu einer deutlichen Verlängerung des Gesamtüberlebens. Trotzdem tritt bei ca. 60% der Patient:innen eine primäre Resistenz gegen PD-1-Inhibitoren auf und bei 20–30% der Patient:innen, die anfangs ansprechen, eine sekundäre Resistenz.1 Daher besteht die Notwendigkeit, prädiktive Biomarker zu identifizieren und in der klinischen Routine zu etablieren, die zuverlässig vorhersagen, welche Patient:innen von einer Therapie profitieren.
Liquid Biopsy
Bei ctDNA („circulating tumor DNA“) handelt es sich um einen vielversprechenden Biomarker, der im Rahmen einer sogenannten Liquid Biopsy, eines minimalinvasiven Bluttests, analysiert werden kann. Die Liquid Biopsy stellt eine Alternative zur klassischen Gewebebiopsie dar, bei der neben ctDNA auch andere vielversprechende Biomarker wie z.B. zirkulierende Tumorzellen („circulating tumor cells“, CTC) oder dem Tumor entstammende extrazelluläre Vesikel („extracellular vesicles“, EV) untersucht werden können. Im Gegensatz zur Gewebebiopsie erlaubt die Liquid Biopsy durch wiederholte Blutentnahmen im Laufe der Therapie eine fortlaufende Überwachung des Therapieansprechens.2
ctDNA stellt den aus Tumorzellen freigesetzten Anteil zellfreier DNA (cfDNA) im Blut dar und korreliert in ihrer Menge mit Metabolismus, Größe und Proliferationsrate des Tumors. Als minimalinvasiver Biomarker bietet ctDNA die Möglichkeit, Krebserkrankungen frühzeitig zu detektieren, die Prognose abzuschätzen, das Therapieansprechen zu überwachen und eine minimale Resterkrankung („minimal residual disease“, MRD) nachzuweisen.3
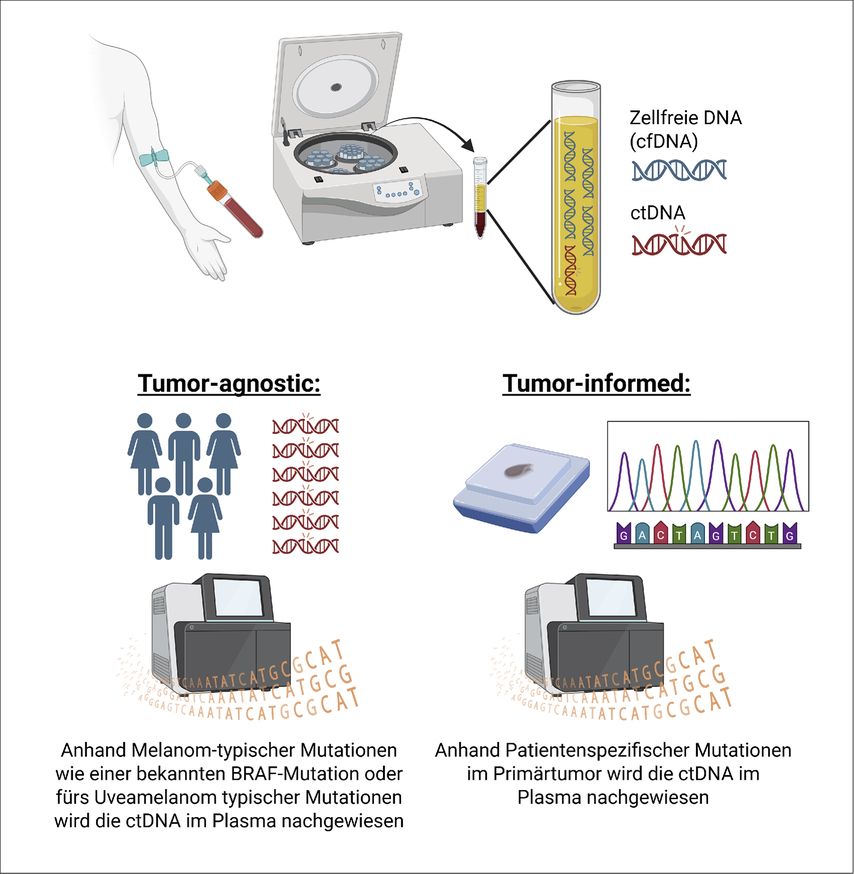
Abb. 1: Prinzipien des „tumor-informed“ und des „tumor-agnostic“ tDNA-Monitorings beim Melanom. cfDNA, zellfreie DNA; ctDNA, zirkulierende Tumor-DNA. Erstellt mit BioRender.com. (modifiziert nach Panet F et al.)4
Die Identifizierung der ctDNA kann entweder „tumor-agnostic“ oder „tumor-informed“ erfolgen. Beim Tumor-agnostischen Ansatz müssen bereits genetische Informationen über den Tumor vorliegen,4 sodass er sich besonders bei kutanen Melanomen mit bekannter BRAF-Mutation, die bei ca. 50% der kutanen Melanome auftritt,1 oder beim Uveamelanom eignet, bei welchem typischerweise Mutationen in den Genen BAP1, GNA11, GNAQ, EIF1AX und SF3B1 auftreten.5 Für eine „tumor-informed“ ctDNA-Analyse müssen zuerst patient:innenspezifische Mutationen im Primärtumor durch Sequenzierung identifiziert werden, um anhand dieser ctDNA im Plasma nachzuweisen.4
Klinische Anwendungsgebiete
ctDNA bietet vielfältige potenzielle Anwendungsmöglichkeiten in der klinischen Praxis. Verschiedene Studien konnten bereits zeigen, dass niedrige oder nicht nachweisbare ctDNA-Werte mit einem längeren progressionsfreien („progression-free survival“, PFS) und Gesamtüberleben („overall survival“, OS) zusammenhängen. Eine Reduktion der ctDNA-Konzentrationen unter Therapie konnte zudem mit einer höheren Gesamtansprechrate („overall response rate“, ORR) und längerem PFS und OS in Verbindung gebracht werden.6
In einer 2024 publizierten prospektiven Studie analysierten Rodrigues et al. bei 69 Patient:innen mit metastasiertem Uveamelanom unter Tebentafusp longitudinal ctDNA: vor Therapiebeginn, nach drei und nach zwölf Wochen sowie bei Krankheitsprogression. Der Nachweis von ctDNA vor Therapiestart war mit einem signifikant kürzeren OS verbunden. Eine Reduktion der ctDNA-Werte um mindestens 90% nach zwölf Wochen korrelierte dagegen mit einem signifikant längeren OS. Diese Ergebnisse zeigen das Potenzial von ctDNA-Analyse in der Überwachung von Therapieansprechen und der Prognoseeinschätzung beim metastasierten Uveamelanom.7
In der prospektiven PET/LIT-Studie mit 104 Melanompatient:innen unter palliativer kombinierter oder adjuvanter Immuntherapie konnten Schroeder et al. zeigen, dass die „tumor-informed“ ctDNA-Analyse eine zuverlässige Überwachung des Therapieansprechens ermöglicht und Rückfälle frühzeitig erkennbar macht. Ein Abfall der ctDNA-Allelfrequenzen zwischen T1 (drei Wochen nach Start der Immuntherapie) und T2 (zwölf Wochen nach Start der Immuntherapie) war in der palliativen Kohorte mit einem signifikant längeren PFS und OS verbunden.8
ctDNA hat das Potenzial, eine Krankheitsprogression früher anzuzeigen, als routinemäßige radiologische Stagings es tun. Aktuell ist es Standard, durch radiologische Stagings anhand von RECIST („Response Evaluation Criteria in Solid Tumors“) den Krankheitsverlauf zu verfolgen und ein Therapieansprechen zu überwachen. So können jedoch nur größere Veränderungen über einen längeren Zeitraum erkannt und frühe Anzeichen von Krankheitsprogression oder Therapieansprechen eventuell übersehen werden. Außerdem ist wiederholte Bildgebung (CT, PET-CT) mit einer Strahlenbelastung verbunden und liefert teils uneindeutige Ergebnisse.
Dynamische Veränderungen der ctDNA stellen einen vielversprechenden Ansatz dar, um Therapieansprechen oder Krankheitsprogression vorherzusagen.9 In einer Kohorte von 96 Patient:innen mit fortgeschrittenem Melanom im Stadium III/IV wurde eine Krankheitsprogression signifikant früher (im Durchschnitt 3,5 Monate) durch erhöhte ctDNA-Werte vorhergesagt als durch konventionelle radiologische Stagings. Auch in dieser Kohorte waren erhöhte ctDNA-Werte zur Baseline-Abnahme prädiktiv für eine Krankheitsprogression, und zwar unabhängig von LDH- (Laktatdehydrogenase) und S100-Werten in multivariaten Analysen.10
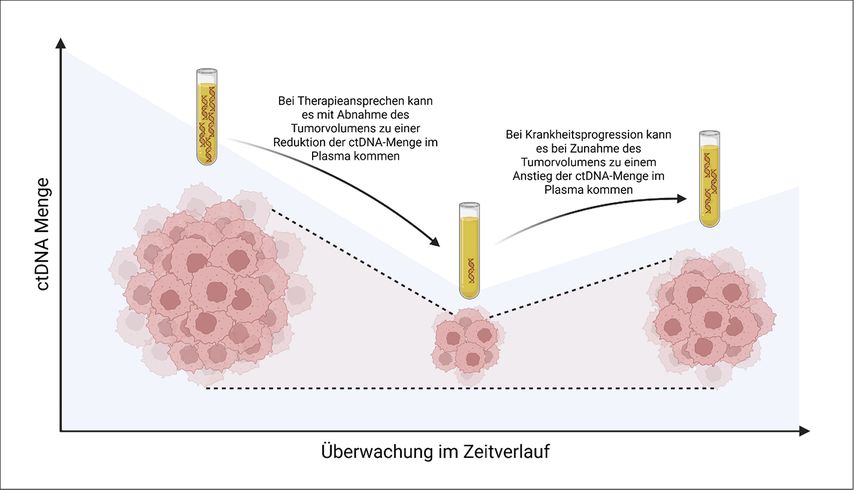
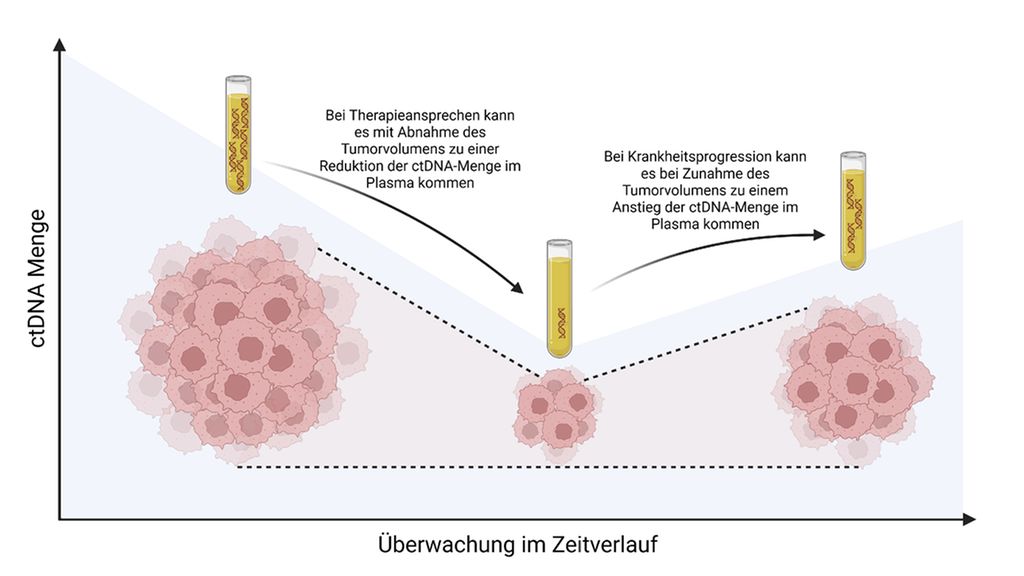
Abb. 2: Nutzen des ctDNA-Monitorings zur Überwachung von Therapieansprechen und Krankheitsprogression. ctDNA, zirkulierende Tumor-DNA. Erstellt mit BioRender.com. (modifiziert nach Gouda MA et al.)9
ctDNA-Messungen könnten auch helfen, zwischen einer Pseudoprogression in der Bildgebung und einer wahren Krankheitsprogression zu unterscheiden. Bei einer Pseudoprogression handelt es sich um eine initiale Größenzunahme von Läsionen in der Bildgebung oder Auftreten von neuen Läsionen zu Beginn einer Immuntherapie, gefolgt von einem Therapieansprechen. Pseudoprogressionen treten bei ca. 10% der Patient:innen auf, die mit PD-1-Antikörpern behandelt werden. In einer Kohortenstudie mit 125 Patient:innen konnten durch den Nachweis einer Reduktion von ctDNA innerhalb von zwölf Wochen nach Therapiestart Patient:innen mit einer Pseudoprogression zuverlässig erkannt werden.11
Die Kombination von ctDNA mit anderen, etablierteren Biomarkern verbessert zudem die Vorhersagekraft in Bezug auf das Überleben bei Melanompatient:innen. In der Studie CheckMate 915 wurde eine adjuvante Monotherapie mit Nivolumab versus Nivolumab in Kombination mit Ipilimumab bei 1844 Patient:innen im resezierten Stadium III/IV untersucht. Der Nachweis von ctDNA vor Therapie und während der Therapie war hier mit einem höheren Rückfallrisiko verbunden. Die Vorhersage des Überlebens verbesserte sich weiter, wenn ctDNA-Messungen gemeinsam mit der Tumormutationslast und dem Interferon-γ-RNA-Signatur-Score bzw. mit Tumor-CD8- oder PD-L1-Expression berücksichtigt wurden.12
Aktuelle Forschungsergebnisse zeigen, dass ctDNA ein vielversprechender Biomarker mit zahlreichen potenziellen klinischen Anwendungsgebieten beim Melanom ist. Für die Anwendung in der Klinik müssten für jede Tumorart und jeden Test genaue Grenzwerte festgelegt werden. Auch der optimale Zeitpunkt der ctDNA-Messung im Vergleich mit der Ausgangsmessung muss festgelegt werden.6 Fraglich ist zudem, ob es in Bezug auf zirkadianen Rhythmus, Mahlzeiten und Bewegung einen optimalen Zeitpunkt im Tagesverlauf für die Probengewinnung gibt.13
Zudem fehlen bislang Interventionsstudien, insbesondere randomisiert-kontrollierte Studien, die den klinischen Nutzen belegen, bevor ctDNA als Grundlage für Therapieeskalation oder -deeskalation und als Standard-Biomarker eingesetzt werden kann.6,13
Literatur:
1 Schadendorf D et al.: Melanoma. Lancet 2018; 392(10151): 971-84 2 Lianidou E, Pantel K: Liquid biopsies. Genes Chromosom Cancer 2019; 58(4): 219-32 3 Keller L et al.: Clinical relevance of blood-based ctDNA analysis: mutation detection and beyond. Br J Cancer 2021; 124(2): 345-58 4 Panet F et al.: Use of ctDNA in early breast cancer: analytical validity and clinical poten-tial. NPJ Breast Cancer 2024; 10(1): 50 5 Decatur CL et al.: Driver mutations in uveal melanoma: associations with gene expression profile and patient outcomes. JAMA Ophthalmol 2016; 134(7): 728-33 6 Stadler JC et al.: Current and future clinical applications of ctDNA in immuno-oncology. Cancer Res 2022; 82(3): 349-58 7 Rodrigues M et al.: Prospective assessment of circulating tumor DNA in patients with metastatic uveal melanoma treated with tebentafusp. Nat Commun 2024; 15(1): 8851 8 Schroeder C et al.: Tumour-informed liquid biopsies to monitor advanced melanoma patients under immune checkpoint inhibition. Nat Commun 2024; 15(1): 8750 9 Gouda MA et al.: Liquid biopsy response evaluation criteria in solid tumors (LB-RECIST). Ann Oncol 2024; 35(3): 267-75 10 Váraljai R et al.: Application of circulating cell-free tumor DNA profiles for therapeutic monitoring and outcome prediction in genet-ically heterogeneous metastatic melanoma. JCO Precis Oncol 2019; 3: 1-10 11 Lee JH et al.: Association between circulating tumor DNA and pseudoprogression in patients with metastatic melanoma treated with anti-programmed cell death 1 antibodies. JAMA Oncol 2018; 4(5): 717 12 Long GV et al.: Pretreatment and on-treatment ctDNA and tissue biomarkers predict recurrence in patients with stage IIIB–D/IV melanoma treated with adjuvant immunotherapy: CheckMate 915. J Immunother Cancer 2025; 13(7): e012034 13 Wyatt AW et al.: Plasma ctDNA as a treatment response biomarker in metastatic cancers: evaluation by the RECIST Working Group. Clin Cancer Res 2024; 30(22): 5034-41
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...