AGO-Jahrestagung 2021
Bericht:
Mag. Dr. Anita Schreiberhuber
Auch wenn die diesjährigeJahrestagung der Arbeitsgemeinschaft für Gynäkologische Onkologie (AGO) virtuell abgehalten wurde, war sie nicht weniger spannend als sonst. Besonders interessant war die „Wrap-up-Sitzung“, in der es um Innovationen im Bereich der Therapie gynäkologischer Tumoren ging, die als „practice-changing“ erachtet werden.
Neue Guidelines für das Endometriumkarzinom
Für das Endometriumkarzinom wurden erst kürzlich neue Guidelines der European Society of Gynaecological Oncology (ESGO), der European Society for Radiotherapy and Oncology (ESTRO) und der European Society of Pathology (ESP) publiziert. Dabei fanden bei der Risikostratifizierung nicht nur die histopathologischen Parameter, sondern auch das molekularpathologische Profil der Tumoren Berücksichtigung.1 Basierend auf den Ergebnissen des „Cancer Genome Atlas“-Projekts, bei dem fast 400 Endometriumkarzinome komplett sequenziert worden waren,2 wurden unter Miteinbezug des Mutationsprofils und der Kopienzahlvariationen vier neue Subgruppen definiert. Der Molekularklasse 1 liegen pathogene Varianten in der Exonukleasedomäne der Polymerase Epsilon (POLE) zugrunde, woraus ein fehlerhaftes Korrekturlesen bei DNA-Replikationen und in weiterer Folge eine hohe Mutationslast resultieren.1,3 Paradox ist, dass das mikroskopische Bild aufgrund der vielen Mutationen und der meist gering differenzierten Zellen einen aggressiven Tumor vermuten lässt, der mit einer schlechten Prognose einhergeht. Das Gegenteil ist jedoch der Fall: Die betroffenen Patientinnen weisen eine exzellente Prognose auf. Es wird vermutet, dass die hohe Mutationslast im Tumor und die dadurch entstehenden Tumorneopeptide eine starke zytolytische Immunantwort auslösen. Darüber hinaus wird möglicherweise auch die Funktion der Tumorzellen beeinträchtigt und das Metastasierungspotenzial verringert.4
Endometriumkarzinome der Molekularklasse 2 zeichnen sich durch eine Mismatch-Repair-Defizienz (MMRd)/Mikrosatelliteninstabilität (MSI) aus. Endometriumkarzinome der Klasse 3 sind durch eine niedrige Kopienzahl und ein sehr heterogenes Mutationsmuster charakterisiert. Endometriumkarzinome der Klasse 4 weisen eine hohe Kopienzahl und eine hohe Rate an TP53-Anomalien (TP53abn) auf.1,2
Immuntherapie beim Endometriumkarzinom
„Wir wissen seit einiger Zeit, dass Tumoren, die eine hohe Mikrosatelliteninstabilität (MSI-H) oder eine MMRd aufweisen, unabhängig von ihrer Entität gut auf eine Immuntherapie ansprechen“, so die einleitenden Worte von Assoc. Prof. Priv.-Doz. Dr. Seebacher-Shariat, Medizinische Universität Wien. Dies war auch in der GARNET-Studie der Fall: In dieser offenen, einarmigen Studie wurde der humanisierte monoklonale PD-1-Antikörper Dostarlimab bei diversen soliden Tumoren, darunter bei 245 Patientinnen mit Endometriumkarzinom, als Monotherapie untersucht. Am Jahreskongress der European Society of Medical Oncology (ESMO) 2020 wurden die Ergebnisse von 126 Patientinnen mit MMRd und 145 mit MMR-Profizienz (MMRp) präsentiert. Die MMRd-Gruppe zeigte mit 45,5% eine klar überlegene Rate des objektiven Ansprechens (ORR) im Vergleich zur MMRp-Gruppe mit 13,9%.Auch die Krankheitskontrollrate (DCR) war bei MMRd vs. MMRp mit 63,6% vs. 42,4% höher. Diese Ergebnisse sind die bislang umfassendsten aus einer prospektiven Studie zur Immuntherapie beim Endometriumkarzinom.5 Gegenwärtig sind mehrere Studien zur Immuntherapie beim Endometriumkarzinom im Gange, darunter die Phase-III-Studien RUBY (NCT03981796) mit Dostarlimab und ENGOT-EN7/AtTEnd (NCT03603184) mit Atezolizumab.
Zervixkarzinom: PD-L1-Expression ist entscheidend
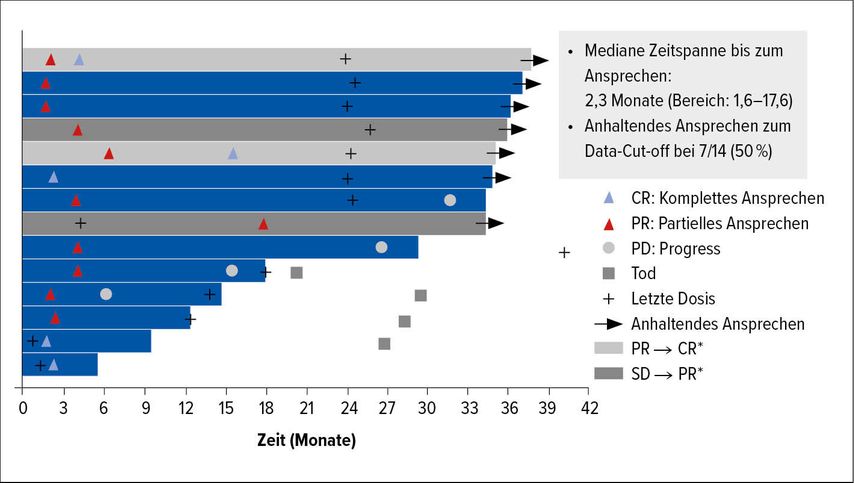
In der offenen Phase-II-Studie KEYNOTE-158 wurde Pembrolizumab an 233 Patienten mit unterschiedlichen Tumorentitäten und dem Nachweis einer MMRd/MSI-H untersucht. Die Patienten waren stark vortherapiert – 65% hatten ≥zwei vorangegangene Therapien erhalten. Am Kongress der Society of Gynecologic Oncology (SGO) 2021 wurden aktualisierte Ergebnisse zum Kollektiv der Zervixkarzinompatientinnen präsentiert: Bei PD-L1-negativen Patientinnen (n=15) lag die Rate des objektiven Ansprechens bei 0%, in der PD-L1-positiven Subgruppe (CPS [„combined positive score“] ≥1; n=82) bei 17%. Interessant ist jedoch, dass von den Respondern nach drei Jahren noch die Hälfte ein Ansprechen zeigte (Abb.1).6 „Die Dauer des Ansprechens (DOR) bei den Respondern ist eindrucksvoll – für einige Patienten ist diese Therapie tatsächlich ein Game-Changer“, merkte Seebacher-Shariat an. Auch bei dieser Tumorentität wird – wie bei vielen anderen – versucht, das Ansprechen durch den Einsatz von Kombinationen zu verbessern. Am ESMO-Kongress 2020 wurden präliminäre Ergebnisse von zwei Phase-II-Studien zur Gabe des PD-1-Inhibitors Balstilimab ± des CTLA-4-Inhibitors Zalifrelimab präsentiert. Dabei wurde bei Monotherapie in der ITT(„Intention to treat“)-Population eine Rate an objektivem Ansprechen von 14% und mit der Kombination eine ORR von 22% erzielt. Die DOR lag unter Balstilimab bei 15,4 Monaten und war unter der Kombination noch nicht erreicht. Zudem ging diese Immuntherapie mit einem akzeptablen Nebenwirkungsprofil einher.7
Zytoreduktive Operation beim rezidivierten Ovarialkarzinom
„Wenn wir uns ansehen, was in den Jahren seit der Einführung von Cisplatin bezüglich des progressionsfreien Überlebens (PFS) passiert ist, erkennt man, dass der Benefit gering ist. D.h., der „Standard of Care“ – Platin + Taxan ± Bevacizumab (BEV) – ist letztlich insuffizient. Wir haben aber in Erfahrung gebracht, dass wir bei der operativen Therapie des Ovarialkarzinoms sehr wohl eine Verbesserung erzielen können“, berichtete Univ.-Prof. Dr. Christian Marth, Medizinische Universität Innsbruck. Die AGO führte dazu eine Reihe von Studien – die DESKTOP-Studien – durch, wobei schon in DESKTOP-OVAR I gezeigt werden konnte, dass eine komplette Resektion zu einer Überlebensverlängerung führt. Je größer der Residualrand im Resektat, umso kürzer ist das Gesamtüberleben (OS).8
In der Studie DESKTOP II wurde ein Score zur Prädiktion einer kompletten Zytoreduktion validiert. Die folgenden Parameter müssen erfüllt sein, damit eine OP bei einem Ovarialkarzinomrezidiv sinnvoll ist: ECOG(Eastern Cooperative Oncology Group)-Performance-Status 0, kein Resttumor bei der Erst-OP, kein Aszites >500ml.9 Dieser Score kam in der Studie DESKTOP III zum Einsatz, in der rezidivierte Patientinnen mit Ovarialkarzinom, die die Kriterien erfüllten, zur zytoreduktiven OP vs. keine OP randomisiert wurden. Das PFS war mit 19,6 Monaten in der Gruppe mit OP um 5,6 Monate länger (14,0 Monate ohne OP; HR: 0,66; p<0,001) und war in der Gruppe mit einer kompletten Resektion mit 21,2 Monaten besonders lang (HR: 0,56; p<0,0001). Nach fünf Jahren gab es immer noch eine Gruppe, die progressionsfrei geblieben war.10
Am Jahreskongress der American Society of Clinical Oncology (ASCO) 2020 wurden die finalen Studienergebnisse präsentiert: Die zytokreduktive OP führte im Vergleich zum Verzicht auf eine OP zu einem signifikanten OS-Benefit im Ausmaß von 7,7 Monaten (53,7 vs. 46,0 Monate; HR: 0,75; p=0,02), das mediane OS belief sich bei Patientinnen mit kompletter Resektion sogar auf 61,9 Monate. Die Autoren wiesen auf die Relevanz einer optimalen Patientenselektion und der Auswahl von Zentren mit hoher Expertise hin.11 Von den drei Studien, die dieser Fragestellung nachgingen, bezeichnete Marth DESKTOP III als „die am saubersten durchgeführte“.
PARP-Inhibitoren sind ein echter Game-Changer
Während sich auf dem Gebiet der Chemotherapie beim Ovarialkarzinom nicht wirklich viel getan hat, hat die Einführung der PARP-Inhibitoren (PARP-I) als Erhaltungstherapie die Behandlungsstrategien beim Ovarialkarzinom revolutioniert, was Marth als die „spannendste Entwicklung innerhalb der letzten Jahre“ bezeichnete.
Für die Erstlinie wurden vier Studien durchgeführt: SOLO-112 bei Patientinnen mit einer BRCAm in der Keimbahn oder im Tumor (gBRCAm bzw. sBRCAm), PAOLA-113 zu Olaparib + BEV bei Patientinnen unabhängig vom Mutationsstatus, PRIMA14 zu Niraparib unabhängig vom Mutationsstatus bei Patientinnen, die einen Residualtumor nach der OP hatten, und VELIA zu Veliparib15 unabhängig vom Mutationsstatus.
Olaparib ist der bislang am längsten verfügbare PARP-I. Bereits nach einem medianen Follow-up von 41 Monaten wurde in SOLO-1 die signifikante Überlegenheit vs. Placebo in Bezug auf den primären Endpunkt, das PFS, bestätigt: Das mediane PFS war unter Olaparib noch nicht erreicht und betrug unter Placebo 13,8 Monate (p<0,001). Olaparib führte zur Reduktion des Risikos für eine Progression oder Tod um 70% (HR: 0,30).12 Die 5-Jahres-Daten bestätigen den anhaltenden Benefit unter diesem PARP-I über das Therapieende von zwei Jahren hinaus: Das mediane PFS vs. Placebo betrug 56,0 vs. 13,8 Monate, was einem Benefit von 42,2 Monaten gleichkommt (HR: 0,33). Zu diesem Zeitpunkt waren im Olaparib-Arm vs. Placebo immer noch fast die Hälfte der Patientinnen progressionsfrei (48 vs. 21%).16
In PAOLA-1 konnte gezeigt werden, dass auch Patientinnen mit einem positiven HRD(„homologous repair deficiency“)-Status von Olaparib + BEV vs. Placebo + BEV profitieren: In der HRD-positiven Gruppe mit BRCA-Wildtyp lag das 2-Jahres-PFS bei 52% vs. 26% im Kontrollarm, wobei der Benefit in der HRD+-Gruppe mit einer BRCAm mit 66 vs. 29% noch ausgeprägter war. In der Gruppe der HRD-negativen Patientinnen konnte mit der Olaparib-haltigen Therapie kein PFS-Vorteil gezeigt werden.13 Dem gegenüber konnte in PRIMA unter Niraparib vs. Placebo auch in diesem Kollektiv ein PFS-Vorteil nachgewiesen werden.14
Für die Rezidivtherapie sind in Europa Olaparib, Niraparib und Rucaparib zugelassen.17
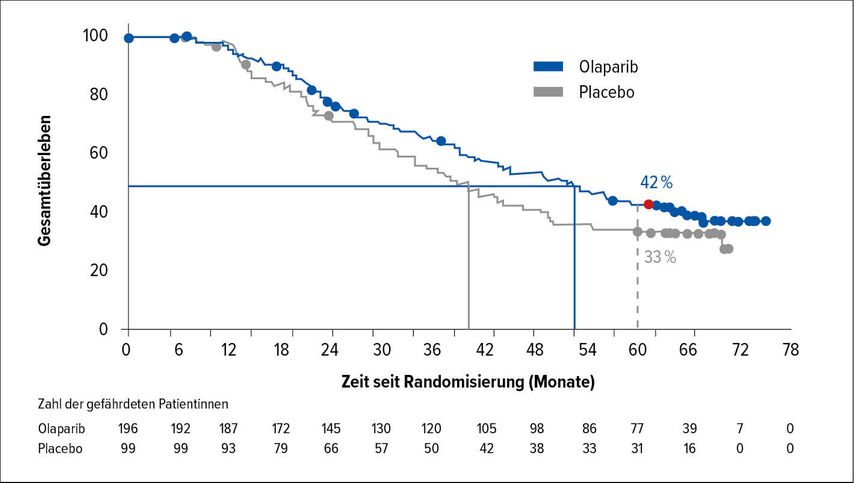
Dabei ist Olaparib insofern erwähnenswert, als für diesen PARP-I als ersten in dieser Substanzklasse OS-Ergebnisse vorliegen, in denen ein signifikanter Vorteil gegenüber Placebo nachgewiesen werden konnte: Die 5-Jahres-Ergebnisse der Phase-II-Studie SOLO-2 zeigen, dass unter Olaparib vs. Placebo nach fünf Jahren ein OS-Benefit von 13 Monaten generiert wurde (51,7 vs. 38,8 Monate). Nach Kaplan-Meier-Schätzung waren 42% der Patienten in der Olaparib-Gruppe und 33% der Patienten in der Placebo-Gruppe nach 60 Monaten noch am Leben. Aus der finalen Analyse geht hervor, dass das mediane OS bei Patientinnen mit einer BRCA1/2m unter Olaparib mit 51,7 Monaten um 13 Monate länger ist als unter Placebo mit 38,8 Monaten (HR: 0,74; p=0,054; nicht adjustiert um die 38% der Patientinnen im Placebo-Arm, die eine weitere PARP-I-Therapie erhielten), was eine bislang nicht gezeigte klinisch bedeutungsvolle Verbesserung ist (Abb.2).18
Abb. 2: 5-Jahres-Überleben bei Patientinnen mit BRCA1/2m in der Studie SOLO-2 (nach Poveda et al.)18
Aktuell in Österreich laufende Studien zum Mammakarzinom
Priv.-Doz. Dr. Gunda Pristauz-Telsnigg, Medizinischen Universität Graz, präsentierte einige laufende Studien zum Mammakarzinom, die an österreichischen Zentren angeboten werden. Eingangs widmete sie sich der Frage, die sich viele Patientinnen stellen: „Ist denn eine Studienteilnahme sinnvoll?“ Dies kann ganz klar mit Ja beantwortet werden: Die Teilnahme an einer klinischen Studie schont nicht nur finanzielle Ressourcen, sondern führt bei Brustkrebspatientinnen auch zu einem Überlebensvorteil – wie aus einer im Jahr 2013 publizierten Arbeit hervorgeht.19
Eine der beiden chirurgischen Studien, die Pristauz-Telsnigg vorgestellt hat, ist EUBREAST (European Breast Cancer Research Association of Surgical Trialists) 1 (NCT04101851). Sie wird von einer der erst kürzlich gegründeten europäischen Studiengruppe durchgeführt, die sich aus Brustchirurgen zusammensetzt. In dieser einarmigen Studie wird der Verzicht auf eine SNLB (Sentinellymphknotenbiopsie) bei HER2+- und tripelnegativen Mammakarzinompatientinnen untersucht, die vor einer neoadjuvanten Chemotherapie (NACT) ein cN0-Stadium und nach der NACT eine pathologisch komplette Remission (pCR) aufweisen. Primärer Endpunkt ist das Überleben frei von einem axillären Rezidiv innerhalb von drei Jahren nach der OP.
Background für die Hypothese, dass in diesen Fällen auf eine SLNB verzichtet werden kann, ist eine retrospektive Untersuchung, in der nachgewiesen werden konnte, dass bei klinisch freier Axilla vor einer NACT der Nachweis einer pCR nach einer NACT zu 100% mit dem Nodalstatus korreliert.20 Diese Studie wird an der Medizinischen Universität Graz und am LKH Leoben durchgeführt.
In der randomisierten, doppelblinden Phase-III-Studie BRCA-P (ABCSG-50; NCT04711109) wird der präventive Effekt von Denosumab (120mg/alle 6 Monate) vs. Placebo bei gesunden Frauen im Alter zwischen 25 und 55 Jahren mit gBRCAm für fünf Jahre im Hinblick auf die Entwicklung eines Mammakarzinoms untersucht. Rationale für diese Studie ist der Nachweis, dass der RANK-Ligand ein potenzielles Target in der Brustkrebsprävention bei gBRCA1m-Trägerinnen darstellt21 und der monoklonale Antikörper Denosumab mit hoher Affinität und Spezifität an den RANK-Liganden bindet.22 Der RANK-Pathway spielt eine wesentliche Rolle in der Tumorgenese des Mammakarzinoms und eine Blockade könnte demnach eine vielversprechende Strategie in der Prävention von Brustkrebs darstellen.21Das Gesamtmanagement und die globale Studienkoordination werden von der ABCSG (Austrian Breast and Colorectal Cancer Group) mit Univ.-Prof. Dr. Christian Singer, Medizinische Universität Wien, als Coordinating Investigator durchgeführt. Neben der Medizinischen Universität Wien zählen die Medizinische Universität Graz, das Ordensklinikum Linz Barmherzige Schwestern, das LKH/Universitätsklinikum Salzburg und das Hanusch-Krankenhaus, Wien, zu den weiteren Zentren, an denen diese Studie durchgeführt wird.
Quelle:
29. Wissenschaftliche Tagung der Arbeitsgemeinschaft für Gynäkologische Onkologie, 15.–17. April 2021, virtuell
Literatur:
1 Concin N et al.: ESGO/ESTRO/ESP guidelines for the management of patients with endometrial carcinoma. Int J Gyn Cancer 2021; 31(1): 12-39 2 Kandoth C et al.: Mutational landscape and significance across 12 major cancer type.s Nature 2013; 502(7471): 333-9 3 Church DN et al.: Prognostic significance of POLE proofreading mutations in endometrial cancer. J Natl Canc Inst 2014; 107(1): 402 4 van Gool IC et al.: POLE proofreading mutation, immune response and prognosis in endometrial cancer. Oncoimmunology 2015; 5(3): e1072675 5 Oaknin A et al.: Safety and antitumor activity of dostarlimab in patients (pts) with advanced or recurrent DNA mismatch repair deficient (dMMR) or proficient (MMRp) endometrial cancer (EC): Results from GARNET. ESMO-Kongress 2020; Abstract #LBA36 6 Chung HC et al.: Pembrolizumab treatment of advanced cervical cancer: Updated results from the phase II KEYNOTE-158 study. SGO-Kongress 2021; Abstract #10440 7 O’Malley DM et al.: Single-agent anti-PD-1 balstilimab or in combination with anti-CTLA-4 zalifrelimab for recurrent/metastatic (R/M) cervical cancer (CC): Preliminary results of two independent phase II trials. ESMO-Kongress 2020; Abstract #LBA34 8 Harter P et al.: Surgery in recurrent ovarian cancer: the Arbeitsgemeinschaft Gynaekologische Onkologie (AGO) DESKTOP OVAR trial. Ann Surg Oncol 2006; 13(12): 1702-10 9 Harter P et al.: Prospective validation study of a predictive score for operability of recurrent ovarian cancer: the Multicenter Intergroup Study DESKTOP II. A project of the AGO Kommission OVAR, AGO Study Group, NOGGO, AGO-Austria, and MITO. Int J Gynecol Cancer 2011; 21(2): 289-95 10 Du Bois A et al.: Randomized controlled phase III study evaluating the impact of secondary cytoreductive surgery in recurrent ovarian cancer: AGO DESKTOP III/ENGOT ov20. ASCO-Kongress 2017; Abstract #5001 11 Du Bois A et al.: Randomized phase III study to evaluate the impact of secondary cytoreductive surgery in recurrent ovarian cancer: Final analysis of AGO DESKTOP III/ENGOT-ov20. ASCO-Kongess 2020; Abstract #6000 12 Moore K et al.: Maintenance olaparib in patients with newly diagnosed advanced ovarian cancer. N Engl J Med 2018; 379(26): 2495-505 13 Ray-Coquard I et al.: Olaparib plus bevacizumab as first-line maintenance in ovarian cancer. N Engl J Med 2019; 381(25): 2416-28 14 González-Martín A et al.: Niraparib in patients with newly diagnosed advanced ovarian cancer. N Engl J Med 2019; 381(25): 2391-402 15 Coleman RL et al.: Veliparib with first-line chemotherapy and as maintenance therapy in ovarian cancer. NEngl J Med 2019; 381(25): 2403-15 16 Bradley W et al.: Maintenance olaparib for patients with newly diagnosed, advanced ovarian cancer and a BRCA mutation: 5-year follow-up from SOLO1. SGO-Kongress 2021: Abstract #ID10520 17 https://www.ema.europa.eu/en 18 Poveda A et al.: Olaparib tablets as maintenance therapy in patients with platinum-sensitive relapsed ovarian cancer and a BRCA1/2 mutation (SOLO2/ENGOT-Ov21): a final analysis of a double-blind, randomised, placebo-controlled, phase 3 trial. Lancet Oncol 2021; 22(5): 620-31 19 Chow CJ: Does enrollment in cancer trials improve survival? Am Coll Surg 2013; 216(4): 774-80 20 Tadros AB et al.: Identification of patients with documented pathologic complete response in the breast after neoadjuvant chemotherapy for omission of axillary surgery. JAMA Surg 2017; 152(7): 665-70 21 Nolan E et al.: RANK ligand as a potential target for breast cancer prevention in BRCA1-mutation carriers. Nat Med 2016: 22(8): 933-9 22 Fachinformation Denosumab (Prolia®), Stand: Dezember 2020
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...