p53-abnormales Endometriumkarzinom
Autorin:
Dr. Magdalena Postl
Universitätsklinik für Frauenheilkunde
Abteilung für Allgemeine Gynäkologie und Gynäkologische Onkologie
Medizinische Universität Wien/AKH Wien
E-Mail: magdalena.postl@meduniwien.ac.at
Der folgende Fallbericht beschreibt den Behandlungsverlauf eines p53-abnormalen Endometriumkarzinoms mit einer auf der DUO-E-Studie1 basierenden Kombinationstherapie.
Onkologische Anamnese
Eine 54-jährige Patientin stellte sich im April 2024 mit postmenopausaler Blutung und Unterbauchschmerzen vor. Klinisch bestand der Verdacht auf ein fortgeschrittenes Endometriumkarzinom mit Zervixinfiltration. Die Biopsie eines aus dem Zervixkalkanal ragenden Tumors ergab ein endometroides, Hormonrezeptor-positives Adenokarzinom des Endometriums, G2.
Immunhistochemisch zeigten sich ein aberrantes p53-Färbemuster und ein regelrechtes Färbemuster der MMR-Proteine. In der molekularpathologischen Analyse bestätigte sich eine TP53-Mutation; eine POLE-Mutation wurde nicht nachgewiesen.
Bildgebend zeigte sich eine ausgedehnte lokoregionäre Tumorausbreitung mit Lymphknotenmetastasen entlang der Arteria iliaca communis, es fanden sich jedoch keine Fernmetastasen. Somit ergab sich als zusammenfassende Diagnose ein p53-abnormales Endometriumkarzinom FIGO IIIC2.
Therapieempfehlung des Tumorboards und Therapieverlauf
Das Tumorboard empfahl eine neoadjuvante Chemotherapie mit Carboplatin/Paclitaxel. Nach drei Zyklen zeigte sich radiologisch ein partielles Ansprechen, begleitet von einem deutlichen Rückgang der initial erhöhten Tumormarker (CA-125, CA 19-9, CEA). Im Anschluss erfolgte ein Intervalldebulking mit Hysterektomie, bilateraler Adnexektomie, Resektion des Beckenperitoneums sowie pelviner und paraaortaler Lymphadenektomie.
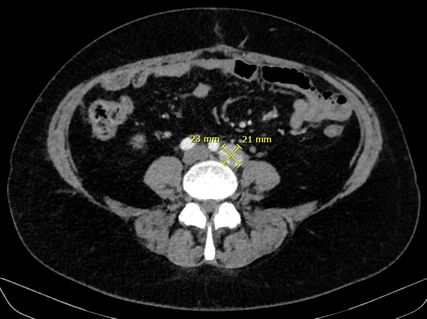
Abb. 1:Persistente parailiakale Lymphknotenmetastase nach sechs Zyklen Chemotherapie und zwei Zyklen Immuntherapie
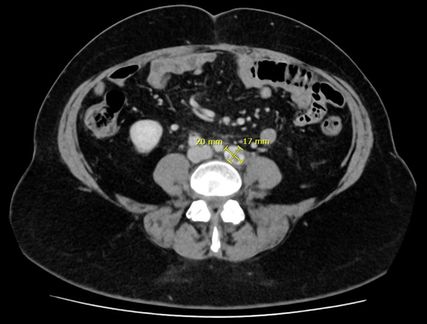
Abb. 2:„Stable disease“ der parailiakalen Lymphknotenmetastase nach sieben Zyklen Immuntherapie
Der postoperative Tumorrest betrug drei Zentimeter im Bereich der parailiakalen und paraaortalen Lymphknoten. Eine vollständige Resektion war aufgrund der Infiltration und Fixierung des paraaortalen Lymphknotens an die Wirbelsäule sowie der Notwendigkeit eines Gefäßersatzes nicht möglich. Postoperativ erhielt die Patientin eine adjuvante kombinierte Tele- und Brachytherapie.
Basierend auf den Ergebnissen der Phase-III-Studie DUO-E wurde eine Erweiterung der systemischen Therapie empfohlen. In DUO-E hatte die Zugabe des PARP-Inhibitors Olaparib zu dem PD-L1-Inhibitor Durvalumab im Sinn einer onkologischen Vierfachtherapie bei non-dMMR-Karzinomen zu einer signifikanten Verlängerung des progressionsfreien Überlebens geführt.1 Die Kombinationstherapie wurde von der Patientin ohne Hinweis auf „immune-related adverse events“ (irAEs) gut vertragen. Serologisch zeigte sich eine Remission mit normwertigen Tumormarkern und radiologisch eine stabile Erkrankung mit größenkonstanten Lymphknotenmetastasen. Die Abbildungen zeigen den Zustand nach sechs Zyklen Chemo- und zwei Zyklen Immuntherapie (Abb.1) sowie nach sieben Zyklen Immuntherapie (Abb.2). Die Patientin befindet sich aktuell weiterhin unter laufender dualer Erhaltungstherapie mit Durvalumab – zuletzt Zyklus 10 – und Olaparib.
Conclusio
Fortgeschrittene oder rezidivierte non-dMMR-Endometriumkarzinome sind eine systemtherapeutische Herausforderung. Mit der Vierfachkombination bestehend aus Carboplatin/Paclitaxel/Durvalumab, gefolgt von einer Erhaltungstherapie mit Durvalumab und Olaparib, steht eine neue, vielversprechende Therapieoption zur Verfügung. Der vorliegende Fall illustriert das klinische Potenzial und die gute Verträglichkeit dieser Kombinationstherapie bei einem primär fortgeschrittenen p53-abnormalen Endometriumkarzinom. Er unterstreicht zudem die Bedeutung einer leitliniengerechten molekularpathologischen Subtypisierung betroffener Patientinnen bereits in der therapeutischen Erstlinie.
Literatur:
1 Westin SN et al.: J Clin Oncol 2024; 42(3): 283-99
Das könnte Sie auch interessieren:
Highlights zu Lymphomen
Assoc.Prof. Dr. Thomas Melchardt, PhD zu diesjährigen Highlights des ASCO und EHA im Bereich der Lymphome, darunter die Ergebnisse der Studien SHINE und ECHELON-1
ASH 2020 – Highlights zu den aggressiven Lymphomen
Highlight-Themen der virtuellen ASH-Jahrestagung im Dezember 2020 waren an erster Stelle die Immunonkologika in all ihren Variationen, aber auch Beispiele für innovative Sequenztherapien ...
Aktualisierte Ergebnisse für Blinatumomab bei neu diagnostizierten Patienten
Die Ergebnisse der D-ALBA-Studie bestätigen die Chemotherapie-freie Induktions- und Konsolidierungsstrategie bei erwachsenen Patienten mit Ph+ ALL. Mit einer 3-jährigen ...