Streptococcus pyogenes: schwere Komplikationen durch Bakterientoxine
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Streptococcus pyogenes kann zu Infektionen mit sehr unterschiedlicher klinischer Ausprägung und Prognose führen. Das Spektrum reicht von der relativ harmlosen Pharyngitis bis zu akut lebensbedrohlichen Zustandsbildern wie der nekrotisierenden Fasziitis oder dem Streptokokken-assoziierten Toxic-Shock-Syndrom. Erfreulicherweise spricht S. pyogenes auf Penicilline problemlos an.
Streptokokken sind in Ketten angeordnete grampositive, katalasenegative Bakterien, die fakultativ anaerob wachsen. Zeigensie Hämolyseverhalten(β-Hämolyse) und sprechen sie auf Bacitracinan, so handelt es sich um sogenannte Gruppe-A-Streptokokken (GAS). Klinisch relevant ist aus dieser Gruppe in erster Linie Streptococcus pyogenes, ein fast ausschließlich humanpathogenes Bakterium mit weltweitem Vorkommen. Ungeachtet eines deutlichen Rückgangs handelt es sich bei S. pyogenesum ein weiterhin sehr relevantes Pathogen, so Dr. Luzia Veletzky von der Universitätsklinik für Innere Medizin I in Wien. Die Übertragung erfolgt durch Tröpfchen- bzw. Schmierinfektionen von Mensch zu Mensch. Die Inkubationszeit ist mit zwischen einem und drei Tagen relativ kurz. Die assoziierte Klinik ist sehr variabel. Meist kommt es zur asymptomatischen Besiedelung, es sind jedoch auch schwerste Krankheitsverläufe mit obligater Intensivbetreuung bzw. Todesfolge möglich. Die Pathogenese ist komplex, der Krankheitsverlauf abhängig von Wirts- und Erregerfaktoren.
Wie sich das Bakterium dem Immunsystem entziehen kann
Typisch für S. pyogenes sind zahlreiche Virulenzfaktoren, die den Gewebetropismus, die Invasivität sowie die Resistenz gegenüber Abwehrmechanismen bestimmen und daher wichtig für den Krankheitsverlauf sind. Dabei kann es sich um Oberflächenproteine, sekretorische Virulenzfaktoren oder Toxine handeln. Von großer Bedeutung ist das vom emm-Gen codierte M-Protein, das auch für die Klassifikation herangezogen wird. Mehr als 200 Genotypen sind bekannt. Das M-Protein wirkt immunmodulatorisch, führt zum Zelltod von Immunzellen und bietet dem Bakterium daher Schutz vor der Immunantwort des Wirts. Das S-Protein ist ein weiteres Oberflächenprotein, das dem Bakterium molekulare Mimikry und die Bindung an Erythrozyten ermöglicht. Auch das S-Protein verhindert die Abtötung des Erregers. Proteasen hemmen die Aktivierung von Neutrophilen und sind dafür verantwortlich, dass S. pyogenes sehr invasiv sein kann. Die Streptokinase ist für die Bakteriendissemination wichtig. Hinzu kommt eine Vielzahl von Toxinen, die wesentlich dazu beitragen, wie sich eine Infektion mit S. pyogenes klinisch äußert.
Klinisch werden Streptokokkenerkrankungen in drei Gruppen eingeteilt: die oberflächlichen Infektionen, die immunologischen Sequelae (Folgeerscheinungen) nach oberflächlichen Infektionen sowie die invasiven Infektionen. Veletzky: „Die klinische Ausprägung ist dabei mit den jeweiligen Virulenzfaktoren assoziiert.“ Die genannten Erkrankungen sind sehr häufig. Allein eine durch S. pyogenes verursachte Pharyngitis betrifft nach Schätzungen fast 300000 Millionen Menschen pro Jahr und verursacht alleine in den USA jährliche Kosten von bis zu 500 Millionen Dollar. Gefährlicher sind die Langzeitfolgen mit einer weltweiten Prävalenz von rund 40 Millionen Fällen und jährlich mehr als 300000 Todesfällen allein für die rheumatische Herzerkrankung. Bakteriämie mit S. pyogenes betrifft jährlich mehr als 600000 Menschen, von denen mehr als 160000 an der Erkrankung sterben.1
Noch keine klinisch relevanten Resistenzen gegen Penicillin
Die globale GAS-Epidemiologie ist gekennzeichnet durch ausgeprägte Schwankungen und das lokal unterschiedliche Auftreten von virulenten Stämmen. Veletzky nannte als Beispiele das Wiederauftreten des zeitweise fast verschwundenen Scharlachs sowie eine Häufung invasiver Erkrankungen in den vergangenen Jahren, die mit dem Auftreten neuer Virulenzfaktoren assoziiert ist. International wird das Auftreten von verminderter Penicillinempfindlichkeit und zunehmender Makrolidresistenz beobachtet. In Österreich stellt dies jedoch bislang kein Problem dar, wie aktuelle Daten der AGES zeigen. Laut dem Antibiotikaresistenz-Bericht (AURES) sind in Österreich 12,6% der Isolate resistent gegen Makrolide, Penicillinresistenzen wurden bislang nicht gefunden.
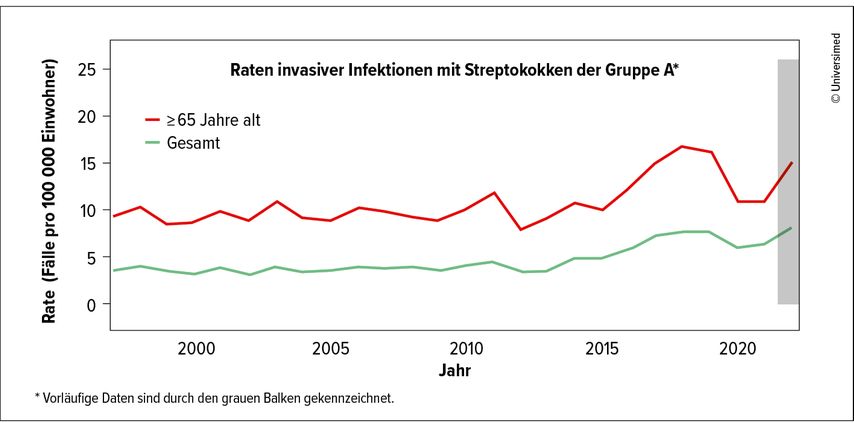
Beobachtet wird auch eine Zunahme invasiver Infektionen mit S. pyogenes. Laut Daten der amerikanischen Centers for Disease Control and Prevention (CDC) zeichnete sich diese Entwicklung etwa ab 2015 ab, wurde dann infolge der Infektionsschutzmaßnahmen während der Covid-Pandemie unterbrochen, nimmt aktuell aber wieder Fahrt auf (Abb. 1).2 In Österreich ist ein ähnlicher Trend zu beobachten, wobei die Erkrankungszahlen das Niveau von 2019 noch nicht erreicht haben.
Abb. 1: Inzidenz invasiver Streptokokkeninfektionen in den USA (modifiziert nach Centers for Disease Control and Prevention 2024)2
Unter den nicht invasiven Krankheitsbildern, die S. pyogenes verursacht, spielt die Pharyngitis die wichtigste Rolle. Sie gehört mit einem Gipfel in der Altersgruppe der 6- bis 12-Jährigen zu den häufigsten bakteriellen Erkrankungen im Kindesalter.3 Saisonal fällt ein Peak im Winter und Frühling auf. Klinisch äußert sich die Infektion mit einer leichten Schwellung oder einem Erythem der Pharynxschleimhaut, möglicherweise mit eitrigem Exsudat. Das Krankheitsgeschehen kann mit einer durchaus intensiven Symptomatik verbunden sein. Die wichtigste lokale Komplikation ist der Peritonsillarabszess. Eine weitere nicht invasive Form der Streptokokkeninfektion ist die ebenfalls vorwiegend bei Kindern auftretende Impetigo, konkret die kleinblasige Form (Impetigo vulgaris), während die großblasige Form (Impetigo bullosa) durch Staphylococcus aureus verursacht wird. Es handelt sich dabei um eine häufige, hochkontagiöse oberflächliche Infektion der Haut. Infektionsquelle kann eine Nasen- und Racheninfektion sein, es kann aber auch eine Übertragung durch Schmierinfektion von Impetigoherden bei Kontaktpersonen vorkommen.
Scharlach und Autoimmun-phänomene sind wieder da
Zahlreiche mit S. pyogenes verbundene Krankheitsbilder werden durch Toxine vermittelt. Das bekannteste ist der Scharlach, der sich unter anderem als Exanthem in Form kleinfleckiger Papeln äußert, beginnend am ersten oder zweiten Krankheitstag am Oberkörper mit zentrifugaler Ausbreitung unter Aussparung der Handinnenflächen und Fußsohlen. Weiters fallen periorale Blässe und die sogenannte „Himbeer-“ oder „Erdbeerzunge“, eine markante Zungenrötung, auf. Verursacher sind pyrogene Streptokokkenexotoxine. Rund zehn Tage nach dem Abklingen der akuten Erkrankung kommt es typischerweise zu Desquamation an den Händen und Füßen. Scharlach hinterlässt Immunität lediglich gegen den involvierten Stamm, mehrfache Erkrankungen sind also möglich.
Potenziell gefährliche Komplikationen der nicht invasiven Infektionen stellen die S.-pyogenes-Autoimmunphänomene dar. Sie können in der Folge von Pharyngitis bzw. Hautinfektionen nach einem symptomfreien Intervall auftreten. Pathophysiologischer Hintergrund ist die Bildung von IgG-Antikörpern gegen M-Proteine. Mögliche Manifestationen sind das akute rheumatische Fieber, die rheumatische Herzerkrankung sowie die postinfektiöse Glomerulonephritis. Diese Erkrankungen waren in den ressourcenreicheren Ländern längere Zeit sehr selten, durch das gehäufte Auftreten von Infektionen könnten diese jedoch auch wieder relevanter werden.
Streptokokken können jedoch nicht nur oberflächliche, sondern auch sehr schwere invasive Infektionen verursachen. Invasiv bedeutet in diesem Fall, dass der Erreger in sonst sterilem Material, wie beispielsweise im Blutstrom, in der Pleura oder in den Gelenken, nachgewiesen werden kann. Häufige invasive Krankheitsbilder sind Zellulitis, Bakteriämie, nekrotisierende Fasziitis, Puerperalsepsis und Pneumonie (potenziell mit Pleuraergüssen, Empyem und häufig Bakteriämie). Letztere kann auch bei jüngeren Menschen einen lebensbedrohlichen Verlauf nehmen, wie Veletzky am Fallbeispiel einer 45-jährigen Patientin erläuterte, die nach viertägiger Erkältung mit Schnupfen, Husten und gering erhöhter Temperatur starke stechende Schmerzen im rechten Hemithorax, ausstrahlend in die rechte Schulter, entwickelte. Mit diesem Beschwerdebild wurde sie nach weiteren zwei Tagen in der Notaufnahme vorstellig. Eine Abklärung auf Pulmonalembolie (PE) mittels CT (PE-Spirale) lieferte keine Hinweise auf PE, zeigte jedoch eine ausgedehnte Pneumonie der rechten Lunge mit geringem Begleiterguss (bis 1,3cm) sowie reaktiver Lymphadenopathie rechts hilär und mediastinal. Das Labor zeigte erhöhte Werte von CRP, Leukozyten und Thrombozyten und damit einen deutlichen Hinweis auf Inflammation. Der Kreatininwert war ebenfalls erhöht. Angesichts dieses Befunds wurde eine empirische Therapie mit Unasyn (Ampicillin plus Sulbactam) und Azithromycin begonnen. Die mikrobiologische Diagnostik war hinsichtlich Legionellen und Pneumokokken negativ, die PCR zeigte jedoch S. pyogenes sowie humanes Metapneumovirus. Veletzky wies darauf hin, dass Koinfektionen mit Streptokokken und Viren keine Seltenheit sind. Die Patientin entwickelte zusätzlich Exantheme an Händen und Füßen, die vermutlich durch Streptokokkentoxine verursacht wurden, bei Streptokokkenpneumonien jedoch unüblich sind. Eine initiale Verschlechterung machte in weiterer Folge auch eine Dekortikation erforderlich. Mit Erhalt des Erregernachweises erfolgte eine Therapieumstellung auf hochdosiertes Penicillin G.
Streptokokken-Toxic-Shock- Syndrom (STSS): 30% Mortalität
In selteneren Fällen kann es zu Gelenksbeteiligung, Meningitis oder Peritonitis kommen. Bei rund einem Drittel der invasiven GAS-Infektionen kommt es zum Streptokokken-Toxic-Shock-Syndrom, das eine extrem gefährliche Komplikation der invasiven Erkrankung darstellt und durch Streptokokkentoxine verursacht wird. Der resultierende Zytokinsturm führt zu Kapillarleckage und Gewebeschäden, Schock und Multiorganversagen. Ein Toxic-Shock-Syndrom kann in allen Altersgruppen und unabhängig von Immunstatus auftreten. Klinisch zeigen sich initial Symptome eines akuten Infektes, gefolgt von raschem Verfall mit Hypotension und Schockzeichen. Die Mortalität liegt bei rund 30%. Das für S. pyogenes typische diffuse scharlachartige Exanthem tritt nur in rund 10% der Fälle auf. Neben dem akuten Schockmanagement und der Behandlung der Bakteriämie sind auch Fokussuche und allfällige Sanierung entscheidend für den Therapieerfolg. Eine weitere gefährliche Manifestation der Infektion mit S. pyogenes ist die nekrotisierende Fasziitis, eine foudroyant verlaufende, nekrotisierende Weichteilinfektion der Haut und Unterhaut unter Beteiligung der Faszie, die sich mit unerträglichem Schmerz als Leitsymptom präsentiert. Dabei handelt es sich um einen absoluten chirurgischen Notfall, der schnellstmöglich radikales Débridement erfordert. Bei Verdacht auf nekrotisierende Fasziitis muss sofort chirurgisch interveniert werden. Keinesfalls bleibt Zeit, die Mikrobiologieergebnisse abzuwarten. Die antibiotische Therapie wird daher empirisch mit Meropenem und Clindamycin (3x1200mg) begonnen. Je nach Verlauf kann eine Deeskalation möglich werden. Allerdings entwickeln etwa 50% der Patienten mit nekrotisierender Fasziitis auch ein Toxic-Shock-Syndrom.
S.-pyogenes-Therapie: Penicilline sind nach wie vor erste Wahl
Da bislang keine klinisch relevanten Betalaktamresistenzen bekannt sind, ist Penicillin die Therapie der Wahl. Bei Pharyngitis und Zellulitis mit S. pyogenes wird Penicillin bzw. Amoxicillin oder Ampicillin (oral oder parenteral über zehn Tage) empfohlen. Veletzky betont die Wichtigkeit einer ausreichend langen Therapie. Bei Penicillinallergie empfiehlt die Paul-Ehrlich-Gesellschaft den Einsatz von Makroliden oder oralem Cephalosporin. Bei Makroliden ist allerdings mit Resistenzraten zwischen 10 und 30% zu rechnen.
Im stationären Setting sind Cephalosporine der dritten Generation i.v. die Alternative zu den Penicillinen. Wenn keine Allergiebesteht, ist parenterales Penicillin-G in ausreichender Dosierung indiziert. Bei schweren systemischen Infektionen, insbesondere wenn toxinvermittelte Komplikationen im Spiel sind (bei STSS und nekrotisierender Fasziitis), wird zusätzlich Clindamycin oder Linezolid/Tedizolid empfohlen. Die Wirksamkeit von Trimethoprim und Fluorchinolon ist bei Infektionen mit S. pyogenes schlecht. Die einzige Ausnahme bildet Moxifloxacin, das bei Streptokokkeninfektionen durchaus eingesetzt werden kann.
Eine Impfung gegen S. pyogenes wäre wünschenswert und könnte zahlreiche schwere Erkrankungen mit hoher Mortalität und Morbidität verhindern. Die Entwicklung eines Impfstoffs gestaltet sich jedoch schwierig, da sowohl die hohe genetische Diversität als auch das ausgeprägte immunogene Potenzial eine Herausforderung darstellen.
Quelle:
„Gruppe-A-Streptokokken“, Vortrag von Dr. Luzia Veletzky, Wien, im Rahmen des ÖIK am 20.März 2025 in Saalfelden
Literatur:
1 Brouwer S et al.: Nat Rev Microbiol 2023; 21: 431-47 2 CDC: Group A strep disease surveillance and trends. 2024. https://www.cdc.gov/group-a-strep/php/surveillance/index.html ; zuletzt aufgerufen am 16.5.2025 3 Di Pietro GM et al.: Pathogens 2024; 13(5): 350
Das könnte Sie auch interessieren:
Ageismus und Wege dagegen – Frauen mit HIV in der ärztlichen Praxis
Seit 2021 ruft die WHO unter dem Hashtag #AWorld4AllAges zum Kampf gegen Ageismus weltweit auf und fordert mehr Forschung und Aufklärung zu diesem Thema.1 Gerade ältere Frauen*, die mit ...
Eradikation bei EHEC-Dauerausscheidung mit Antibiotika
Mit dem Akronym EHEC (enterohämorrhagische Escherichia coli) werden Shigatoxin (Stx) produzierende, humanpathogene E.-coli-Stämme (STEC) bezeichnet. Neben zytotoxischen, mit einem ...
Malaria: Diagnostik und Behandlung nach aktuellen Leitlinien
Gleich mehrere Leitlinien zum Thema Malaria wurden im vergangenen Jahr aktualisiert. Dies betrifft die WHO-Guidelines, die deutsche S1-Leitlinie und die Malaria Treatment Recommendations ...