Eosinophilie und Reiseanamnese: an Parasiten denken
Bericht:
Reno Barth
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Eine erhöhte Zahl von eosinophilen Granulozyten im Blut kann unter anderem ein Hinweis auf eine Infektion mit Parasiten sein. Vor allem bei entsprechender Reise- oder Migrationsanamnese sollte eine Abklärung in diese Richtung erfolgen. Eine britische Guideline liefert einen detaillierten Algorithmus für das diagnostische und therapeutische Vorgehen.
Eosinophile Granulozyten sind eine Untergruppe der Granulozyten und werden im Knochenmark gebildet. Wenn beispielsweise infolge einer Parasiteninfektion Interleukin-5 ausgeschüttet wird, so werden Eosinophile in das Blut ausgeschwemmt, wo sie acht bis zwölf Stunden verbleiben und von wo sie in ihre Zielorgane wandern. Ab einer Zellzahl von mindestens 500 pro Mikroliter spricht man von Eosinophilie, ab 1500 Zellen von Hypereosinophilie.1
Funktionen von Eosinophilen
Eosinophile haben eine Vielzahl von Funktionen, die allerdings erst zum Teil verstanden werden, so OÄ Priv.-Doz. Dr. Tamara Clodi-Seitz, PhD, DTM&H, Abteilung für Infektiologie und Tropenmedizin der Klinik Favoriten in Wien. Unter anderem sind Eosinophile wichtig für die Immunabwehr gegen Parasiten, für die Regeneration von Muskeln und Leber, für die Regulation der Darmbarriere und des Mikrobioms, im Knochenmark sind sie erforderlich für Aktivierung, Entwicklung und Überleben von Plasmazellen. Hinzu kommen zahlreiche weitere Funktionen in verschiedenen Organsystemen. Die vielfältigen Funktionen der Eosinophilen erklären auch, dass verschiedenste Organsysteme von eosinophiler Entzündung betroffen sein können. Mögliche Erkrankungen sind unter anderem Asthma, eosinophile chronisch obstruktive Lungenerkrankung (COPD), eosinophile Pneumonie, chronische Rhinosinusitis mit Nasenpolypen, eosinophile Ösophagitis, chronisch-entzündliche Darmerkrankungen, eosinophile Granulomatose mit Polyangiitis. Auch bei manchen hämatologischen Malignomen besteht Eosinophilie.2
Sekundäre Eosinophilie kann vielfältige Ursachen haben
Eine wichtige Unterscheidung wird getroffen zwischen den seltenen primären Formen der Eosinophilie, die vom Knochenmark ausgehen, und sekundären Formen, die auf mannigfaltige Ursachen zurückgehen können. Gründe für sekundäre Eosinophilie sind Allergien, Infektionen, Medikamente, Tumoren, Autoimmunerkrankungen sowie – vermittelt durch den resultierenden Cortisolmangel – Insuffizienz der Nebennieren. Durch Medikamente induzierte Eosinophilie kann eine relevante unerwünschte Wirkung von Checkpoint-Inhibitoren sein und im schlimmsten Fall tödlich verlaufen.
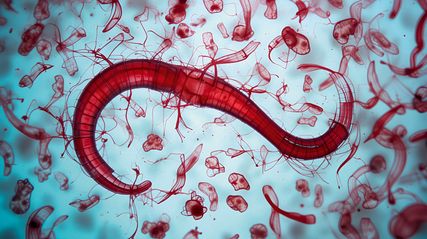
Unter den Infektionen führen vor allem Parasiten und da besonders Würmer zu Eosinophilie. Clodi-Seitz wies speziell auf Schistosomiasis (Abb.1) und Infektionen mit Strongyloides hin, die in Europa immer wieder als Reiseinfektionen oder im Kontext von Migration gesehen werden. Ebenso können Ektoparasiten wie Sarcoptes scabiei zu Eosinophilie führen. Auch an Pilzinfektionen oder eine allergische bronchopulmonale Aspergillose oder eine HIV-Infektion müsse gedacht werden. Auch Bakterien können in seltenen Fällen mit erhöhten Eosinophilenzahlen in Zusammenhang stehen. Differenzialdiagnosen wie Syphilis und Tuberkulose sollten abgeklärt werden.
Wird im klinischen Alltag eine Eosinophilie festgestellt, so ist zunächst deren Ausprägung zu quantifizieren, wobei die absolute Eosinophilenzahl und nicht die relative entscheidend ist.
Umfangreiche Anamnese ist bei Eosinophilie unverzichtbar
Bei einer leichten Eosinophilie besteht, wenn weder eine verdächtige Reiseanamnese noch eine Organbeteiligung vorliegt, nicht immer sofortiger Handlungsbedarf. In solchen Fällen kann das Blutbild mit einem Abstand von ein paar Monaten wiederholt werden. Die Reise- und Migrationsanamnese betrifft das ganze Leben und nicht nur die vergangenen sechs Monate, so Clodi-Seitz.
Neben Fragen nach Reisen oder Migrationshintergrund sollte im Rahmen der Anamnese auch nach Erkrankungen in der Familie, nach Medikamenteneinnahme sowie nach dem Konsum potenziell kontaminierter Lebensmittel gefragt werden. Im nächsten Schritt werden Symptome erfragt und es wird nach Organbeteiligungen gesucht. Ein komplexer, aber praxistauglicher Algorithmus wurde kürzlich in Großbritannien in Form einer Leitlinie publiziert.3 Darin werden mögliche Diagnosen in Zusammenhang mit Reise- oder Migrationsanamnese gelistet. Es werden auch Empfehlungen für das weitere Vorgehen gegeben, sollte keine Ursache gefunden werden oder die Eosinophilie nach erfolgreicher Behandlung der Parasiteninfektion weiter bestehen. Clodi-Seitz: „Das ist zwar aufwendig zu lesen, aber grandios. Neben den infektiösen werden auch nichtinfektiöse Ursachen von Eosinophilie aufgeführt.“ Wichtig im Algorithmus ist auch die Frage nach etwaigen Reisedestinationen. Beispielsweise ist auch bei asymptomatischen Patient:innen mit Eosinophilie eine Schistosoma-Serologie indiziert, wenn diese in einem Endemiegebiet waren. Da Endemiegebiete variieren, wird empfohlen, den aktuellen Status der Reisedestination abzufragen. Eine mikroskopische Untersuchung von Stuhl und Harn sollte durchgeführt und im Hinblick auf die Reisedestination ausgewertet werden. Bei asymptomatischen Patient:innen kann auch (Reiseanamnese vorausgesetzt) eine empirische Therapie mit Albendazol und Ivermectin versucht werden. Davor sollte nach Aufenthalten in Afrika jedoch Loa loa (Augenwurm) ausgeschlossen werden, da dieser eine Kontraindikation für Ivermectin bedeutet. Mögliche Organbeteiligungen werden mit den zugehörigen Parasiten und den Regionen, in denen diese vorkommen, detailliert gelistet.
Fast alles ist möglich: Eosinophilie, Organbeteiligung und Symptome
Beispielsweise können respiratorische Symptome in Kombination mit Eosinophilie auf eine akute Schistosomiasis, eine pulmonale Schistosomiasis, einen Lungenegel oder ein Löffler-Syndrom als Reaktion auf durch die Lunge migrierende Würmer hindeuten. Deutlich häufigere Ursachen sind in Mitteleuropa jedoch Asthma bronchiale, allergische Rhinosinusitis, eine eosinophile Pneumonie oder eine allergische bronchopulmonale Aspergillose. Auch Autoimmunerkrankungen wie die eosinophile Granulomatose mit Polyangiitis (EGPA) kommen infrage, ebenso zählen Pilze und TBC zu den Differenzialdiagnosen.
Hinter Eosinophilie und gastrointestinalen Symptomen können eine hepatosplenische oder intestinale Schistosomiasis, Strongyloides-Infektion, Ascariasis, Hakenwürmer, Leberegel oder Trichinellose stehen. Auch hier kommen nicht infektiöse Ursachen wie eosinophile Ösophagitis, Gastritis oder Kolitis infrage. Auch die Kombination von Eosinophilie und neurologischen Beschwerden lenkt den Verdacht auf Parasiten. Bildgebung und Liquorpunktion sind indiziert. Infrage kommen unter anderem zerebrale Schistosomiasis, Gnathostomiasis oder Angiostrongylus cantonensis, der typischerweise durch den Verzehr roher Schnecken in Endemiegebieten übertragen wird, die sich u.a. in Salat befinden können. Bei dermatologischen Symptomen und Eosinophilie sind ebenfalls Parasiten als mögliche Ursache von nichtinfektiösen Ursachen abzugrenzen. Das ist beispielsweise der Fall bei DRESS („drug rash with eosinophilia and systemic symptoms“) als schwerem Arzneimittelexanthem, Lupus erythematodes oder Allergien. Parasitäre Erkrankungen, die eine Hautsymptomatik verursachen können, sind unter anderem Schistosomiasis, kutane Larva migrans, Larva currens, Onchozerkose, lymphatische Filariasis oder Loa-loa-Infektionen.
Fallbeispiele: Eosinophilie im klinischen Alltag
Wie sich Eosinophilie als Folge von Infektionen mit Parasiten im klinischen Alltag darstellen kann, erläuterte Clodi-Seitz an mehreren Fallbeispielen. Eine von den Philippinen stammende 52-jährige Patientin ohne Vorerkrankungen wurde akut wegen einer Ösophagusvarizenblutung aufgenommen. Das Blutbild zeigte eine ausgeprägte Eosinophilie, der Ultraschall eine Hepatosplenomegalie und eine periportale Fibrose. Die Anamnese wies in diesem Fall den Weg zur Diagnose, denn im Reisanbaugebiet Tacloban ist der Plattwurm Schistosoma endemisch. Schistosoma benötigt im Wasser lebende Schnecken als Zwischenwirt, seine Zerkarien dringen bei Kontakt mit kontaminiertem Wasser über die Haut in den menschlichen Organismus, wo sich der adulte Wurm entwickelt und sich in verschiedensten Organsystemen ansiedeln kann. Seine Eier werden mit dem Urin oder Stuhl ausgeschieden und gelangen so wieder ins Wasser. Die Infektion kann je nach Organbefall zu vielfältigen Symptomen führen. Typischerweise führt das Eindringen des Parasiten durch die Haut zu einer Dermatitis, auf die eine lange asymptomatische Phase folgt. Am häufigsten kommt es zu Symptomen in Zusammenhang mit chronischer Entzündung des periportalen Systems oder der ableitenden Harnwege, ausgelöst durch die Produktion von Schistosoma-Eiern. Weltweit sind rund 250 Millionen Menschen von der Parasitose betroffen, vorwiegend in Afrika und Südostasien.
Wie kompliziert die Diagnostik bei Eosinophilie sein kann, illustrierte Clodi-Seitz mit dem Fall eines 67-jährigen Patienten mit seit Monaten bestehender, massiver Eosinophilie mit mehr als 9000 Eosinophilen/μl im Blut. Die Reiseanamnese ergab lediglich einen lange zurückliegenden jahrelangen Aufenthalt in den USA sowie regelmäßige Reisen in die USA. Der starke Raucher litt unter Asthma, möglicherweise auch unter COPD, und wurde mit Kortison behandelt. Zudem besteht eine chronische Sinusitis mit Nasenpolypen. Aufgrund immer wieder auftretender Atemnot wurde eine Lungenfunktionsdiagnostik durchgeführt und eine mittelgradige Diffusionsstörung festgestellt. Im Sputum wurde Aspergillus fumigatus gefunden, der Verdacht auf eine allergische bronchopulmonale Aspergillose bestätigte sich jedoch nicht. Im Lungen-CT fielen beidseitige Infiltrate auf. Nach breiter infektiologischer Abklärung, die durchwegs negative Ergebnisse erbrachte, entschloss man sich zur Lungenbiopsie, die zur Diagnose einer Autoimmunerkrankung führte. Der Patient litt unter der seltenen eosinophilen Granulomatose mit Polyangiitis.
Quelle:
„Patient:innen mit Eosinophilie“, Vortrag von OÄ Priv.-Doz. Dr. Tamara Clodi-Seitz, Wien, im Rahmen des 18. ÖIK am 20. März 2026 in Saalfelden
Literatur:
1 Shomali W, Gotlib J: World Health Organization-defined eosinophilic disorders: 2022 update on diagnosis, risk stratification, and management. Am J Hematol 2022; 97(1): 129-48 2 Wechsler ME et al.: Eosinophils in health and disease: A state-of-the-art review. Mayo Clin Proc 2021; 96(10): 2694-2707 3 Thakker C et al.: UK guidelines for the investigation and management of eosinophilia in returning travellers and migrants. J Infect 2025; 90(2): 106328
Das könnte Sie auch interessieren:
„Infektiologie ist das Fach der Zukunft!“
Auf dem heurigen Infektionskongress in Saalfelden werden sich zum ersten Mal junge, engagierte infektiologisch Interessierte treffen, um das Projekt „Junge OEGIT“ voranzubringen. Was ...
Gürtelrosevakzine auch bei Autoimmunkrankheiten gut verträglich
Patient:innen mit Autoimmunkrankheiten fürchten oft, dass Impfungen ihre Symptome verschlimmern könnten, vor allem wenn sie für Nebenwirkungen bekannt sind, wie der Herpes-Zoster- ...
HIV und Aids: eine Nebenbaustelle?
Die antiviralen Behandlungsmöglichkeiten der HIV-Infektion verbessern sich kontinuierlich. Auf der anderen Seite rücken Probleme der Komorbiditäten zunehmend in den Vordergrund, da diese ...