Wer braucht GLP-1-Agonisten in Zeiten der SGLT2-Hemmer?
Autor:
Apl. Prof. Dr. Baptist Gallwitz
Stellvertretender Ärztlicher Direktor
Medizinische Klinik Innere Medizin IV Diabetologie, Endokrinologie, Nephrologie
Universitätsklinikum Tübingen
Für welche Indikationen ist der Einsatz von GLP-1-Rezeptoragonisten (GLP-1-RA) vorteilhaft? Diese Frage stellt sich in der aktuellen Situation immer wieder – der vorliegende Artikel fasst dies zusammen und gibt auch eine Antwort zur Zukunftsentwicklung der GLP-1-RA.
Keypoints
-
GLP-1-RA haben ihren Stellenwert bei Patienten mit kardiovaskulärer Vorerkrankung. Insbesondere bei atherosklerotischen Komplikationen haben sie kardiovaskuläre Vorteile gezeigt.
-
Bei der Gewichtsreduktion sind GLP-1-RA den SGLT2-I deutlich überlegen.
-
In den Leitlinien haben GLP-1-RA als erste mittels Injektion applizierbare Therapie Insulin abgelöst.
-
Der GLP-1-RA Liraglutid kann unabhängig vom Vorliegen eines Diabetes zur Adipositastherapie eingesetzt werden.
-
Doppel- und Dreifachagonisten, die an den GLP-1-, GIP- und/oder den Glukagonrezeptor binden, sind in Entwicklung.
GLP-1-Rezeptoragonisten (GLP-1-RA) und SGLT2-Hemmer (SGLT2-I) haben durch ihre vorteilhaften Ergebnisse in kardiovaskulären Sicherheitsstudien mit signifikanter Reduktion von Endpunkten einen frühen und bevorzugten Platz in den Leitlinien zur Behandlung des Typ-2-Diabetes (T2D). SGLT2-I werden als orale Therapie bei Patienten mit kardiovaskulärer oder kardiorenaler Vorerkrankung unabhängig vom HbA1c-Wert empfohlen. Mittlerweile sind sie auch außerhalb des T2D zur Behandlung der Herzinsuffizienz und der chronischen Niereninsuffizienz zugelassen. Für welche Indikationen GLP-1-RA vor diesem Hintergrund trotzdem vorteilhaft sind, fasst dieser Artikel zusammen und stellt auch die Zukunftsentwicklung der GLP-1-RA dar.
Rationale der Therapie des Typ-2-Diabetes mit GLP-1-RA
Seit 2005 sind GLP-1-RA zur Therapie des T2D zugelassen und seit 2016 gibt es erste Ergebnisse, die einen Vorteil bezüglich kardiovaskulärer Endpunkte (s.u.) gezeigt haben. Daher hat in den letzten Jahren diese Therapie zunehmend an Bedeutung gewonnen und ist auch in den Leitlinien implementiert. GLP-1-RA stimulieren glukoseabhängig nur bei Hyperglykämie die Insulinsekretion und hemmen die Glukagonsekretion. Auf diesen beiden Wegen tragen sie zur Normalisierung der Stoffwechsellage bei, ohne Risiko, eine Hypoglykämie zu provozieren. Als nicht glykämische Wirkungen sind die Körpergewichtsabnahme und die leichte Senkung des systolischen Blutdrucks attraktiv.1
Die Platzierung der GLP-1-RA in den Leitlinien für Menschen mit T2D und kardiovaskulärer Vorerkrankung sieht eine Therapie direkt nach Beginn einer Metformin-Therapie vor, unabhängig vom HbA1c.2 Auch in der Therapie der Adipositas können GLP-1-RA mit entsprechender Zulassung eingesetzt werden und sind hier gut wirksam. Der Effekt auf die Gewichtsreduktion ist bei den GLP-1-RA stärker ausgeprägt als bei den SGLT2-I.
Ergebnisse kardiovaskulärer Sicherheitsstudien mit GLP-1-RA
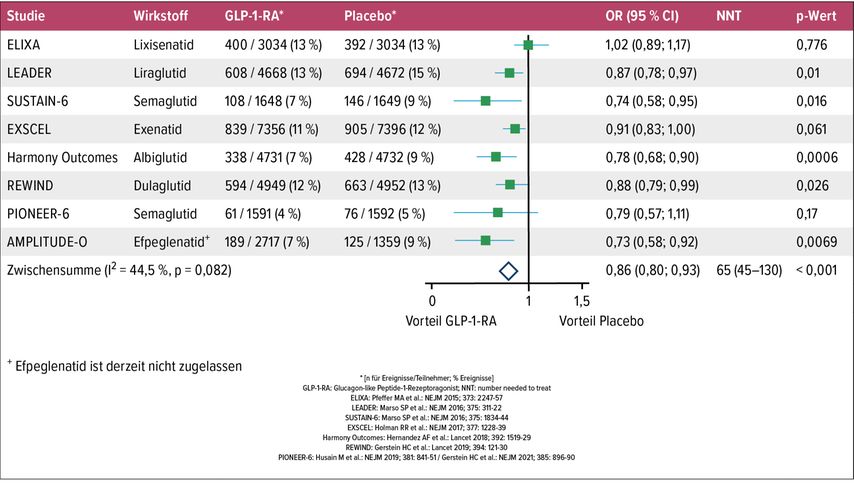
Bisher liegen Ergebnisse von insgesamt acht kardiovaskulären Sicherheitsstudien vor, die die Vorteile im zusammengesetzten Endpunkt MACE-3 (MACE = „major adverse cardiovascular event“, bestehend aus kardiovaskulärem Tod, nicht tödlichem Myokardinfarkt und nicht tödlichem Schlaganfall) untersucht haben. Fünf dieser Studien zeigten einen signifikanten Vorteil des jeweils untersuchten GLP-1-RA auf den Endpunkt MACE-3 im Vergleich zur Standardtherapie bei T2D und kardiovaskulärer Vorerkrankung. Zu diesen GLP-1-RA, die diese Studienergebnisse zeigten, zählen (in alphabetischer Reihenfolge) Albiglutid, Dulaglutid, Efpeglenatid, Liraglutid und Semaglutid.3–7 Eine Metaanalyse aller acht kardiovaskulären Sicherheitsstudien erbrachte eine signifikante Reduktion des relativen Risikos durch eine GLP-1-RA-Therapie von 14% (OR 86; 95% CI: 83–90) (Abb.1).8
Abb. 1: Metaanalyse kardiovaskulärer Endpunktstudien für GLP-1-Rezeptoragonisten 2021/22 (adaptiert nach Sattar N et al.8)
Die erste Studie, die für einen GLP-1-RA eine Überlegenheit in der Reduktion kardiovaskulärer Endpunkte gegenüber Standardtherapie gezeigt hat, war die LEADER-Studie mit Liraglutid, die eine Reduktion des relativen Risikos von 13% beim kombinierten Endpunkt MACE-3 bei kardiovaskulär vorerkrankten Patienten gezeigt hat (HR: 0,87; 95% CI: 0,78–0,97).6 In der REWIND-Studie mit Dulaglutid zeigten sich ähnliche Ergebnisse. In dieser Studie waren jedoch auch Patienten eingeschlossen, die zu Beginn der Studie noch nicht kardiovaskulär vorerkrankt waren, was möglicherweise auf einen starken kardiovaskulär protektiven Effekt dieses GLP-1-RA hinweist. Die Frage, ob dieses Ergebnis auf andere GLP-1-RA übertragbar ist, ist derzeit offen.4 In einigen der kardiovaskulären Sicherheitsstudien zeigten sich auch unter der Therapie mit GLP-1-RA Verbesserungen in Parametern, die eine Hemmung der Progression einer chronischen Nierenfunktionsstörung anzeigten.9
Typ-2-Diabetes: additive Effekte von SGLT2-I und GLP-1-RA
Beide Substanzklassen haben in der Kombinationstherapie nicht nur additive Effekte auf die Glykämieparameter, sondern auch auf die Körpergewichtsreduktion und die Blutdruckreduktion. Dies wurde in der dreiarmigen Studie DURATION-8 gezeigt, in der die Kombination des SGLT2-I Dapagliflozin mit dem GLP-1-RA Exenatid LAR („long-acting-release“) über einen Zeitraum von zwei Jahren untersucht wurde.10
In der AWARD-10-Studie konnte bei Patienten, die unter einer Therapie mit einem SGLT2-I noch keine optimale Stoffwechselkontrolle erreicht hatten, gezeigt werden, dass eine zusätzliche Therapie mit dem GLP-1-RA Dulaglutid deutlich mehr Patienten dosisabhängig den zusammengesetzten Endpunkt aus HbA1c <7%, Körpergewichtsverlust >5% und dem Fehlen von therapiebedingten Hypoglykämien erreichen lassen.11 Eine kürzlich publizierte retrospektive Metaanalyse solcher Kombinationsstudien bestätigte die additive Wirkung der Kombinationstherapie und zeigte auch Hinweise auf eine Reduktion von kardiovaskulären Ereignissen.12
GLP-1-RA zur Adipositastherapie
Liraglutid ist in einer Dosierung von 3,0mg täglich zur Therapie der Adipositas außerhalb der Diabetesindikation zugelassen und es ist damit zu rechnen, dass Semaglutid ebenfalls in einer höheren Dosierung als bei T2D (2,4mg einmal wöchentlich) die Zulassung dafür auf der Grundlage des hierfür durchgeführten STEP-Studienprogramms erhalten wird.13–16
Die Effekte von GLP-1-RA auf die Gewichstreduktion sind stärker als die der bislang gebräuchlichen und mittlerweile aufgrund von Nebenwirkungen wieder vom Markt genommenen Medikamente zur Gewichtsreduktion.17 Die bisherigen Ergebnisse der STEP-Studie zeigen einen Gewichtsverlust von ca. 15% des Körpergewichts unter einer Behandlung mit Semaglutid.13–16
Doppel- und Dreifachagonisten von Inkretinen oder Glukagon
Praxistipp
Bei Beginn mit GLP-1-RA können passagere Nebenwirkungen (Völlegefühl und Übelkeit) auftreten. Daher einschleichend bis zur maximal tolerierten, zugelassenen Dosis auftitrieren.Durch Doppel- und Dreifachagonisten von GLP-1, GIP („glucose-dependent insulinotropic polypeptide“) und Glukagon könnten möglicherweise mehrere metabolische Stoffwechselwege im Kohlenhydrat- und Lipidstoffwechsel simultan beeinflusst werden. GIP und GLP-1 sind von ihrer Peptidsequenz her ähnlich, sie binden aber an unterschiedliche spezifische Rezeptoren. Auch Glukagon und GLP-1 haben ähnliche Peptidsequenzen. Aus diesen Überlegungen heraus wurden in den letzten Jahren GLP-1/GIP-Doppelagonisten als auch GLP-1/Glukagon-Doppelagonisten sowie Dreifachagonisten zur Therapie des T2D und der Adipositas entwickelt.17–19 Sehr weit entwickelt ist der GLP-1-RA/GIP-Koagonist Tirzepatid. Im Studienprogramm SURPASS für die Zulassung zur Therapie des T2D senkte Tirzepatid den HbA1c dosisabhängig deutlich stärker als die etablierten Diabetesmedikamente inklusive der GLP-1-RA. Unter Tirzepatid wurden HbA1c-Senkungen von ca. 1,8–2,6% beobachtet.20 Die Körpergewichtsabnahme betrug in diesen Studien dosisabhängig ca. 7–13%.20 Die Nebenwirkungen sind ähnlich denen der GLP-1-RA. Ergebnisse einer kardiovaskulären Sicherheitsstudie mit Tirzepatid werden 2024 erwartet. Mit einer europäischen Zulassung ist voraussichtlich Anfang 2023 zu rechnen.
Literatur:
1 Nauck MA et al.: GLP-1 receptor agonists in the treatment of type 2 diabetes - state-of-the-art. Mol Metab 2021; 46: 101102 2 Draznin B et al.: 9. Pharmacologic Approaches to Glycemic Treatment: Standards of Medical Care in Diabetes-2022. Diabetes Care 2022; 45(1): 125-43 3 Hernandez AF et al.: Albiglutide and cardiovascular outcomes in patients with type 2 diabetes and cardiovascular disease (Harmony Outcomes): a double-blind, randomised placebo-controlled trial. Lancet 2018; 392(10157): 1519-29 4 Gerstein HC et al.: Dulaglutide and cardiovascular outcomes in type 2 diabetes (REWIND): a double-blind, randomised placebo-controlled trial. Lancet 2019; 394(10193): 121-30 5 Gerstein HC et al.: Cardiovascular and renal outcomes with Efpeglenatide in type 2 diabetes. N Engl J Med 2021; 385(10): 896-907 6 Marso SP et al.: Liraglutide and cardiovascular outcomes in type 2 diabetes. N Engl J Med 2016; 375(4): 311-22 7 Marso SP et al.: Semaglutide and cardiovascular outcomes in patients with type 2 diabetes. N Engl J Med 2016; 375(19): 1834-44 8 Sattar N et al.: Cardiovascular, mortality, and kidney outcomes with GLP-1 receptor agonists in patients with type 2 diabetes: a systematic review and meta-analysis of randomised trials. Lancet Diabetes Endocrinol 2021; 9(10): 653-62 9 Yoshiji S et al.: Effects of glucagon-like peptide-1 receptor agonists on cardiovascular and renal outcomes: A meta-analysis and meta-regression analysis. Diabetes Obes Metab 2022; (6): 1029-37 10 Jabbour SA et al.: Efficacy and safety over 2 years of exenatide plus Dapagliflozin in the DURATION-8-study: A multicenter, double-blind, phase 3, randomized controlled trial. Diabetes Care 2020; (10): 2528-36 11 Ludvik B et al.: Dulaglutide as add-on therapy to SGLT2 inhibitors in patients with inadequately controlled type 2 diabetes (AWARD-10): a 24-week, randomised, double-blind, placebo-controlled trial. Lancet Diabetes Endocrinol 2018; (5): 370-81 12 Wright AK et al.: Primary prevention of cardiovascular and heart failure events with SGLT2 Inhibitors, GLP-1 receptor agonists, and their combination in type 2 diabetes. Diabetes Care 2022; 45(4): 909-18 13 Wilding JPH et al.: Once-weekly semaglutide in adults with overweight or obesity. N Engl J Med 2021; 384(11): 989 14 Davies M et al.: Semaglutide 2,4mg once a week in adults with overweight or obesity, and type 2 diabetes (STEP 2): a randomised, double-blind, double-dummy, placebo-controlled, phase 3 trial. Lancet 2021; 397(10278): 971-84 15 Wadden TA et al.: Effect of subcutaneous Semaglutide vs Placebo as an adjunct to intensive behavioral therapy on body weight in adults with overweight or obesity: The STEP 3 randomized clinical trial. JAMA 2021; 325(14): 1403-13 16 Rubino D et al.: Effect of continued weekly subcutaneous Semaglutide vs placebo on weight loss maintenance in adults with overweight or obesity: The STEP 4 randomized clinical trial. JAMA 2021; 325(14): 1414-25 17 Del Prato S et al.: The incretin/glucagon system as a target for pharmacotherapy of obesity. Obes Rev 2022; (2): e13372 18 Brandt SJ et al.: Are peptide conjugates the golden therapy against obesity? J Endocrinol 2018; 238(2): 109-19 19 Finan B et al.: A rationally designed monomeric peptide triagonist corrects obesity and diabetes in rodents. Nat Med 2015; (1): 27-36 20 Bhagavathula AS et al.: Efficacy and safety of Tirzepatide in patients with type 2 diabetes mellitus: A systematic review and meta-analysis of randomized phase II/III Trials. Pharmaceuticals (Basel) 2021; 14(10): 991
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Notfall Diabetische Ketoazidose: Leitliniengerechtes Handeln kann Leben retten
Akute Stoffwechselentgleisungen können lebensbedrohlich sein und erfordern eine rasche und leitliniengerechte Diagnostik und Therapie. Pathogenese, Klinik, typische Befunde und die ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...