Konsensuspapier zur metabolisch bedingten steatotischen Lebererkrankung
Bericht:
Mag. Andrea Fallent
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Bei der ÖGGH-Jahrestagung präsentierten Ap. Prof. Priv.-Doz. DDr. Mattias Mandorfer und DDr. Georg Semmler, Klinische Abteilung für Gastroenterologie und Hepatologie an der MedUni Wien, die wichtigsten Punkte des Konsensus dreier österreichischer Fachgesellschaften zu Diagnose, Monitoring und Therapie der metabolisch bedingten steatotischen Lebererkrankung (MASLD)
Das neue Konsensuspapier zur MASLD/MASH wurde von den drei Fachgesellschaften ÖGGH (Österreichische Gesellschaft für Gastroenterologie und Hepatologie), ÖDG (Österreichische Diabetes Gesellschaft) und ÖAG (Österreichische Adipositas Gesellschaft) erstellt und setzt den Fokus auf die metabolisch bedingte steatotische Lebererkrankung (MASLD), die metabolisch bedingte Steatohepatitis (MASH) sowie die kombiniert metabolisch und Alkohol-assoziierte steatotische Lebererkrankung (MetALD).1 Der Inhalt des österreichischen Konsensus orientiert sich an den europäischen Leitlinien von 20242, wurde für die klinische Praxis bewusst kurz gehalten und auf direkt anwendbare Handlungsempfehlungen zugeschnitten. Koordiniert von Ap. Prof. Priv.-Doz. DDr. Mattias Mandorfer und DDr. Georg Semmler, Wien, erarbeiteten Expert:innen aller drei Fachgesellschaften den Inhalt in 5 Panels.
Steatose: Eingrenzung und Terminologie
Auf den diskriminierenden Begriff „Fettleber“ wurde im Konsens zugunsten des Fachterminus Steatose verzichtet. Für die Diagnose kommen bildgebende Verfahren (Ultraschall, CT, MRT, „controlled attenuation parameter“ [CAP] etc.) zum Einsatz. Dabei sollte auch an sekundäre Steatoseformen gedacht werden – wichtig ist der Ausschluss von Differenzialdiagnosen wie u.a. arzneimittelinduzierten Leberschäden („drug-induced liver injury“; DILI) und genetisch bedingten Erkrankungen wie der lysosomalen sauren Lipase-Defizienz (LAL-D) und der Hypobetalipoproteinämie sowie Formen der Lipodystrophie (u.a. HIV-assoziiert), endokrinologischen Erkrankungen wie Hypothyreose, Zöliakie u.a., die mit Steatose einhergehen können. Die Prävalenz der Steatose in Österreich beträgt ca. 35–55%, davon weisen 3–7% eine signifikante Fibrose auf, 1% eine fortgeschrittene Fibrose (siehe Referat in dieser Ausgabe auf Seite 16).
Die Subformen der steatotischen Lebererkrankung (SLD) sind MASLD, MASH, MetALD und ALD. Die ALD wurde bewusst aus dem Konsensus herausgelassen, weil dafür andere Kooperationspartner angesprochen werden müssten. Therapieentscheidend sei nicht das Vorliegen einer MASH, sondern einer fortgeschrittenen Fibrose, so Mandorfer.
SLD-Klassifikation
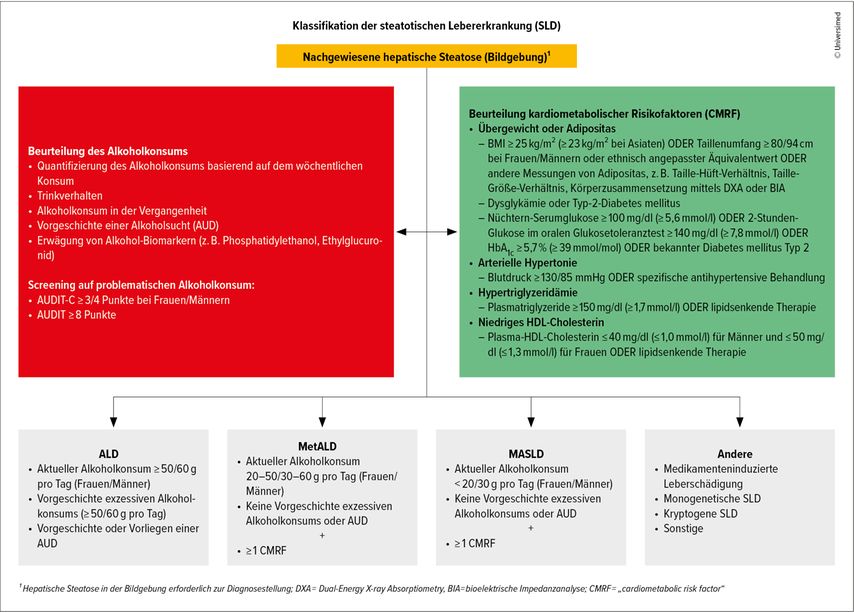
Die Abbildung 1 zeigt die Einteilung der Patient:innen mit SLD. Sie erfolgt anhand von zwei Komponenten: einmal mittels Bewertung des Alkoholkonsums und des Trinkverhaltens. Dabei sollen spezielle Screening-Tools wie der AUDIT-C eingesetzt werden, um pathologischen Alkoholkonsum zu detektieren. Biomarker wie Peth, EtG etc. können bei der Einschätzung helfen, wenn sie verfügbar sind. Die zweite zentrale Komponente der Klassifikation ist die metabolische Dysfunktion mit der Bewertung der fünf kardiometabolischen Risikofaktoren:
-
Übergewicht bzw. Adipositas
-
Dysglykämie bzw. Diabetes mellitus Typ2
-
Arterieller Bluthochdruck
-
Hypertriglyzeridämie
-
Niedriges HDL-Cholesterin
Abb. 1: Klassifikation der steatotischen Lebererkrankung (modifiziert nach Mandorfer M, Semmler G 2025)
Mithilfe dieser Parameter erfolgt die Klassifizierung in ALD, MetALD, MASLD und weitere SLD (Abb. 1).
Screening, Risikostratifizierung und Monitoring
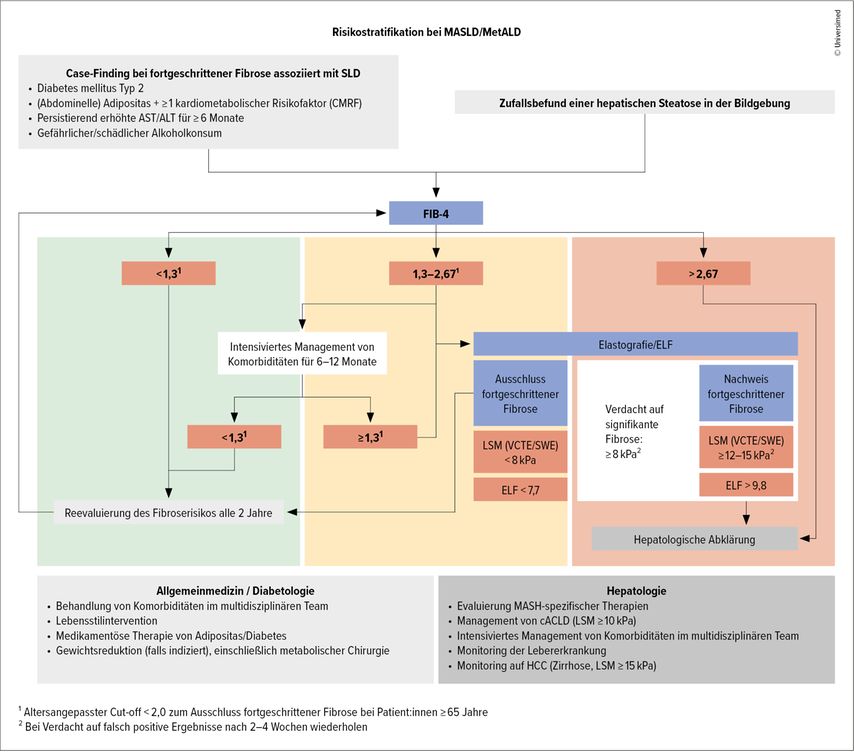
Ein generelles Screening in der Allgemeinbevölkerung wird nicht empfohlen. Stattdessen soll ein „Case-Finding“ von Fällen von fortgeschrittener Fibrose in den folgenden Risikogruppen erfolgen (Abb. 2): Personen mit Diabetes, mit Übergewicht und mindestens einem zusätzlichen metabolischen Risikofaktor, mit persistent erhöhten Leberenzymen (AST/ALT) und jene mit schädlichem Alkoholkonsum (>20/30g pro Tag oder AUDIT-C ≥ 3–4 Pkt. oder AUDIT ≥8 Pkt.).
Ist die MASLD/MetALD diagnostiziert, erfolgt die Risikostratifizierung per FIB-4-Test (Abb. 2; anhand Alter, Thrombozytenzahl und Transaminasen). Liegt der Score unter 1,3, ist keine leberspezifische Abklärung notwendig, das Fibroserisiko soll alle 2 Jahre mittels FIB-4-Test erneut kontrolliert werden. Bei einem FIB-4-Wert zwischen 1,3 und 2,67 sollte ein intensiviertes Management der Komorbiditäten für 6–12 Monate mit Reevaluierung oder eine weiterführende Abklärung mittels Elastografie bzw. ein „Enhanced liver fibrosis“(ELF)-Test erfolgen. Diese Abklärung ist auch bei einem FIB-4 >2,67 indiziert.
Liegt der Wert der Lebersteifigkeitsmessung (LSM) mittels VCTE („vibration-con-trolled transient elastography“; Fibro-Scan)/SWE (Scherwellen-Elastografie) bei <8kPa bzw. ein ELF-Score <7,7 vor, besteht eine niedrige Wahrscheinlichkeit für das Vorliegen einer signifikanten Fibrose. In diesem Fall ist eine Reevaluierung alle 2 Jahre empfohlen, um die Wahrscheinlichkeit einer Fibrose neu zu bewerten. Bei höheren Werten ist eine weitere Abklärung indiziert. Andere nichtinvasive Tests (NIT) können abhängig vom klinischen Kontext bzw. von Risikofaktoren wiederholt werden.
Bei Patient:innen mit kompensierter fortgeschrittener Fibrose/Zirrhose („compensated advanced chronic liver disease“; cACLD) mit einem LSM-Wert ≥10kPa sollten nichtinvasive Tests alle 12 Monate wiederholt werden, weiters ist eine hepatologische Betreuung indiziert. Für Patient:innen mit einem LSM-Wert von 8–10kPa besteht aktuell nichtgenügend Evidenz, um spezifische Intervalle zur Überwachung der Lebererkrankung zu empfehlen. Diese können jedoch abhängig vom Vorhandensein von Risikofaktoren alle 12 Monate durchgeführt werden.
Ein regelmäßiges Monitoring der hepatischen Steatose wird aktuell nicht empfohlen,da die Dynamik nicht zuverlässig durch verfügbare ultraschallbasierte Methoden abgebildet werden kann und Veränderungen desGrades der hepatischen Steatose die klinische Therapieentscheidung nicht beeinflussen.
Leberbiopsie
Eine Leberbiopsie sollte nur zum Ausschluss anderer Lebererkrankungen eingesetzt werden. Ein routinemäßiger Einsatz, insbesondere zur Abschätzung der Fibrose, wird nicht empfohlen. Auch zur Bewertung des Fibrosegrades ist eine Leberbiopsie nicht indiziert.
Lebensstilinterventionen
Ein wichtiger Bestandteil des Managements bei MASLD/MetALD ist die Gewichtsreduktion durch Lebensstilinterventionen (v.a. Ernährung, Bewegung und Verhaltenstherapie). Bei Erwachsenen mit Übergewicht/Adipositas sollte eine anhaltende Gewichtsreduktion in folgendem Ausmaß angepeilt werden:
-
≥5% zur Verbesserung der hepatischen Steatose
-
7–10% zur Verbesserung der Inflammation und
-
≥10% zur Verbesserung der Leberfibrose
Da die Verbesserung der Fibrose das entscheidende Therapieziel darstellt, sollte eine Gewichtsabnahme von ≥10% angestrebt werden. Ernährungs- und Bewegungsinterventionen werden auch bei normalgewichtigen Erwachsenen mit MASLD empfohlen, um die Steatose zu reduzieren. Allerdings gibt es derzeit keine Evidenz bezüglich der positiven Auswirkungen auf Entzündung, Fibrose oder unerwünschte leberbezogene Ergebnisse.
Zu Diät bzw. Ernährung werden im Konsensus spezifische Empfehlungen angegeben: Bei MASLD sollten den Patient:innen eine Verbesserung der Ernährung (z.B. mediterrane Ernährung) sowie die Einschränkung des Fruktosekonsums (z.B. zuckerhaltige Getränke) und stark verarbeiteter Lebensmittel nahegelegt werden. Dasselbe gilt auch für MetALD, wobei hier die Alkoholabstinenz von zentraler Bedeutung ist.
Bedeutend ist regelmäßige körperliche Aktivität in Form von sowohl Ausdauer- als auch Krafttraining im Umfang von >150min/Woche bei moderater Intensität oder >75min/Woche bei hoher Intensität, wobei die Umsetzung individuell an die Präferenzen und Fähigkeiten der Patient:innen angepasst werden sollte. Als sinnvoll werden 3 bis 5 Einheiten von je 30–60 Minuten angesehen.
Medikamentöse Therapieoptionen
Bei Patient:innen mit MASLD/MetALD und Nachweis einer signifikanten Leberfibrose (d.h. ≥8kPa) sollten die für MASH spezifischen Therapien (z.B. Resmetirom bzw. künftige zugelassene Medikamente) in Betracht gezogen werden. Bei Patient:innen mit cACLD (LSM ≥10kPa) ist aufgrund des erhöhten Risikos für unerwünschte leberbezogene Ereignisse eine medikamentöse Therapie besonders dringlich.
Resmetirom kann für Erwachsene mit einer hohen Zirrhosewahrscheinlichkeit (d.h. ≥20kPa) nicht empfohlen werden, solange keine Phase-III-Studiendaten zur Sicherheit und Wirksamkeit in dieser Patient:innengruppe vorliegen.
Inkretinbasierte Therapien sind indiziert bei Typ-2-Diabetes, zum Gewichtsmanagement bei Patient:innen mit Adipositas oder BMI ≥27kg/m2 und Begleiterkrankungen (z.B. signifikante Fibrose) und sollten bei MASLD/MetALD und Nachweis einer signifikanten Leberfibrose (d.h. ≥8kPa) eingesetzt werden, da sie kardiometabolische Ergebnisse verbessern und MASH günstig beeinflussen. Daten aus Phase-II- und Phase-III-Studien mit Tirzepatid und Semaglutid zeigen hier eine signifikante Verbesserung der MASH und der Fibrose. Ähnliche Ergebnisse wurden mit Survodutid erzielt, das zum Zeitpunkt der Konsensus-Erstellung noch nicht zugelassen war. Bei Patient:innen mit MASLD/MetALD und Nachweis einer signifikanten Leberfibrose (≥8kPa) sollten inkretinbasierte Therapien von Fachärzt:innen für Innere Medizin verordnet werden.
Aus hepatologischer Sicht ist Pioglitazon bei Patient:innen ohne Zirrhose sicher anwendbar. Allerdings kann es nicht als gezielte MASH-Therapie empfohlen werden. Ebenso ist Metformin bei MASLD/MetALD sicher anwendbar und sollte für die jeweilige Indikation (insbesondere Typ-2-Diabetes) eingesetzt werden, allerdings kann es ebenfalls nicht als gezielte MASH-Therapie empfohlen werden. Gleiches gilt für SGLT2-Hemmer, die entsprechend ihrer jeweiligen Indikation (Typ-2-Diabetes, Herzinsuffizienz, chronische Nierenerkrankung) zum Einsatz kommen. Eine Insulintherapie wird ebenfalls nicht als gezielte MASH-Therapie angesehen.
Trotz eingeschränkter Evidenz könnten Patient:innen mit MASLD/MetALD und einer Vorgeschichte von Lebertransplantation prinzipiell ähnlich behandelt werden wie Patient:innen ohne Transplantation.
Therapie bei Zirrhose
Während Metformin bei Erwachsenen mit kompensierter fortgeschrittener chronischer Lebererkrankung (cACLD) und erhaltener Nierenfunktion (GFR >30ml/min) angewendet werden kann, sollte es bei Erwachsenen mit dekompensierter Zirrhose nicht eingesetzt werden. Aufgrund des Risikos für eine Hypoglykämie sollten Sulfonylharnstoffe bei dekompensierter Zirrhose ebenfalls vermieden werden.
Inkretin-basierte Therapien können bei Erwachsenen mit Child-Pugh-Klasse-A-Zirrhose eingesetzt werden. Studiendaten bezüglich Leberfunktionsstörung bei der Anwendung von Semaglutid, Tirzepatid und Survodutid deuten darauf hin, dass pharmakokinetisch bei leichter bis schwerer Leberfunktionsstörung (Child-Pugh-Klasse A–C) keine Anpassung der Dosis erforderlich ist, obwohl aufgrund des Sarkopenierisikos besondere Vorsicht geboten ist. Begrenzte klinische Erfahrungen zeigen, dass inkretinbasierte Therapien möglicherweise zur Gewichtsregulation bei Patient:innen auf der Warteliste für eine Lebertransplantation eingesetzt werden können, allerdings ist auch bei ihnen aufgrund des Sarkopenierisikos besondere Vorsicht geboten. SGLT2-Inhibitoren sind bei Child-Pugh-Klasse-A- und -B-Zirrhose sicher anwendbar.
Der Einsatz von Statinen sollte bei cACLD/Zirrhose entsprechend den spezifischen Leitlinien erfolgen, um kardiovaskuläre Ereignisse zu reduzieren. Bei Patient:innen mit Child-Pugh B/C können sie in niedrigerer Dosierung eingesetzt werden (z.B. Simvastatin maximal 20mg pro Tag oder Atorvastatin 10mg pro Tag), wobei sorgfältig hinsichtlich Muskel- (Rhabdomyolyse) und Lebertoxizität überwacht werden sollte. Falls eine klinisch signifikante portale Hypertension (CSPH) vorliegt, soll Carvedilol eingesetzt werden, sofern keine Kontraindikation vorliegt.
Monitoring auf HCC
Die Maßnahmen zur Früherkennung eines hepatozellulären Karzinoms (HCC) sollten gemäß den entsprechenden Leitlinien erfolgen und unterscheiden sich nicht von jenen bei anderen chronischen Lebererkrankungen. Das HCC-Monitoring mittels Ultraschall und Alpha-Fetoprotein-Bestimmung ist bei Patient:innen mit SLD-assoziierter Zirrhose indiziert. Ein LSM-Wert von ≥15kPa kann als nichtinvasiver Cut-off-Wert herangezogen werden (Abb.2). Obwohl möglicherweise eine höhere HCC-Inzidenz bei Patient:innen mit MASLD und fortgeschrittener Fibrose besteht, wird aktuell ein HCC-Monitoring bei Patient:innen ohne Zirrhose nicht empfohlen, da dies aufgrund der Kosteneffizienz derzeit nicht gerechtfertigt erscheint.
Zusammenfassung
Für die Diagnose einer MASLD muss die hepatische Steatose per Bildgebung bzw. Histologie bestätigt sein und mindestens einkardiometabolischer Risikofaktor vorliegen. Besteht ein Alkoholkonsum von 30–60g/Tag (Männer) bzw. 20–50g/Tag (Frauen), liegt die Zwischenform zur ALD vor, die MetALD. Patient:innen mit einem höheren Alkoholkonsum werden der ALD zugeordnet. Andere Ursachen einer Steatose wie arzneimittelinduzierte Leberschäden, genetische oder virale Erkrankungen sollten differenzialdiagnostisch ausgeschlossen werden.
Nach der MASLD/MetALD-Diagnose erfolgt die Risikostratifizierung per FIB-4-Test. Liegt der Wert unter 1,3, sollte das Fibroserisiko alle zwei Jahre mittels wiederholten FIB-4-Tests kontrolliert werden. Bei einem FIB-4 zwischen 1,3 und 2,67 sollte ein intensiviertes Management der Komorbiditäten für 6–12 Monate oder eine Elastografie erfolgen. Liegt der Wert >2,67, soll eine hepatologische Anbindung erfolgen. Liegt in der weiteren Abklärung der LSM-Wert <8kPa, wird wie bei Niedrigrisiko vorgegangen, bei einem Wert ≥8kPa werden MASH-spezifische Therapien empfohlen. Eine Leberbiopsie sollte nur zum Ausschluss anderer Lebererkrankungen eingesetzt werden.
Zu den Lebensstilinterventionen bei MASLD/MetALD zählen Gewichtsverlust, Ernährungsumstellung und körperliche Aktivität. Eine Zulassung für MASH-spezifische medikamentöse Therapien liegt in Europa gegenwärtig nicht vor. Anhand der vorhandenen Studiendaten wird eine MASH-spezifische Behandlung mit Resmetirom für Patient:innen mit signifikanter Fibrose empfohlen. Ebenso belegen Studiendaten von Inkretin-basierten Therapien bei MASLD/MetALD und signifikanter Fibrose signifikante Verbesserungen der MASH und der Fibrose. Bei Vorliegen einer Zirrhose ist die Überwachung in Bezug auf HCC (Ultraschall und Alpha-Fetoprotein) angezeigt.
Quelle:
„ÖGGH/ÖDG/ÖAG-Konsens zur MASLD/MASH“; Vortrag von Ap. Prof. Priv.-Doz. DDr. Mattias Mandorfer und DDr. Georg Semmler, Wien, im Rahmen der 58. ÖGGH-Jahrestagung in Wels am 13.Juni 2025
Literatur:
1 Mandorfer M, Semmler G et al.: Austrian multisociety consensus on metabolic dysfunction-associated steatotic liver disease. Wien Klin Wochenschr 2025; 137 (10): 307-31 2 Tacke F et al.: EASL–EASD–EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). J Hepatol 2024; 81(3): 492-542
Das könnte Sie auch interessieren:
Lege artis vs. klinische Realität: präemptiver TIPS
Die Implantation eines präemptiven transjugulären intrahepatischen portosystemischen Shunts (TIPS) ist eine hocheffektive Therapie, die die Reblutungsrate reduziert und das Überleben ...
UEGW 2025: Neues aus der Hepatologie
In der Indikation metabolisch bedingte Lebersteatose bzw. Steatohepatitis scheiterten über viele Jahre zahlreiche Therapieversuche. Seit Kurzem stehen erstmals wirksame und zugelassene ...
Lebersteatose und Fibrose: unerwartete Prävalenzverteilungen und Aussagekraft moderner Diagnostik
Eine aktuelle österreichische Studie untersuchte die Prävalenz von hepatischer Steatose und Fibrose in fünf österreichischen Versorgungseinheiten. Zudem wurden in diesem Zusammenhang ...