Können kontinuierliche Glukosemesssysteme das HbA1c ersetzen?
Autor:
Dr. Paul Fellinger
Univ.-Klinik für Innere Medizin III
Abteilung für Endokrinologie und Stoffwechsel Medizinische Universität Wien
E-Mail: paul.fellinger@meduniwien.ac.at
Seit den letzten Jahren spielen kontinuierliche Glukosemesssysteme (CGM) eine immer bedeutendere Rolle. CGM-basierte Parameter lassen uns teils sehr genaue Rückschlüsse auf die Blutzuckerkontrolle ziehen. Neue Studien liefern jedoch Hinweise auf mögliche Probleme bei der Verwendung von GMI als „Ersatz“ für HbA1c.
Keypoints
-
GMI schätzt die glykämische Kontrolle tendenziell als „besser“ ein, als das HbA1c ist. Dies gilt insbesondere bei schlechter glykämischen Kontrolle.
-
Die Anwendbarkeit von GMI bei Typ-2-Diabetes und bei unterschiedlichen Sensortypen ist unklar.
-
Die Kombination aus Parametern wie z.B. der Time in Range, aber auch anderen Parametern, die CGM-Systeme bieten, und dem HbA1c ist optimal, um die glykämische Kontrolle einzuschätzen.
Durch das regelmäßige Messen von Blutzuckerwerten aus dem Unterhautfettgewebe mithilfe von CGM-Geräten können heutzutage wesentlich genauere Blutzuckerprofile erstellt werden als früher und das blutige Messen mit Nadelstiches konnte deutlich reduziert werden. Durch die damit unter anderem deutlich verbesserte Lebensqualität im Umgang mit Diabetes wurden CGM-Systeme in letzter Zeit zur neuen Standardmethode des Blutzuckermessens.1 Grundsätzlich unterscheidet man zwischen zwei unterschiedlichen Messsystemen: dem „intermittent scanning CGM (isCGM)“, welches alle paar Minuten den Blutzuckerspiegel bestimmt, und dem „real-time CGM (rtCGM)“, welches alle paar Sekunden und in Echtzeit die Blutzuckerwerte an das Endgerät liefert.
Messparameter zur Einschätzung der glykämischen Kontrolle
Sowohl für Patienten mit Diabetes wie auch für behandelnde Ärzte erleichtert ein genaues Blutzuckerprofil die Einschätzung der glykämischen Kontrolle wesentlich. Insbesondere neue Parameter, welche nun aus den genauen Blutzuckerprofilen ableitbar wurden, helfen bei dieser Einschätzung sehr. Um die CGM-basierten Parameter zu errechnen, werden meist die Blutzuckerwerte der letzten 14 Tage verwendet. Wichtige Parameter sind dabei etwa die Zeit im Zielbereich („Time in Range“; TiR), die Zeit über dem Zielbereich („Time above Range“; TaR), die Zeit unter dem Zielbereich („Time below Range“; TbR) und die Glukosevariabilität (CV). Außerdem wurde eine Formel entwickelt, um aus den durchschnittlichen kontinuierlichen Glukosemessungen ein Äquivalent für den HbA1c-Wert, den derzeitigen Goldstandard zur Bestimmung der glykämischen Kontrolle, zu errechnen. Dies ist der sogenannte „Glucose Management Indicator“ (GMI).2 Insbesondere bei der telemedizinischen Betreuung muss mangels HbA1c-Bestimmung auf die CGM-basierten Parameter zurückgegriffen werden, sofern diese verfügbar sind. Diese Methode zur Betreuung der Patienten erlangte in den letzten eineinhalb Jahren aufgrund der Covid-Pandemie einen immer höheren Stellenwert im klinischen Alltag. Dabei spielt auch der Parameter GMI eine zunehmend bedeutende Rolle für Patienten wie auch für behandelnde Ärzte, um die empfohlenen Zielwerte zu erreichen und die Therapie dahingehend anzupassen. Ob aber der GMI verlässlich als Ersatz für den HbA1c-Wert verwendet werden kann, wurde bisher nur in wenigen Studien mit einem breiten Patientenkollektiv analysiert.3
Im Mittel gute Korrelation von HbA1c und GMI
Im Rahmen der diesjährigen Jahrestagung der Europäischen Diabetesgesellschaft (EASD) konnten wir nun ein Abstract über eine Arbeit aus unserer Arbeitsgruppe aus dem AKH Wien vorstellen, in der wir versuchten, die Verlässlichkeit von GMI zu ergründen.
Dabei untersuchten wir, inwiefern die gemessenen HbA1c-Werte der von uns in der Diabetesambulanz betreuten Patienten mit den errechneten GMI-Werten kongruieren. Wir verglichen nicht nur die CGM-Parameter, welche sich anhand der letzten 14 Tage vor der HbA1c-Messung berechneten, sondern berechneten auch den GMI vor der HbA1c-Messung aus den Daten über 30 Tage. In Summe konnten wir dabei Daten von 170 Patientinnen und Patienten auswerten. Die meisten davon hatten Typ-1-Diabetes (66,5%) und verwendeten den Sensor von Freestyle Libre (98%). Der mittlere HbA1c -Wert war dabei 7,53%, wobei 5,1% der niedrigste und 12,1% der höchste war. Im Vergleich dazu war der mittlere GMI-Wert, der anhand von Daten aus den letzten 14 Tagen berechnet wurde, 7,19% und quasi ident mit dem GMI-Wert, welcher aus den letzten 30 Tagen berechnet wurde (7,21%). Wie zu erwarten war, korrelierten dabei GMI und HbA1c-Wert signifikant miteinander (R2=0,82, p<0,01). Eine Verlängerung des Zeitraums von 14 auf 30 Tage ergab, dass die Werte noch etwas besser korrelierten, wobei der Unterschied jedoch nicht sehr groß war (R2=0,85; p<0,01).
Bei hohem und niedrigem HbA1c relevante Abweichungen zwischen HbA1c und GMI
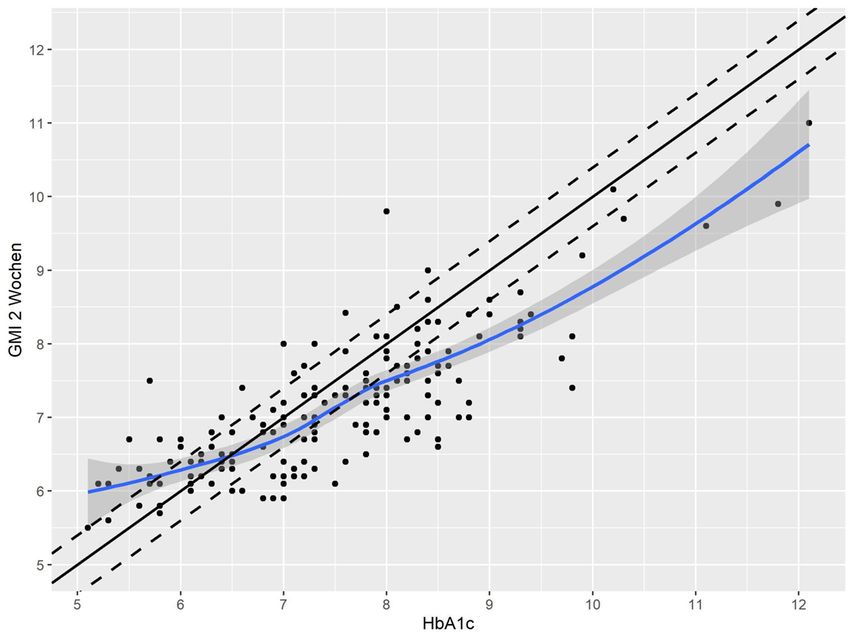
Bei der Analyse, inwiefern GMI und HbA1c-Wert bei den einzelnen Patienten voneinander abweichen, konnten wir allerdings doch teils große Unterschiede erkennen. Im Mittel gab es dabei eine Abweichung zwischen dem HbA1c-Wert und dem GMI von 0,63% mit einer minimalen Abweichung von 0% und einer maximalen von 2,4%. Um die Unterschiede zwischen den einzelnen Messungen deutlicher sichtbar zu machen, stellten wir, wie in Abbildung 1 gezeigt, GMI und HbA1c-Werte mittels Streudiagramm dar und berechneten eine lokal gewichtete Regressionsfunktion (Loess). Da eine Abweichung von ungefähr 0,4% oft eine therapeutische Konsequenz nach sich zieht, legten wir diese Abweichung als signifikante Abweichung fest. In dieser grafischen Gegenüberstellung sieht man, dass diese GMI-Regressionsfunktion nur in einem schmalen Bereich dem HbA1c-Wert entspricht.
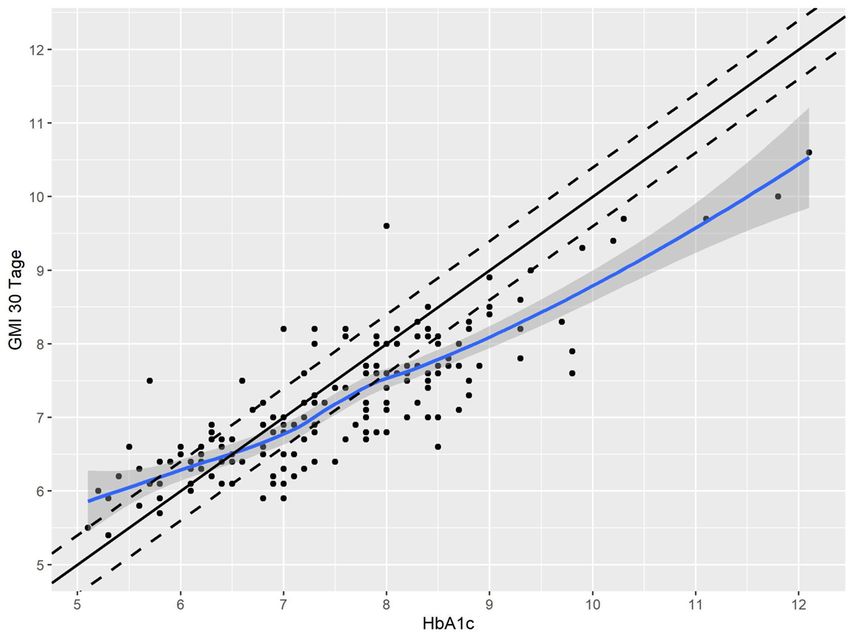
Der Bereich, in dem GMI weniger als 0,4% von der HbA1c-Messung abweicht, entspricht anhand unserer Daten einer relativ guten Blutzuckereinstellung. Dabei scheint es so zu sein, dass die Berechnung von GMI aus den mittleren Glukosewerten die glykämische Kontrolle als tendenziell besser einschätzt, als mittels HbA1c bestimmt wird. Übersteigt der GMI einen Wert von ca. 7,5%, erkennt man, dass die Abweichung zwischen GMI und HbA1c mehr als 0,4% beträgt, auch unter Berücksichtigung des 95%-Konfidenzintervalls. Dieser im Vergleich mit dem HbA1c falsch niedrige Wert bleibt bei zunehmend schlechter glykämischer Kontrolle bestehen. Bei Patienten mit sehr niedrigem HbA1c scheint es wiederum so zu sein, dass die Verwendung von GMI die glykämische Kontrolle als schlechter einschätzt, als sie tatsächlich ist. Da jedoch nur wenige Patienten in diesem Kollektiv in diesen Bereich mit sehr niedrigem HbA1c fielen, ist es schwierig, darüber eine fundierte Aussage zu treffen. Wie der Vergleich der Abbildungen 1 und 2 zeigt, sind diese Abweichungen ähnlich, egal ob man für die Berechnung des GMI Daten von 14 Tagen oder 30 Tage verwendet.
Abb. 1: 14-Tage-Streudiagramm von GMI und HbA1c-Werten und lokal gewichtete Regressionsfunktion (Loess)
Abb. 2: 30-Tage-Streudiagramm von GMI und HbA1c-Werten und lokal gewichtete Regressionsfunktion (Loess)
Eine rezent veröffentlichte Studie kam zu einem ähnlichen Ergebnis und beschrieb dabei ebenfalls teils deutliche Abweichungen.3 Auch in dieser Studie nahmen die Abweichungen zwischen GMI und HbA1c zu, je schlechter die glykämische Kontrolle war.
Welche Faktoren diese oft klinisch relevanten Abweichungen beeinflussen, ist noch nicht vollends geklärt.
Verbesserungsmöglichkeiten und Typ-2-Diabetes
Grundsätzlich wurden die meisten CGM-basierten Parameter anhand von rtCGM bei Patienten mit Typ-1-Diabetes entwickelt. Daten, inwiefern diese Parameter bei Patienten mit Typ-2-Diabetes ähnlich sind, fehlen derzeit noch. In unserem Kollektiv verwendeten die meisten PatientInnen isCGM-Systeme, wobei sich die Messungenauigkeit zwischen den unterschiedlichen Systemen jedoch nicht grundlegend unterscheidet.4 Faktoren, die Einfluss auf die Lebensdauer der Erythrozyten beziehungsweise die Hämatopoese haben, wie Anämie, chronische Nierenfunktionsstörung oder Hämoglobinopathien, beeinträchtigen häufig die Beurteilbarkeit des HbA1c. Diese Faktoren tragen insofern auch häufig zu größeren Unterschieden zwischen GMI und HbA1c bei.3 Um diese Einflüsse zu korrigieren, gibt es Ansätze, mittels HbA1c-Messungen und CGM-Daten individuelle kinetische Modelle für den Umsatz von Erythrozyten zu bestimmen, um in weiterer Folge mittels eines kinetischen Modells das HbA1c zu berechnen.5 Inwiefern unterschiedliche Arten von Diabetes einen Einfluss haben könnten und ob die entwickelte Formel für GMI auch bei unterschiedlichen Sensortypen gleich gut anwendbar ist, ist derzeit noch nicht vollends in größeren Kollektiven geklärt worden.
Praxistipp
Die alleinige Anwendung des GMI ist kein verlässliches Instrument zur Steuerung der Therapie bei Menschen mit Diabetes, die CGM-Systeme benützen.Zusammenfassend kann man nach derzeitigem Wissen sagen, dass die routinemäßige Verwendung von GMI als Ersatz für HbA1c aufgrund der oft klinisch signifikanten Abweichungen insbesondere bei PatientInnen mit schlechter glykämischer Kontrolle nur in eingeschränktem Rahmen stattfinden sollte. Eine kombinierte Verwendung der CGM-basierten Parameter, insbesondere TiR, TbR, TaR, und CV gemeinsam mit HbA1c, erlauben einen wesentlich genaueren Blick auf individuelle Unterschiede und damit eine noch präzisere Möglichkeit, Blutzuckertherapien individuell anzupassen.
Literatur:
1 Charleer S et al.: Quality of life and glucose control after 1 year of nationwide reimbursement of intermittently scanned continuous glucose monitoring in adults living with type 1 diabetes (FUTURE): A prospective observational real-world cohort study. Diabetes Care 2020; 43: 389-97 2 Bergenstal RM et al.: Glucose management indicator (GMI): A new term for estimating A1C from continuous glucose monitoring. Diabetes Care 2018; 41: 2275-80 3 Perlman JE et al.: HbA1c and glucose management indicator discordance: a real-world analysis. Diabetes Technology & Therapeutics 2021; 23: 253-8 4 Pleus S et al.: Time in specific glucose ranges, glucose management indicator, and glycemic variability: impact of continuous glucose monitoring (CGM) system model and sensor on CGM metrics. J Diabetes Sci Technol June 2020: 1932296820931825 5 Xu Y et al.: Personal glycation factors and calculated hemoglobin a1c for diabetes management: real-world data from the diabetes prospective follow-up (DPV) registry. Diabetes Technology & Therapeutics 2021; 23: 452-9
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Notfall Diabetische Ketoazidose: Leitliniengerechtes Handeln kann Leben retten
Akute Stoffwechselentgleisungen können lebensbedrohlich sein und erfordern eine rasche und leitliniengerechte Diagnostik und Therapie. Pathogenese, Klinik, typische Befunde und die ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...