Diabetes bei zystischer Fibrose in Zeiten moderner Modulatortherapie
Autor:
OA Dr. Thomas Hörtenhuber
Universitätsklinik für Kinder- & Jugendheilkunde, Johannes Kepler Universität, Linz
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Zystische Fibrose (CF) ist eine der häufigsten monogenetischen Erkrankungen in Europa. Sie ist durch eine chronisch progressive Lungenerkrankung gekennzeichnet. Bisher sorgte man sich hier um die Malnutrition, nun rückt jedoch vermehrt der Diabetes mellitus in den Fokus.
Keypoints
-
Diabetes mellitus ist die häufigste Komorbidität bei CF, die 50% aller Betroffenen im Alter von 30 Jahren betrifft.
-
Die glykämische Kontrolle ist eng verknüpft mit der Lungenfunktion und der Mortalität.
-
Ein regelmäßiges jährliches Screening mit oralem Glukosetoleranztest ist ab dem zehnten Lebensjahr empfohlen.
-
Der HbA1c-Wert ist explizit kein brauchbares Screeningtool.
-
Übergewicht und Adipositas werden in Zukunft auch bei Menschen mit CF eine Rolle spielen.
Diabetes mellitus ist neben der primären Lungenproblematik und der exokrinen Pankreasinsuffizienz die häufigste Komorbidität bei Menschen mit zystischer Fibrose. Diese Form wird auch als eigene Unterform klassifiziert: „CF-related diabetes“ (CFRD). Sie unterscheidet sich von anderen Diabetesformen stark, da bei Menschen mit CF die glykämische Kontrolle mittelbare Auswirkungen auf Lungenfunktion und Mortalität hat.
Moderne Modulatortherapie – der „Gamechanger“ bei CF
Mit der Einführung der modernen Modulatortherapie „highly effective modulator therapy“ (HEMT), die direkt die Funktion des betroffenen Chloridkanals deutlich verbessert, hat sich der klinische Verlauf von CF merklich verändert. Die Triple-Therapie mit Elexacaftor, Tezacaftor und Ivacaftor, die seit 2020 in Europa zugelassen ist, zeigt signifikante Vorteile für Menschen mit CF. Sie führt zu einer Verbesserung der Lungenfunktion auch im fortgeschrittenen Erkrankungsstadium, einer Steigerung des Body-Mass-Index (BMI) sowie einer Reduktion von pulmonalen Exazerbationen.1
2021 wies das US-CF-Register erstmalig eine Verbesserung der Lungenfunktion für alle Altersgruppen aus. Die Zahl der CF-assoziierten Lungentransplantationen ist auch seit 2020 deutlich rückläufig.2 Vor der Einführung der HEMT lag die durchschnittliche Lebenserwartung bei rund 40 Jahren. Eine aktuelle Studie aus Großbritannien prognostiziert mit der modernen HEMT einen Anstieg der Lebenserwartung auf über 70 Jahre.3 Dies bedeutet auch, dass die klassischen Langzeitkomplikationen eines Diabetes in Zukunft zunehmend an Bedeutung gewinnen.
Prognose und Verlauf von CFRD
Studien belegen, dass Kinder mit CF bereits im Kleinkindalter eine veränderte glykämische Kontrolle aufweisen, die sich in erhöhten Glukoseserumwerten im Vergleich zu gesunden Kontrollen zeigt.4 Auch bei Erwachsenen mit CF und normaler Glukosetoleranz wurden erhöhte Glukoseserumwerte sowie eine verminderte bzw. verzögerte Insulinausschüttung im Vergleich zu gesunden Personen festgestellt.5
Im Verlauf entwickeln ca. 20% der Jugendlichen und jungen Erwachsenen mit CF einen Diabetes, während bei Betroffenen über 30 Jahre die Prävalenz bei 50% liegt. Besonders in der Altersgruppe zwischen 30 und 40 Jahren sind Frauen mit einer Prävalenz von 60% deutlich häufiger betroffen.6 Aufgrund der historisch geringeren Lebenserwartung von Menschen mit CF liegen kaum Daten zu Langzeitkomplikationen bei CFRD vor. Eine Studie von 2007 zeigt aber bei CFRD mikrovaskuläre Komplikationen zu einem ähnlichen Prozentsatz wie bei Menschen mit Typ-1- oder Typ-2-Diabetes. Zu makrovaskulären Komplikationen liegen bislang keine soliden Daten vor.7
Screening auf CFRD
Aufgrund des engen Zusammenhangs zwischen glykämischer Kontrolle und klinischem Verlauf (Lungenfunktion, Mortalität) ist eine Früherkennung eines CFRD besonders wichtig. Entsprechend den aktuellen Leitlinien der American Diabetes Association (ADA) und der International Society for Pediatric and Adolescent Diabetes (ISPAD) ist der Goldstandard für das CFRD-Screening ein jährlicher oraler Glukosetoleranztest (oGTT).8
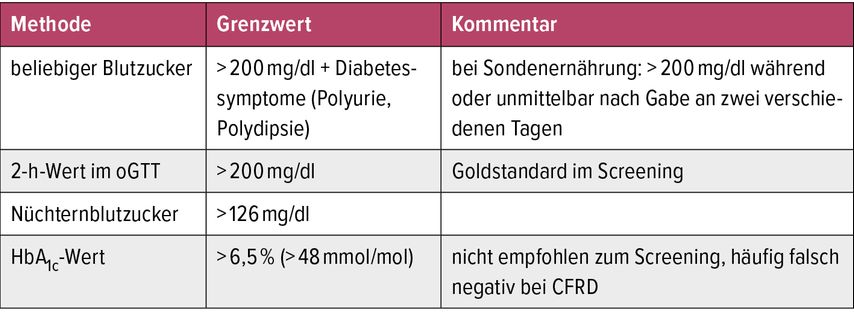
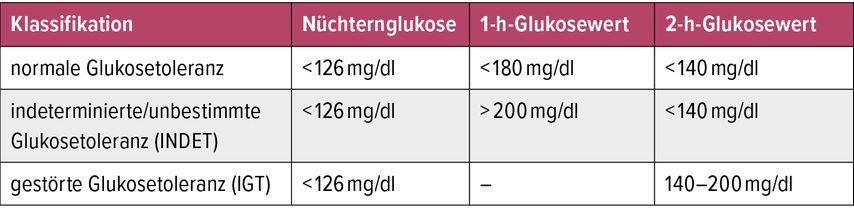
Es gelten die gleichen diagnostischen Grenzwerte wie bei allen Diabetesformen, wobei zusätzlich ein 1-Stunden-Wert von >200mg/dl als unbestimmte Glukosetoleranz – „indeterminate glucose tolerance“ (INDET) – definiert wird. Dieser Grenzwert geht mit einem sehr hohen Risiko für Progression zum CFRD einher (Tab.1 u.2)8. Zu beachten ist, dass der HbA1c-Wert für ein CFRD-Screening nicht empfohlen wird, da zwei Drittel der Patienten mit CFRD einen normalen HbA1c-Wert aufweisen.9 Ein Screening mittels kontinuierlicher Glukosemessung (CGM) wird von einigen Zentren bereits durchgeführt, es existiert allerdings noch kein internationaler Konsensus über die diagnostischen Grenzwerte.9
Tab. 1: Verschiedene Screeningmethoden für Diabetes bei Patient:innen mit zystischer Fibrose (modifiziert nach Ode KL et al. 2022)8
Tab. 2: Einteilung der Glukosetoleranz bei Patient:innen mit zystischer Fibrose mittels oralen Glukosetests (modifiziert nach Ode KL et al. 2022)8
Insulinspiegel bei Modulatortherapie
Erste Studien zeigen einen tendenziell positiven Einfluss auf die Insulinsekretion und glykämische Kontrolle nach Beginn einer HEMT bei CFRD. Größere Studien mit längerfristigen Daten fehlen allerdings noch. Mehrere Studien konnten ein Absinken des HbA1c-Wertes nach Beginn einer HEMT zeigen, was teilweise auch mit einer reduzierten Insulindosis einherging. Die CGM-Daten weisen jedoch uneinheitliche Ergebnisse auf. Während einige Studien eine Verbesserung zeigen, berichten andere von keinem signifikanten Effekt.10,11
Langzeitdaten zu den Auswirkungen eines frühen HEMT-Starts in der Kindheit und dem möglichen Einfluss auf eine verbesserte Betazellfunktion bzw. geringere oder spätere Diabetesmanifestation fehlen.
Therapie
Primär wird der CFRD mit Insulin behandelt, wobei hier von einer einfachen basal unterstützten oralen Therapie (BOT) über eine volle funktionelle Insulintherapie bis hin zur Insulinpumpe bzw. automatischen Insulindosierung (AID) sämtliche Therapieformen Einsatz finden. Seit der Verwendung von CGM zeigt sich, dass die Patienten vor allem postprandial deutliche Hyperglykämien haben und daher eine reine BOT oft nicht zielführend ist. Entsprechend dem generellen Trend in der modernen Diabetestherapie nimmt auch bei Patienten mit CFRD die Verwendung von Insulinpumpen bzw. AID-Systemen zu. Neben einer Verbesserung der glykämischen Kontrolle konnte eine Verbesserung der Körperzusammensetzung im Vergleich zur Insulinpentherapie (MDI) nachgewiesen werden.12
Eine Therapie mit anderen Antidiabetika wird bei CFRD aktuell nicht empfohlen. Allerdings rückt insbesondere die Substanzklasse der „Glucagon-like peptide-1“-Rezeptor-Agonisten (GLP-1-RA) zunehmend in den Fokus: Menschen mit CF haben niedrigere GLP-1-Spiegel. Zudem führt die Gabe von GLP-1-RA zu einem Anstieg der Insulinausschüttung in der zweiten Phase. Im Gegensatz dazu führt die Gabe des anderenInkretinhormons „glucose-dependent insulinotropic polypeptide“ (GIP) – anders als bei Typ-2-Diabetes – zu keinem Effekt.13 Aufgrund dieser Veränderungen stellen Inkretinanaloga eine interessante Therapiemöglichkeit dar, vor allem auch wegen der steigenden Adipositasrate bei Menschen mit CF.
Neues Problem – Adipositas bei CF
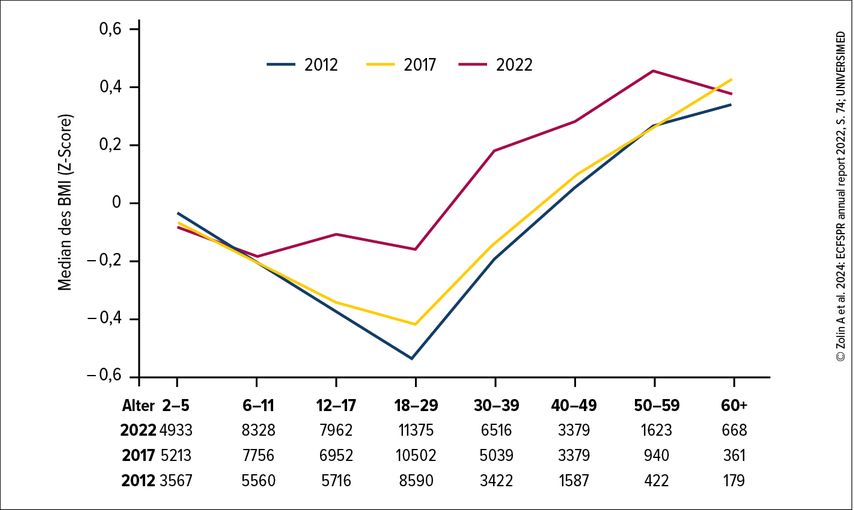
Die Therapieerfolge durch die HEMT verschieben zunehmend die Prioritäten bei der Betreuung von Menschen mit CF: Einerseits werden in Zukunft auch die mikro- und makrovaskulären Komplikationen eines Diabetes aufgrund der höheren Lebenserwartung eine Rolle spielen. Andererseits müssen auch etablierte Therapiekonzepte neu bewertet werden. So wurde bislang ab der Diagnosestellung im Säuglingsalter auf eine hochkalorische Diät geachtet, um Malnutrition entgegenzuwirken. Hier zeigt sich in den letzten Jahren in allen großen Registern ein deutlicher Rückgang der Untergewichtsrate. Gleichzeitig ist eine Zunahme von Übergewicht und sogar dem Auftreten von Adipositas bei Menschen mit CF zu verzeichnen. Laut aktuellen US-Registerdaten sind 17% der Betroffenen übergewichtig und 6% weisen eine Adipositas auf. Das europäische Register bestätigt diesen Trend mit einem deutlichen Anstieg des Durchschnittsgewichts, allerdings ist in der letzten Auswertung 2022 kein nennenswerter Anstieg der Adipositas sichtbar (Abb. 1).14
Abb. 1: Median des BMI (Z-Score) in Abhängigkeit vom Alter von europäischen Patient:innen mit CF: Seit der Einführung der Modulatortherapie verbesserten sich die BMI-Werte erheblich. Die Gefahr der Malnutrition weicht nun langsam dem Risiko der Adipositas (modifiziert nach Zolin A et al. 2024)14
Die Adipositas stellt bei CF eine völlig neue Problematik dar, vor allem vor dem Hintergrund eines bestehenden (progressiven) Insulinmangels. Zusätzlich zu der verminderten und verzögerten Insulinsekretion konnte auch eine verminderteGLP-1-Antwort gezeigt werden. Diese liegt bei allen Menschen mit CF vor und korreliert mit dem Ausmaß der Glukosetoleranz.15
Angesichts des bereits beschriebenen GLP-1-Mangels bei CF stellen hier natürlich GLP-1-RA eine naheliegende Therapieoption dar. Hierzu liegen noch keine randomisierten Studien vor. Eine Fallserie mit 11 übergewichtigen Patienten mit CFRD zeigte jedoch gute Therapieerfolge mit Gewichtsverlust, reduziertem Insulinbedarf und teils sogar verbesserter Lungenfunktion.16 Weitere und vor allem größere multizentrische Studien sind notwendig, um die Sicherheit und Effektivität dieser Substanzgruppe bei Menschen mit CFRD zu erfassen.
Literatur:
1 Burgener EB, Cornfield DN: Delivering a new future for people with cystic fibrosis. Pediatrics 2023; 152(4): e2023062985 2 Cystic Fibrosis Foundation: 2021 patient registry annual data report. https://www.cff.org/sites/default/files/2021-11/Patient-Registry-Annual-Data-Report.pdf; zuletzt aufgerufen am 7.2.2025 3 Lopez A et al.: Elexacaftor/Tezacaftor/Ivacaftor projected survival and long-term health outcomes in people with cystic fibrosis homozygous for F508del. J Cyst Fibros 2023; 22(4): 607-14 4 Yi Y et al.: Abnormal glucose tolerance in infants and young children with cystic fibrosis. Am J Respir Crit Care Med 2016; 194(8): 974-80 5 Nyirjesy SC et al.: β-cell secretory defects are present in pancreatic insufficient cystic fibrosis with 1-hour oral glucose tolerance test glucose ≥155mg/dL. Pediatr Diabetes 2018; 19(7): 1173-82 6 Moran A et al.: Cystic fibrosis-related diabetes: current trends in prevalence, incidence, and mortality.Diabetes Care2009; 32 (9): 1626-31 7 Schwarzenberg SJ et al.: Microvascular complications in cystic fibrosis-related diabetes. Diabetes Care 2007; 30(5): 1056-61 8 Ode KL et al.: Management of cystic fibrosis-related diabetes in children and adolescents. Pediatr Diabetes 2022; 23(8): 1212-28 9 Costa M et al.: Increased glucose excursion in cystic fibrosis and its association with a worse clinical status.J Cyst Fibros 2007; 6(6): 376-83 10 Park J et al.: Improvements in glucose regulation in children and young people with cystic fibrosis-related diabetes following initiation of Elexacaftor/Tezacaftor/Ivacaftor. Horm Res Paediatr 2024; 97(1): 94-8 11 Petersen MC et al.: Effect of Elexacaftor-Tezacaftor-Ivacaftor on body weight and metabolic parameters in adults with cystic fibrosis. J Cyst Fibros 2022; 21(2): 265-71 12 Grancini V et al.: Effects of insulin therapy optimization with sensor augmented pumps on glycemic control and body composition in people with cystic fibrosis-related diabetes. Front Endocrinol (Lausanne) 2023; 14: 1228153 13 Nyirjesy SC et al.: Effects of GLP-1 and GIP on islet function in glucose-intolerant, pancreatic-insufficient cystic fibrosis. Diabetes 2022; 71(10): 2153-65 14 Zolin A et al.: ECFSPR annual report 2022. Karup 2024; 1-182 15 Sheikh S et al.: Reduced β-cell secretory capacity in pancreatic-insufficient, but not pancreatic-sufficient, cystic fibrosis despite normal glucose tolerance. Diabetes 2017; 66(1): 134-44 16 Park S et al.: Glucagon-like-peptide-1 agonist therapy in adults with cystic fibrosis. J Cyst Fibros 2024; 24(1): 40-6
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Notfall Diabetische Ketoazidose: Leitliniengerechtes Handeln kann Leben retten
Akute Stoffwechselentgleisungen können lebensbedrohlich sein und erfordern eine rasche und leitliniengerechte Diagnostik und Therapie. Pathogenese, Klinik, typische Befunde und die ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...