Diabetes mellitus im Kindes- und Jugendalter
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
An Diabetes im Kindesalter denken – in den letzten zwei Dekaden hat die Manifestation von Diabetes im Kindesalter deutlich zugenommen. Immer mehr schulpflichtige Kinder und Jugendliche sind von dieser chronischen Stoffwechselerkrankung betroffen.
Um eine entsprechende Unterstützung dieser Kinder im Umfeld Schule sicherzustellen, soll dieses Fortbildungsmodul für Schulärzte ein Update über die aktuellen Behandlungsmöglichkeiten und Behandlungsziele bei Kindern mit Diabetes liefern.
Klassifikation und Epidemiologie
Die derzeit gültige Diabetesklassifikation (ADA 2018) teilt die verschiedenen Diabetesformen in Typ I–IV ein. Im Kindes- und Jugendalter tritt zu >95% ein Diabetes mellitus Typ 1 (T1D) auf, der aufgrund des Insulinmangels rasch zu einer diabetischen Ketoazidose führen kann. Die Erstmanifestation eines T1D kann in jedem Kindes- und Jugendalter auftreten, auch im Säuglingsalter, der Erkrankungsgipfel liegt im Volksschulalter, es sind aber zunehmend immer jüngere Kinder betroffen. Weitere im Kindes- und Jugendalter vorkommende Diabetesformen sind Diabetes mellitus Typ 2 (T2D), spezifische Diabetes-mellitus-Typen (z.B. MODY, CFrelated Diabetes, Diabetes nach Transplantation, bei Kortison-Therapie) sowie Diabetes assoziiert bei verschiedenen Syndromen (z.B. Trisomie 21, Prader-Willi-Syndrom u.a.). Der T1D ist die häufigste Stoffwechsel erkrankung im Kindes- und Jugendalter. Die Inzidenz der Erkrankung bei Kindern und Jugendlichen unter 15 Jahren nimmt auch in Österreich – sowie weltweit – kontinuierlich zu. Die aktuellsten Daten des österreichischen Diabetes-Inzidenz-Registers zeigten im Jahr 2015 in der Altersgruppe der 0- bis 14-Jährigen 237 neu diagnostizierte Typ-1- sowie vier Typ-2-Diabetesfälle. Dies entspricht einer Inzidenzrate von 19,2 bzw. 0,3 Kindern pro 100 000 pro Jahr in dieser Altersgruppe. Im Beobachtungszeitraum 1999 bis 2015 gab es Schwankungen der Typ-1-Diabetes-Inzidenzrate bei Kindern mit einer jährlichen Zuwachsrate von 3,6%. Die Inzidenzrate des Typ-2-Diabetes ist weiterhin konstant niedrig und zeigt keinen Anstieg in dieser Altersgruppe.
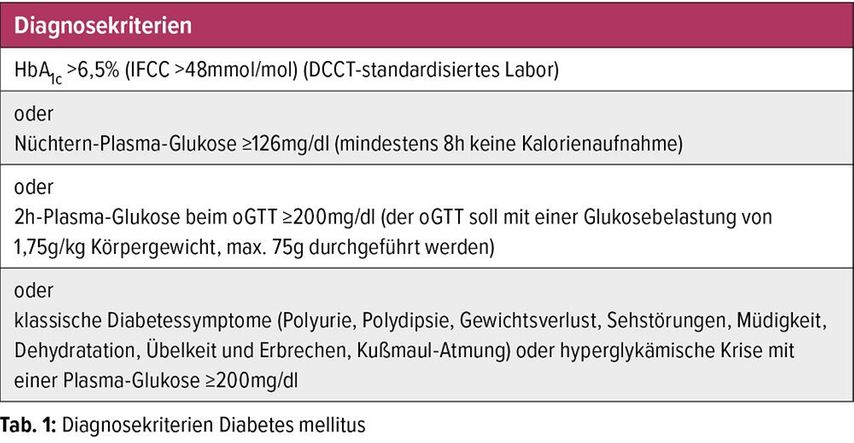
Diagnose
Die Diagnose eines T1D im Kindesalter wird meist anhand der typischen Symptome (Polyurie, Polydipsie, Gewichtsverlust, Sehstörungen, Müdigkeit, Dehydratation, nächtliches Einnässen [Enuresis nocturna], Übelkeit und Erbrechen, Kussmaul- Atmung), einer Harnuntersuchung, der Blutzucker- und HbA1c-Bestimmung gestellt. Es gelten in der Pädiatrie dieselben Diagnosekriterien wie bei Erwachsenen, lediglich die Glukosebelastung beim oralen Glukosetoleranztest (oGTT) ist gewichtsbedingt unterschiedlich. Ein oGTT ist bei Kindern und Jugendlichen mit T1D nur selten notwendig, spielt aber bei der Diagnose seltenerer Diabetesformen (z.B. T2D, MODY, CF-related Diabetes) eine wichtige Rolle. Zur Differenzierung können Antikörperbestimmungen helfen, um eine autoimmune Genese zu bestätigen (GAD-, IA2-, Insulin-, Inselzell-, Zinktransporter- 8-Antikörper).
Akute Komplikationen bei Diabetes mellitus im Kindesalter
Diabetische Ketoazidose (DKA)
Die akute Stoffwechselentgleisung – diabetische Ketoazidose (DKA) – ist ein akuter Notfall und bedarf einer sofortigen adäquaten Therapie. In Österreich zeigt über ein Drittel der Kinder bei Diabetesmanifestation eine diabetische Ketoazidose. Es ist notwendig, auf typische diabetesspezifische Symptome (Polydipsie, Polyurie, Gewichtsverlust) zu achten und mittels Harnteststreifen und Blutzuckermessung eine Diabeteserkrankung auszuschließen oder zu diagnostizieren. Aufgrund der zerebralen Komplikationen („cerebral injury“) im Rahmen einer DKA gilt es, diese akute Stoffwechselentgleisung sowohl im Rahmen der Erstmanifestation der Erkrankung als auch im weiteren Verlauf möglichst zu vermeiden.
Die diabetische Ketoazidose, einhergehend mit den klinischen Symptomen der Polyurie, Polydipsie, Dehydratation, Tachykardie und Tachypnoe, besonders tiefer Bauchatmung, der sogenannten Kußmaul- Atmung, sowie Bauchschmerzen, Übelkeit und Erbrechen kann sowohl im Rahmen der Erstdiagnose Diabetes wie auch bei bereits bekanntem Diabetes auftreten. In Österreich ist die Anzahl der Kinder und Jugendlichen mit Ketoazidose im Rahmen der Diagnosestellung Diabetes mit über 30% sehr hoch. Zahlreiche Präventionskampagnen wie die Plakatkampagne 2009, bei der Informationsplakate an Kindergärten, Schulen, Apotheken und Arztpraxen verschickt wurden, oder das Ketoazidose-Filmprojekt 2016, bei dem Kinder mit Diabetes in Zusammenarbeit mit der Diabetesambulanz des Preyer’schen Kinderspitales rund um Dr. Andrea Jäger einen Aufklärungsfilm gedreht haben (der Film steht als Download unter www.typ1diabetes.at kostenlos zur Verfügung), verliefen bisher ohne Wirkung. Die Rate an Ketoazidosen ist über die vergangenen 20 Jahre unverändert hoch geblieben. Als besonders für das Auftreten einer Ketoazidose gefährdete Gruppe wurden Kleinkinder identifiziert.
Risikofaktoren für Ketoazidosen bei Kindern und Jugendlichen mit bekanntem Diabetes sind fieberhafte Infektionen, chronisch schlechte Stoffwechseleinstellung und mangelhafte Compliance sowie Katheterokklusionen bei Insulinpumpentherapie.
Pathophysiologie, Diagnose und Behandlung
Pathophysiologisch liegt der Entstehung der diabetischen Ketoazidose die absolute oder relative Insulindefizienz zugrunde. Infolge des Insulinmangels ist die Glukoseutilisation eingeschränkt, wodurch eine Hyperglykämie entsteht. Diese führt zur Überschreitung der Nierenschwelle mit nachfolgender Glukosurie und Dehydratation gefolgt von einem Anstieg der Osmolalität.
Aufgrund der fehlenden Glukoseutilisation wird zur Energiegewinnung die Lipolyse herangezogen. Diese führt zur Freisetzung von freien Fettsäuren und Ketonkörper-Produktion mit Verbrauch der Puffersysteme und Ausbildung der Azidose. Diese pathophysiologischen Veränderungen sichern die Diagnose: Hyperglykämie, Azidose und Dehydratation mit Hyperosmolalität.
Daraus ergibt sich die therapeutische Konsequenz der Flüssigkeitszufuhr, Ausgleich der Elektrolytdefizite und Zufuhr von Insulin als kausaler Therapieansatz. Dabei zu beachten ist eine kontinuierliche Behandlung mit Rehydrierung und Elektrolytsubstitution (Kalium!) über mindestens 24 bis 48 Stunden, einer langsamen Senkung der Hyperglykämie von max. 50 bis 100mg/dl pro Stunde sowie der Zufuhr von Kalorien, um die katabole Stoffwechsellage zu beenden.
Aufgrund der hohen Morbidität und Mortalität ist das Auftreten zerebraler Veränderungen im Rahmen einer Ketoazidose gefürchtet. Zerebrale Veränderungen können sowohl vor als auch während der Behandlung der Ketoazidose auftreten und sind von kognitiven Defiziten begleitet, die teils reversibel sind, teils aber auch irreversibel bestehen bleiben können.
In neueren pathophysiologischen Modellen zur Ätiologie zerebraler Beteiligung im Rahmen einer diabetischen Ketoazidose werden mehrere Faktoren und deren komplexe Interaktion diskutiert. Die Schwere der Azidose, Hypokapnie, Vasokonstriktion, Dehydratation, Hyperglykämie und Ketose führen allesamt zur Reduktion des zerebralen Blutflusses. Inflammatorische Faktoren und Zytokine sowie mikrogliale strukturelle Veränderungen bedingen sowohl auf zellulärer als auch vaskulärer Ebene Veränderungen, die für Verletzungen des Gehirns mit klinischer Symptomatik verantwortlich sind. Dies ist besonders im Kindesalter von großer Bedeutung, da die Entwicklung des kindlichen Gehirnes in den ersten Lebensjahren noch nicht abgeschlossen und damit besonders vulnerabel ist.
Eine akute Behandlung der diabetischen Ketoazidose in einem Zentrum mit Erfahrung in pädiatrischer Diabetologie ist wesentlich, um ein gutes Outcome bei dieser schweren und lebensbedrohlichen Stoffwechselentgleisung zu erreichen.
Akute schwere Hypoglykämie
Die Prävalenz von akuten schweren Hypoglykämien hat in den letzten Dekaden abgenommen, stellt aber immer noch einen limitierenden Faktor in der Diabetestherapie im Kindesalter dar.
Longitudinale Studien anhand von Diabetesregistern konnten nun zeigen, dass die Häufigkeit von Hypoglykämien in den vergangenen 20 Jahren zurückgegangen ist. Bemerkenswerterweise auch bei jenem pädiatrischen Patientenkollektiv, welches die niedrigsten HbA1c-Werte und damit beste metabolische Kontrolle zeigte.
Der Grund für die Reduktion der schweren Hypoglykämien dürfte in der Veränderung der therapeutischen Möglichkeiten in den letzten 10 bis 15 Jahren liegen. Die Einführung von schnell und lang wirksamen Insulinanaloga und der breite Einsatz von Insulinpumpen in der Pädiatrie haben in den letzten Jahrzenten nicht nur zu einer Verbesserung der metabolischen Einstellung, sondern auch zu einer Reduktion der Hypoglykämien geführt. Bleibt abzuwarten, inwieweit der zunehmende Einsatz von subkutanen Glukosesensoren als Stand-alone-Geräte oder in Kombination mit Insulinpumpen im Sinne einer sensorunterstützten Pumpentherapie die Hypoglykämie-Rate bei Kindern und Jugendlichen beeinflussen wird.
Trotz aller Verbesserungen in der Behandlung von kindlichem Diabetes gilt es aufgrund der Unreife des kindlichen Gehirns Häufigkeit und Schwere von Unterzuckerungen zu reduzieren bzw. diese gänzlich zu vermeiden. Dies gilt vor allem für schwere Hypoglykämien, welche als Ereignis mit Bewusstseinsbeeinträchtigung (Koma oder Krampfanfall) definiert sind, die einer Fremdhilfe bedürfen. Das noch unreife kindliche Gehirn ist sowohl durch schwere Hypoglykämien als auch durch Hyperglykämien gefährdet. Die Gratwanderung, möglichst viel Zeit im glykämischen Zielbereich („time-in-target“) zu erreichen mit so wenig Ausreißern in Hypo- oder Hyperglykämien wie möglich, steht immer mehr im Fokus der kindlichen Diabetestherapie.
Risiken im Kindesalter für das Auftreten von Hypoglykämien entstehen durch ein Missmanagement der Insulindosierung, insbesondere der Bolusgaben für Mahlzeiten. Rechenprogramme, Apps, BERechner wären vorstellbare Hilfsmittel, um eine exaktere Berechnung sowohl der Broteinheiten als auch der individuell benötigten Insulinmenge zu gewährleisten.
Ein weiteres Risiko für das Auftreten von Hypoglykämien sind körperliche Aktivität und Sport. Grundsätzlich als Teil der Diabetestherapie zu betrachten ist eine intensive Patientenschulung zum Thema Insulindosierung bei Sport. Zusätzlich zum akuten Hypoglykämie-Risiko während körperlicher Aktivität ist ein weiteres Absinken der Blutglukose noch viele Stunden nach der sportlichen Betätigung zu erwarten. Entsprechende Vorkehrungen, um nächtliche Hypoglykämien nach sportlichen Leistungen zu verhindern, müssen mittels Reduktion der nächtlichen Insulindosis und/oder zusätzlicher Kohlenhydratzufuhr getroffen werden.
Nächtliche Hypoglykämien können nicht nur nach sportlicher Aktivität auftreten. Aufgrund einer veränderten nächtlichen Glukosehomöostase und einer veränderten neuroendokrinen Schlafarchitektur bei Kindern mit Typ-1-Diabetes kommen nächtliche Hypoglykämien häufig vor. Die Hälfte der nächtlichen Hypoglykämien wird nicht bemerkt. Durch verbesserte Glukoseaufzeichnung mittels Flash-Glukosemessung und kontinuierlicher subkutaner Glukosemesssysteme stehen nun Tools zur Verfügung, um die nächtliche Glukosevariabilität sichtbarer zu machen.
Kleinkinder sind besonders gefährdet, Hypoglykämien zu entwickeln. Zum einen haben Kleinkinder eine hohe Insulinsensitivität, zum anderen eine schlechte Hypoglykämie- Wahrnehmung. Kleinkinder können schwer zwischen vegetativen und neurokognitiven Hypoglykämie-Zeichen unterscheiden, ihre Möglichkeiten, Hypoglykämien zu kommunizieren, sind begrenzt. Faktoren, die die Hypoglykämie-Wahrnehmung von Kindern beeinflussen, sind das Alter des Kindes, die Qualität der Stoffwechseleinstellung, der Blutzuckerausgangswert und die Dynamik des Blutzuckerabfalls. Auch die Häufigkeit aufeinanderfolgender Hypoglykämien kann die Fähigkeit zur Wahrnehmung von Unterzuckerungen negativ beeinflussen. Ein Drittel aller Kinder mit Diabetes zeigt eine Hypoglykämie- Wahrnehmungsstörung – und ist somit besonders für das Auftreten von Hypoglykämien gefährdet. Das Alter der Kinder zum Zeitpunkt von schweren Hypoglykämien ist entscheidend für deren kognitive Entwicklung. Kleinkinder mit schweren Hypoglykämien zeigen in verschiedenen kognitiven Bereichen Teilleistungsstörungen im Vergleich zu Kleinkindern ohne Auftreten von schweren Hypoglykämien.
Ein weiterer Aspekt im Zusammenhang mit dem Auftreten von Hypoglykämien im Kindesalter ist das jugendliche Risikoverhalten. Ähnlich der nicht diabetischen Peer-Group gehen Jugendliche mit Diabetes ein risikohaftes Verhalten ein. Bei Konsum von Alkohol steigt das Risiko für eine Hypoglykämie deutlich an, entsprechende Schulungen im Umgang mit Insulin bei Alkoholkonsum sollten daher Teil jeder Diabetesschulung im Jugendalter sein.
Die Behandlung von schweren Hypoglykämien erfolgt zu Hause im familiären Umfeld mit Glukagon (0,5–1mg) i.m. oder s.c. bzw. in der Klinik mit Glukose i.v. (2–3ml/kgKG 10% Glukose). Die Glukagon- Fertigspritze sollte in jedem Haushalt/ in jeder Schule mit einem Kind mit T1D vorhanden sein. Der Einsatz der Glukagon- Notfallspritze setzt eine entsprechende Schulung voraus. Andere Applikationsarten (nasales Glukagon) sind derzeit in Österreich noch nicht erhältlich.
Behandlung von Kindern und Jugendlichen mit Diabetes mellitus Typ 1
Die Therapieziele in der Behandlung von Kindern und Jugendlichen mit Diabetes mellitus Typ 1 sind in nationalen und internationalen Guidelines klar definiert und zusammengefasst. Neben der Vermeidung von akuten Stoffwechselentgleisungen (akute Hypoglykämien, akute Ketoazidosen) und der Prävention von diabetischen mikro- und makrovaskulären Folgeerkrankungen zählt bei Kindern und Jugendlichen auch eine normale körperliche und kognitive Entwicklung zu den wichtigen Behandlungszielen. Als metabolisches Ziel bei Kindern und Jugendlichen wurde von der österreichischen Arbeitsgruppe für pädiatrische Endokrinologie und Diabetes (APEDÖ) ein HbA1c-Wert ≤7,0% (≤53mmol/mol) ohne schwere Hypoglykämien festgesetzt.
Insulinsubstitution
Eine Insulinsubstitution ist die kausale Therapie bei Kindern mit T1D, wobei die Insulinsubstitution lebenslang durchgeführt werden muss. Die Substitution von Insulin sollte mehrfach täglich möglichst physiologisch durchgeführt werden, man spricht von einer individualisierten intensivierten Insulintherapie. Diese kann mittels Insulinpen und Applikation von lang wirksamen Insulinen (Basalbedarf) und kurz/schnell wirksamen Insulinen zu den Mahlzeiten (prandialer Insulinbedarf, Korrekturinsulin bei zu hohen Werten) oder mittels Insulinpumpe (nur kurz/ schnell wirksames Insulin und einprogrammierte Basalrate) erfolgen.
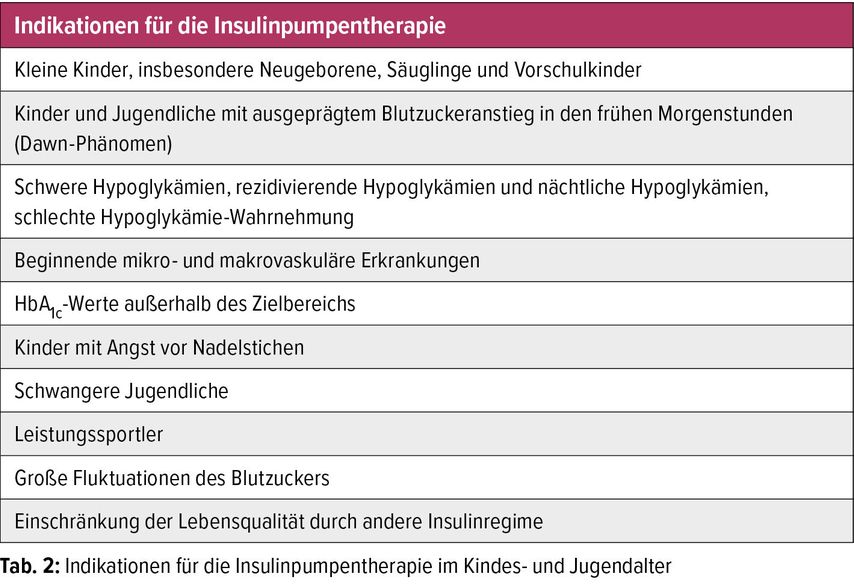
Die Insulinpumpentherapie ist dabei für Kinder unter sieben Jahren die bevorzugte Behandlungsmethode, wie die Richtlinien der internationalen Gesellschaft für pädiatrischen und adoleszenten Diabetes (ISPAD) festhalten.
Insulinpumpentherapie
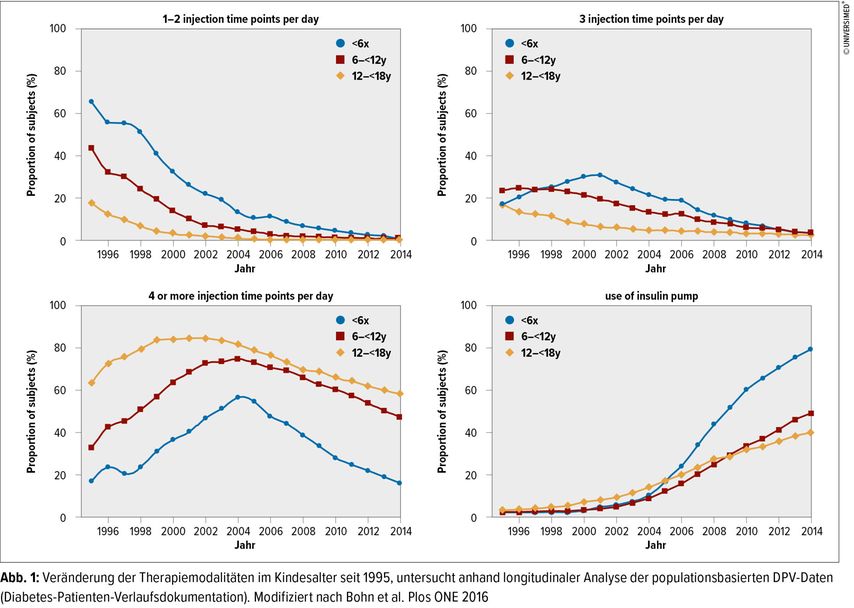
Die Insulinpumpentherapie als Behandlungsmethode bei Kindern und Jugendlichen mit Diabetes ist seit den frühen 2000er-Jahren in der pädiatrischen Diabetologie fest verankert, siehe Abbildung 1.
Waren es zunächst vor allem Jugendliche mit ausgeprägtem Dawn-Phänomen (hormonell bedingter morgendlicher Blutzuckeranstieg), die auf Insulinpumpe eingestellt wurden, so zeigte sich in den Folgejahren eine starke Zunahme der Pumpentherapie in allen Altersklassen, insbesondere bei Kleinkindern. Kinder zeigen Ängste und Abneigungen gegen Insulininjektionen, die zu verabreichenden Mengen an Insulin sind minimal und mit herkömmlichen Pens nicht ausreichend niedrig dosierbar. Unvorhersehbare Mengen der Nahrungsaufnahme sowie spontane körperliche Aktivität erschweren die Behandlung bei ganz jungen Kindern.
Für diese Situationen bietet die Therapie mit Insulinpumpe zahlreiche Vorteile im Vergleich zur Basis-Bolus-Therapie mit Pens. Die Anlage eines Katheters alle zwei bis drei Tage ins subkutane Fettgewebe führt zu einer deutlichen Reduktion der Nadelstiche. Die Bolusgaben erfolgen vor, während und in seltenen Fällen nach der Mahlzeit, sodass die Insulinmenge akkurat dem Kohlenhydratgehalt der Nahrungsmenge angepasst werden kann. Die Insulinabgabe kann bei Pumpensystemen unter Zuhilfenahme von Rechensystemen (BolusExpert) erfolgen. Diese erleichtern für Betreuungspersonen die Entscheidung über die richtige Dosis und helfen, Hemmungen aufseiten der Betreuungspersonen (Kindergärten, Schulen, Hort), Insulin zu injizieren, abzubauen. Für Kleinkinder in Fremdbetreuung, aber auch für Schulkinder und Jugendliche in Schulen oder anderen Betreuungseinrichtungen ist die Pumpentherapie daher eine bevorzugte Behandlungsmethode.
Blutzuckermessung, Glukose-Monitoring
Regelmäßige Messungen der Glukosewerte mehrmals täglich sind notwendig, um die Therapie effizient durchführen zu können. Die blutige Messung aus kapillärem Blut der Fingerbeere ist die empfohlene Art der Blutzuckerüberwachung. Diese Messungen entsprechen einer Momentaufnahme des aktuellen Blutglukosewertes. Mindestens 6 gemessene Glukosewerte täglich werden empfohlen, wobei ein direkter Zusammenhang zwischen Anzahl der täglichen Glukosemessungen und der Qualität der metabolischen Kontrolle festgestellt werden konnte.
Neuere Systeme zur kontinuierlichen Glukosemessung erweitern die Information für den Anwender. Im Gegensatz zur punktuellen Messung erlauben kontinuierliche Messsysteme (CGM) Informationen über den fortdauernden Glukosespiegel inklusive Angaben von Trends (meist in Pfeilformat) zum weiteren zu erwartenden Glukoseverlauf. Manche Systeme alarmieren bei Hypo- und Hyperglykämien, je nach individueller Schwellenangabe. Neben der Angabe des weiteren Glukosetrends können mit der Insulinpumpe kombinierte Systeme (sensorunterstützte Pumpentherapie) auch eine Abschaltung der Insulinzufuhr VOR Auftreten einer Hypoglykämie leisten („predictive low suspend“).
Kinder im Kindergarten- und Schulalter werden zunehmend mit Insulinpumpe behandelt und in den letzten Jahren in steigendem Ausmaß mit Sensoren und/ oder sensorunterstützter Pumpentherapie versorgt. Das Wissen um diese Behandlungsmethoden ist daher im schulischen Umfeld (Lehrpersonen, Schulärzte) von großer Bedeutung. Die zuletzt häufig eingesetzte Flash-Glukosemessung ersetzt teilweise die kapilläre Blutzuckermessung und ist so insbesondere im schulischen Umfeld/bei Fremdbetreuung vorteilhaft.
Ernährung
In der Therapie des T1D stellt die Ernährung eine wichtige Therapiesäule dar. Die Berechnung des Kohlenhydratanteils der Nahrung und deren Wirkung auf den Blutzucker sind für den Therapieerfolg wichtig.
Für ein Kind mit T1D wird eine gesunde, ausgewogene, ballaststoffreiche Ernährung mit einem Kohlenhydratanteil von 50 bis 55% empfohlen. Bei der Erstellung eines Ernährungsplans sollte auf die individuellen Gewohnheiten und Vorlieben des Kindes so weit wie möglich Rücksicht genommen werden.
Die Berechnung der Kohlenhydrate (KH) erfolgt meist in Broteinheiten (12g KH = 1 BE) oder in Gramm KH. Die genaue Berechnung der KH ist notwendig, um die Insulindosierung darauf abstimmen zu können. Zusätzlich ist es notwendig, die Familien auf die Unterschiede im glykämischen Index der KH hinzuweisen, ebenso wie auf den Einfluss von größeren Mengen von Eiweiß und/oder Fett auf den Blutzuckerspiegel.
Üblicherweise werden Kinder mit dem sogenannten „Bolus-Faktor“ geschult, welche Menge Insulin pro gegessene BE individuell verabreicht werden muss (z.B. 1,5 IE Insulin pro BE). Bei Behandlung mit Insulinpumpen besteht die Möglichkeit, diese Information im sogenannten Bolusrechenprogramm/Bolusexpert der Pumpe zu speichern. Dadurch erfolgt eine automatische Berechnung der notwendigen Insulinmenge, wenn der aktuelle Blutzuckerwert und die Menge der zu essenden BE in die Pumpe eingegeben werden.
Bewegung
Körperliche Bewegung und Sport wurden schon früh als Therapiesäulen bei Kindern mit Diabetes erkannt. Die durch regelmäßige körperliche Aktivität gewährleistete Insulinsensitivität erleichtert die metabolische Einstellung. Die verabreichte Insulinmenge ist der jeweiligen körperlichen Aktivität anzupassen, um Hypoglykämien während und nach dem Sport zu vermeiden.
Hypoglykämien bei und nach körperlicher Aktivität können entweder durch temporäre Reduktion der Basalrate (Pumpentherapie), Reduktion des Mahlzeitenbolus oder durch Zufuhr von zusätzlichen Broteinheiten (Sport-BE) vermieden werden.
Schulung
Eine strukturierte, altersgerechte und qualitätsgesicherte Schulung im Selbstmanagement der Erkrankung stellt die Grundlage einer erfolgreichen Diabetestherapie dar und muss allen betroffenen Kindern und deren Eltern bzw. Betreuern ermöglicht werden.
Neben dem Anspruch einer strukturierten und altersgerechten Schulung sollen Schulungen auch individuell konzipiert sein, um den jeweiligen Alltag der Kinder bewältigbar zu gestalten. Die Schulung wird von einem multidisziplinären Team durchgeführt, bestehend aus einem Kinderarzt oder einer Kinderärztin mit Spezialisierung in pädiatrischer Endokrinologie und Diabetologie, einer Diabetesberaterin oder einem Diabetesberater, diabeteserfahrenem Pflegepersonal, einem Diätologen oder einer Diätologin und einer Psychologin oder einem Psychologen.
Ziel ist es, Grundkenntnisse über die Erkrankung, Kenntnisse und Fertigkeiten der Selbstkontrolle, Insulintherapie, Injektionstechniken, Erkennen und Management von Hyper- und Hypoglykämien, Ketoazidosen, über Ernährung, Dosisanpassung bei Sport, Erkrankung oder Reisen, Folgeerkrankungen, Schwangerschaft, Umgang mit Alkohol (ab Jugendalter) und psychosoziale Fragen zu vermitteln. Die Inhalte müssen in einer dem kindlichen Alter und Entwicklungsstand angepassten Form erfolgen.
Wesentlich ist auch die ausreichende diabetologische Schulung von Betreuungspersonal in der Schule. In einigen Teilen Österreichs besuchen sogenannte Diabetes-Nannys die Schulen mit an Diabetes erkrankten Kindern, um die Lehrpersonen diabetologisch zu schulen. Damit können Unsicherheit und Angst im Umgang mit einem diabetischen Schulkind abgebaut werden und die Inklusion des Kindes im Schulalltag kann problemlos funktionieren.
Die Schulärzte und -ärztinnen können hier als wichtiges Bindeglied fungieren und im Austausch zu gesundheitlichen Fragen zwischen Schülern mit Diabetes und Lehrpersonen beratend unterstützen.
Diabetesassoziierte Erkrankungen
Kinder mit Typ-1-Diabetes haben ein erhöhtes Risiko, eine zweite oder weitere Autoimmunerkrankungen zu entwickeln. Klinisch verlaufen diese Erkrankungen oft asymptomatisch, weshalb in regelmäßigen Abständen Screening-Untersuchungen empfohlen sind.
Mit bis zu 29% der Patienten mit T1D sind das Auftreten von Schilddrüsenautoantikörpern und die Entwicklung einer Hashimoto-Thyreoiditis die häufigste diabetesassoziierte Erkrankung, die vor allem bei jugendlichen Mädchen manifestiert.
Die Zöliakie (7–10%) entwickelt sich meist schleichend und klinisch „silent“, sodass aktiv auf das Vorliegen einer diabetesassoziierten Zöliakie gescreent werden muss. Die internationalen Guidelines beschreiben den empfohlenen Screening-Algorithmus in Abhängigkeit von Diabetesmanifestationsalter und Diabetesdauer.
Weitere Autoimmunerkrankungen wie Hyperthyreose, Nebenniereninsuffizienz, Vitiligo, Alopecia areata, Autoimmungastritis oder Polyendokrinopathien sind seltener. Bei Symptomen sollten Diabetologen auch an die Möglichkeit dieser selteneren assoziierten Autoimmunerkrankungen denken.
Diabetische Spätkomplikationen
Die Entwicklung von mikrovaskulären und makrovaskulären Veränderungen zu verhindern ist wesentliches Ziel einer guten metabolischen Einstellung.
Neben HbA1c als Maß für die Qualität der Stoffwechseleinstellung spielen auch der Blutdruck, der Body-Mass-Index, der Lipidstatus und Rauchen eine Rolle hinsichtlich der vaskulären Gesundheit.
Das Ausmaß und die Frequenz der Screening-Untersuchungen zum Vorliegen einer diabetischen Retinopathie, Nephropathie und Neuropathie sind in den internationalen Guidelines in Abhängigkeit vom Erkrankungsalter und der Erkrankungsdauer festgelegt, diese Untersuchungen sollten in erfahrenen Zentren durchgeführt werden.
Literatur
American Diabetes Association: Standards of Medical Care in Diabetesd. Diabetes Care 2018; 41(Suppl1)
Bjørgaas MR: Cerebral effects of severe hypoglycemia in young people with type 1 diabetes. Pediatr Diabetes 2012; 13: 100-7
Fritsch M et al.: Diabetic ketoacidosis at diagnosis in Austrian children: a population-based analysis, 1989- 2011. J Pediatr 2013; 163: 1484-8.e1
Glaser N et al.: Effects of hyperglycemia and effects of ketosis on cerebral perfusion, cerebral water distribution, and cerebral metabolism. Diabetes 2012; 61: 1831-7
ISPAD Practical Consensus Guidelines 2018; Pediatric Diabetes 2018; 19 (Suppl. 27)
Karges B et al.; DPV Initiative: Hospital admission for diabetic ketoacidosis or severe hypoglycemia in 31,330 young patients with type 1 diabetes. Eur J Endocrinol 2015; 173: 341-50
Maahs DM et al.; DPV Initiative; T1D Exchange Clinic Network: Contrasting the clinical care and outcomes of 2,622 children with type 1 diabetes less than 6 years of age in the United States T1D Exchange and German/Austrian DPV registries. Diabetologia 2014; 57: 1578-85
Neu A et al.: Diagnostik, Therapie und Verlaufskontrolle des Diabetes mellitus im Kindes- und Jugendalter. Diabetologie 2017; 12: S190-202
Rami-Merhar et al.: P154. Incidence trends of type 1 and type 2 diabetes in Austrian children <15 years (1999–2015). Pediatric Diabetes 2016; 17: 94
Schober E et al; Austrian Diabetes Incidence Study Group: Diabetic ketoacidosis at diagnosis in Austrian children in 1989-2008: a population-based analysis. Diabetologia 2010; 53: 1057-61
www.typ1diabetes.at - Film „Beinah zu spät“ – kostenloser Download
Das könnte Sie auch interessieren:
Diabetes erhöht das Sturzrisiko deutlich
Eine dänische Studie kommt zu dem Ergebnis, dass sowohl Patienten mit Typ-1- als auch Patienten mit Typ-2-Diabetes öfter stürzen und häufiger Frakturen erleiden als Menschen aus einer ...
Notfall Diabetische Ketoazidose: Leitliniengerechtes Handeln kann Leben retten
Akute Stoffwechselentgleisungen können lebensbedrohlich sein und erfordern eine rasche und leitliniengerechte Diagnostik und Therapie. Pathogenese, Klinik, typische Befunde und die ...
Wie oft wird Diabetes nicht oder spät erkannt?
Im Allgemeinen wird von einer hohen Dunkelziffer an Personen mit undiagnostiziertem Typ-2-Diabetes ausgegangen. Ein Teil davon sind von Ärzten „übersehene“ Fälle. Eine von der University ...