Alopecia areata im Kindes- und Jugendalter
Autorinnen:
Dr.in Viktoria Gruber
Dr.in Maria Repelnig
Universitätsklinik für Dermatologie und Venerologie
Medizinische Universität Graz
E-Mail: viktoria.gruber@medunigraz.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Die Alopecia areata (AA), der „kreisrunde Haarausfall“, ist eine chronische, immunvermittelte Erkrankung, die durch reversiblen, nicht vernarbenden Haarverlust gekennzeichnet ist. Typischerweise kommt es zu einem abrupt einsetzenden, umschriebenen Haarausfall. Er kann von einzelnen herdförmigen Läsionen bis hin zum vollständigen Verlust der Kopf- oder Körperhaare reichen.
Keypoints
-
Die Diagnose einer Alopecia areata kann in der Regel klinisch gestellt werden. Nur in unklaren Fällen oder bei Therapieresistenz sollte eine Biopsie erfolgen.
-
Mögliche Komorbiditäten sollten berücksichtigt und eine entsprechende Abklärung bzw. Therapie sollte eingeleitet werden.
-
In der Therapie der Alopecia areata bei Kindern und Jugendlichen gilt: „Weniger ist mehr“ – insbesondere bei milder Ausprägung.
-
Die Alopecia areata kann für Betroffene stigmatisierend sein – eine psychologische Betreuung zur Stärkung des Selbstbewusstseins und zum Erlernen von Coping-Strategien sollte immer angeboten werden.
Die psychosoziale Belastung von Betroffenen und deren Familien spielt aufgrund der Sichtbarkeit der Erkrankung häufig eine große Rolle. Wegen der hohen Rate an Spontanremissionen sind therapeutische Maßnahmen oftmals nicht notwendig. Bei schwerer Ausprägung steht jedoch ein zugelassener oraler Januskinase(JAK)-Inhibitor als Systemtherapeutikum zur Verfügung. Im Mittelpunkt der Betreuung sollte stets die Stärkung des Selbstbewusstseins des betroffenen Kindes/des/der Jugendlichen stehen.
Häufigkeit und Entstehung
Die Inzidenz beträgt in der Altersgruppe der 0- bis 9-Jährigen etwa 20 Fälle pro 100000 Personen und Jahr und steigt in der Gruppe der 10- bis 19-Jährigen auf 57 Fälle pro 100000 Personen und Jahr an. In einkommensstarken Ländern wird insgesamt eine langsamer zunehmende Erkrankungshäufigkeit beobachtet. Zudem zeigen sich deutliche regionale Unterschiede: Die höchsten Erkrankungsraten finden sich in Nordafrika und dem Mittleren Osten, gefolgt von Nordamerika, Asien und Europa. Die niedrigsten Raten werden in Lateinamerika und im subsaharischen Afrika verzeichnet. Mädchen sind etwas häufiger als Jungen betroffen (Verhältnis 1,5:1), wobei der Krankheitsverlauf bei Jungen meist schwerer ausfällt. Etwa eine von 50 Personen entwickelt im Laufe des Lebens eine Alopecia areata (AA), und familiäre Häufungen legen eine genetische Disposition nahe.
Die Pathophysiologie der AA beruht auf einer Fehlsteuerung der zellulären Immunantwort. Der Haarfollikel hat normalerweise ein sogenanntes „Immunprivileg“, welches ihn vor dem körpereigenen Immunsystem „abschirmt“. Bei der AA geht dieses Privileg verloren. Bei genetisch prädisponierten Individuen – insbesondere Trägern bestimmter Varianten im HLA-Genkomplex – können Triggerfaktoren wie akute oder chronische Infektionen, psychischer oder physischer Stress, oxidativer Stress, Medikamente oder Immuntherapien zu einer Aktivierung autoreaktiver T-Zellen führen. Diese greifen die Zellen des Haarfollikelepithels an und lösen über die Sekretion von Interferon γ eine Entzündungskaskade über den JAK/STAT-Signalweg aus. In der Folge wird das Anagenhaar dystroph, die Matrixkeratinozyten können den Haarschaft nicht mehr vollständig verhornen – die für die AA pathognomonischen „Ausrufezeichenhaare“ entstehen. Die Anagenphase ist deutlich verkürzt und geht vorzeitig in die Telogenphase über, was den abrupten Haarausfall zur Folge hat. Da die Entzündung nicht die Stammzellen des Haarfollikels betrifft, besteht die Fähigkeit zur Restitutio ad integrum. Nach Abklingen der Entzündungsreaktion kann der Haarfollikel wieder in die Anagen-phase eintreten und es beginnt ein neuer Haarzyklus.
Klinische Manifestationen
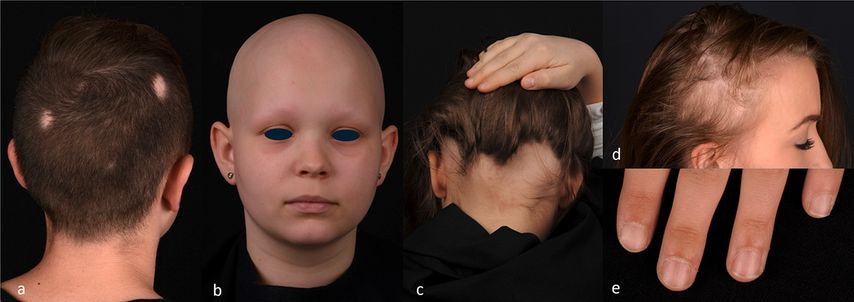
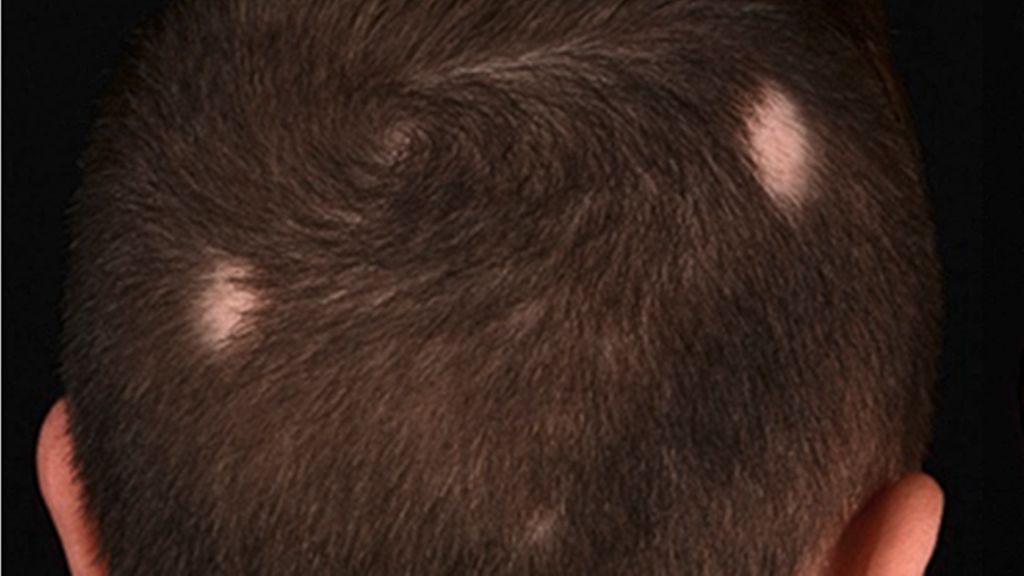
Die AA zeigt ein breites Spektrum klinischer Formen, die sich in Bezug auf Ausprägung, Lokalisation und Prognose unterscheiden. Die häufigste Form bildet die umschriebene AA („patchy alopecia“), bei der die Haare in der Regel im Bereich der Kopfhaut ausfallen (Abb.1a). Es können aber auch andere haartragende Areale wie Augenbrauen, Wimpern, der Körper und der Bartbereich bei Jugendlichen betroffen sein. Die meisten Betroffenen weisen ein bis zwei haarlose Areale auf. Die Kopfhaut innerhalb dieser Herde ist glatt und unauffällig, eine Rötung der Haut ist normalerweise nicht zu beobachten. Anzumerken ist, dass die klinische Ausprägung der umschriebenen AA zu Erkrankungsbeginn keine Rückschlüsse auf die Prognose bzw. das Rezidivrisiko zulässt.
Von einer Alopecia universalis spricht man bei komplettem Verlust der Kopf- und Körperbehaarung (Abb.1b).
Neben der Alopecia universalis unterscheidet man noch die Alopecia totalis, bei der nur die Kopfbehaarung betroffen ist, während die übrige Behaarung inklusive Wimpern und Augenbrauen erhalten bleibt.
Eine seltene Form ist die AA vom Ophiasis-Typ, die mit einem bandförmigen Haarausfall im Okzipital- und Temporalbereich und einer schlechteren Prognose einhergeht (Abb.1c).
Am seltensten tritt die AA vom inversen Ophiasis-Typ („Sisaipho-Typ“) auf. Hier kommt es zu einem Haarverlust im Oberkopfbereich, wobei die seitlichen und hinteren Kopfpartien meist ausgespart bleiben. Ein diffuser Haarausfall mit verringerter Haardichte, insbesondere im mittleren Scheitelbereich, kommt bei der diffusen AA vor (Abb.1d).
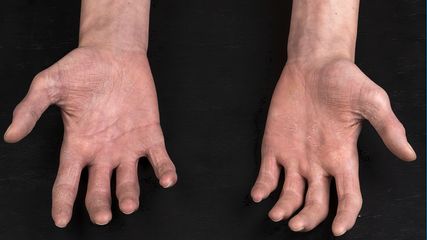
In etwa 40% der AA-Fälle sind Nagelveränderungen festzustellen. Typischerweise finden sich Tüpfelnägel (Abb.1e), es können aber auch andere Nagelveränderungen wie Längsrillen, Trachyonychie (grobe, raue Nagelplatte), eine rote Lunula, eine Ausdünnung der Nagelplatten oder Onycholysen vorliegen. Insgesamt sind Nagelveränderungen mit einem ausgedehnteren Haarausfall assoziiert. Sie können dem Haarausfall vorausgehen oder noch Monate bis Jahre nach dem Haarausfall auftreten. Auch nach dem Nachwachsen der Haare können die Nagelveränderungen bestehen bleiben.
Abb. 1: Verschiedene klinische Manifestationen der Alopecia areata (AA): a) umschriebene AA („patchy alopecia“) mit zwei münzgroßen haarlosen Arealen. b) Alopecia universalis mit völligem Fehlen der Kopf- und Körperbehaarung. c) AA vom Ophiasis-Typ mit bandförmigem haarlosen Areal occipital, welches sich nach temporal erstreckt. d) diffuse AA mit verminderter Haardichte parietal. e) Nagelveränderungen bei AA (Tüpfelnägel)
Diagnostik und Differenzialdiagnosen
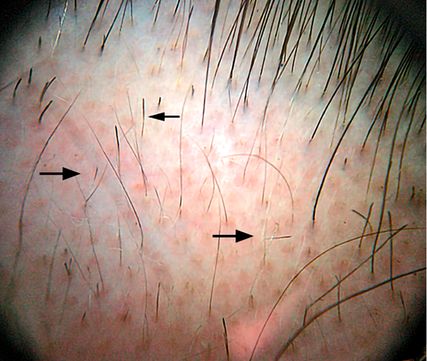
Abb. 2: „Ausrufezeichenhaare“ als pathognomonisches trichoskopisches Merkmal der AA mit Verjüngung des Haarschaftes nach proximal
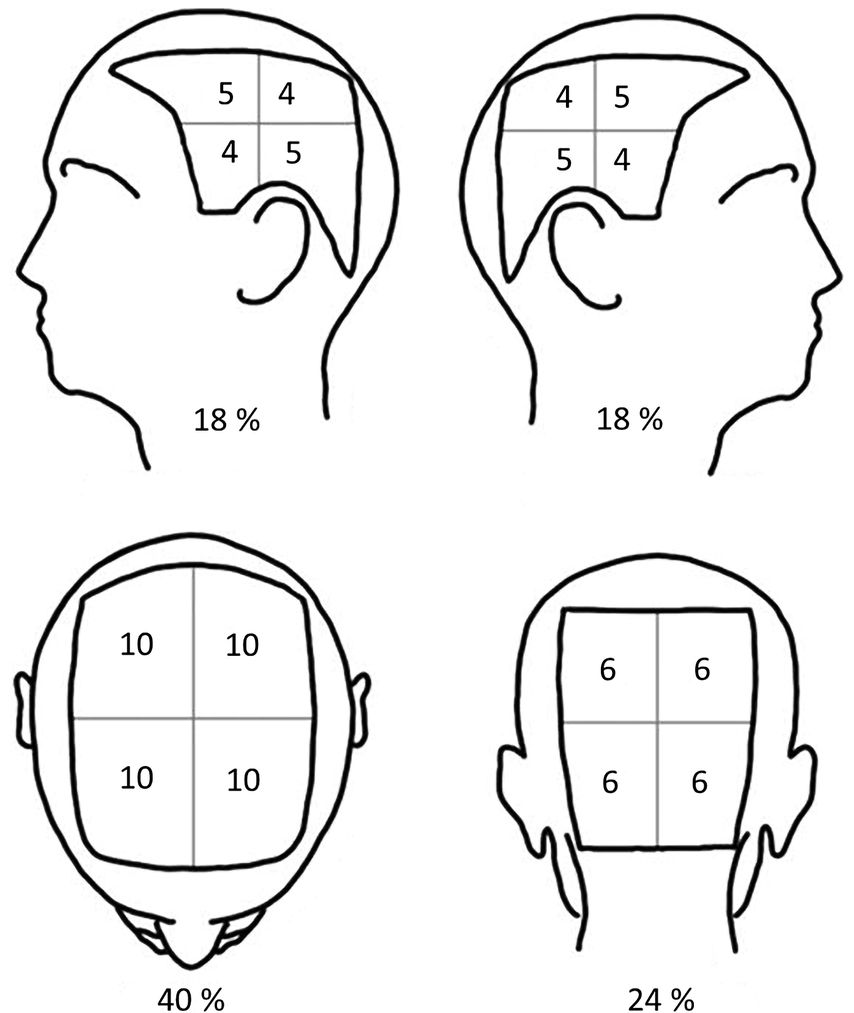
In der Diagnostik der AA wird zunächst eine ausführliche Eigen- und Familienanamnese erhoben. Zusätzlich erfolgt eine sorgfältige Inspektion der gesamten Haut sowie des Nagelorgans. Beim Haarzupftest wird ein Büschel von etwa 50–60 Haaren kopfhautnah erfasst und mit mäßigem Zug in Wuchsrichtung gezogen. Fällt ein Anteil von mehr als 10 Prozent der Haare aus, gilt der Test als positiv und spricht für eine aktive Erkrankung. Die Trichoskopie erweist sich in der Diagnostik als besonders hilfreich. Typische Merkmale der AA sind unter anderem „Ausrufezeichenhaare“, die als pathognomonisch gelten. Dabei handelt es sich um kurze, abgebrochene Haare, die sich zum proximalen Ende hin verjüngen (Abb.2). Weitere Merkmale umfassen „yellow dots“ (intakte Haarfollikelöffnungen gefüllt mit Talg oder Keratinozytenresten), „black dots“ (Reste abgebrochener Haare in den Haarkanälen) und „pigtail hairs“ (kurze, eingerollte Haare, die typischerweise in der Remissionsphase auftreten). Eine Hautbiopsie ist nur dann erforderlich, wenn klinisch eine vernarbende Alopezie nicht sicher ausgeschlossen werden kann oder wenn trotz adäquater Behandlung keine Besserung eintritt. Zur Beurteilung des Schweregrades kommt der sogenannte SALT-Score (Severity of Alopecia Tool Score) zur Anwendung. Hierfür wird die Kopfhaut in vier Regionen unterteilt, der Prozentsatz des Haarverlustes in jeder Region geschätzt und mit dem entsprechenden Flächenanteil multipliziert. Die Summe aller Werte ergibt den SALT-Score, wobei der Wert „0“ keinem Haarausfall und „100“ einem kompletten Haarausfall entspricht (Abb.3).
Abb. 3: Schematische Darstellung zur Berechnung des SALT-Scores (modifiziert nach Olsen EA et al. JAAD 2016; 75(6): 1268-70)
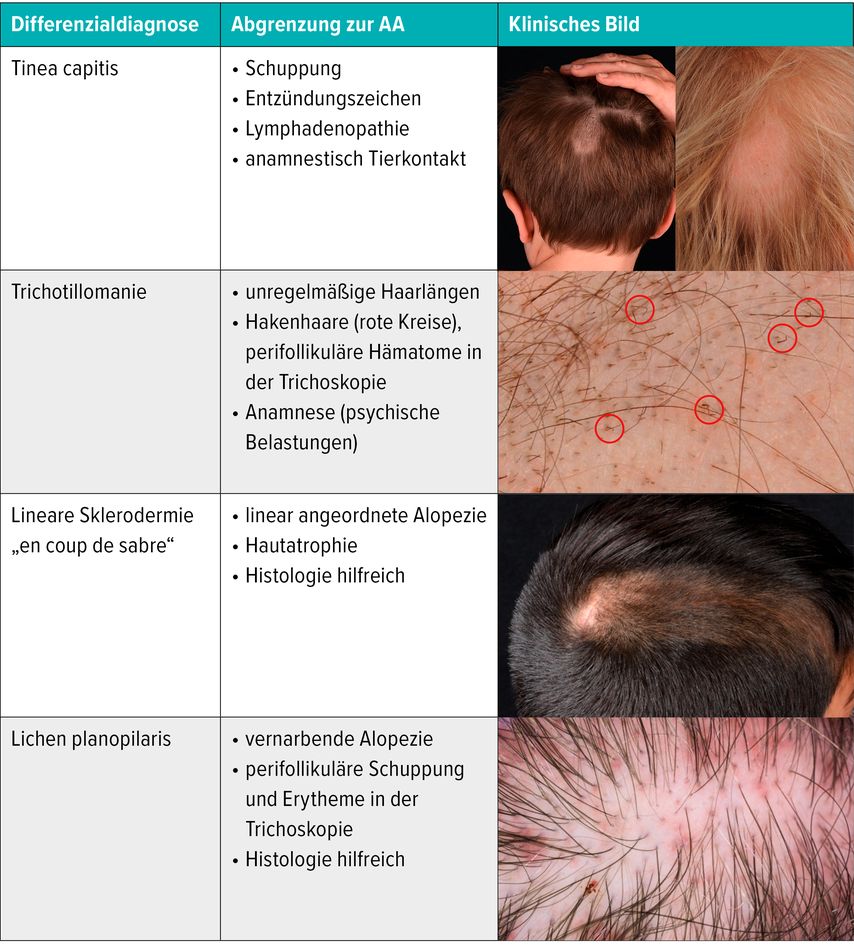
Zu den wichtigsten Differenzialdiagnosen der AA im Kindes- und Jugendalter zählen Tinea capitis, Trichotillomanie, lineare Sklerodermie „en coup de sabre“ und Lichen planopilaris. Eine Übersicht über die jeweiligen Differenzialdiagnosen und deren Abgrenzung zur AA findet sich in Tabelle 1.
Tab. 1: Übersicht über die wichtigsten Differenzialdiagnosen und deren Abgrenzungsmerkmale zur AA
Assoziierte Komorbiditäten
Es ist bekannt, dass die AA mit verschiedenen anderen Erkankungen einhergehen kann. Die atopische Dermatitis stellt die häufigste Komorbidität dar und liegt bei etwa 17 Prozent der betroffenen Kinder mit AA zusätzlich vor. Das Vorhandensein einer Erkrankung aus dem atopischen Formenkreis erhöht das Risiko, eine AA zu entwickeln, auf das bis zu 10-Fache. Die zweithäufigste Komorbidität bildet die Vitiligo, die oft mit einem schweren Verlauf der AA vergesellschaftet ist. Darüber hinaus besteht eine Assoziation zwischen der AA und anderen Autoimmun-erkrankungen wie etwa Hashimoto-Thyreoiditis, Psoriasis, Zöliakie, rheumatoider Arthritis, Colitis ulcerosa, juveniler idiopathischer Arthritis und dem systemischen Lupus erythematodes. Auch metabolische Erkrankungen wie Adipositas, Hyperlipidämie, Diabetes mellitus oder arterielle Hypertonie treten gehäuft auf. Ein beachtlicher Anteil, nämlich etwa 60 Prozent aller Kinder und Jugendlichen mit AA, weist mindestens eine psychiatrische Erkrankung auf, allen voran Depression und Angststörung. Durch die AA kommt es häufig zu vermindertem Selbstwertgefühl, negativen Auswirkungen auf das Körperbild, sozialer Ausgrenzung, Stigmatisierung, Hänseleien und somit zu einer verminderten Lebensqualität.
Therapeutische Möglichkeiten und Prognose
Die Therapie der AA bei Kindern und Jugendlichen kann herausfordernd sein, da viele Behandlungsoptionen „off-label“ sind und deren Einfluss auf den langfristigen Erkrankungsverlauf nicht bekannt ist. Grundsätzlich richtet sich das therapeutische Vorgehen nach Schweregrad, Alter des Kindes und psychosozialem Leidensdruck. Insgesamt gilt in der Behandlung der AA bei Kindern und Jugendlichen der Leitsatz „Weniger ist mehr“. Da Spontanremissionen häufig sind und viele gängige Therapien nur geringe Evidenz, aber relevante Nebenwirkungen aufweisen, gilt eine abwartende Haltung zunächst als „Therapie der Wahl“. Von belastenden Behandlungsversuchen ist insbesondere im Kindesalter dringend abzuraten. Angesichts möglicher Stigmatisierung und der oft beeinträchtigten Lebensqualität kann eine kinderpsychologische Unterstützung sinnvoll sein. Sie hilft, das Selbstbewusstsein zu stärken und Coping-Strategien zu erlernen. Eine übermäßige Thematisierung der Erkrankung durch die Eltern kann dem betroffenen Kind vermitteln, dass mit ihm etwas „nicht stimme“ – das verstärkt Ängste und das Gefühl der Ausgrenzung. Wird trotz der begrenzten Evidenzlage eine Therapie gewünscht, können ausgewählte topische oder systemische Behandlungsansätze erwogen werden.
Topische Kortikosteroide der Klasse III (bei Kindern unter 12 Jahren) oder IV (bei Kindern ab 12 Jahren) sind die Therapien der ersten Wahl bei milder Ausprägung der AA. Nebenwirkungen sind selten, können aber lokale Hautatrophie umfassen, weshalb die Behandlung bei beginnendem Haarwuchs reduziert oder bei fehlender Besserung abgesetzt wird. Die Anwendung sollte 12 Wochen nicht überschreiten. Topische Calcineurininhibitoren, wie etwa Tacrolimus, können im Gesichtsbereich (Augenbrauen) für maximal 6 Monate angewandt werden.
Intraläsionell angewandte Kortikosteroide, wie beispielsweise Triamcinolon, ermöglichen hohe Wirkstoffkonzentrationen direkt am Haarfollikel und können bei älteren Kindern und Jugendlichen mit einer umschriebenen AA zur Anwendung kommen. Aufgrund der Schmerzhaftigkeit der Behandlung sollte diese nur in Einzelfällen eingesetzt werden, insbesondere wenn topische Kortikosteroide nicht ausreichend wirken und Injektionen toleriert werden.
Topisches Minoxidil wirkt vasodilatierend und verlängert die Anagenphase des Haarfollikels. Da es keine antientzündlichen Eigenschaften hat, ist lediglich ein additiver Einsatz zu anderen lokalen oder systemischen Therapien sinnvoll.
Weitere topische Therapieverfahren wie die Irritationsbehandlung mit Dithranol oder die Kontaktimmuntherapie mit SADBE („squaric acid dibutylester“) haben einen untergeordneten Stellenwert in der klinischen Praxis, zumal kontrollierte Langzeituntersuchungen fehlen und beide Stoffe nicht als Arzneimittel zugelassen sind.
Ritlecitinib (Litfulo®) ist ein oraler selektiver JAK-Inhibitor (hemmt irreversibel und selektiv die JAK3 sowie Enzyme aus der Familie der TEC-Kinasen), der zur Behandlung der schweren AA bei Kindern ab 12 Jahren zugelassen ist. Die empfohlene Dosis beträgt 50mg einmal pro Tag in Form einer Hartkapsel. Wenn sich nach 36 Behandlungswochen kein klinisches Ansprechen abzeichnet, ist eine Beendigung der Therapie in Betracht zu ziehen. Wie bei allen oralen JAK-Inhibitoren sind regelmäßige Laborkontrollen während der Therapie erforderlich. Zu den berichteten häufigsten Nebenwirkungen gehören Kopfschmerzen, Akne und Infektionen der oberen Atemwege. Mit einer Zulassung bei Kindern ab 6 Jahren ist in naher Zukunft zu rechnen.
Es existieren noch weitere systemische Therapieoptionen, welche allerdings über keine Zulassung für die Behandlung der AA im Kindes- und Jugendalter verfügen, und deren Wirksamkeit unklar ist. Diese umfassen orale oder intravenöse Kortiko-steroide, orales Minoxidil, klassische Immunsuppressiva wie Methotrexat, Azathioprin und Ciclosporin sowie Biologika wie Dupilumab und Ustekinumab.
Fazit
Die Prognose der AA ist insgesamt gut, insbesondere bei Auftreten des Haarausfalls nach dem 10. Lebensjahr. Bei 95% der Kinder und Jugendlichen wachsen die Haare innerhalb eines Jahres komplett nach. In etwa 30% der Fälle kommt es zu einem Rezidiv. Etwa 7% weisen einen chronisch-rezidivierenden Verlauf auf. Das Risiko für eine Progression einer umschriebenen AA zur Alopecia totalis/universalis ist gering und liegt bei etwa 5%. Als ungünstige prognostische Parameter sind die Erstmanifestation vor dem 10. Lebensjahr, häufige Rezidive sowie der Ophiasis-Typ zu nennen.
Literatur:
● Adhanom R et al.: Epidemiology of pediatric alopecia areata. Pediatr Dermatol 2025; 42 Suppl 1(Suppl 1): 12-23 ● Betz RC Et al.: Genome-wide meta-analysis in alopecia areata resolves HLA associations and reveals two new susceptibility loci. Nat Commun 2015; 6: 5966 ● Blume-Peytavi U et al.: Atlas der Pädiatrischen Dermatologie. Weinheim: Wiley 2018; p541 ● Conic RZ et al.: Comorbidities in pediatric alopecia areata. J Eur Acad Dermatol Venereol 2020; 34(12): 2898-901 ● Fitzhugh MH et al.: Pathophysiology of alopecia areata in the pediatric patient. Pediatr Dermatol 2025; 42 Suppl 1(Suppl 1): 24-30 ● Katakam BK et al.: IADVL SIG Pediatric Dermatology (Academy) recommendations on childhood alopecia areata. Indian Dermatol Online J 2022; 13(6): 710-20 ● Olsen EA, Canfield D: SALT II: A new take on the Severity of Alopecia Tool (SALT) for determining percentage scalp hair loss. JAAD 2016: 75(6): 1268-70 ● Patel HA et al.: A clinician’s guide to pediatric alopecia areata treatments. JAAD Reviews 2024; 2: 57-66 ● Rudnicka L et al.: European expert consensus on the systemic treatment of alopecia areata. J Eur Acad Dermatol Venereol 2024; 38(4): 687-94 ● Shim WH et al.: Dermoscopic approach to a small round to oval hairless patch on the scalp. Ann Dermatol2014; 26(2): 214-20 ● Thompson AR et al.: Lifetime incidence and healthcare disparities in alopecia areata: a UK population-based cohort study. Br J Dermatol 2024; 191(6): 924-35
Das könnte Sie auch interessieren:
Tägliche Tablette gegen Psoriasis
Die US-Arzneimittelbehörde FDA hat mit Icotrokinra ein orales Medikament gegen Schuppenflechte zugelassen, welches die Rezeptoren für Interleukin-23 (IL-23) hemmt. Eine EU-Zulassung ...
Juveniles Polymyositis/Sklerodermie-Overlap-Syndrom
Die Komplexität von Kollagenosen und Autoimmunerkrankungen stellt oft eine diagnostische und therapeutische Herausforderung dar, da viele Patient:innen nicht nur einer einzigen Entität ...
Funktionalisierung bakterieller Nanocellulose
Chronische Wunden unterschiedlicher Ätiologie, etwa bei arterieller und venöser Insuffizienz oder Diabetes mellitus, prägen die tägliche Wundversorgung.Neben chronischen Wunden verlangen ...