Die Top-8-Interaktionen bei Arzneimitteln
Bericht:
Regina Scharf , MPH
Redaktorin
Review:
Prof. Dr. med. Anne A. Leuppi-Taegtmeyer, PhD
Universitätsspital und Universität Basel
Selina Späni
Dipl. Apothekerin
FPH Klinische Pharmazie
Kantonsspital Baselland
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Ob «To-dos» oder Wunschzettel – fast jeder von uns schreibt Listen. Auf einer persönlichen Liste der Pharmakologin Prof. Dr. med. Anne A. Leuppi-Taegtmeyer aus Basel stehen wichtige Arzneimittelinteraktionen, wie wir seit dem SGAIM-Kongress im letzten Jahr wissen. Ein eindrückliches Referat zu einem wichtigen Thema, über das wir hier ausführlich berichten.
Als Arzneimittelinteraktion bezeichnet man das Auftreten einer Wechselwirkung nach der gleichzeitigen Einnahme von mehreren Medikamenten oder auch Medikamenten und Nahrungsmitteln.
Die Interaktionen können die Pharmakokinetik oder Pharmakodynamik verändern. Dabei ist sowohl eine Verstärkung als auch eine Abschwächung der Wirkung möglich. «Pharmakodynamische Interaktionen sind oft die Folge additiver Effekte», sagte Prof. Dr. med. Anne A. Leuppi-Taegtmeyer vom Universitätsspital Basel am SGAIM-Kongress und nannte als Beispiel die Zunahme der Blutungsneigung infolge einer gleichzeitigen Einnahme von einem Antikoagulans und einem Thrombozytenaggregationshemmer.
Die Mechanismen der pharmakokinetischen Interaktionen sind aus pharmakologischer Sicht interessanter. Diese können an verschiedenen Etappen der Medikamentenpassage durch den Körper auftreten, beispielsweise infolge der Hemmung oder Induktion enzymatischer Prozesse oder Transportmechanismen im Darm bzw. in der Leber. Möglich sei auch ein kompetitives Verhalten der Stoffwechselprodukte an der Niere: In der Folge wird das eine ausgeschieden und das andere retiniert.
Arzneimittelinteraktionen können durch eine sorgfältige Medikamentenanamnese minimiert werden. Diese sollte auch Fragen nach freiverkäuflichen (OTC-)Produkten, Kräutern, Drogen sowie zur Ernährung enthalten. Eine wichtige Massnahme bei der Betreuung von Patienten ist die regelmässige Überprüfung der Medikation. Von grosser Bedeutung sind zudem die Schulung und die Instruktion der Patienten über die verordneten Medikamente. Bei Unsicherheiten lohnt sich ein Blick in das Arzneimittelkompendium oder die Kontaktaufnahme mit der klinischen Pharmakologie resp. klinischen Pharmazie. Informationen zu möglichen Interaktionen liefern das Clinical Decision Support System (CDSS) oder auch Datenbanken zu spezifischen Medikamenten wie die Liverpool COVID-19 Drug Interactions.
Nr. 1: Kationen und Chinolone
Bei zeitgleicher Einnahme von polyvalenten Kationen wie Kalzium, Magnesium, Aluminium, Eisen oder Zink und grossen, negativ geladenen Medikamenten kann im Magen eine Komplexbildung erfolgen. Die daraus enstehenden Chelate werden nicht resorbiert, was die Aufnahme der Medikamente reduziert bzw. verhindert. Ein solches Beispiel ist das Auftreten von Chelaten nach der gleichzeitigen Einnahme von Ciprofloxacin und Magnesium per os.1 Die therapeutische antibiotische Wirkung bleibt in diesem Fall aus, denn die nötigen Ciprofloxacin-Plasmaspiegel zur Hemmung der Bakterien werden nicht erreicht. Die Interaktion lässt sich vermeiden, indem man zuerst Ciprofloxacin und frühestens zwei Stunden danach das Magnesium einnimmt. Bis dahin sei das Ciprofloxacin üblicherweise gut resorbiert.
Eine Komplexbildung mit polyvalenten Kationen findet auch bei anderen Kombinationen statt, zum Beispiel mit anderen Chinolonen wie Levofloxacin, mit Tetrazyklinen wie Doxycyclin sowie mit Isoniazid, Levothyroxin, Levodopa und Bisphosphonaten. «Bereits die in Joghurt enthaltene Menge Kalzium ist ausreichend, um die Resorption der Substanzen deutlich zu reduzieren», erklärte A. A. Leuppi-Taegtmeyer.
Nr. 2: Clarithromycin und Statine
Dazu ein Fallbeispiel: Eine 78-jährige Frau stellt sich einige Tage nach einem Spitalaufenthalt wegen einer Pneumonie mit Schwäche auf dem Notfall vor. Die ältere Dame leidet an einer koronaren Herzkrankheit und einer arteriellen Hypertonie. Ihre aktuelle Medikation umfasst: Acetylsalicylsäure 100mg, Bisoprolol 2,5mg, Irbesartan/Hydrochlorothiazid 150/12,5mg und Simvastatin 20mg. Bei der Aufnahme zeigt das Labor eine CK von 4160U/l im Blut. Der CK-Vergleichswert bei Spitalentlassung vor zwei Wochen fiel normwertig aus (<200U/l).
Was war passiert? Während ihrer Hospitalisation hatte die Patientin zur Behandlung der Pneumonie für die Dauer von sieben Tagen eine antibiotische Therapie mit Clarithromycin und Amoxicillin erhalten. Clarithromycin ist ein starker Hemmer des Cytochroms P4503A4 (CYP3A4) und des Transportproteins OATP1B1, wodurch die Aufnahme von Simvastatin in die Leber und die Metabolisierung verhindert werden. Die Folge war ein signifikanter Anstieg der systemischen Simvastatinkonzentration. Im Falle von Simvastatin in Kombination mit Clarithromycin kann die Exposition um bis das Fünffache ansteigen, wodurch das Risiko für eine Rhabdomyolyse signifikant erhöht ist. Zudem ist die Wirkung des Statins nicht mehr gewährleistet.
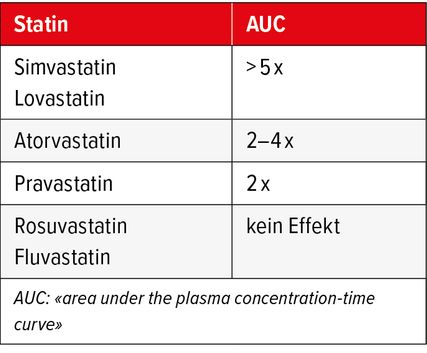
Tab. 1: Zunahme der systemischen Statinexposition bei einer Therapie mit Makrolidantibiotika wie Clarithromycin oder Erythromycin (adaptiert nach Hougaard Christensen MM et al. 2020)2
Nicht alle Statine werden gleich verstoffwechselt. «Die allermeisten Statine werden über den OATP1B1-Transporter in die Leber aufgenommen, bei einigen besteht zusätzlich eine Beteiligung von CYP3A4 bei der Metabolisierung», so die Pharmakologin. Das Ausmass der Arzneimittelinteraktion bei geichzeitiger Anwendung von Clarithromycin ist also abhängig davon, welches Statin eingenommen wird (Tab. 1).2
Die Empfehlung der Pharmakologin, um das Auftreten der beschriebenen Interaktion zu vermeiden, lautete:
-
Kombinationen von Clarithromycin mit Simvastatin, Lovastatin oder Atorvastatin vermeiden. Alternativ sollte geprüft werden, ob die Statintherapie während der Gabe von Clarithromycin und bis zu 2 Wochen nach Therapieende pausiert werden kann.
-
Pravastatin, Rosuvastatin und Fluvastatin sind in geringerem Ausmass von der Interaktion betroffen. Bei gleichzeitiger Gabe von Clarithromycin ist Vorsicht geboten. Eine engmaschige Überwachung bezüglich unerwünschter Arzneimittelwirkungen wird empfohlen.
-
Alternatives Makrolidantibiotikum einsetzen, z.B. Azithromycin.
Nr. 3: Johanniskraut
Johanniskraut (Hypericum perforatum) ist auch als OTC-Produkt erhältlich und wird oft gegen saisonale Depressionen eingenommen. Die aktiven antidepressiven Wirkstoffe sind Hypericin und Hyperforin, wobei Letzteres für das Auftreten von Interaktionen verantwortlich ist. Hyperforin induziert die Aktivität verschiedener Cytochrome und kann zu einem Wirkungsverlust von zahlreichen Medikamenten führen, wie z.B. von Antikonzeptiva, Coumarinen, direkten oralen Antikoagulanzien (DOAK), Ciclosporin, Digoxin, antiretroviralen und antitumoralen Therapien (Irinotecan, Imatinib).
«Da einige Johanniskrautpräparate frei verkäuflich sind, weiss man oft nicht, dass die Patienten solche einnehmen», sagte A.A. Leuppi-Taegtmeyer. Die plötzliche Abstossungsreaktion bei einer Patientin nach Organtransplantation, die zuvor mit Ciclosporin als immunsuppressiver Therapie gut eingestellt war, sorgte deshalb für Überraschung. Auf Nachfrage berichtete die Patientin, dass sie wegen einer saisonalen Depression in den Wintermonaten ein Johanniskrautpräparat eingenommen hatte. Die Interaktion ist in der Zwischenzeit gut bekannt. Seit einigen Jahren ist zudem mit Rebalance® ein Johanniskrautpräparat auf dem Markt erhältlich, das reich an Hypericin und arm an Hyperforin ist. Im zugelassenen Dosierungsbereich ist für dieses Präparat eine antidepressive Wirkung ohne Auftreten der unerwünschten Enzyminduktion nachgewiesen.
Weitere bekannte starke Enzyminduktoren, die häufig eingesetzt werden, sind Rifampicin und Carbamazepin. «Bevor man diese Substanzen neu mit bestehenden Medikamenten kombiniert, ist ein Interaktionscheck empfehlenswert», sagte die Spezialistin.
Nr. 4: Digoxin und Amiodaron
Auch hier ein Fallbeispiel: Ein 81-jähriger Mann, polymorbid, wird wegen einer zunehmenden Verschlechterung des Allgemeinzustands seit 2 Wochen, Appetitlosigkeit, Schwäche, Schwindel und eines Gewichtsverlusts von 11 Kilogramm hospitalisiert. Er ist polymediziert: Zuoberst auf der Medikamentenliste stehen Digoxin und Amiodaron – die Therapie mit Amiodaron wurde eine Woche vor dem Spitaleintritt begonnen. Bei der Aufnahme ist er afebril und örtlich desorientiert, was für ihn ungewöhnlich ist. Er hat einen Schrittmacher in situ, eine Herzfrequenz von 80 Schlägen pro Minute und einen arteriellen Blutdruck von 95/50mmHg. Die Laboranalyse zeigt eine eingeschränkte Nierenfunktion und einen supratherapeutischen bzw. toxischen Digoxinspiegel (4,2nmol/l). Vor dem Beginn der Amiodarontherapie waren die Digoxinspiegel im therapeutischen Bereich (0,7–1,1nmol/l).
Verursacht wurde die Situation durch die Kombination von Digoxin und Amiodaron, die um die renale Ausscheidung konkurrieren. Amiodaron hemmt die Ausscheidung von Digoxin: Die Folge ist ein Anstieg des Digoxinspiegels. Diese Interaktion lässt sich durch eine deutliche Reduktion der Digoxindosis und engmaschige Kontrollen des Digoxinspiegels vermeiden.
Ein weiteres Beispiel für ein erhöhtes Toxizitätsrisiko, das durch eine Änderung der renalen Ausscheidung verursacht wird, ist die Kombination von Lithium und nichtsteroidalen Antirheumatika (NSAR). Ebenso wird dieser Interaktionsmechanismus bei hohen Dosen Methotrexat (MTX) kombiniert mit Amoxicillin postuliert. «Bei niedrig dosiertem MTX und Amoxicillin-Dosen, die bei leichten bis mittelschweren Infektionen angewendet werden, sehen wir diese Interaktion in der Regel nicht.»
Nr. 5: Methotrexat und Metamizol
Ein 67-jähriger Mann wird aufgrund einer Sepsis und mit einer respiratorischen Globalinsuffizienz auf der Intensivpflegestation hospitalisiert. Die Vorgeschichte zeigt eine rheumatologische Erkrankung, die seit mehreren Jahren mit MTX (1x wöchentlich 15mg s.c.) behandelt wird, eine arterielle Hypertonie und eine Dyslipidämie. Wegen anhaltender Schmerzen unter Opioiden und Pregabalin hat er in den letzten 2 Wochen zusätzlich das Pyrazolderivat Metamizol erhalten. Das Labor zeigt eine schwere Panzytopenie und eine eingeschränkte Nierenfunktion (eGFR von 35ml/min/1,73m2).
Die Ursache der Panzytopenie war möglicherweise eine pharmakodynamische und pharmakokinetische Interaktion: Die Kombination von MTX und Metamizol führt zu einer additiven Knochenmarksuppression. Zusätzlich ist eine verminderte renale Ausscheidung von MTX wahrscheinlich, was wiederum das Hämatotoxizitätsrisiko erhöht.
«Die Kombination von MTX und Metamizol hat ein hohes Interaktionspotenzial und kann zu einem schwerwiegenden Krankheitsverlauf führen», sagte die Pharmakologin. Eine Studie von 2015, die die Pharmakovigilanz-Daten in der gesamten Schweiz analysierte, beziffert die Zahl der tödlichen Agranulozytosefälle unter Metamizol auf 7 – 4 Fälle davon waren in Kombination mit MTX aufgetreten.3
Ein wirksames Instrument, um auf solche Fälle aufmerksam zu machen, ist die Pharmakovigilanz-Meldung. In diesem Fall sei die Meldung besonders wichtig, weil die Fachinformationen von MTX und Metamizol inkonsistent seien. Während in der Fachinformation von MTX lediglich darauf hingewiesen wird, dass es bei einer länger andauernden Vorbehandlung mit Pyrazolderivaten zu einer myelosuppressiven Wirkung kommen könne, erwähnt die Fachinformation von Metamizol dagegen explizit die Kombination mit MTX. Wenn man hier etwas ändern will, muss man die beobachteten Fälle bei Swissmedic melden.
Eine Behandlung mit Metamizol wird nicht empfohlen oder ist kontraindiziert bei hämatologischen Grunderkrankungen, myelotoxischen antitumoralen Therapien und bei der Behandlung mit Biologika, bei denen das Auftreten von Leukopenien oder Neutropenien zu den häufigen unerwünschten Nebenwirkungen gehört. Zudem ist bei der Kombination mit diversen antirheumatischen Substanzen und Antibiotika Vorsicht geboten.
Nr. 6: Ibuprofen
Ein 47-jähriger Mann, der aufgrund einer 1-Gefäss-Erkrankung vor 3 Jahren einen ST-Hebungsinfarkt (STEMI) erlitten hat, wird wegen einer In-Stent-Restenose und eines Nicht-ST-Hebungsinfarkts (NSTEMI) des proximalen RIVA erneut hospitalisiert. Wegen Schulterschmerzen unklarer Ätiologie wurde er vor der Spitaleinweisung seit zwei Wochen mit Ibuprofen (4x600mg/d) behandelt. Weiter hatte der Mann Acetylsalicylsäure (ASS 1x100mg/d) und Pantoprazol eingenommen.
Das Auftreten der Restenose ist vermutlich auf die Interaktion zwischen ASS und Ibuprofen zurückzuführen. ASS ist ein irreversibler Cyclooxygenase-1(COX-1)-Inhibitor, der die Thrombozytenaggregation für die gesamte Lebensdauer der Blutplättchen hemmt. Ibuprofen hemmt ebenfalls die Wirkung von COX-1, jedoch nur reversibel. Verabreicht man Ibuprofen vor oder zeitgleich mit ASS, wird die COX-1-Bindungsstelle vorübergehend blockiert. In der Zwischenzeit wird ASS ausgeschieden und die Thrombozytenaggregation bleibt, nachdem die Ibuprofenwirkung aufgehoben ist, ungehemmt. «Die Kombination von ASS und Ibuprofen ist auch aus anderen Gründen, zum Beispiel wegen des erhöhten Blutungsrisikos, nicht empfehlenswert», sagte die Spezialistin. Wenn sich eine Einnahme von beiden Substanzen nicht vermeiden liesse, dann sei es empfehlenswert, zuerst ASS und ca. 2 Stunden später Ibuprofen einzunehmen.
Nr. 7: Methadon und Neuroleptika
Eine 50-jährige Frau hat nach anfallsweiser Atemnot in den letzten drei Nächten jeweils eine kurze Synkope erlitten. Aus der Vorgeschichte sind keine Krampfanfälle bekannt. Auf der Notfallstation kommt es erneut zu zwei kurzen selbstlimitierenden Episoden von Bewusstlosigkeit. Dabei zeigte sich auf dem Monitor eine Torsade-de-pointes-Tachykardie, gefolgt von einer kurzen Kammertachykardie. Die Frau ist im Methadon-Substitutionsprogramm und wird neu seit zwei Wochen mit einem Neuroleptikum (Chlorprothixenhydrochlorid) behandelt. Das EKG zeigt eine Verlängerung der QT-Zeit von 485msec. Der Normwert für Frauen beträgt <450msec, ein QT-Intervall von 450–470 gilt als grenzwertig.
Was war passiert? Methadon führt über die Blockierung der hERG-Kanäle in den Herzmuskelzellen zu einer Destabilisierung des Myokards und zu einer Verlängerung der QT-Zeit. Die Folge kann das Auftreten von Torsades-de-pointes-Tachykardien mit einem erhöhten Risiko für Kammerflimmern sein. Aus diesem Grund ist es wichtig, die Kombination von Methadon mit anderen Medikamenten, die die QT-Zeit verlängern, zu vermeiden. Zu solchen Substanzen gehören Clarithromycin, Chinolone, Neuroleptika, Amiodaron, Domperidon, Ondansetron etc. Bei Patienten und Patientinnen unter Methadon-Substitutionstherapie ist bei Neubeginn einer Medikation immer die Fachinformation zu konsultieren.
Nr. 8: Grapefruit
Vor allem ältere Menschen essen gerne Grapefruits. Der Grund ist das veränderte Geschmacksempfinden im Alter. Dieser ist auf den Verlust des Geschmackssinns von der Zungenspitze zum Zungengrund zurückzuführen und damit in dieser Reihenfolge: süss, salzig, bitter, sauer. Das Geschmacksempfinden für Grapefruit ist bei älteren Menschen länger intakt.
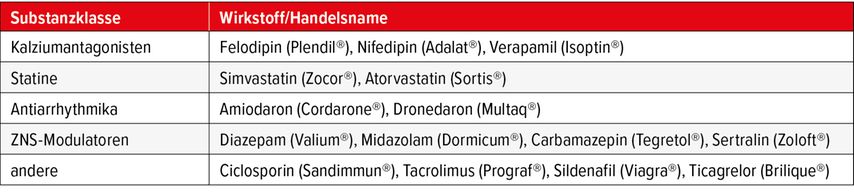
Obwohl Grapefruit die Exposition von diversen CYP3A4-Substraten (Tab. 2) erhöht, sprach sich die Spezialistin dagegen aus, den Genuss der Frucht zu verbieten.4 Besser sei, eine Anamnese zu erheben und dann Medikamente auszusuchen, die nicht so stark mit Grapefruitsaft oder gekochter Grapefruit interagieren.
Tab. 2: Medikamente, deren systemische Exposition durch den Konsum von Grapefruit zunimmt (adaptiert nach Bailey DG et al. 2013)4
Quelle:
SGAIM-Frühjahrskongress, 10. bis 12. Mai 2023, Basel
Literatur:
1 Sahai J et al.: Cations in the didanosine tablet reduce ciprofloxacin bioavailability. Clin Pharmacol Ther 1993; 53: 292-7 2 Hougaard Christensen MM et al.: Interaction potential between clarithromycin and individual statins - a systematic review. Basic Clin Pharmacol Toxicol 2020; 126: 307-17 3 Blaser LS et al.: Hematological safety of metamizole: retrospective analysis of WHO and Swiss spontaneous safety reports. Eur J Clin Pharmacol 2015; 71: 209-17 4 Bailey DG et al.: Grapefruit-medication interactions: forbidden fruit or avoidable consequences? CMAJ 2013; 185: 309-16
Das könnte Sie auch interessieren:
«Planetary Health» – Interaktion von Gesundheit und Klimawandel
Der Klimawandel ist längst bei uns angekommen – in der Schweiz waren die letzten zehn Jahre 2,5°C wärmer als der vorindustrielle Durchschnitt und die Temperaturen steigen weiter an. Dies ...
Eine starke Stimme für die globale Gesundheit
Am Frühjahrskongress der Schweizerischen Gesellschaft für Allgemeine Innere Medizin (SGAIM) sprach die renommierte Soziologin und Politikwissenschaftlerin Ilona Kickbusch über die ...
Nachhaltigkeit im Spital am Beispiel der Radiologie
Betrachtet man das weltweite Gesundheitssystem als Land, liegt es in der globalen Rangliste der Länder mit den höchsten CO2-Emissionen nach China, den USA, Indien und Russland auf Platz 5.1 Innerhalb eines Spitals gehört die Radiologie zu den ...