Offene Nierenteilresektion – bereits eine historische Operation?
Autor:
Univ.-Doz. Dr. Michael Rauchenwald
Facharzt für Urologie und Andrologie, Klagenfurt
E-Mail: m.rauchenwald@aon.at
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit diesem Titel habe ich bereits 2006 einen Vortrag gehalten – damals noch im Vergleich zur laparoskopischen Technik, die doch einige Einschränkungen aufwies und nur für ausgewählte Tumoren gut geeignet erschien. Heute ist diese Frage durch die breite Verfügbarkeit der robotisch assistierten Technik eher mit „ja“ zu beantworten.
Keypoints
-
Durch die breite Verfügbarkeit der robotisch assistierten Technik ist die offene Nierenteilresektion eher als historisch zu sehen.
-
Nierentumoren sind in offener Technik in nahezu allen Lokalisationen organerhaltend zu operieren.
-
Tumoren imponieren im CT meist ausgedehnter als intraoperativ, sodass mehr Nierengewebe erhalten werden kann als aufgrund der Bildgebung zu vermuten wäre.
Durch die zunehmend seltenere Anwendung der offenen Technik erscheint es sinnvoll, die eigenen Erfahrungen in der nun über 30-jährigen Anwendung dieser Technik für Interessierte festzuhalten.
Präoperativ ist es wichtig, sich in erster Linie anhand des CTs die Lage, Größe und Beziehung des Tumors zu kritischen Strukturen zu visualisieren – wie sieht die Gefäßversorgung aus?
Lagerung
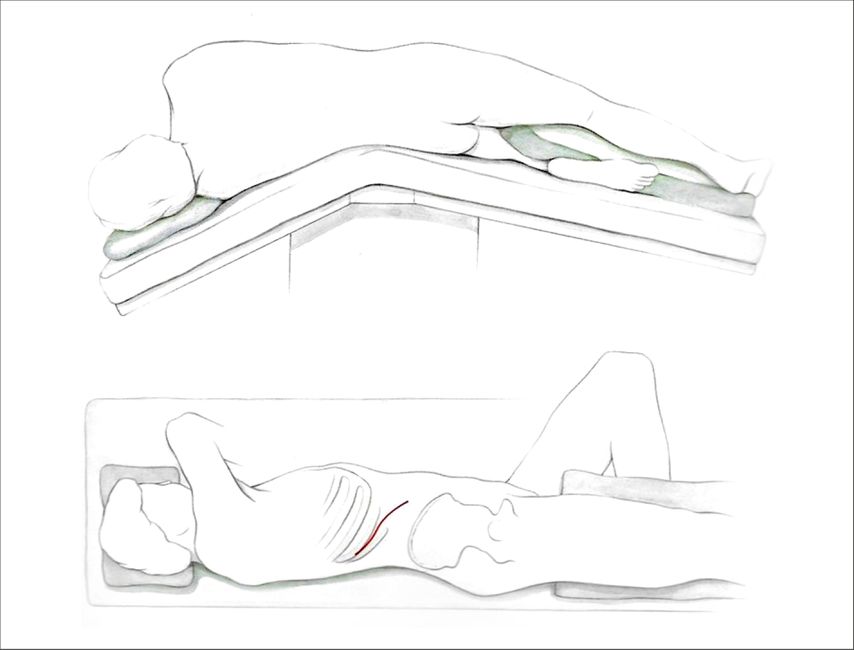
Die Operation erfolgt in strenger, zur tumortragenden Niere kontralateraler Seitenlage mit einem Ballon unter dem Rippenbogen und Abknicken des Tisches zur Überstreckung – der obere Arm wird unter leichtem Zug nach vorne auf einer Schiene gelagert, die gleichseitige Hüfte wird nach hinten gespannt und mit einem Gurt fixiert, damit der Raum zwischen Rippenbogen und Darmbeinkamm aufgeht (Abb. 1).
Zugang
Der Zugang erfolgt im 11. Interkostalraum mit einer Inzision über der Spitze bzw. dem Ende der 12. Rippe und in Verlängerung derselben nach ventral distal mit dem Skalpell durch Haut und Subkutis bis auf die Faszie. Mit dem Kauter werden die Fasern des Musculus obliquus externus abdominis bzw. dorsal eventuell auch noch teilweise des distalen M. latissimus dorsi bis auf den Rippenknochen bzw. von der Spitze der 12. Rippe in Verlängerung der Oberkante der Rippe (= interkostal) nach ventral der M. oliquus externus und darunter der M. internus abdominis durchtrennt. Dann erfolgt mit dem Skalpell die vorsichtige Inzision der Faszie des M. transversus abdominis und dann ein stumpfes Auseinanderdrängen der Muskelfasern dieser innersten Schicht.
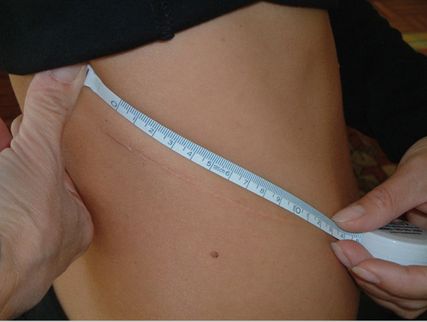
Mit diesem Zugang ist praktisch immer eine Resektion der 12. Rippe zu vermeiden. Der Schnitt kann je nach Konstitution des/der Patient:in relativ klein gehalten werden (Abb. 2).
Präparation der Niere
Es folgt ein stumpfes Abschieben des Peritoneums nach medial und distal sowie der Pleura mit dem Finger bzw. einem Stieltupfer im laterokranialen Wundwinkel. Vorsichtige Inzision der Interkostalmuskulatur im dorsokranialen Wundwinkel unmittelbar an der Oberkante der Rippe. Einsetzen eines Wundspreitzers bzw. Bauchdeckenhalters bevorzugt nach Ricard oder Holzbach mit den jeweils großen Branchen unter Unterlegung mit einem gefalteten feuchten Bauchtuch.
Spannen der Gerota’schen Faszie und parallel zum Rand des Musculus psoas ca. 1cm ventral desselben Inzision der Faszie mit dem Skalpell – weiteres Spalten der Faszie nach kranial und distal mit der Schere unter Beachtung der retroperitoneal verlaufenden Nerven. Es ist wichtig, die Nerven zu schonen, um eine postoperative Muskelatonie der Flanke („Brotlaib“) zu vermeiden.
Mobilisation der retrorenalen Nierenfettkapsel distal des meist bereits tastbaren oder sichtbaren unteren Nierenpols und Aufsuchen und Darstellen des proximalen Harnleiters. Vorsichtiges Umfahren und Anschlingen desselben mit einem (gelben) Vesselloop unter Schonung der begleitenden Gefäße. Nun dorsal der Niere Spalten der Fettkapsel und Eingehen auf die Rückfläche der Niere. Fassen der „oberen“ Lefze der Fettkapsel mit einer Triangel- oder runden Lungenfasszange und damit Spannen des Gewebes und Anheben der Niere. Scharfes und, wenn möglich, stumpfes Abpräparieren der Fettkapsel von der fibrösen Nierenkapsel. Hierbei Belassen von Teilen der Fettkapsel direkt über dem die Niere überragenden Tumoranteil. Komplettes Freilegen der gesamten Niere bis an den Hilus. Identifizieren der Nierenarterie(n) von dorsal-kranial kommend. Mobilisieren und Anschlingen des Arterienhauptstamms mit einem (roten) Vessellloop, wobei genug Platz für das Ansetzen eines Gefäß-Bulldogs geschaffen werden muss. Am besten von ventral (bzw. von wo immer am besten zugänglich) Darstellen und Anschlingen des Venenhauptstamms mit einem (blauen) Vesselloop, der doppelt um die Vene geschlungen wird, um diese später damit drosseln zu können. Die subtile Präparation des Gefäßstiels ist wichtig, um kein weiteres arterielles Gefäß zu übersehen, welches später bei der Tumorresektion zu einer die Übersicht beeinträchtigenden Blutung führen könnte.
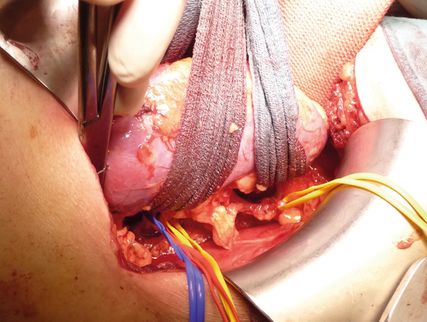
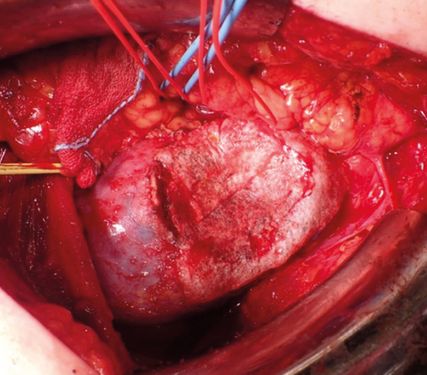
Abb. 3: Die Niere wird schonend und übersichtlich aus der Wunde gehoben
Wenn man mit einem genähten Tupfer-Streifen („Schauta-Tuch“) mit einer Schlinge jeweils den oberen und unteren Nierenpol umschlingt und alle 4 Streifenteile mit einer Klemme fasst, kann man die gesamte Niere schonend und übersichtlich aus der Wunde herausheben (Abb. 3).
Tumorresektion
Speziell bei hilusnahen, zentralen Tumoren sollte eine subtile und ausgiebige Präparation bis in den Hilus erfolgen. Von dorsal kann man über dem Nierenbecken gut unter die dorsale Parenchymlefze präparieren und diese quasi unterfahren. Von ventral muss man entlang der Gefäße sehr vorsichtig vorgehen. Als nächster Schritt erfolgt die intravenöse Gabe von ca. 100ml 20% Mannit zur Nephroprotektion. Außerdem wird Crashed Ice in einem sterilen Plastiksackerl zum externen Kühlen vorbereitet. Hierzu wird der Inhalt eines gefrorenen Beutels mit steriler physiologischer NaCl-Lösung mit dem Hammer zerkleinert.
Markieren der Resektionslinie mit dem Kauter ca. 1mm vom Tumorrand entfernt. Intrarenal gelegene Tumoren können intraoperativ mit Ultraschall (Small-Parts-Linear-Schallkopf) lokalisiert werden und am darüberliegenden Parenchym mit dem Kauter markiert werden.
Klemmen der Nierenarterie(n) nach der intravenösen Mannitgabe mit einem Gefäß-Bulldog. Ca. 1min später Drosseln der Vene durch Anspannen des doppelt umschlungenen Vesselloops. Nun sollte die Niere deutlich Abblassen. Wenn möglich sofort nach Klemmen der Arterie ventral und dorsal Platzieren eines „flachen“ Sackerls mit dem sterilen Crashed Ice zur Oberflächenkühlung.
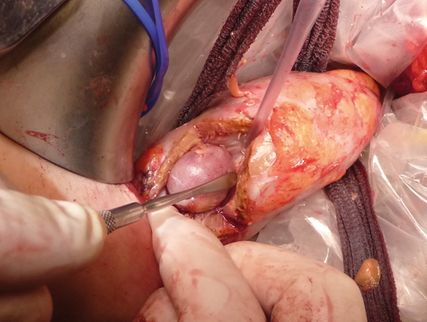
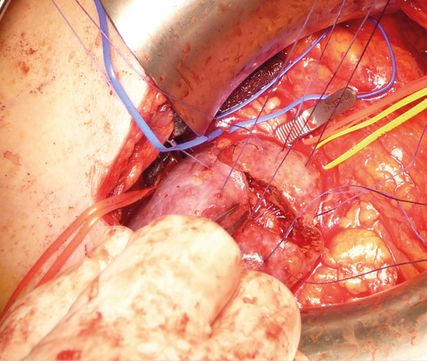
Abb. 4: Stumpfes Mobilisieren des Tumors im gesunden umgebenden Gewebe und Durchtrennen von Gefäßen
Oberflächliche Inzision des gesunden Nierengewebes entlang der markierten Linie mit dem Kauter. Dann mit einem Hirnspatel bzw. flachen Dissektor stumpfes Mobilisieren des Tumors im gesunden umgebenden Gewebe, wobei auftauchende Gefäße vor allem zum verbleibenden Nierengewebe hin bipolar koaguliert, „größere“ Gefäße durchtrennt und mit 4–0 Monocryl umstochen werden (Abb. 4).
Nach allseitigem „Ausschälen“ des Tumors im gesunden Nierengewebe, Absetzen über einer zarten Klemme in der Tiefe oder Umstechung der Absetzungsstelle. Zentrale Tumoren werden vom Nierenbecken und den größeren Gefäßen möglichst abgelöst. Ein eröffnetes Hohlraumsystem wird mit 4–0 Monocryl 2-reihig fortlaufend verschlossen und die Dichtigkeit überprüft, indem das Hohlraumsystem retrograd, über eine oberhalb des angespannten gelben Vesselloops in den Nierenbecken-Harnleiter-Übergang eingestochene dünne Subkutannadel mit ca. 5ml verdünnter Betaisodona-Lösung gefüllt wird. BI-Lösung kann abgespült werden, Methylenblau würde alles intensiv einfärben. Bei sehr breiter Eröffnung des Hohlraumsystems ist es ratsam, gleich antegrad eine Doppel-J-Harnleiterschiene über diese Öffnung einzulegen.
Nach Absetzen des Tumors kann am Tumorgrund oder an Stellen, wo der Verdacht entstand, dass die Tumorkapsel verletzt worden wäre, ein Kontrollschnitt entnommen werden. Versorgen weiterer Gefäßlumina mit gezielten Umstechungen.
Abschluss der Operation
Eröffnen des venösen Blutstroms durch Lockern des Vesselloops und weitere Umstechung bei Bedarf. Entscheidung zum lediglichen Auskleben der Resektionsfläche mit einem oder mehreren Tachosil-Vliesen oder Verschluss der Nierenwunde durch möglichst spannungsfreie Adaptation der Resektionsflächen mittels parenchymdurchgreifender 1er oder 2er PDS-Nähte mit großer CT-1-Nadel. Letztere Methode hat den Vorteil der besseren Abdichtung auch des Hohlraumsystems bei dem Nachteil von mehr geschädigten Nephronen. Wichtig ist, die Nahtlinie so zu legen und die Parenchymränder so zu adaptieren, dass die geringste Spannung auf das Nierengewebe kommt. Vor Spannen der im Abstand von 8–10mm gelegten Nähte Unterlegen derselben in der Tiefe der Wunde mit einem Tabotamp-Röllchen und Ausfüllen der Wunde mit Floseal oder einem vergleichbaren Hämostyptikum. Gleichmäßiges Spannen der Nähte und Knüpfen derselben von den Ecken der Naht kommend.
Eröffnen auch des arteriellen Blutstroms und Notieren der Ischämiezeit, die unter 30min bleiben sollte. Allerdings sind eine saubere Resektion im Gesunden und eine subtile Blutstillung wichtiger als das exakte Einhalten dieser Zeitgrenze. Neuerliche Gabe von Mannit – 2. Hälfte der Infusionsflasche von 200ml.
Das Auskleben der Resektionsfläche ist sicher die nephronsparendste Methode. Bei arteriellen Blutungen von der auszuklebenden Resektionsfläche müssen weitere gezielte Umstechungen gesetzt werden. Geringe venöse Blutungen stehen üblicherweise durch das Abkleben.
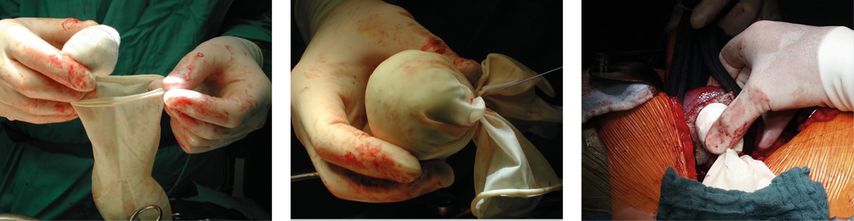
Ein Tachosil-Vlies von entsprechender Größe, es sollte allseits den Resektionsrand um ca. ¾–1cm überlappen, erst beim Auflegen gut anfeuchten und in den Resektionstrichter anmodellieren und mindestens 3min mit einem „Stempel“ anpressen. Der „Stempel“ wird durch Füllen eines sterilen OP-Handschuhs mit Kugeltupfern in Größe des entfernten Tumors geformt, wobei meist am besten der „Daumen“ des Handschuhs geeignet ist. Damit wird garantiert, dass das Vlies allseits gut angepresst wird (Abb. 5). Dabei muss eine ausreichende Befeuchtung durch Überschütten mit steriler Kochsalzlösung garantiert sein. Am Ende der Anpresszeit den „Stempel“ vorsichtig entfernen und dabei mit dem Rücken einer Pinzette das Vlies niederhalten (Abb. 6).
Abb. 5: Der „Stempel“ wird durch Füllen eines sterilen OP-Handschuhs mit Kugeltupfern in Größe des entfernten Tumors geformt
Abb. 6: „Stempel“ vorsichtig entfernen und das Vlies vorsichtig niederhalten
Bei unzureichender Blutstillung eventuell Anpresszeit verlängern und/oder mit einem weiteren Vlies ergänzen. Wenn das Vlies deutliche „Blasen“ aufwirft, muss es nochmals entfernt werden und die Blutungsquelle gesucht und umstochen werden.
Auch bei Nahtverschluss des Parenchyms kann die Nahtlinie mit einem Tachosil-Vlies abgedeckt werden, um Stichkanalblutungen zu stoppen (Abb. 7). Die Niere wird in ihre Loge reponiert und die Fettkapsel darüber locker adaptiert, wobei bei lediglich ausgeklebter Nierenwunde ein Teil der Fettkapsel in die Vertiefung eingefügt und die Kapsel darüber verschlossen werden sollte. Hinter die Niere Einlegen eines Blake-Drains und Wundverschluss durch 2-schichtige Adaptation der Muskulatur (tiefe Schicht = Mm. transversus et obliquus internus bzw. oberflächliche Schicht = M. obliquus externus) mit sogenannten Flaschenzugnähten, die die Muskelränder einerseits gut adaptieren und die Durchblutung andererseits nicht zu sehr abschnüren.
Fazit
Aus meiner Sicht ist es mit dieser Methode möglich, Nierentumoren in nahezu allen Lokalisationen organerhaltend zu operieren. Erfahrungsgemäß imponieren die Tumoren im CT ausgedehnter als intraoperativ, sodass meist viel mehr Nierengewebe erhalten werden kann als aufgrund der Bildgebung zu vermuten wäre.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Korrelation von Stoffwechselmetaboliten mit bildmorphologischen, genetischen und biologischen Markern bei Verdacht auf ein Prostatakarzinom
Das Prostata-spezifische Antigen (PSA), die multiparametrische Magnetresonanztomografie (mpMRT) der Prostata und seltener noch der Prostate-Cancer-Antigen-3-Test (PCA-3) haben sich als ...
Netzwerk-Metaanalyse zur Integration der ARANOTE-Daten
Die Therapie des metastasierten hormonsensitiven Prostatakarzinoms befindet sich in einem dynamischen Wandel. Mit der Integration der ARANOTE-Daten in eine aktuelle Netzwerk-Metaanalyse ...
„Low-carb“, „high-protein“ oder vegane Ernährung: Risiko oder Benefit?
Wer sich heute mit Ernährung beschäftigt, kommt an den Schlagwörtern „low-carb“, keto, „high-protein“ oder vegan kaum vorbei. Fitness- und Lifestyle-Influencer und zunehmend auch ...