Erstlinientherapie des metastasierten, klarzelligen Nierenzellkarzinoms
Autorin:
A.o. Univ.-Prof. Dr. Manuela Schmidinger
Universitätsklinik für Urologie
Medizinische Universität Wien
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
In den letzten 5 Jahren haben sich Immuncheckpoint-Inhibitor(ICI)-Kombinationen in der Erstlinientherapie des metastasierten, klarzelligen Nierenzellkarzinoms (RCC) als Therapiestandard durchgesetzt. Mittlerweile stehen vier verschiedene Therapieoptionen zur Verfügung. Jede davon wurde aufgrund ihrer Überlegenheit gegenüber Sunitinib im Gesamtüberleben (OS) und/oder progressionsfreien Überleben (PFS) und in der objektiven Remissionsrate (ORR) zugelassen.
Keypoints
-
Alle ICI-Kombinationstherapien verlängern im Vergleich zu Sunitinib das Überleben in der ITT-Population und bei Patienten mit intermediär-ungünstigem Risiko.
-
Bei Patienten mit günstigem IMDC-Risiko konnte bislang keine ICI-Kombination das Überleben verbessern.
-
Doppelt so viele Komplettremissionen mit ICI-Kombination sollten Anlass genug sein, (nahezu) alle Patienten mit einer ICI(bzw. mit einer ICI-TKI)-Kombination zu behandeln.
-
Die beste Therapiewahl kann wegen fehlender Vergleichsstudien und unterschiedlicher Populationen/Beobachtungszeiträume nur schwer definiert werden.
-
Derzeit sind klinische Faktoren wie Remissionsdruck, Differenzierungsgrad, Inflammationsstatus, Metastasenlokalisationen und Toxizitätsprofile therapieentscheidend.
-
Ausständige Daten müssen ehebaldigst zur Verfügung gestellt werden.
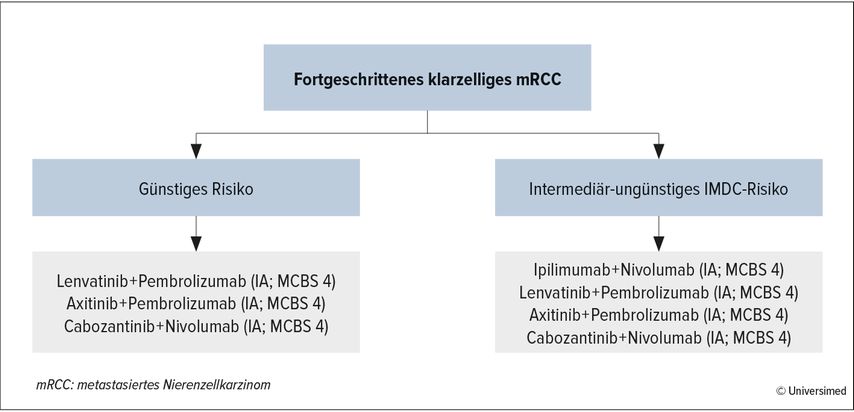
Für Patienten mit günstigem International-Metastatic-Renal-Cell-Carcinoma-Database-Consortium(IMDC)-Risiko1 gibt es drei mögliche Therapiekombinationen zur Auswahl. Diese bestehen aus einem Tyrosinkinase-Inhibitor (TKI) und einem PD-1-Inhibitor: Lenvatinib+Pembrolizumab, Axitinib+Pembrolizumab oder Cabozantinib+Nivolumab. Für Patienten mit intermediärem oder ungünstigem IMDC-Score bestehen diese drei Optionen ebenfalls und darüber hinaus noch die Möglichkeit einer dualen ICI-Inhibition, bestehend aus dem PD-1-Inhibitor Nivolumab in Kombination mit dem CTLA4-Inhibitor („cytotoxic T lymphocyte associated protein 4 inhibitor“) Ipilimumab. Der Therapiealgorithmus wird in den ESMO-Leitlinien2 (European Society for Medical Oncology) dargestellt (Abb. 1).
Aufgrund von wenigen Vergleichsstudien zwischen diesen insgesamt vier Optionen werden die Studienergebnisse oft indirekt miteinander verglichen. Hierbei muss aber bedacht werden, dass sich die Nachbeobachtungszeit zwischen den einzelnen Studien erheblich unterscheidet und dass auch die Populationen zum Teil schwer vergleichbar waren. In den Studien mit Lenvatinib+Pembrolizumab oder Axitinib+Pembrolizumab waren deutlich mehr Patienten mit günstigem IMDC-Risiko als in den beiden anderen Studien mit Nivolumab+Ipilimumab oder Nivolumab+Cabozantinib (32% und 31% vs. jeweils 23%). In beiden Studien mit Pembrolizumab waren auch weniger Patienten mit zwei oder mehr Organen mit Metastasen vertreten (71,7% und 73% vs. 79% und 80%).
Nachbeobachtungszeit & OS in „Intention to treat“(ITT)-Population
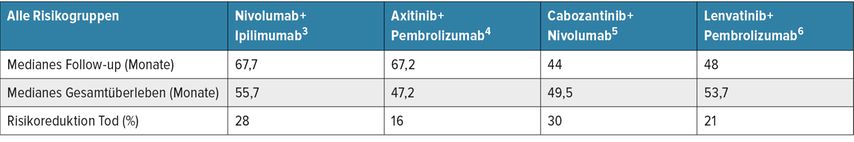
Das mediane Überleben in der ITT-Population kann bei allen vier Kombinationen mehr oder weniger verglichen werden und beträgt zwischen 47,2 und 55,7 Monaten (Tab.1). Die größte Risikoreduktion bezüglich Tod wurde bei den Kombinationen Nivolumab+Cabozantinib (30%) und Nivolumab+Ipilimumab (28%) beobachtet.
Medianes PFS, Ansprechraten und Ansprechdauer in ITT-Population
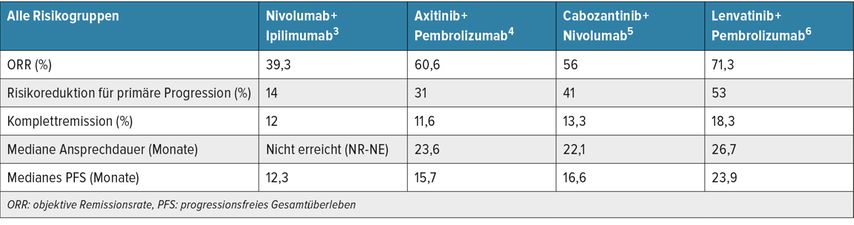
Aus der tabellarischen Darstellung des medianen PFS, der Ansprechraten und der Dauer des Ansprechens in der ITT-Population (Tab. 2) wird ersichtlich, dass mit einer TKI-ICI-Kombination zwar im indirekten Vergleich höhere Remissionsraten erreicht wurden, Komplettremissionen wurden aber mit allen vier Therapiemöglichkeiten erzielt und die Dauer des Ansprechens erscheint mit Abstand am besten mit der dualen ICI-Kombination – hierbei ist nach einer medianen Beobachtungszeit von 67,7 Monaten die mediane Ansprechdauer noch nicht erreicht.
Ergebnisse in der intermediär-ungünstigen Population
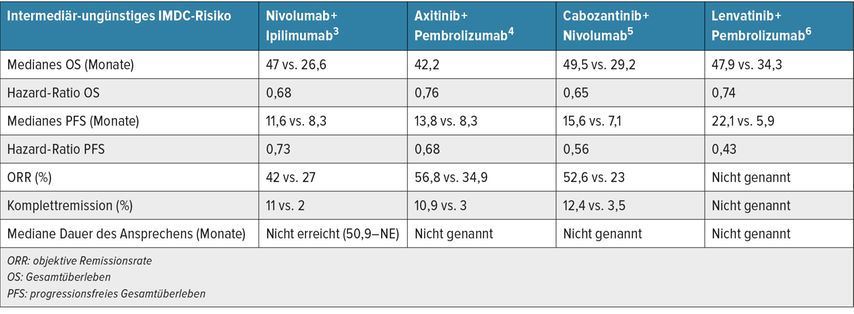
In den Ergebnissen für Überleben, Ansprechrate, Dauer des Ansprechens und PFS der intermediär-ungünstigen Population (Tab. 3) fällt auf, dass die Risikoreduktion in Bezug auf Tod am besten für Nivolumab+Ipilimumab (HR:0,68) und Nivolumab+Cabozantinib (HR:0,65) ausfällt. ICI-TKI-Kombinationen sind hingegen besser als duale ICI-Kombinationen bezogen auf das längere PFS und auch die höhere Ansprechrate. Leider werden einige wichtige Daten nicht berichtet, obgleich diese vorhanden sein müssen. Darunter fallen Remissionsraten und Komplettremissionsraten in der intermediär-ungünstigen Population mit Lenvatinib+Pembrolizumab und weiters die Dauer des Ansprechens mit allen TKI-ICI-Kombinationen. Hier liegen nur Daten für die duale ICI-Kombination vor. Wenn Daten nicht gezeigt werden, gewinnt man schnell den Eindruck, sie sollen bewusst nicht gezeigt werden, was die Euphorie über die initialen Ergebnisse ein wenig reduziert.
Tab. 3: Überleben, Ansprechrate, Dauer des Ansprechens und PFS in der intermediär-ungünstigen Population3–6
Ergebnisse in der Population mit günstigem IMDC-Risiko
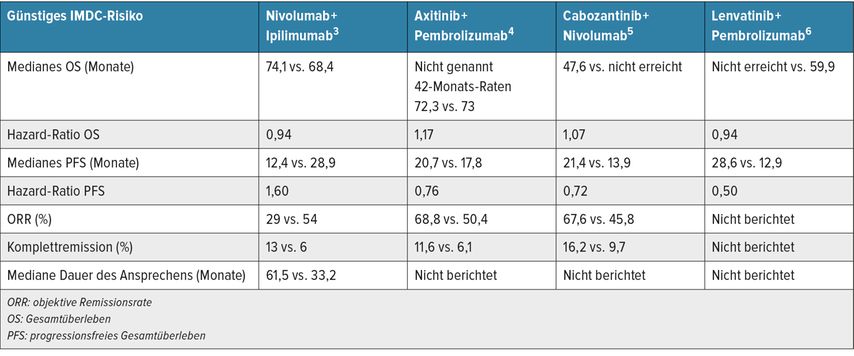
Die tabellarische Darstellung der Ergebnisse für die Population mit günstigem IMDC-Risiko (Tab. 4) zeigt keinen Überlebensvorteil der neuen ICI-Kombinationen gegenüber Sunitinib. TKI-ICI-Kombinationen sind jedoch in Bezug auf das PFS und die Remissionsrate besser. Wenn man aber die Komplettremissionsrate betrachtet, so ist sie bei allen ICI-Kombinationen, selbst bei dualer ICI-Kombination, höher als bei Sunitinib. Wie schon zuvor angemerkt ist es bedauerlich, dass die Dauer des Ansprechens für die drei ICI-TKI-Kombinationen bislang nicht gezeigt wurde.
Tab. 4: Überleben, Ansprechrate, Dauer des Ansprechens und PFS in der Population mit günstigem IMDC-Risiko3–6
Sicherheitsprofile im indirekten Vergleich
Die Toxizitätsprofile der vier Kombinationen unterscheiden sich sichtlich voneinander. Bei der dualen ICI-Kombination stellen die vier Gaben Ipilimumab oft eine Herausforderung dar und dabei ist auch der Bedarf an Hochdosiskortikosteroiden am höchsten (30%). Dafür ist die Erhaltungsphase danach mit einer Nivolumab-Monotherapie vergleichsweise einfach. Bei den ICI-TKI-Kombinationen stellt die permanente Gabe des TKI wiederum die Herausforderung dar, weswegen man im klinischen Alltag bei gutem Ansprechen oft zu einer Therapiedeeskalation übergeht, die entweder eine TKI-Dosisreduktion beinhaltet oder sogar das Weglassen des TKI.
Fazit
Insgesamt muss festgehalten werden, dass diese Therapien in die Hände eines erfahrenen Betreuers mit hohen Fallzahlen gehören, denn das frühzeitige Erkennen von Toxizitäten und die korrekte und zeitnahe Intervention sind von erheblicher Bedeutung.
Literatur:
1 Heng DY et al.: External validation and comparison with other models of the International Metastatic Renal-Cell Carcinoma Database Consortium prognostic model: a population-based study. Lancet Oncol 2013; 14(2): 141-8 2 Powles T et al.: ESMO Clinical Practice Guideline update on the use of immunotherapy in early stage and advanced renal cell carcinoma. Ann Oncol 2021; 32(12): 1511-9 3 Motzer RJ et al.: Conditional survival and long-term efficacy with nivolumab plus ipilimumab versus sunitinib in patients with advanced renal cell carcinoma. Cancer 2022; 128(11): 2085-97 4 Rini BI et al.: Pembrolizumab plus axitinib versus sunitinib as first-line therapy for advanced clear cell renal cell carcinoma: 5-year analysis of KEYNOTE-426. J Clin Oncol 2023; 41(17): Abstract No. LBA4501 5 Burotto M et al.: Nivolumab plus cabozantinib vs sunitinib for first-line treatment of advanced renal cell carcinoma (aRCC): 3-year follow-up from the phase 3 CheckMate 9ER trial. J Clin Oncol 2023; 41(6): Abstract No. 603/Erratum 6 Motzer RJ et al.: Final prespecified overall survival (OS) analysis of CLEAR: 4-year follow-up of lenvatinib plus pembrolizumab (L+P) vs sunitinib (S) in patients (pts) with advanced renal cell carcinoma (aRCC). J Clin Oncol 2023; 41(16): Abstract No. 4502
Das könnte Sie auch interessieren:
Korrelation von Stoffwechselmetaboliten mit bildmorphologischen, genetischen und biologischen Markern bei Verdacht auf ein Prostatakarzinom
Das Prostata-spezifische Antigen (PSA), die multiparametrische Magnetresonanztomografie (mpMRT) der Prostata und seltener noch der Prostate-Cancer-Antigen-3-Test (PCA-3) haben sich als ...
Netzwerk-Metaanalyse zur Integration der ARANOTE-Daten
Die Therapie des metastasierten hormonsensitiven Prostatakarzinoms befindet sich in einem dynamischen Wandel. Mit der Integration der ARANOTE-Daten in eine aktuelle Netzwerk-Metaanalyse ...
„Low-carb“, „high-protein“ oder vegane Ernährung: Risiko oder Benefit?
Wer sich heute mit Ernährung beschäftigt, kommt an den Schlagwörtern „low-carb“, keto, „high-protein“ oder vegan kaum vorbei. Fitness- und Lifestyle-Influencer und zunehmend auch ...