Neue Therapien und Impfansprechen bei Autoimmunerkrankungen
Bericht:
Mag. Irene Senn, PhD
Bereits zum zweiten Mal fand der Wachauer Rheumatag als Online-Veranstaltung statt. Das Programm spiegelte die breite Vielfalt der Rheumatologie wider. Im Mittelpunkt standen wichtige Neuerungen bei der Therapie der Psoriasisarthritis, der Osteoporose sowie verschiedener Kollagenosen. Besonders großes Interesse weckten die aktuellen Studiendaten rund um den Einsatz von SARS-CoV-2-Impfstoffen bei Personen mit rheumatologischen Erkrankungen.
Spannende Diskussionen, kritisches Hinterfragen und konstruktive Gespräche – dafür steht der Wachauer Rheumatag seit vielen Jahren. „Dass das Interesse an der Rheumatologie groß ist, bestätigen uns die 540 angemeldeten Teilnehmer“, zeigte sich der wissenschaftliche Leiter, Doz. Dr. Burkhard Leeb, erfreut.
Psoriasisarthritis: Die Pipeline ist gut gefüllt
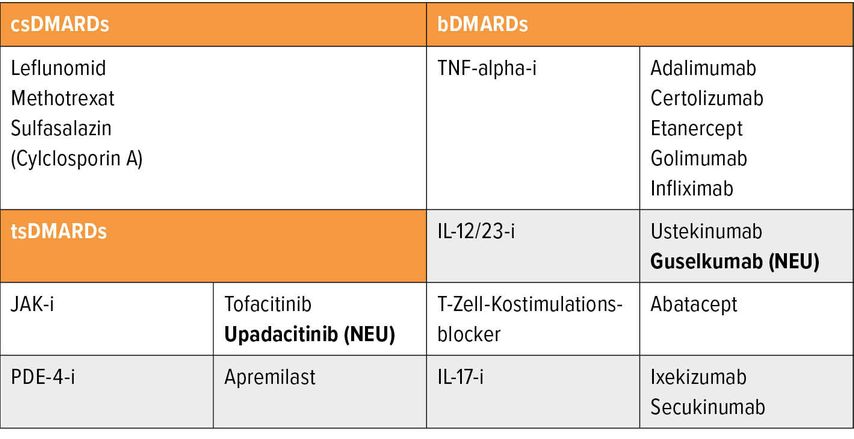
Dr. Judith Sautner schaffte es in 30 Minuten, einen hervorragenden Überblick über die aktuell verfügbaren Therapieoptionen bei der Psoriasisarthritis (PsA) zu geben (Tab.1). Die EULAR-Empfehlungen wurden 2019 überarbeitet.1 „Sie berücksichtigen nun verstärkt die klinische Vielfalt der PsA und haben sich formal den GRAPPA-Empfehlungen angenähert“, so Sautner.
Methotrexat (MTX) wirkt sehr gut auf Gelenke und Haut, dem Präparat wurde allerdings sehr lange das Fehlen von evidenzbasierten Studien angelastet. In der SEAM-Studie erreichte MTX in Monotherapie aber immerhin 51% ACR-20-Ansprechen, wenngleich es schlechter performte als der Comparator Etanercept.2
Für TNF-α-Inhibitoren (TNF-α-i) gibt es mittlerweile über 20 Jahre klinische Erfahrung. Solide Malignome – mit Ausnahme von Mammakarzinomen und Melanomen – sind heute keine Kontraindikationen mehr. Unerlässlich ist ein Tbc-Screening, da es zu Reaktivierungen kommen kann.
IL-17-Inhibitoren (IL-17-i) zeichnen sich durch eine sehr gute Hautwirkung aus und sind in diesem Punkt TNF-α-i überlegen. „Aus Studien wissen wir, dass IL-17-i besonders effizient für bDMARD-naive Patienten sind“, ergänzt Sautner. „Dies ist aber leider nicht immer mit der Verschreibungsmöglichkeit in Einklang zu bringen.“
Auch IL-12/23-Inhibitoren (IL-12/23-i) haben eine gute Hautwirkung, jedoch keine Wirkung auf das Stammskelett. Im Hinblick auf die Gelenkswirkung sind IL12/23-i bei Biologika-naiven Patienten den TNF-α-i unterlegen, das zeigte zumindest ein rezenter Review.3 Für den IL-23-i Guselkumab gab es Anfang 2021 – nach der Zulassung für Psoriasis vulgaris – eine Indikationserweiterung für die aktive PsA. Die EMA-Zulassung basiert auf den Daten aus den beiden Phase-III-Studien DISCOVER-14 und DISCOVER-2.5 Das ACR-20-Ansprechen war als primärer Endpunkt in beiden Studien Placebo signifikant überlegen, bei gleichzeitig guter Verträglichkeit.
JAK-Inhibitoren (JAK-i) sind bei Hautbeteiligung gut wirksam, noch bessere Effekte zeigen sie bei Manifestationen an Gelenken und Wirbelsäule. Der JAK-i Upadacitinib ist als zweiter Neuzugang (neben Guselkumab) 2020/2021 seit Kurzem auch in der Indikation PsA zugelassen. Die Daten aus den Zulassungsstudien SELECT-PsA-1 und SELECT-PsA-2 zeigten in allen ACR-Domänen gutes Ansprechen, auch Hautbild und körperliche Funktionen besserten sich.6
„Die Bücher der PsA-Therapien sind heute noch lange nicht geschlossen, die Pipeline ist gut gefüllt“, so Sautner. Remtolumab verfolgt als dualer Antikörper gegen TNF-α und IL-17A ein vielversprechendes Wirkprinzip. „Die aktuellen Daten zeigen im Vergleich zu Adalimumab zwar ein ähnliches Wirksamkeits- und Sicherheitsprofil, aber kein besseres – der große Wurf ist damit also noch nicht gelungen“, so Sautners Einschätzung. Weitere interessante Substanzen, die in der Dermatologie bereits zugelassen sind, stehen in klinischer Erprobung für PsA, z.B Brodalumab, Bimekizumab, Risankizumab und Tildrakizumab. Zudem sind auch topische Substanzen in der Pipeline, darunter Apremilast, Crisaborol, Roflumilast und Tofacitinib.
Sautner betonte abschließend, dass Betroffene unbedingt über den enormen Benefit einer Gewichtsreduktion aufgeklärt werden sollten, der sich gerade bei PsA auch positiv auf das Therapieansprechen auswirkt. In einer kürzlich publizierten kleinen skandinavischen Studie konnte die Krankheitsaktivität (DAPSA-Score) durch Gewichtsreduktion signifikant gesenkt werden – und blieb auch nach neuerlicher Gewichtszunahme erniedrigt.7
Kollagenosen: neue Kriterien, neue Therapieoptionen
Auch im Bereich der Kollagenosen gab es in den letzten Jahren einige Neuerungen, die Doz. Dr. Jochen Zwerina umfassend präsentierte. Für den systemischen Lupus erythematodes (SLE) wurden 2019 von der EULAR/ACR neue Klassifikationskriterien erarbeitet.8 Ein positiver ANA-Befund gilt nun als Eingangskriterium. Die neuen Kriterien weisen eine hohe Spezifität (96%) und Sensitivität (98%) auf und sind im klinischen Alltag gut einsetzbar.
Bei fehlendem Ansprechen auf die Standardtherapie, wie z.B. Glukokortikoide (GC), Hydroxychloroquin, Azathioprin, ist das erste spezifisch für den SLE zugelassene Biologikum Belimumab indiziert. „Schnelle Effekte darf man sich bei Belimumab nicht erwarten. Langfristig können aber GC eingespart bzw. zum Teil vollkommen abgesetzt werden“, sagt Zwerina. Gute Erfahrungen gibt es bei moderater bis hoher Aktivität bzw. bei hämatologischen und immunologischen Manifestationen. Belimumab ist insbesondere bei Autoantikörper-positiven aktiven Patienten mit Komplementverbrauch einzusetzen.
Weitere vielversprechende Wirkstoffe sind in der Pipeline. Anifrolumab (anti-IFN) wird derzeit in klinischen Studien getestet (TULIP-1 und TULIP-2). Ebenso wird der bereits für andere Indikationen zugelassene JAK-i Baricitinib aktuell in Phase-III-Studien in der Indikation SLE geprüft.
In der Indikation Lupusnephritis steht der Calcineurin-Inhibitor Voclosporin kurz vor der Zulassung. In der Phase-III-Studie AURORA zeigten nach einem Beobachtungszeitraum von 53 Wochen 40,8% der Probanden ein renales Ansprechen vs. 22,5% unter Placebo (beide Gruppen plus Standardtherapie).9 Die FDA-Zulassung erhielt der Wirkstoff bereits Anfang des Jahres, eine EMA-Einreichung ist geplant.
Ein häufiges Symptom der systemischen Sklerose (SSc) ist eine prognostisch ungünstige Dyspnoe. Ursächlich hierfür sind entweder eine pulmonale arterielle Hypertonie oder eine interstitielle Lungenerkrankung (SSc-ILD). Etablierte Therapien für die SSc-ILD sind Cyclophosphamid (CP) oder Mycophenolat (MMF), vergleichsweise neu ist die Option einer autologen Stammzelltransplantation (ASZT). In der letzten größeren Studie hierzu (n=75) konnten über einen Beobachtungszeitraum von 54 Monaten in der ASZT-Gruppe deutlich bessere Behandlungsergebnisse als in der CP-Vergleichsgruppe erzielt werden.10 Der Nutzen der ASZT überwiegt deren Risiken bei noch nicht lange dauernder rasch progredienter SSc, so die Schlussfolgerung. Die hierfür infrage kommenden Patienten müssen jedoch analog zu den Studieneinschlusskriterien sorgfältig ausgewählt und in Zentren behandelt werden.
Eine weitere neue Therapieoption für die SSc-ILD ist der Tyrosinkinaseinhibitor Nintedanib, welcher zuvor bereits in der Indikation idiopathische Lungenfibrose eine Zulassung hatte. In der SENSCIS-Studie betrug der Verlust der Lungenfunktion (gemessen an der forcierten Vitalkapazität über 52 Wochen) unter Nintedanib nur 52,5ml/Jahr vs. 93,3ml/Jahr unter Placebo.11 Die häufig als Nebenwirkung auftretende Diarrhö ist in der Regel gut kontrollierbar. Die Therapie ist spezifisch in der Lunge wirksam, auf andere Organmanifestationen der Sklerodermie nimmt sie keinerlei Einfluss.
SARS-CoV-2-Impfung und Autoimmunerkrankungen
Prof. Dr. Stefan Winkler machte deutlich, dass wir in Hinblick auf die SARS-CoV-2-Impfstoffe derzeit mit einem „Prozentsalat“ arbeiten: Daten zum Schutz vor Infektion, Erkrankung und schwerer Erkrankung ebenso wie Daten aus Studien und Real World werden wild vermischt. Zusätzlich ist die Zielpopulation ein wichtiges Kriterium. Bei immunsupprimierten Personen weiß man bislang sehr wenig, erste rudimentäre Daten liegen jedoch bereits vor.
In einer kürzlich publizierten Studie an 436 organtransplantierten Personen wurde das Impfansprechen nach der ersten Dosis eines mRNA-Impfstoffes untersucht. Bei 360 Probanden konnten keine Anti-Spike-IgG-AK nachgewiesen werden. Die beste Immunantwort wurde bei jüngeren Studienteilnehmern und bei fehlender Therapie mit einem Antimetaboliten (MMF, Azathioprin) beobachtet.12 „Man weiß allerdings, dass gerade bei Organtransplantierten die zweite Booster-Impfung enorm wichtig ist“, relativiert Winkler die Ergebnisse.
Eine andere Publikation aus Israel untersuchte die Immunantwort nach der zweiten mRNA-Dosis an 156 Patienten mit verschiedenen rheumatischen Erkrankungen (entzündliche Gelenkserkrankungen, Kollagenosen, Vaskulitiden) und unterschiedlichen Therapien (csDMARDs, b/tsDMARDs, GCs). Die Spike-IgG-AK-Antwort war bei 88% der Probanden 4–6 Wochen nach der zweiten Dosis positiv. Die AK-Titer waren in erster Linie von der Art der immunmodulierenden Therapie abhängig, wobei sich eine B-Zell-depletierende Therapie erwartungsgemäß am unvorteilhaftesten auswirkte. Es bestand jedoch keine Korrelation mit Alter oder Diagnose.13
Zu einem ähnlich positiven Ergebnis kam eine Studie an 404 Patienten mit rheumatischen bzw. muskuloskelettalen Erkrankungen. Nach der zweiten Dosis eines mRNA-Impfstoffes zeigten 94% ein Ansprechen. Die niedrigsten AK-Titer wurden bei Patienten mit MMF- und Rituximab(RTX)-Therapie gefunden. Auch eine GC-Therapie und eine Myositisdiagnose waren mit einem schlechten Impfansprechen assoziiert. Erfreulicherweise zeigten 100% der Probanden auf TNF-α-Therapie eine Impfantwort.14
Etwas bessere Ergebnisse in Hinblick auf das Impfansprechen unter RTX zeigen aktuelle Studiendaten der Universität Wien. Untersucht wurden 49 RTX-Patienten, der letzte Therapiezyklus lag allerdings im Durchschnitt bereits 7 Monate zurück. Bei etwa der Hälfte der Probanden (n=24) waren B-Zellen vorhanden. „Die Daten zeigen, dass das Potenzial für eine Antikörperantwort besteht, sobald B-Zellen vorhanden sind“, so Winkler. „Es gibt dafür keinen Cut-off, auch 1% kann bereits ausreichend sein.“ Zudem zeigten alle RTX-Patienten eine ausgezeichnete T-Zell-Antwort.
„Ein frommer Wunsch wäre es natürlich, dass vor der Gabe einer immunsuppressiven/immunmodulierenden Therapie geimpft wird. Es sollten aber keinesfalls notwendige Therapien wegen der Impfung aufgeschoben werden“, betonte Winkler. Auch sollte eine laufende Therapie grundsätzlich nicht abgesetzt werden, um das Impfansprechen zu verbessern. Laut ACR sollte jedoch MTX im Anschluss an die Impfung einmal ausgesetzt und JAK-Inhibitoren sollten für eine Woche pausiert werden.15 Diese Empfehlungen basieren auf Erfahrungen mit Influenza- und Pneumokokkenimpfungen.
Osteoporose: Trend zur Sequenztherapie
Klinisch praktische Aspekte der Osteoporosetherapie beleuchtete Prof. Dr. Heinrich Resch. Der Trend geht ganz klar dahin, das Frakturrisiko möglichst früh zu erkennen und zu senken. Die einfachste und effektivste Möglichkeit zur Risikoabschätzung ist das FRAX-Tool, bei Bedarf kann der „Trabecular Bone Score“ (TBS) ergänzt werden. Beträgt das Risiko mehr als 20%, so wird die Einleitung einer Therapie als sinnvoll erachtet.
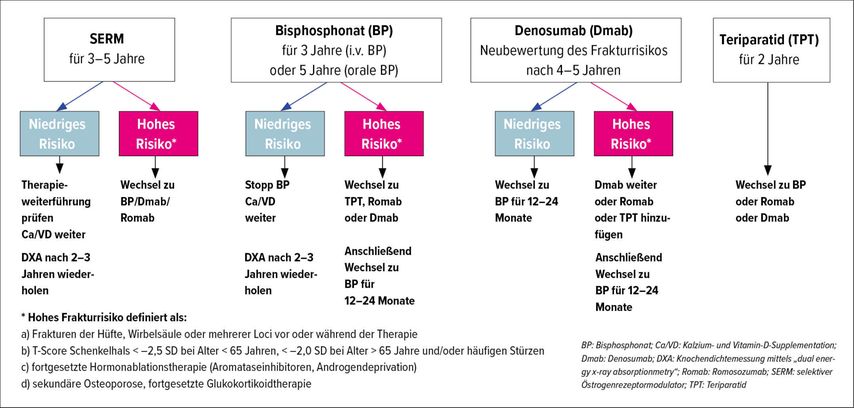
Bei der medikamentösen Therapie orientiert man sich heute zunehmend in Richtung Sequenztherapie (Abb.1), da in der Regel eine Langzeittherapie über Jahre bis Jahrzehnte erforderlich ist. Dadurch kann ein Optimum an strukturellem Knochenaufbau erzielt werden. Die aktuell verfügbaren Therapieoptionen umfassen einerseits die bekannten Antiresorptiva (Bisphosphonate, Denosumab, Raloxifen), andererseits die Osteoanabolika.
Abb. 1: Empfehlungen zur Langzeittherapie bei postmenopausaler Osteoporose (ergänzt und adaptiert nach Meier C et al.: Swiss Med Wkly 2017)
Bis vor Kurzem war Teriparatid das einzige zugelassene Osteoanabolikum. Im vergangenen Jahr ist – nach über 10 Jahren Stillstand in der Entwicklung von Osteoporosetherapeutika – die Sprunginnovation Romosozumab neu dazugekommen. Das neue Therapieprinzip beruht auf einer Hemmung des Knochenregulators Sclerostin. Dadurch kommt es indirekt zu einem vermehrten Knochenaufbau sowie zu einem verringerten Knochenabbau. In den Zulassungsstudien senkte Romosozumab das Risiko von Wirbelkörperfrakturen signifikant. Die Reduktion des relativen Risikos betrug in der Verumgruppe 73% (12 Monate) und 75% (24 Monate) im Vergleich zu Placebo.16Der Effekt fällt in den ersten 6 Behandlungsmonaten am stärksten aus, im Anschluss muss auf eine antiresorptive Therapie umgestellt werden. Ansonsten ist nach dem Absetzen binnen Monaten mit einem Verlust an Knochenmasse zu rechnen. Die Verhandlungen über die Erstattung von Romosozumab sollten aller Voraussicht nach bis Ende des Jahres abgeschlossen sein.
Für Denosumab sind mittlerweile Langzeitdaten über mehr als 10 Jahre verfügbar. Sowohl an der Wirbelsäule als auch im Hüftbereich kann die Knochendichte deutlich verbessert werden.17Negativ angelastet wird dem Wirkstoff immer wieder das Rebound-Phänomen. „Zu bedenken ist allerdings, dass die Osteoporose eine chronische Erkrankung ist“, erläuterte Resch. „Wenn sich das zugrundeliegende Risiko nicht ändert, ist auch nicht an ein Absetzen der Therapie zu denken.“ Möglicherweise könnte das 6-Monats-Intervall von Denosumab vorsichtig verlängert werden. „Dazu gibt es bislang aber nur wenige Daten“, so Resch.
Kiefernekrosen sind eine schwere, aber seltene Nebenwirkung von Antiresorptiva. „Die Osteoporosetherapie ist ein Gespenst für die Zahnärzte“, bestätigte Resch in der Diskussion. Tatsächlich treten Kiefernekrosen unter Antiresorptiva bei Patienten ohne Risikofaktoren sehr selten (ca. 1:100000 bis 1:200000) auf und werden eher bei vorgeschädigtem Gebiss beobachtet. Jedem Patienten sollte vor Aufnahme einer antiresorptiven Therapie zur Abklärung des Zahnstatus geraten werden. Keinesfalls sollte der Therapiebeginn während Interventionen im Kieferbereich angesetzt werden. Denosumab eignet sich hier sehr gut. Denn hier kann der Termin der zahnärztlichen Intervention in Monat 3 oder 4 nach Denosumab gewählt werden.
Quellen:
● 19. Wachauer Rheumatag, 24. April 2021, virtuell; ●„Rheumapatient/innen und COVID-19 … Immunsuppression …was wissen wir? – Update“, Webinar am 31. Mai 2021
Literatur:
1 Gossec L et al.: Ann Rheum Dis 2020; 79(6): 700-12 2 Mease PJ et al.: Arthritis Rheumatol 2019; 71(7): 1112-24 3 Zhang H et al.: RMD Open 2021; 7(1): ): e001399 4 Deodhar A et al.: Lancet 2020; 395(10230): 1115-25 5 Mease PJ et al.: Lancet 2020; 395(10230): 1126-36 6 Mease PJ et al.: Rheumatol Ther 2021; doi: 10.1007/s40744-021-00305-z (online ahead of print) 7 Klingberg E et al.: Arthritis Res Ther 2020; 22(1): 254 8 Aringer M: Semin Arthritis Rheum 2019; 49(3s): 14-7 9 Arriens C et al.: Ann Rheum Dis 2020; 79(1): 172 10 Sullivan KM et al.: N Engl J Med 2018; 378(1): 35-47 11 Distler O et al.: N Engl J Med 2019; 380(26): 2518-28 12 Boyarsky BJ et al.: JAMA 2021; 325(17): 1784-6 13 Braun-Moscovici Y et al.: medRxiv 2021; doi: 10.1101/2021.04.02.21254493 (online ahead of print) 14 Ruddy JA et al.: Ann Rheum Dis 2021; doi: 10.1136/annrheumdis-2021-220656 (online ahead of print)
Das könnte Sie auch interessieren:
Schwierig zu behandelnde oder therapierefraktäre SpA
Die Behandlungsmöglichkeiten bei Spondyloarthritis haben sich mit Einführung der Biologika dramatisch verbessert. Das bedeutet allerdings nicht, dass alle Patient:innen in ausreichendem ...
Biologikatherapien in der Schwangerschaft
„Biologika sind in der Schwangerschaft in Ordnung“ – mit dieser klaren Aussage fasste Prof.Dr. Ian Giles, University College London, im Rahmen der RheumaPreg-2025- Konferenz in Wien die ...
Spondyloarthritis: Schäden sind bei frühzeitiger Therapie reversibel
Das alte Konzept der nichtradiografischen axialen Spondyloarthritis und der radiografischen ankylosierenden Spondylitis wird zunehmend verlassen und in der Diagnose axiale ...