Biologikatherapien in der Schwangerschaft
Bericht: Mag. pharm. Irene Senn, PhD
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
„Biologika sind in der Schwangerschaft in Ordnung“ – mit dieser klaren Aussage fasste Prof.Dr. Ian Giles, University College London, im Rahmen der RheumaPreg-2025- Konferenz in Wien die aktuelle Evidenzlage zusammen. Neue Studiendaten zeigen, dass die Fortsetzung der Biologikatherapie Schwangerschaftsoutcomes signifikant verbessert, während ein Absetzen mit einem erhöhten Risiko für Krankheitsschübe und Frühgeburtlichkeit assoziiert ist. Das BRAN-Konzept bietet einen strukturierten Entscheidungsrahmen für die Praxis.
Die lange verbreitete Annahme, dass sich die rheumatoide Arthritis (RA) in der Schwangerschaft bei 80–90% der Patientinnen spontan bessert, wurde durch aktuellere Daten relativiert. Eine Metaanalyse prospektiver Studien mit objektiven Aktivitätsscores ergab, dass sich die Krankheitsaktivität tatsächlich nur bei 60% der Patientinnen während der Schwangerschaft verbesserte und bei knapp der Hälfte postpartale Schübe auftraten.1 Diese Ergebnisse unterstreichen die Notwendigkeit einer effektiven medikamentösen Therapie auch während der Schwangerschaft, um sowohl mütterliche als auch fetale Komplikationen zu minimieren.
Paradigmenwechsel in der Behandlungsstrategie
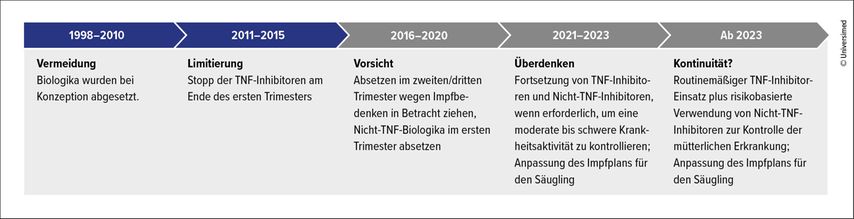
Die Haltung zum Biologikaeinsatz während der Schwangerschaft hat sich in den letzten 25 Jahren fundamental gewandelt (Abb.1).2 Während in den Jahren von 1998–2010 Biologika reflexartig bei Konzeption abgesetzt wurden, folgte ab 2011 eine Phase der vorsichtigen Limitierung mit Stopp der TNF-Inhibitoren am Ende des ersten Trimesters. „Wir befinden uns jetzt an einem Punkt, an dem wir die Verwendung neu überdenken“, erläuterte Giles. Seit 2021 zeichnet sich ein klarer Trend ab: TNF-Inhibitoren werden routinemäßig fortgeführt, während bei Nicht-TNF-Inhibitoren eine individuelle Risikostratifizierung erfolgt. Diese Entwicklung basiert auf einer wachsenden Evidenzbasis und spiegelt sich auch in den internationalen Leitlinien wider.
Abb. 1: Zeitliche Entwicklung der Anwendung von biologischen DMARDs in der Schwangerschaft (nach Giles I et al. 2024)2
Das BRAN-Konzept als Entscheidungshilfe
Für die strukturierte Beratung von schwangeren Patientinnen stellte Giles das BRAN-Konzept vor. Es handelt sich dabei um eine Entscheidungshilfe aus der „Choosing Wisely“-Kampagne, die vier zentrale Fragen in den Mittelpunkt stellt:
-
„Benefits“ (Vorteile): Welche Vorteile bringt die Therapiefortsetzung?
-
„Risks“ (Risiken): Welche Risiken bestehen?
-
„Alternatives“ (Alternativen): Gibt es gleichwertige Alternativen?
-
„Nothing“ (nichts tun): Was sind die Folgen eines Therapieverzichts?
Diese systematische Betrachtung führt in der Praxis laut Giles sehr häufig zum Ergebnis, dass die Vorteile einer kontinuierlichen Therapie die potenziellen Risiken überwiegen. Aktuelle Kohortenstudien untermauern diese Einschätzung.
Krankheitsaktivität bestimmt Schwangerschaftsverlauf
Die PreCARA-Studie lieferte hier wichtige Real-World-Daten zur Biologikatherapie während der Schwangerschaft.3 In dieser prospektiven Kohorte mit 309 Frauen erhielten 47% TNF-Inhibitoren. „90% der Patientinnen erreichten eine Remission oder niedrige Krankheitsaktivität“, berichtete Giles.Dies steht in deutlichem Kontrast zu historischen Vergleichsdaten aus der Prä-Biologika-Ära.
Der Einsatz von TNF-Inhibitoren war zudem mit einem signifikant höheren mittleren Geburtsgewicht assoziiert (3344g versus 3171g bei Nichtanwenderinnen; p=0,03). Die mittlere Differenz betrug 173Gramm. „Das sind alles gute Gründe, diese Medikamente in der Schwangerschaft einzusetzen“, betonte Giles. Auffallend war zudem die niedrigere Rate an SGA(„small for gestational age“)-Neugeborenen unter TNF-Inhibitor-Therapie (9,8% versus 20,0%; p=0,05).4
Hohe Krankheitsaktivität erhöht Komplikationsrisiko
Aktuelle Metaanalysen belegen die Bedeutung einer adäquaten Krankheitskontrolle: Eine systematische Übersichtsarbeit von Huang et al. analysierte 18 Studien mit über 50 Millionen Teilnehmerinnen.5 Im Vergleich zu gesunden Schwangeren zeigten Frauen mit RA signifikant erhöhte Risiken für Frühgeburtlichkeit (OR: 1,58; 95%CI: 1,44–1,74), niedriges Geburtsgewicht (OR: 1,45; 95%CI: 1,30–1,63), SGA-Neugeborene (OR: 1,49; 95%CI: 1,22–1,82) und Präeklampsie (OR: 1,48; 95%CI: 1,19–1,83). Auch die Kaiserschnittrate war erhöht (OR: 1,39; 95%CI: 1,24–1,55).
Diese Daten verdeutlichen, dass eine gut kontrollierte Erkrankung während der Schwangerschaft essenziell ist, um diese Komplikationen zu minimieren.
Absetzen von Biologika birgt Risiken
Die Konsequenzen eines vorschnellen Therapiestopps wurden in einer italienischen Kohortenstudie mit 75 RA-Patientinnen untersucht.6 Wenn Patientinnen ihre bDMARD-Therapie unmittelbar nach Feststellen der Schwangerschaft beendeten, stieg ihr Risiko für Krankheitsflares um das 2,8-Fache (OR: 2,857; 95%CI: 1,112–8,323; p=0,034). Ein solcher Schub war wiederum mit einem 4,6-fach höheren Risiko für Frühgeburtlichkeit verknüpft (OR: 4,625; 95%CI:1,027–20,829; p=0,034). Frauen, die bereits vor der Schwangerschaft mehr als ein Biologikum benötigt hatten, waren zusätzlich gefährdet, einen Flare zu erleiden (OR: 4,1; 95%CI: 1,204–13,966; p=0,019). „Das Absetzen eines Biologikums in der frühen Schwangerschaft verschlechtert also tatsächlich die Ergebnisse“, betonte Giles. Diese Erkenntnisse untermauern den Paradigmenwechsel: Anstatt von reflexartigem Absetzen bei Schwangerschaftswunsch empfiehlt Giles die individualisierte Fortführung kompatibler Biologika unter Abwägung des Nutzen-Risiko-Profils.
Impfungen bei exponierten Säuglingen
Lange Zeit bestanden Bedenken, dass eine intrauterine Biologikaexposition die Impfantwort von Säuglingen beeinträchtigen könnte. Die prospektive Studie von Fitzpatrick et al. mit 191 exponierten Säuglingen lieferte diesbezüglich beruhigende Daten.7 Die überwiegende Mehrheit (93%) der Säuglinge war bis ins dritte Trimester exponiert, ohne dass sich klinisch relevante Veränderungen im Immunsystem zeigten – weder bei Lymphozyten-Subsets noch bei Immunglobulinen oder der Reaktion auf Mitogene. Die Rotavirus-Impfung wurde bei 187 Säuglingen empfohlen: 90% erhielten die Vakzine und 80% absolvierten die komplette Impfserie. Es traten keine schwerwiegenden unerwünschten Ereignisse nach der Immunisierung auf.
Praktischer 4D-Algorithmus für den klinischen Alltag
Für die strukturierte Schwangerschaftsberatung entwickelte Giles gemeinsam mit Beth Gordon einen praktischen Gesprächsleitfaden – die „vier D“:
„discuss“ (Diskussion): aktive Thematisierung von Schwangerschaftsplanung und -management;
„damage“ (Schaden): systematische Berücksichtigung vorbestehender Organschäden, insbesondere renaler Dysfunktion, pulmonaler, kardialer oder zerebraler Beteiligung, die Schwangerschaftsverlauf und -management beeinflussen können;
„disease activity“ (Krankheitsaktivität): Krankheitskontrolle als wichtigster prognostischer Faktor für mütterliche und fetale Outcomes;
„drug safety“ (Arzneimittelsicherheit): schwangerschaftskompatible Medikation fortführen, unangemessene Therapieangst verhindern.
Fazit
Die vorgestellten Daten belegen, dass der Nutzen einer guten Krankheitskontrolle die theoretischen Risiken der Biologika-therapie in der Regel deutlich überwiegt. Rheumatologen sollten ihre Patientinnen ermutigen, eine effektive Therapie auch während der Schwangerschaft fortzuführen, so Giles. Die Angst vor Biologika in der Schwangerschaft sei angesichts der aktuellen Evidenzlage nicht mehr gerechtfertigt. Vielmehr gefährdet ein unkritisches Absetzen sowohl die mütterliche Gesundheit als auch das fetale Outcome.
Quelle:
„Biologics in pregnancy“, Vortrag von Prof. Ian Giles, London, im Rahmen der 13th International Conference on Reproduction, Pregnancy and Rheumatic diseases (RheumaPreg 2025) vom 8.–10. Mai 2025 in Wien
Literatur:
1 Jethwa H et al.: Does rheumatoid arthritis really improve during pregnancy? A systematic review and metaanalysis. J Rheumatol 2019; 46(3): 245-50 2 Giles I et al.: The time of equipoise on the use of biological DMARDs in for inflammatory arthritis during pregnancy is finally over: a reappraisal of evidence to optimise pregnancy management. Lancet Rheumatol 2024; 6(8): e546-e559 3 Smeele HT et al.: Modern treatment approach results in low disease activity in 90% of pregnant rheumatoid arthritis patients: the PreCARA study. Ann Rheum Dis 2021; 80(7): 859-64 4 Smeele HTW et al.: Tumour necrosis factor inhibitor use during pregnancy is associated with increased birth weight of rheumatoid arthritis patients’ offspring. Ann Rheum Dis 2022; 81(10): 1367-73 5 Huang W et al.: Maternal and fetal outcomes in pregnant women with rheumatoid arthritis: a systematic review and meta-analysis. Clin Rheumatol 2023; 42(3): 855-70 6 Gerardi MC et al.: Stopping bDMARDs at the beginning of pregnancy is associated with disease flares and preterm delivery in women with rheumatoid arthritis. Front Pharmacol 2022; 13: 887462 7 Fitzpatrick T et al.: Immunological effects and safety of live rotavirus vaccination after antenatal exposure to immunomodulatory biologic agents: a prospective cohort study from the Canadian Immunization Research Network. Lancet Child Adolesc Health 2023; 7(9): 648-56
Das könnte Sie auch interessieren:
Schwierig zu behandelnde oder therapierefraktäre SpA
Die Behandlungsmöglichkeiten bei Spondyloarthritis haben sich mit Einführung der Biologika dramatisch verbessert. Das bedeutet allerdings nicht, dass alle Patient:innen in ausreichendem ...
Neue Lupustherapien in der Schwangerschaft
Innovative Biologika (bDMARD) und zielgerichtete Therapien (tsDMARD) bieten Kliniker:innen neue therapeutische Werkzeuge bei der Behandlung des systemischen Lupus erythematodes (SLE). Im ...
Spondyloarthritis: Schäden sind bei frühzeitiger Therapie reversibel
Das alte Konzept der nichtradiografischen axialen Spondyloarthritis und der radiografischen ankylosierenden Spondylitis wird zunehmend verlassen und in der Diagnose axiale ...