Strategien der COPD-Therapie aus der Grundlagenforschung
Bericht: Mag. Andrea Fallent
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Während die personalisierte Asthmatherapie große Fortschritte macht, tritt die Behandlung der COPD im Wesentlichen auf der Stelle. Zwei Vorträge des Kongresses der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin (DGP) 2022 präsentierten aktuelle Erkenntnisse zu den zellulären Pathomechanismen bei der COPD und ihrer Bedeutung für die Entwicklung individueller Behandlungsmöglichkeiten.
Für die Medikamentenentwicklung und in der Folge für die Auswahl des Therapieregimes ist die Kenntnis über die Pathomechanismen einer Krankheit ein entscheidender Faktor: Je besser diese erforscht sind, desto leichter lassen sich Ansatzpunkte für die Therapie entdecken.
Am Anfang der Entstehung von COPD stehen verschiedene Umweltnoxen, allen voran das Rauchen. „Die Ätiologie wird aber auch von genetischen und epigenetischen Prädispositionen sowie von pränatalen und frühkindlichen Entwicklungsstörungen der Lunge beeinflusst, die zur Ausprägung von unterschiedlichen Phänotypen der COPD beitragen können“, erklärte PD Dr. Natascha Sommer, Justus-Liebig-Universität Gießen, zu Beginn ihres Vortrags. „Demzufolge teilen wir Patienten nach bestimmten Kriterien ein – zum Beispiel danach, ob sie häufige Exazerbationen haben, eine Hyperinflammation aufweisen oder zum pulmonal-vaskulären Phänotyp zählen. Und wir versuchen aktuell, über die LABA/LAMA/ICS-Therapie hinaus jeden dieser Patienten individuell – mit Rücksicht auf den Phäno- und wenn möglich den Endotyp – zu behandeln, zum Beispiel einen Patienten mit einer Eosinophiliemit einem inhalativen Kortikoid.“
Identifikation von Phänotypen
Im Gegensatz zum Asthma stehen für die individualisierte COPD-Therapie allerdings meist nicht ausreichend Informationen und Wirkstoffe zur Verfügung. Dennoch gelingt es laut Sommer immer besser, anhand von Biomarkern spezifische Phänotypen zu identifizieren.
Ein wichtiger Schritt in Richtung maßgeschneiderter Therapie der COPD ist daher die weitere Erforschung der zugrundeliegenden Pathomechanismen. Nach heutigem Wissen setzen sich diese aus den Faktoren „Schaden“ durch Noxen, „Verteidigung“ – z.B. durch inflammatorische Zellen und Hypersekretion – sowie „Reparaturmechanismen“ zusammen, so Sommer: „Aktuelle Forschungsergebnisse zeigen, dass bei der Reaktion der Atemwege auf Noxen auch B- und T-Zellen im Rahmen einer Autoimmunantwort mit Th-17-Zellen und Antikörpern eine wichtige Rolle spielen. Weiters tragen reaktive Sauerstoffspezies, ein Ungleichgewicht von Proteasen und Antiproteasen, Perforine und Granzyme, zur Apoptose von Epithel- und Endothelzellen bei.“
Durch einen fehlgeleiteten Reparaturmechanismus wird dieser destruktive Prozess häufig noch verstärkt. Daraus ergibt sich ein Circulus vitiosus aus Inflammation und Zellschädigung, den man laut Sommer häufig bei COPD-Patienten nach einem Rauchstopp beobachten kann: „Diesen Teufelskreis gilt es therapeutisch zu durchbrechen – und zwar frühzeitig.“
Forschungsschwerpunkte
Inflammation
In der jüngeren Vergangenheit wurde mehrfach – aber leider wenig erfolgreich – versucht, mit monoklonalen Antikörpern gegen Entzündungsmediatoren vorzugehen. So erwies sich Mepolizumab laut Sommer als nur bedingt, Benralizumab als gar nicht wirksam. „Die Frage ist, ob die Probanden fürdiese Entwicklungen zu wenig charakterisiert wurden und ob gewisse Subpopulationen nicht besser ansprechen würden als ein Kollektiv.“ Um die Forschung diesbezüglich zu optimieren, orientiert sich die Wissenschaft nun verstärkt an den Ansätzen aus der Asthmatherapie, bei der die Phänotypisierung weiter fortgeschritten ist. Als Beispiel nannte Sommer Studien mit einem Schwerpunkt auf jenen Prozessen, die zu einer Eosinophilie bei COPD-Patienten führen. Ein aktueller Ansatz konzentriert sich dabei auf die Hemmung der globalen Inflammation durch Interleukin 33 (IL-33):1 „Hier konnten mit dem Antikörper Itepekimab eine Reduktion der Exazerbationen sowie eine Verbesserung der FEV1 bei einer Subgruppe von Ex-Rauchern mit COPD erreicht werden. Aktuell werden dazu zwei Phase-III-Studien durchgeführt.“
Ein anderer Schwerpunkt der Grundlagenforschung fokussiert auf die Inflammation im lymphoiden Gewebe: Mit der Inhibierung von Lymphotoxin-β-Rezeptoren (LTβR), die in Immunzellen bei COPD erhöht sind, konnte die Entstehung eines Emphysems vermindert und die Regeneration von Lungengewebe induziert werden.2
Oxidativer Stress
„Oxidativer Stress stellt wie die Inflammationen einen zentralen Patomechanismus bei der COPD dar, der unterschiedlichste Auswirkungen haben kann“, führte Sommer weiter aus. „Auch dazu gibt es einige vielversprechende Ansätze im Tierversuch, zum Beispiel in Zusammenhang mit den antientzündlichen Effekten der Superoxiddismutase (SOD) und der Glutathionperoxidase (GPx).“ Sommer selbst untersucht mithilfe von Mausmodellen mit humanem Krankheitsbezug (Zigarettenrauch- und Raumluftexposition) die Pathomechanismen bei der Induktion von Emphysemen bzw. von pulmonaler Hypertonie durch NO-Synthasen und NADPH-Oxidasen.3
Weiters erwähnte Sommer eine Studie, die das sogenannte „Single-cell Sequencing“ nützt, um „Karten“ mit einzelnen Zellclustern, z.B. jenem der distalen Lungenabschnitte, herzustellen. Dadurch können Prozesse wie die Veränderung der Zellzusammensetzung genauer erforscht werden. In diesem Zusammenhang wurde sogar ein neuer, möglicherweise regenerativer Zelltyp identifiziert, jener der „respiratory airway secretory (RAS) cells“.4
Drug Repurposing
Abschließend zitierte Sommer aktuelle Erkenntnisse zum „Repurposing“ bestehender Therapeutika bei der COPD. Gleich zwei rezente Studien beschäftigten sich mit Metformin, einem der am längsten verwendeten Wirkstoffe in der oralen Diabetestherapie. Darin konnte gezeigt werden, dass sich Metformin günstig auf den Verlauf von COPD auswirkt: Konkret schützte es im Mausmodell vor durch Zigarettenrauch induziertem Lungenemphysem bzw. war es bei Patienten mit einem langsameren Fortschreiten des Emphysems assoziiert.5,6
Altern und Regeneration in der Lunge
„Wir haben in der Lunge verschiedene epitheliale Stammzellen, die durchaus in der Lage sind, Atemwegs- und Alveolarstrukturen zu regenerieren. Allerdings funktioniert das in der COPD nicht“, erläuterte Dr. Mareike Lehmann, Deutsches Zentrum für Lungenforschung in München. Daher sei es ein großes Ziel der Forschung, die Regenerationsfähigkeit der Lunge zu verbessern, um diese häufige Erkrankung irgendwann heilen zu können.
Bis das gelingt, bleibt das Alter generell der größte Risikofaktor für chronische Lungenerkrankungen. In Studien konnte gezeigt werden, dass das Risiko, durch Rauchexposition ein Emphysem zu entwickeln, mit zunehmendem Alter steigt. Bei der weiteren Untersuchung des „betagten“ Lungengewebes, im Speziellen im Zuge der Transkriptomanalyse, können als pathologische Faktoren dafür die Hochregulierung entzündlicher Prozesse und die Unterdrückung von Signalwegen, die zum Zellzyklus bzw. zur Zellteilung beitragen, nachgewiesen werden.7
Zelluläre Seneszenz in Epithelzellen
Früher dachte man, dass eine seneszente Stammzelle einfach untätig bleibt. „Mittlerweile wissen wir, dass sich die Zelle zwar nicht mehr teilt, sie sezerniert allerdings weiterhin viele verschiedene Faktoren, wie proinflammatorische Zytokine und Wachstumsfaktoren – das Sekretom“, so Lehmann. Durch diesen Prozess werden nicht nur Nachbarzellen, sondern möglicherweise auch Zellen in anderen Organen beeinflusst. Lehmann: „Damit bildet die zelluläre Seneszenz eine doppelte Hürde für die Regeneration in der alternden Lunge, einerseits durch das Ausschalten der Stammzelle selbst, andererseits durch das Entstehen einer hemmenden Nische aus proinflammatorischen Zytokinen.“
Bei COPD-Patienten wurde Seneszenz im Atemwegs- und Alveolarepithel sowie in Fibroblasten und im Endothel gefunden, was für eine vorschnelle Alterung in der Lunge bei dieser Erkrankung spricht. Lehmann: „Als eine der möglichen Gegenstrategien setzen wir sogenannte Senolytika ein, die zur Apoptose von seneszenten Zellen beitragen.“ 8
Senolytische Therapie als Anti-Aging-Strategie
Der Einsatz von Senolytika wird bereits bei anderen Erkrankungen im präklinischen Setting eingesetzt, bei der Lungenfibrose konnte die Wirksamkeit bislang in Mausmodellen nachgewiesen werden, so Lehmann: „Eine Phase-IIa-Studie dazu ist in Planung“.9 Bei der COPD wird daran weiter in Tierversuchen geforscht.
Senolytika binden sich nicht an ein bestimmtes Molekül, sondern intervenieren im Netzwerk der antiapoptotischen Faktoren und weisen damit eine relativ breite Spezifität auf, so Lehmann. Damit ist auch die Wahrscheinlichkeit einer Resistenzbildung gering. „Unsere Hoffnung ist, dass wir diese Senolytika in Zukunft für mehrere chronische oder auch akute Lungenkrankheiten einsetzen können. Aktuell läuft in diesem Zusammenhang eine Studie mit vielversprechenden Ansätzen bei Covid-19“,10 resümierte Lehmann.
In Zusammenhang mit anderen Anti-Aging-Strategien bei der COPD wurden neben Metformin
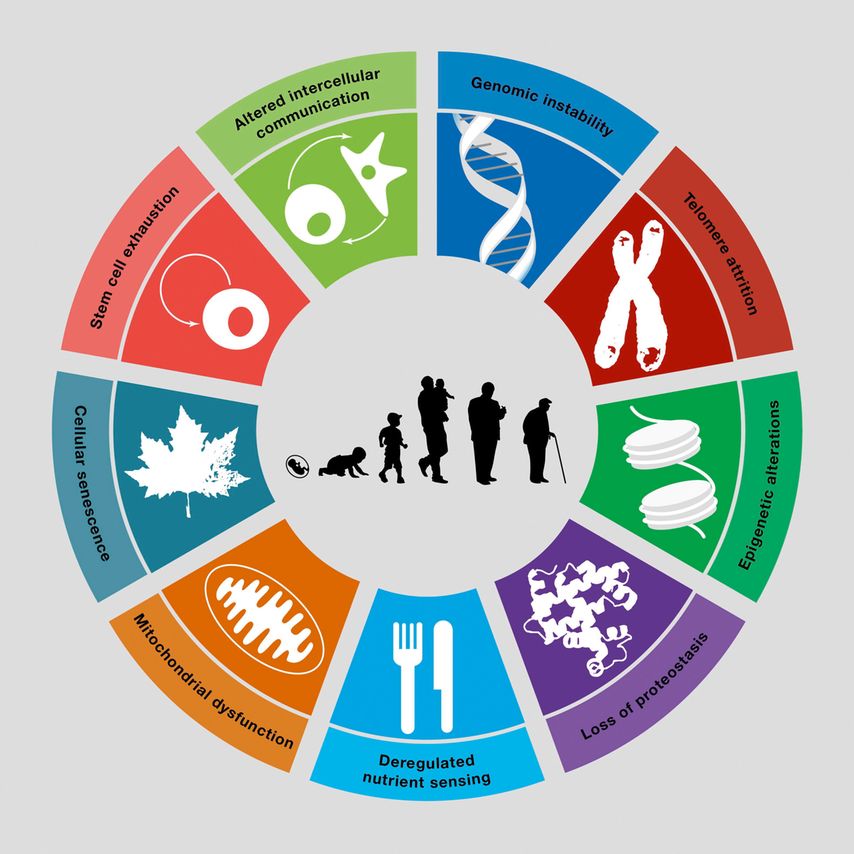
u.a. auch präklinische und klinische Daten zum Einsatz von Rapamycin publiziert. Aus den bisherigen Erkenntnissen ergeben sich Hinweise darauf, dass die Intervention in einem Bereich der „Hallmarks of Aging“(Abb. 1) auch die anderen Faktoren der Zellalterung beeinflussen und diese verlangsamen kann: „Damit besteht die Hoffnung, auf diesem Weg den Teufelskreis der Seneszenz von Zellen unterbrechen zu können.“
Quelle:
„Neue Therapiestrategien der COPD aus der Grundlagenforschung“ und „Altern und Regeneration in der Lunge – Bedeutung für die COPD?“, Vorträge im Rahmen des 62. Kongresses der DGP am 28.Mai 2022, Leipzig
Literatur:
1 Rabe KF et al.: Lancet Med 2021; 9(11): 1288-98 2 Conlon TM et al.: Nature 2020; 588 (7836):151-6 3 Gredic M et al.: Eur Respir J 2022; 59(4): 2101153 4 Sauler M et al.: Nat Commun 2022; 13: 494 5 Sauler M et al.: Nat Commun 2022; 13: 494 6 Kahnert K et al.: Sci Rep 2022; 12: 1435 7 Lehmann M et al.: Cellular Signaling 2020; 70:109588 8 Kirkland J et al.: J of Inter Med 2020; 288(5): 518-36 9 Justice JN et al.: eBioMedicine 2019; 40: 554-63 10 Camell CD et al.: Science 2021; 6552(373) 11 Lopez-Otin C et al.: Cell 2013; 153(6): 1194-217
Das könnte Sie auch interessieren:
Kreuzfahrtmedizin in der Karibik
Wer sich auf eine Kreuzfahrt in die Karibik begibt, sollte (vorab) mögliche gesundheitliche Risiken bedenken: Infektiöse Tropenkrankheiten lauern vor allem bei Landgängen, an Bord ist ...
Management von Rückenschmerzen
Wirbelsäulenschmerzen zählen zu den häufigsten Beschwerden in der Hausarztpraxis, auch Kinder und Jugendliche sind bereits davon betroffen. Ein richtungsweisendes Kriterium für ...
HIV-PrEP: die „Pille davor“
Die HIV-PrEP bietet einen effektiven Schutz vor HIV. Hausärzt:innen sind oft die ersten Ansprechpartner für potenzielle Nutzende und sollten daher Grundkenntnisse über PrEP besitzen. ...