<p class="article-intro">Die frakturassoziierte Infektion («fracture-related infection», FRI) ist eine der schwersten Komplikationen nach Knochenbruch und stellt eine grosse Herausforderung für das multidisziplinäre Behandlungsteam und den Patienten dar.<sup>1, 2</sup></p>
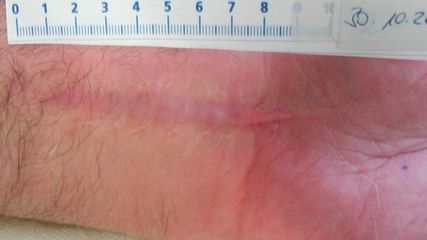
<p class="article-content"><div id="keypoints"> <h2>Kernpunkte</h2> <p><strong>Definition und Diagnose von frakturassoziierten Infektionen (adaptiert nach Govaert et al. 2019)<sup>5</sup></strong></p> <ul> <li>Ein multidisziplinärer Ansatz ist der Schlüssel für eine erfolgreiche Behandlung von frakturassoziierten Infektionen («fracture-related infections», FRI). Komplexe Fälle sollten in einem dafür spezialisierten Zentrum behandelt werden.</li> <li>Bei einer verzögerten oder ausbleibenden Knochenheilung sollte immer an eine FRI gedacht werden.</li> <li>Das Vorliegen mindestens eines «bestätigenden Kriteriums» («confirmatory sign») (Tab. 1) erlaubt die Diagnose eines FRI. Das multidisziplinäre Behandlungsteam sollte eine weitere Abklärung im Rahmen des diagnostischen Algorithmus veranlassen und eine Behandlungsstrategie entwickeln.</li> <li>Das Vorhandensein «hinweisender Kriterien» («suggestive signs») (Tab. 1) sollte das multidisziplinäre Behandlungsteam veranlassen, eine weitere Abklärung im Rahmen des diagnostischen Algorithmus durchzuführen, um die Verdachtsdiagnose zu erhärten oder zu widerlegen.</li> <li>Die einzigen klinischen «bestätigenden» Kriterien sind eine Fistel oder Wunddehiszenz (mit Kontakt zum Knochen oder Implantat) und/oder der makroskopische Nachweis von Eiter im Bereich der Wunde oder des Operationssitus.</li> <li>Während des operativen Débridements sollen mindestens 3 (vorzugsweise 5) tiefe Gewebeproben vom Ort des Infektgeschehens entnommen werden und zeitnah der mikrobiologischen und histologischen Untersuchung zugeführt werden. Zur Vermeidung von falsch-negativen Kulturen sollte wenn möglich vor Abnahme der Gewebeproben für die Mikrobiologie keine antibiotische Therapie begonnen werden.</li> <li>Laborchemische Analysen der Infektparameter (CRP, Leukozyten, BSG) müssen mit Vorsicht interpretiert werden, da ihr Vorhersagewert für eine FRI gering ist.</li> <li>Nebst dem konventionellen Röntgen richtet sich die Indikation von weiteren bildgebenden Modalitäten (CT, MRI, SPECT/CT, FDG/PET, Leukozytenszintigrafie) nach der Fragestellung und lokalen Verfügbarkeit.</li> </ul> </div> <p>Die klinische Manifestation des frakturassoziierten Infektes kann mannigfaltig sein und lässt sich nicht immer eindeutig von nicht infizierten posttraumatischen Komplikationen (wie beispielsweise der aseptischen Pseudarthrose) unterscheiden. Bei akuten Frühinfektionen liegen oftmals die klassischen klinischen Infektzeichen wie Schmerz, Rötung, Überwärmung und Schwellung vor, wohingegen chronische Infektionen in der Regel nur mit subtilen Symptomen wie ausbleibender knöcherner Konsolidierung oder Belastungsschmerzen einhergehen.<sup>1, 2</sup> <br />Da in bis zu 40 % aller Pseudarthrosen eine Infektion ursächlich für die ausbleibende Knochenbruchheilung ist, ist eine Pseudarthrose bis zum Ausschluss als frakturassoziierte Infektion zu werten.<sup>3</sup> Die korrekte Diagnosestellung mit Erhebung eines umfassenden Patientenstatus ist von besonderer Bedeutung, um ein individualisiertes Behandlungskonzept entwerfen zu können.<sup>4</sup> Ein interdisziplinäres Team, welches sich aus Orthopäden/Traumatologen, Radiologen, Infektiologen, Ärzten für plastische Chirurgie und weiteren Fachrichtungen zusammensetzt, ist unerlässlich, um die Infektion korrekt zu behandeln sowie die Knochenbruchheilung erreichen zu können. Im folgenden Übersichtsartikel werden die aktuellen Empfehlungen einer internationalen multidisziplinären Expertengruppe zur Diagnosestellung von frakturassoziierten Infektionen zusammengefasst.<sup>5</sup></p> <p><img src="/custom/img/files/files_datafiles_data_Zeitungen_2019_Leading Opinions_Ortho_1903_Weblinks_lo_ortho_1903_s16_tab1.jpg" alt="" width="1419" height="1414" /></p> <h2>Definition</h2> <p>Im Jahre 2018 hat eine internationale, multidisziplinäre Expertengruppe unter der Schirmherrschaft der AO Foundation sowie der European Bone and Joint Infection Society (EBJIS) nach einem Vorbereitungs- und Konsensusprozess erstmalig eine Definition für frakturassoziierte Infektionen publiziert.<sup>6</sup> Es wurde für septische Komplikationen nach Knochenbruch der allgemeine Begriff «fracture-related infection» (FRI), zu Deutsch frakturassoziierte Infektion, eingeführt. Es wurde beschlossen, dass einige diagnostische Merkmale die definitive Diagnosestellung eines frakturassoziierten Infektes erlauben. Das Vorhandensein mindestens eines dieser sogenannten «bestätigenden Kriterien» («confirmatory criteria») sichert die Diagnose einer frakturassoziierten Infektion. <br />Des Weiteren wurde eine Reihe von weniger spezifischen Merkmalen, sogenannten «hinweisenden Kriterien» («suggestive criteria»), definiert.<sup>6</sup> <br />Diese Kriterien können auch bei aseptischen Komplikationen vorliegen, sollten jedoch das Behandlungsteam dazu veranlassen, weitere Untersuchungen in die Wege zu leiten, um eine Infektion auszuschliessen oder zu bestätigen.<sup>6</sup> <br />In einem zweiten internationalen Konsensustreffen, welches neben AO Foundation und EBJIS von der Orthopaedic Trauma Association (OTA) sowie der Pro-Implant Foundation unterstützt wurde, wurde die FRI-Definition entsprechend neuer Evidenz aktualisiert und Empfehlungen zur Diagnosestellung und Behandlung von frakturassoziierten Infektionen wurden formuliert. Die aktuelle FRI-Definition mit den «bestätigenden» und «hinweisenden» Kriterien ist in Tabelle 1 zusammengefasst.<sup>5</sup></p> <h2>Diagnostische Kriterien</h2> <p>Die Diagnostik der FRI umfasst neben der detaillierten Anamnese und klinischen Untersuchung auch Laboruntersuchungen sowie bildgebende Verfahren. Sämtliche Befunde werden interdisziplinär besprochen, um einen gemeinsamen chirurgisch- medizinischen Behandlungsplan zu erstellen. Möglicherweise sind weitere Untersuchungen oder Interventionen notwendig, um lokale (z. B. Durchblutungsstörungen) oder systemische (z. B. entgleister Diabetes mellitus) Einschränkungen zu behandeln und damit eine bessere Ausgangssituation für das operative Vorgehen zu schaffen.<sup>4</sup> Das genau geplante chirurgische Débridement und die intraoperative Entnahme von tiefen sowie repräsentativen Biopsien stellen einen wesentlichen Kernpunkt sowohl der Diagnostik als auch der Behandlung dar. Oftmals ist die Diagnosestellung erst nach Eingang der mikrobiologischen und histologischen Ergebnisse möglich.<sup>4</sup></p> <p><strong>Klinische Kriterien<br /></strong>Nur zwei klinische Merkmale erlauben die definitive Diagnose einer FRI und gelten somit als «bestätigende Kriterien» (Tab. 1): einerseits die Eitersekretion aus der Operationswunde bzw. die Detektion von Eiter während der chirurgischen Exploration, andererseits das Vorhandensein einer Wunddehiszenz/Fistel bis auf den Knochen oder das Implantat.<sup>6</sup> Aufgrund mangelnder Evidenz zur prädiktiven Wertigkeit von systemischen und lokalen Infektzeichen (Tab. 1) sind diese als «hinweisende » Kriterien zu sehen, welche eine weitere Abklärung erfordern.<sup>5, 6</sup></p> <p><strong>Infektionsparameter im Blut</strong> <br />Die am häufigsten gemessenen Infektionsparameter im Blut sind die Leukozyten bzw. Neutrophilen, das CRP (C-reaktives Protein) sowie die Blutsenkungsgeschwindigkeit. Ein Anstieg der Leukozyten wie auch des CRP kann ein Hinweis auf einen Infekt sein, wird aber auch bei etlichen nicht infektiösen Zuständen, wie nach einem Trauma, nach einer Operation, bei steriler Entzündung, systemischen entzündlichen Erkrankungen und Neoplasien, gesehen. So wurden nach spinalchirurgischen Eingriffen maximale Leukozytenwerte am 3. postoperativen Tag gemessen, wonach es zur Normalisierung zwischen dem 4. und 6. Tag kam.<sup>7</sup> Bei Frakturpatienten kommt es zu einem CRP-Anstieg bis zu einem Maximum am 2. Tag und dann zu einem Rückgang zu normalen Werten nach 2 Wochen.<sup>8</sup> Die Blutsenkungsgeschwindigkeit erreicht ihr Maximum 7–11 Tage nach spinaler Chirurgie und normalisiert sich graduell innerhalb von 6 Wochen. Eine kürzlich publizierte Metaanalyse ergab, dass die erwähnten Parameter nur eine ungenügende Sensitivität/Spezifität besitzen, um alleine eine späte/chronische FRI nachzuweisen oder auszuschliessen.<sup>9</sup> Die Laborparameter sind daher nur im Gesamtkontext des individuellen Patienten zu interpretieren und können als «hinweisende Kriterien» für einen frakturassoziierten Infekt benutzt werden, um weitere diagnostische Schritte einzuleiten.</p> <p><strong>Bildgebung</strong> <br />Die drei Indikationen für die diagnostische Bildgebung zur Abklärung einer FRI sind:</p> <ol> <li>mehr Gewissheit über die Anwesenheit oder Abwesenheit einer FRI,</li> <li>Darstellung von pathologischen Details für die Operationsplanung (wie Sequester, Fistelgänge oder Abszesse),</li> <li>Erfassung der Vitalität des Knochens sowie der Knochenbruchheilung und der Stabilität des osteosynthetischen Konstruktes.</li> </ol> <p>Für diese Zwecke hat der Kliniker die Wahl zwischen verschiedenen radiologischen und nuklearmedizinischen Bildgebungstechniken. Diese hängt von den örtlichen Vorlieben und der Verfügbarkeit ab, wobei konventionelle Radiografie, Computertomografie (CT), Magnetresonanztomografie (MRT), Dreiphasen-Knochenscan, Fluorodesoxyglukose-Positronenemissionstomografie (FDG-PET) und Leukozytenszintigrafie am gebräuchlichsten sind.<sup>5<br /></sup>Das konventionelle Röntgen ist die Modalität der ersten Wahl.<sup>10</sup> Es ist generell verfügbar, kostengünstig, schnell durchzuführen und weist eine geringe Strahlenbelastung auf. Die Röntgenaufnahme liefert Basisinformationen zur Anatomie, zur Integrität und Stabilität des osteosynthetischen Konstruktes sowie zur Vitalität des Knochens und damit zur fortschreitenden Knochenbruchheilung.<sup>1, 4</sup> Aufgrund der generellen Verfügbarkeit eignet sich das konventionelle Röntgen besonders für die Nachfolgeuntersuchungen. Die CT-Untersuchung kann durchgeführt werden, wenn weitere Details erforderlich sind, und sie ist besser geeignet, um das Vorhandensein von Sequester aufzudecken. Allgemein anerkannte, auf eine Infektion «hinweisende Kriterien» in der konventionellen Radiografie und CT sind Implantatlockerung, Osteolyse, nicht voranschreitende Knochenbruchheilung (Pseudarthrose), Sequestrierung und periostale Knochenbildung.<sup>6</sup><br />Das MRT ist besonders geeignet, um Pathologien der Weichteile zu visualisieren, und besitzt eine hohe Sensitivität, um morphologische Knochenstrukturveränderungen zu detektieren. Dies sind wichtige Informationen für die detaillierte Operationsplanung. Es kann jedoch schwierig sein, zwischen Veränderungen aufgrund von Infektionen, von Entzündungen und normaler Gewebeheilung zu unterscheiden. Weiter können Artefakte durch einliegendes Osteosynthesematerial die Beurteilung beeinträchtigen.<sup>5, 11, 12</sup><br />Die nuklearmedizinischen Untersuchungstechniken (FDG-PET/CT, Leukozytenszintigrafie, SPECT/CT) weisen eine höhere diagnostische Genauigkeit auf, sind jedoch für sich alleine noch nicht ausreichend für die definitive Diagnosestellung einer FRI. Daher wurden nuklearmedizinische Infektzeichen in der Konsensusdefinition als «hinweisende Kriterien» aufgenommen.<sup>5</sup><br />Zusammenfassend lässt sich festhalten, dass jedes radiologische Verfahren sowohl Vor- als auch Nachteile hat und je nach Fragestellung eingesetzt wird. Derzeit gibt es keine Evidenz dafür, dass eine Technik einer anderen überlegen ist.<sup>5, 6</sup></p> <p><strong>Mikrobiologie</strong><br />Der kulturelle Nachweis des gleichen Erregers in zwei separaten tiefen Gewebeproben (inkl. Sonikationsflüssigkeit) gilt als «bestätigendes Kriterium» für die Diagnose einer FRI.<sup>6</sup> Nur mit der Kultur lässt sich die antibiotische Empfindlichkeit des verantwortlichen Erregers untersuchen, um die antibiotische Therapie gezielt daran anzupassen. Um falsch-negative Kulturen zu vermeiden, sollten mindestens 2 Wochen vor Probenentnahme keine Antibiotika verabreicht worden sein. Während des operativen Débridements sollten vorzugsweise 5 oder mehr tiefe Gewebe-/Flüssigkeitsproben dem Ort des Infektgeschehens entnommen und unmittelbar der mikrobiologischen und histologischen Untersuchung zugeführt werden. Es wird empfohlen, während der Probenentnahme gleichzeitige Manipulationen zu minimieren («No-touch»-Technik) und jeweils separate, ungebrauchte Instrumente für die Probengewinnung zu benutzen, um Kontaminationen zu vermeiden. Oberflächliche Proben der Haut oder von Fistelgängen sollten vermieden werden, da diese mehrheitlich die kolonisierenden und nicht die infektverantwortlichen Erreger in der Tiefe nachweisen.<sup>13</sup> Ebenso sollten Abstriche aufgrund der niedrigen Sensitivität im Vergleich zu Gewebeproben vermieden werden.<sup>14</sup> Falls Implantatmaterial entnommen wird (wie Platten oder Marknägel), kann dieses dem mikrobiologischen Labor zur Sonikation gesendet werden. Die Sonikation kann die auf einem Implantat sesshaften Mikroorganismen lösen und der Kultur zugänglich machen. Allerdings ist aufgrund spärlicher Datenlage der zusätzliche Nutzen der Sonikation bei FRI noch unklar und muss erst noch etabliert werden.<sup>15</sup> Ebenso sind weitere Studien nötig, um den Nutzen des Nachweises von bakterieller DNA mittels PCR («polymerase chain reaction») bei FRI zu bewerten.<sup>5</sup><br /> Zusammenfassend kann ein klares Protokoll der Probengewinnung und -verarbeitung die Diagnose und somit die Behandlungsmöglichkeiten bei Patienten mit FRI verbessern.</p> <p><strong>Histologie</strong><br />Der direkte histopathologische Erregernachweis in tiefen Gewebeproben mit spezifischen Färbemethoden für Bakterien oder Pilze (z. B. Gram-Färbung) ist ein «bestätigendes Kriterium» für eine FRI. Bei chronischen Infektionen sowie Spätinfektionen (wie beispielsweise bei der Pseudarthrose) ist der histologische Nachweis von mehr als 5 Neutrophilen pro Gesichtsfeld (bei 400-facher Vergrösserung) diagnostisch für eine FRI. Die gänzliche Abwesenheit von Neutrophilen schliesst sehr wahrscheinlich eine Infektion aus.<sup>6, 16</sup></p> <h2>Schlussfolgerung</h2> <p>Ein multidisziplinärer Ansatz ist der Schlüssel für eine erfolgreiche Behandlung von FRI, und komplexere Fälle sollten in einem dafür spezialisierten Zentrum behandelt werden. Die klinischen Symptome sind nicht immer eindeutig. Deshalb sollte besonders bei einer verzögerten oder ausbleibenden Knochenheilung immer an eine FRI gedacht werden. Im Rahmen des diagnostischen Algorithmus sollen die oben aufgeführten diagnostischen Kriterien untersucht und die Befunde interdisziplinär besprochen werden.<br />Das Vorliegen mindestens eines «bestätigenden Kriteriums» erlaubt die Diagnose einer FRI, wobei das Vorliegen «hinweisender Kriterien» (Tab. 1) das multidisziplinäre Behandlungsteam veranlassen sollte, eine weitere Abklärung im Rahmen des diagnostischen Algorithmus durchzuführen, um die Verdachtsdiagnose zu erhärten oder zu widerlegen.</p> <p><strong>Anmerkungen und Danksagung</strong> <br />Dieser Artikel fasst die Empfehlungen der internationalen FRI Consensus Group, unterstützt durch AO Foundation, Orthopaedic Trauma Association (OTA), Pro-Implant Foundation und European Bone and Joint Infection Society (EBJIS), zur Definition und Diagnosestellung von frakturassoziierten Infektionen zusammen.<sup>5</sup> Ein besonderer Dank gilt allen Mitgliedern der FRI Consensus Group.</p></p>
<p class="article-footer">
<a class="literatur" data-toggle="collapse" href="#collapseLiteratur" aria-expanded="false" aria-controls="collapseLiteratur" >Literatur</a>
<div class="collapse" id="collapseLiteratur">
<p><strong>1</strong> Metsemakers WJ et al.: Infection after fracture fixation: current surgical and microbiological concepts. Injury 2018; 49: 511-22 <strong>2</strong> Depypere M et al.: Pathogenesis and management of fracture-related infection. Clin Microbiol Infect 2019; S1198-743X(19)30447 <strong>3</strong> Mills L et al.: The multifactorial aetiology of fracture nonunion and the importance of searching for latent infection. Bone Joint Res 2016; 5: 512-9 <strong>4</strong> Morgenstern M et al.: Diagnostic challenges and future perspectives in fracture-related infection. Injury 2018; 49(Suppl 1): S83-S90 <strong>5</strong> Govaert GA et al.: Diagnosing fracture-related infection: current concepts and recommendations. J Orthop Trauma 2019; doi: 10.1097/BOT.0000000000001614 <strong>6</strong> Metsemakers WJ et al.: Fracture-related infection: a consensus on definition from an international expert group. Injury 2018; 49: 505- 10 <strong>7</strong> Kraft CN et al.: CRP and leukocyte-count after lumbar spine surgery: fusion vs. nucleotomy. Acta Orthop 2011; 82: 489-93 <strong>8</strong> Neumaier M, Scherer MA: C-reactive protein levels for early detection of postoperative infection after fracture surgery in 787 patients. Acta Orthop 2008; 79: 428-32 <strong>9</strong> van den Kieboom J et al.: Diagnostic accuracy of serum inflammatory markers in late fracture-related infection: a systematic review and meta-analysis. Bone Joint J 2018; 100-B: 1542-50 <strong>10</strong> Govaert GA et al.: Diagnostic strategies for posttraumatic osteomyelitis: a survey amongst Dutch medical specialists demonstrates the need for a consensus protocol. Eur J Trauma Emerg Surg 2018; 44: 417-26 <strong>11</strong> Govaert GA et al.: Accuracy of diagnostic imaging modalities for peripheral post-traumatic osteomyelitis – a systematic review of the recent literature. Eur J Nucl Med Mol Imaging 2017; 44: 1393-407 <strong>12</strong> Kaim A et al.: Chronic post-traumatic osteomyelitis of the lower extremity: comparison of magnetic resonance imaging and combined bone scintigraphy/immunoscintigraphy with radiolabelled monoclonal antigranulocyte antibodies. Skeletal Radiol 2000; 29: 378-86 <strong>13</strong> Mackowiak PA et al.: Diagnostic value of sinus-tract cultures in chronic osteomyelitis. JAMA 1978; 239: 2772-5 <strong>14</strong> Aggarwal VK et al.: Swab cultures are not as effective as tissue cultures for diagnosis of periprosthetic joint infection. Clin Orthop Relat Res 2013; 471: 3196-203 <strong>15</strong> Onsea J et al.: Accuracy of tissue and sonication fluid sampling for the diagnosis of fracture-related infection: a systematic review and critical appraisal. J Bone Jt Infect 2018; 3: 173-81 <strong>16</strong> Morgenstern M et al.: The value of quantitative histology in the diagnosis of fracture-related infection. Bone Joint J 2018; 100-B: 966-72</p>
</div>
</p>