Der native Gelenkinfekt: „State of the Art“-Versorgung
Autoren:
Dr. Philipp Proier
Prof. Dr. Tobias Gotterbarm
Dr. Bernhard Schauer
Universitätsklinik für Orthopädie und Traumatologie
Kepler Universitätsklinikum Linz
Korrespondierender Autor:
Dr. Philipp Proier
Die bakterielle septische Arthritis der großen Gelenke ist ein orthopädischer Notfall. Sie führt bei verzögerter Behandlung unumgänglich zur irreversiblen Gelenkdestruktion und zum Funktionsverlust. Eine Mortalität von 11–15%1 wird von den Behandlern gerne verdrängt, sollte aber in der Entscheidungsfindung zur aktiven operativen Indikation dringend berücksichtigt werden.
Keypoints
Native Gelenkinfektionen sind ein Notfall und treten gehäuft bei schwachem Immunsystem, infektiöser Grunderkrankung oder in zunehmendem Alter auf.
Die laborchemischen Parameter zeigen uns den Infektzustand vor 24 Stunden, entscheidend für die Indikation sind die Synoviaanalyse und – für die postoperative Therapie – die Bakterienkultur.
Die frühe Diagnose, der Nachweis von spezifischen Erregern sowie die anschließende operative Intervention mit abgestimmten antibiotischen Behandlungen führen zum Erfolg.
Die arthroskopische Gächter-Klassifikation ist ein nützliches Tool, um eine Prognose zu stellen oder die Notwendigkeit eines radikalen offenen Débridements zu indizieren.
Die Gelenksimmobilisation nach operativer Intervention ist obsolet.
Ätiologisch können endogene und exogene Ursachen für eine Gelenkinfektion unterschieden werden. Endogene Ursache ist die hämatogene Streuung im Rahmen einer Bakteriämie, exogene Ursachen können intraartikuläre Punktionen oder Injektionen von Medikamenten sein. Insbesondere Steroidinjektionen stellen ein erhebliches, vom Behandler häufig unterschätztes Risiko dar.2 Es bedarf in jeder orthopädisch-traumatologischen Behandlungseinheit eines standardisierten Algorithmus zur schnellen und exakten Diagnosestellung sowie anschließend einer unmittelbaren und längerfristigen Therapie.
Die Unterscheidung zwischen akuten, subakuten und chronischen Infekten wird in der Literatur mit unterschiedlichen Zeitintervallen definiert, die genaue Definition spielt aber für die klinische Behandlung eine untergeordnete Rolle. Entscheidend zur Rettung der Gelenksintegrität ist die rasche Behandlung der akuten Gelenkinfektion, die durch ein ausgeprägtes klinisches Beschwerdebild mit den Kardinalzeichen einer Entzündung (Rötung, Schwellung, Überwärmung, Schmerzen, eingeschränkte Funktion) und in 50% mit Fieber einhergeht.3 Der chronische Infekt oder Low-grade-Infekt tritt zeitlich verzögert auf und präsentiert sich klinisch sehr vielfältig, wird daher häufig verkannt und geht mit einer schleichenden Gelenksdestruktion einher. Therapie und Vorgehensweise unterscheiden sich dahingehend, dass bei der akuten Infektion die Therapie der endgültigen Diagnostik vorangestellt ist, bei der chronischen Infektion steht die Diagnostik (Keimbestimmung) vor der Therapie.
Pathogenese
Unabhängig vom Infektionsweg führen Mikroorganismen im Gelenkraum zu einer akuten synovialen Entzündungsreaktion, welche zum Gelenkempyem führt. Innerhalb von Stunden füllen aktivierte Entzündungszellen den Synovialraum und setzen Enzyme und Zytokine frei. Durch den Entzündungsprozess erhöht sich der intraartikuläre Druck und somit wird die Nährstoffversorgung der Synovialis eingeschränkt. Die Folge ist eine irreversible chemisch-toxische Schädigung des Knorpels und des darunterliegenden subchondralen Knochens binnen weniger Stunden.4
Die Virulenz des Erregers sowie die individuelle Immunantwort des Patienten sind entscheidend dafür, ob eine akute oder eine chronische Symptomatik auftritt. Die häufigsten Erreger von akuten Gelenkinfektionen sind Staphylococcus aureus, Streptokokken und eine Vielzahl von gramnegativen Erregern, wie z.B. Pseudomonas aeruginosa.4–6
Chronische Gelenkinfekte werden häufig von gering virulenten Erregern der physiologischen Hautflora wie koagulasenegativen Staphylokokken und Cutibakterien ausgelöst.7 In 80–90% der septischen Arthritiden ist nur ein Gelenk betroffen: in absteigender Häufigkeit Knie-, Hüft-, Schulter-, Sprung-, Ellenbogen- und Handgelenk.8
Diagnostisches Vorgehen
Anamnese
Der genaue Symptombeginn und die klinische Präsentation sind entscheidend für die Einleitung des akuten oder chronischen Therapiepfades. Risikofaktoren für die Entwicklung einer Gelenkinfektion sind ein Alter von über 60 Jahren, eine durchgemachte Bakteriämie, Grunderkrankungen wie Diabetes mellitus, Malignom, Leberzirrhose, Nierenerkrankungen und rheumatoide Arthritis, aber auch Drogen- oder Alkoholmissbrauch. Unterschätzt werden iatrogene Ursachen, wie die Infiltration eines Gelenkes, insbesondere mitCortison, und vorhergehende Gelenksoperationen.5
Labor
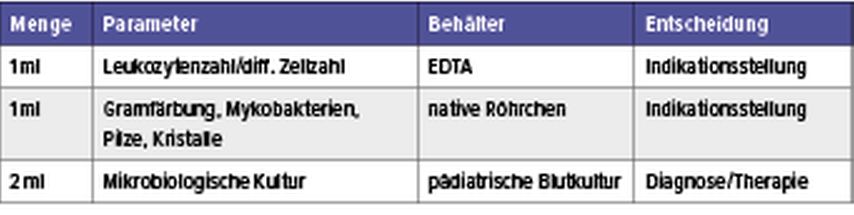
Laborwerte und Entzündungsmarker aus Serum und Gelenkflüssigkeit dienen als Hilfsmittel, wenn der klinische Verdacht auf einen nativen Gelenkinfekt besteht. Blutkulturen müssen vor der Antibiotikagabe abgenommen werden, um falsch negative Ergebnisse zu vermeiden. Leukozytenzahl, C-reaktives Protein (CRP) aus dem Blut, kombiniert mit Gerinnungs-, Nieren- und Leberparametern als Ausgangswert für die Planung des antibiotischen Regimes, sind postoperativ wiederholt zu erheben. Procalcitonin kann als Parameter zur Unterscheidung einer septischen von einer reaktiven Arthritis verwendet werden. Die laborchemischen Parameter hinken dem Infektgeschehen etwa 24 Stunden hinterher und sollten weder als alleinige Entscheidungsträger dienen noch sollte bei eindeutiger Klinik deren Anstieg abgewartet werden.
Gelenkspunktion und Synoviaanalyse
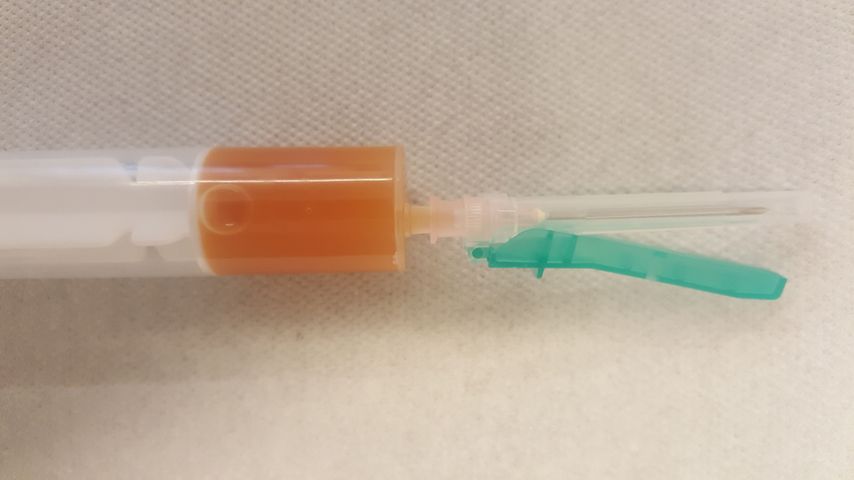
Eine entscheidende diagnostische Säule und Goldstandard ist die zwingende Punktion des Gelenkes zur Aspiration der Synovialflüssigkeit. Auch in der akuten Infektsituation ist zur Prophylaxe einer iatrogen verursachten Infektion die sterile Durchführung der Gelenkspunktion (Stempeldruck nach Perforation der Kutis oder Stichinzision an der Punktionsstelle) zur Vermeidung einer Gelenkskontamination essenziell. Bei liegender Kanüle erfolgt die Abpunktion des Ergusses durch Spritzenwechsel, um weitere Punktionen zu vermeiden. Die Infiltration der Punktionsstelle mit Lokalanästhetikum führt zu einem geringeren Keimnachweis bei der mikrobiologischen Analyse. Transportbehältnisse sind durch die Assistenz anzureichen, um die Befüllung ohne Berührung zu ermöglichen („Don’t touch“-Technik). Die Bebrütungsdauer sollte 14 Tage betragen, um niedrig virulente Keime insbesondere bei der chronischen Infektsituation darstellen zu können.
Analog zur Detektion eines periprothetischen Infekts (EBJIS-Diagnosekriterien: >2000 Leu/μl oder >70% polymorph)9 hilft die Zellzahlbestimmung im Gelenkpunktat differenzialdiagnostisch auch beim nativen Gelenkinfekt. Für das native Gelenk existieren viele Differenzialdiagnosen, welche zu einer falsch positiven Diagnose führen können. Eine erhöhte, in der Quantität stark variierende Zellzahl tritt bei rheumatischen Erkrankungen, Kristallarthropathien, chronischer Instabilität bzw. in den ersten Wochen nach einer Operation auf. Das Vorhandensein von Kristallen bzw. das Fehlen von Mikroorganismen bei der Gramfärbung lässt keinen Ausschluss einer Infektion zu und es sollte ein Zweifelsfall immer als Gelenkinfektion therapiert werden.
Einzig der Erregernachweis in der Gramfärbung (50% der Infekte) ist sicher beweisend für einen Gelenkinfekt. Eine Leukozytenzahl von über 20000/µl mit mehr als 90% polymorphkernigen Zellen macht eine Gelenkinfektion sehr wahrscheinlich.6 Chronische Gelenkinfektionen können oft oligo- bis asymptomatisch sein. Die geringere Immunantwort auf gering virulente Erreger führt auch zu einer geringen Leukozytenzahl bei der Punktion. Werte von >10000 Leukozyten/µl sind bereits auffällig für eine chronische Gelenkinfektion.
Bildgebung
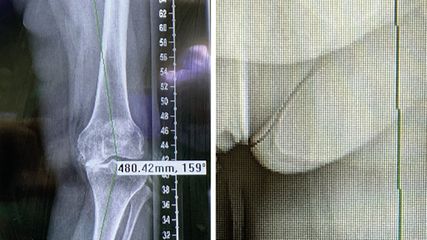
Für das akute Infektmanagement ist eine Bildgebung nicht zwingend erforderlich. Das konventionelle Röntgenbild hilft jedoch, vorbestehende Gelenkserkrankungen zu dokumentieren. Das Vorliegen von Fremdmaterial (Implantate, Sehnenplastiken etc.) nach Frakturversorgung oder Bandplastiken ändert nicht die Dringlichkeit der operativen Akutintervention, nur ist zusätzlich die Entfernung aller Fremdmaterialien zu erwägen, insbesondere bei nicht mehr benötigtem Material, z.B. Osteosyntheseplatte bei verheilter Fraktur (siehe Pro-implant-Foundation: Guidelines zu Implantat-assoziierten Infektionen nach Frakturversorgung). Oft ist eine Entfernung von Fremdmaterial unumgänglich; zumindest tauschbare Anteile müssen bei Erstintervention gewechselt werden.
Bei immunmodulierten Patienten fehlen die klinischen Kardinalsymptome und Schmerzen. Der isolierte Gelenkserguss muss den Behandler an eine Gelenkinfektion denken lassen und die Indikation zum operativen Vorgehen, auch bei normwertigen synovialen Leukozyten und Infektparametern, ist großzügig stellen.
Die Magnetresonanztomografie wird vor allem beim chronischen Gelenkinfekt zur Darstellung einer Begleitosteomyelitis, von Gewebeabszessen und gekämmerten Infektlogen angewandt und präzisiert die Planung der Infektsanierung und Resektion.
Therapeutisches Vorgehen
Die Therapie des Gelenkinfektes beruht auf drei Säulen:
chirurgische Erregerreduktion im Gelenk
antibiotische Erregerbekämpfung
physiotherapeutische Prävention der Arthrofibrose
Der Schlüssel zum Erfolg sind die frühzeitige Diagnose und Einleitung der chirurgischen und antibiotischen Therapie.10
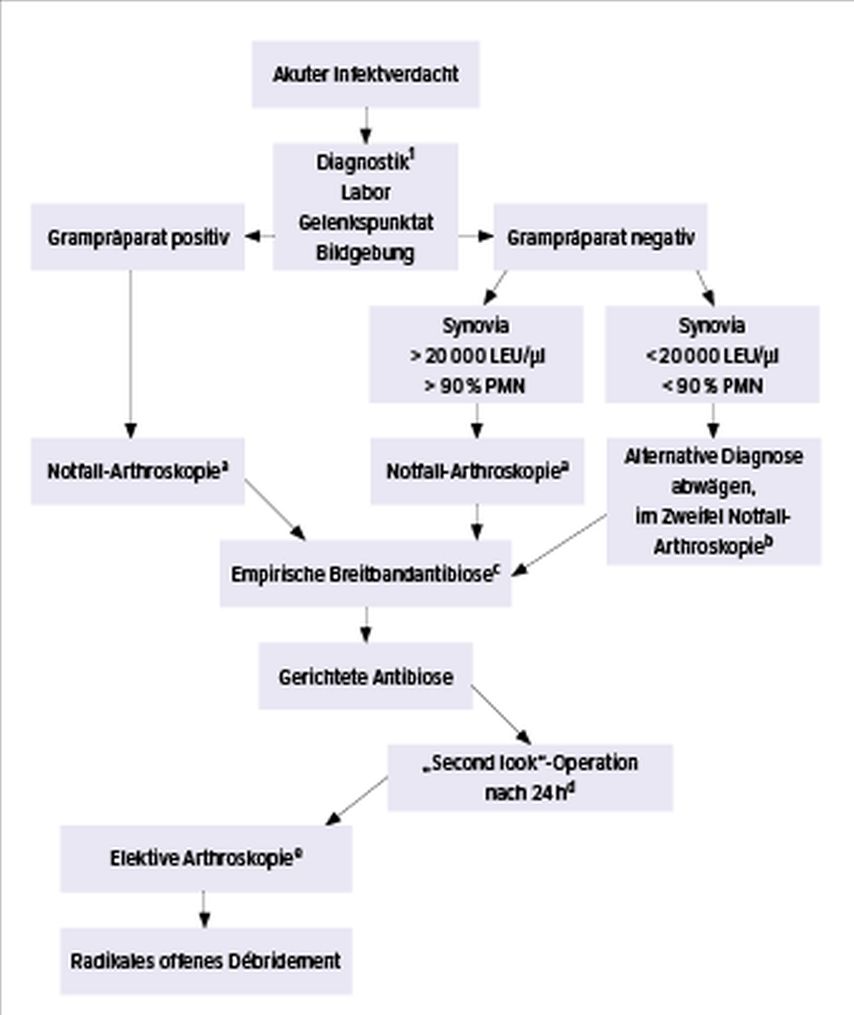
Abb. 2:
1 Blutlabor: CRP, LEU, Blutkultur, LFP, NFP, Prokalzitonin; Gelenkpunktat: LEU, PMN %, Gramfärbung, Kultur, Kristalle; Bildgebung: Röntgen, ggf. MRT, Sonografie
a Singleshot-Antibiose -- trockene Arthroskopie, Entnahme von 5 Gewebeproben zur mikrobiologischen und histologischen Aufarbeitung, arthroskopische Spülung von mind. 9 l, Gächter-Stadium 4: Konversion auf Gelenksarthrotomie und radikales Débridement
b Rheumatische Erkrankung, aktivierte Arthrose, extraartikulärer Infekt, Gicht abwägen; im Zweifel immer diagnostische Arthroskopie und Gewebeproben entnehmen (z. B. PVNS)
c Empirische Antibiose unter Berücksichtigung von MRSA, grampos. und -neg. Mikroorganismen; bei einliegendem Fremdmaterial biofilmaktives Antibiotikum
d Bei Zustandsverschlechterung (Sekretion, Schwellung, Schmerz) erneuter Anstieg der Infektparameter.
e Operation wie a, Entfernung von einliegenden Fremdmaterialien, nach der dritten insuffizienten arthroskopischen Spülung offenes radikales Débridement
Chirurgische operative Therapie
Die Überlegenheit der Arthroskopie gegenüber dem offenen Débridement konnte in unterschiedlichen Arbeitsgruppen dargestellt werden.11 Die Therapie folgt angelehnt an die von Gächter12 beschriebenen Stadien der Gelenksinfektion (Tab.2). Im Stadium I–III erfolgt eine arthroskopische Spülung des gesamten Gelenkes. Débridiert werden im Stadium III die Fibrinablagerungen. Die Indikation zur Synovialektomie sollte zurückhaltend gestellt werden, um die natürliche Barrierefunktion zu erhalten.13
Intraoperativ werden in der Regel 5 Gewebeproben von unterschiedlicher Lokalisation für die mikrobiologische und histologische Untersuchung gewonnen. Ob und wie häufig eine Arthroskopie wiederholt werden muss, ist vom klinischen und laborchemischen Therapieansprechen abhängig. V.A.C.®, V.A.C. Instill® oder eine Spül-Saug-Drainage im Gelenk erhöhen das Risiko für Sekundärinfektionen und führen zur Knorpeldestruktion. Die gängigen Antiseptika (Chlorhexidin und Polyhexanid) führen zur Chondrolyse und Zerstörung des hyalinen Knorpels und sollten nicht zur Spülung angewendet werden.14
Im Stadium IV oder bei Therapieversagen ist eine offene Arthrotomie mit radikalen Débridement, totaler Synovektomie und Entfernung des infizierten Knorpels und der evtl. begleitenden Osteomyelits erforderlich, da die Infektpersistenz häufig auf das bradytrophe Knorpelgewebe zurückzuführen ist. Das Einlegen intraartikulärer Antibiotikaträger induziert eine chemische Synovitis und ist daher erst bei vollständiger Gelenksdestruktion sinnvoll. Eine Versorgung mit antibiotikabeladenem artikulierendem Zementspacer zur Vorbereitung einer sekundären Gelenksendoprothese kann auch erwogen werden und ist häufig bei chronischen Infekten als letzte Maßnahme sinnvoll. Zwischen den operativen Eingriffen sollte das Gelenk physiotherapeutisch mobilisiert werden, um eine Anschlussarthrofibrose zu verhindern. Physiotherapie sollte auch in der weiteren Nachbehandlung fortgeführt werden. Eine Immobilisation des Gelenkes gilt heute als obsolet.10
Praktisches Vorgehen
Der Behandlungsalgorithmus des Gelenkinfektes sieht die erste Antibiotikagabe erst im Operationssaal vor. Eine „Singleshot“-Antibiose dient zur perioperativen Prophylaxe einer sekundären Infektion durch intraoperativ eindringende Erreger und reduziert dabei nicht die mikrobiologische Nachweisbarkeit von Erregern aus den entnommenen Proben.15
Im eigenen Vorgehen erfolgt die Gewebeprobengewinnung im Zuge einer anfangs „trocken“ durchgeführten Arthroskopie mit dem Rongeur. Auf Abstriche oder Proben aus einem Fistelgang soll aufgrund der Kreuzkontamination durch die Hautflora verzichtet werden.
Die molekularbiologischen Proben werden in einem COPAN-ESwab™-Röhrchen bei Raumtemperatur abgelegt. Im abgepufferten Nährmedium können insbesondere die anaeroben Keime 48Stunden überdauern, während sie nach der Lagerung in nativen Röhrchen nicht nachgewiesen werden können.
Zusätzlich zu den benötigten Standardportalen zur Darstellung des ganzen Gelenkes wird in diagonaler Richtung ein weiteres akzessorisches Portal mit Arbeitskanüle angelegt, über welche die Absaugung durchgeführt werden kann. Dies führt dazu, dass ein schnellerer Durchsatz von mindestens 10 l Ringerlösung möglich ist, und gleichzeitig kommt es zu einer effektiveren Spülstromrichtung im Gelenk, da „Inflow“ und „Outflow“ konträr zueinander gelegen sind.
Am Beispiel des Kniegelenkes wird ein laterales suprapatelläres Portal etwa 1cm proximal des superolateralen Patellapols angelegt. Die Anlage erfolgt in Outside-in-Technik bei gestrecktem Kniegelenk. Wird das Arthroskop über das anterolaterale Portal durch die Notch medial des VKB ins dorsale Kompartiment geschoben, so kann auch der posteriore Recessus effektiv gespült werden. Bei anhaltenden Infektionssymptomen unter Antibiose wird die arthroskopische Spülung bis zu 3x wiederholt. In der Regel werden im Verlauf 3 Gewebeproben für die mikrobiologische Untersuchung gewonnen, um eine Veränderung des Keimspektrums detektieren zu können.
Antibiotische medikamentöse Therapie
Nach der Operation erfolgt die initiale empirische Breitspektrumantibiose. Sobald ein Antibiogramm vorliegt, erfolgt die Antibiose orientiert an der Resistenz des Erregers.
Das empirische Antibiotikaregime sollte je nach Komorbiditäten Methicillin-resistenten Staphylococcus aureus sowie gramnegative und grampositive Mikroorganismen abdecken.
Entscheidend sind die adäquate intravenöse Dosierung, die bakterizide Wirkung des Antibiotikums und die Gewebegängigkeit. Im eigenen Vorgehen erfolgt die intravenöse Therapie für die Dauer des stationären Aufenthaltes (1–2 Wochen), gefolgt von einer 4-wöchigen oralen Antibiose unter Berücksichtigung des Resistogramms der oralen Bioverfügbarkeit und Knochengängigkeit des Antibiotikums. Auf orale Betalaktame sollte aufgrund der genannten Kriterien verzichtet werden, dies entspricht leider nicht der gängigen Praxis.16
Eine verlängerte Antibiose wird bei einem zugrunde liegenden Primärfokus (z.B. beherdeter Zahn) oder nicht entfernbarem einliegendem Fremdmaterial (z.B. Kreuzbandplastik) erwogen, im zweiten Fall in der Kombination mit einer biofilmgängigen Kombinationstherapie (Rifampicin/Chinolone bei biofilmproduzierenden Bakterien und trockener Wunde), wenn das Gelenk erhalten werden kann und in den 12 Folgemonaten keine Gelenksendoprothese implantiert werden soll.
Resümee
Entscheidend für die Infektprophylaxe sind der internistisch „optimierte“ Patient, hohe Hygienestandards, das kritische Abwägen jeder invasiven Intervention und die frühe Mobilisation des Patienten. Retrospektiv zeigen sich bei anhaltender Infektion oder Gelenksdestruktion meistens typische vermeidbare Fehler, wie eine verzögerte oder unzureichende chirurgische Therapie oder ein fehlender Keimnachweis, z.B. durch verfrühte, undifferenzierte Antibiotikagabe. Ein standardisierter Therapiepfad ermöglicht eine gute Infektkontrolle, eine hohe Wahrscheinlichkeit einer Infektionsfreiheit und einen guten Funktionserhalt des zuvor infizierten nativen Gelenkes.
Literatur:
1 Gupta MN et al.: Prospective comparative study of patients with culture proven and high suspicion of adult onset septic arthritis. Ann Rheum Dis 2003; 62 2 Cole BJ, Schumacher HR: Injectable corticosteroids in modern practice. J Am Acad Orthop Surg 2005; 13 3 Margaretten ME et al.: Does this adult patient have septic arthritis? JAMA 2007; 297 4 Margaryan D et al.: Septic arthritis of the native joint and after ligamentoplasty: Diagnosis and treatment. Orthopade 2020; 49 5 Elsissy JG et al.: Bacterial septic arthritis of the adult native knee joint: a review. JBJS Rev 2020; 8 6 Mathews CJ et al.: Bacterial septic arthritis in adults. Lancet 2010; 375 7 Mühlhofer HML et al.: Native joint infections. Orthopade 2020; 49 8 Kaandorp CJE et al.: Incidence and sources of native and prosthetic joint infection: a community based prospective survey. Ann Rheum Dis 1997; 56 9 McNally M et al.: The EBJIS definition of periprosthetic joint infection. Bone Joint J 2021; 103-B 10 Petersen W et al.: Stage-adapted treatment of infection after reconstruction of the anterior cruciate ligament. Oper Orthop Traumatol 2014; 26 11 Böhler C et al.: Surgical treatment of shoulder infections: a comparison between arthroscopy and arthrotomy. J Shoulder Elb Surg 2017; 26 12 Stutz G, Gächter A: Diagnostik und stadiengerechte therapie von Gelenkinfekten. Unfallchirurg 2001; 104 13 Schuster P et al.: Septic arthritis after arthroscopic anterior cruciate ligament reconstruction: evaluation of an arthroscopic graft-retaining treatment protocol. Am J Sports Med 2015; 43 14 van Huyssteen AL, Bracey DJ: Chlorhexidine and chondrolysis in the knee. J Bone Joint Surg Br 1999; 81 15 Anagnostopoulos A et al.: Perioperative antibiotic prophylaxis has no effect on time to positivity and proportion of positive samples: a cohort study of 64 cutibacterium acnes bone and joint infections. J Clin Microbiol 2018; 56 16 Pérez-Prieto D et al.: Infections after anterior cruciate ligament reconstruction: which antibiotic after arthroscopic debridement? J Knee Surg 2017; 30
Das könnte Sie auch interessieren:
«Auch Patienten mit Demenz profitieren von einer chirurgischen Stabilisierung»
Patienten mit Hüftfraktur und einer leichten, mittelschweren oder schweren Demenz haben ein geringeres Risiko zu sterben, wenn sie operiert werden – vor allem wenn es sich um Kopf-Hals- ...
Stellenwert des individuellen Alignments in der Knieendoprothetik
Dieser Artikel erläutert die unterschiedlichen Alignmentkonzepte in der Knieendoprothetik und deren Stellenwert. Es ist davon auszugehen, dass die Rekonstruktion der individuellen ...
Patientenoptimierung in der orthopädischen Chirurgie
Die Patientenoptimierung vor orthopädischen Eingriffen, insbesondere in der Endoprothetik, spielt eine entscheidende Rolle für den Erfolg der Operation und die Zufriedenheit der ...