Krankheitsstabilisierung über 14 Monate
Autor:
OA Dr. Laurenz Schöffmann, MSc
Department für Hämatologie-Onkologie
Landeskrankenhaus Hochsteiermark
Standort Leoben
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Mit Trifluridin/Tipiracil (Lonsurf®) steht für Patienten mit metastasiertem kolorektalem Karzinom eine potente und etablierte orale Behandlungsoption ab der dritten Therapielinie zur Verfügung. In der Praxis zeigen sich Vorteile durch die Verträglichkeit mit Erhaltung der Lebensqualität über längere Zeiträume, wie der im Folgenden geschilderte Patientenfall von OA Dr. Laurenz Schöffmann demonstriert.
Keypoints
-
Der Zustand des Patienten war unter Trifluridin/Tipiracil mehr als ein Jahr stabil.
-
Der ECOG PS von 0–1 konnte während der Trifluridin/Tipiracil-Behandlung erhalten werden.
-
Die orale Applikation unterstützte den aktiven Lebensstil des Patienten.
-
Der Patient war fit genug für eine Viertlinientherapie.
Basierend auf der Phase-III-Studie RECOURSE erfolgte 2016 die Zulassung von Trifluridin/Tipiracil (Lonsurf®) für die Behandlung von Patienten mit metastasiertem kolorektalem Karzinom (mCRC), die bereits Fluoropyrimidin-, Oxaliplatin- und Irinotecan-basierte Chemotherapien sowie VEGF- und EGFR-Inhibitoren (nur bei RAS-Wildtyp) erhalten haben bzw. für diese nicht geeignet sind.1 In RECOURSE bewirkte Trifluridin/Tipiracil bei Patienten mit Adenokarzinom des Kolons oder Rektums nach zumindest zwei Standard-Chemotherapien gegenüber Placebo eine signifikante Verbesserung des medianen Gesamtüberlebens (7,1 vs. 5,3 Monate; HR: 0,68; p<0,001).2 2019 wurde die Zulassung um die Indikation des metastasierten Magenkarzinoms und Adenokarzinoms des gastroösophagealen Übergangs nach mindestens zwei systemischen Therapien im metastasierten Stadium erweitert.1
Essenzielle Entscheidung ab der Drittlinie
Bei entsprechend günstiger Tumorbiologie und langsamerem Wachstum überleben mCRC-Patienten oft Jahre; dies ist allerdings umso mehr ein Grund zu therapieren, da mit adäquaten Strategien häufig viele zusätzliche Monate (oder Jahre) an Lebenszeit gewonnen werden können und sich die Outcomes summieren. Viele Patienten erreichen dank der modernen Strategien die dritte oder vierte Behandlungslinie, in der für eine weitere Verbesserung der Prognose die Wahl der Therapeutika unter Berücksichtigung des Nebenwirkungsprofils ausschlaggebend ist. Aus meiner Sicht kommt insbesondere der Entscheidung zwischen Regorafenib und Trifluridin/Tipiracil Bedeutung zu, die als einzige orale Therapien eine IB-Empfehlung in der dritten Linie erhalten haben.3
Für die Gabe von Trifluridin/Tipiracil vor Regorafenib sprechenmeiner Ansicht nach die gute Verträglichkeit, die hohe Wirksamkeit mit teilweise langen Stabilisierungsraten und die Aussicht auf Kombinationen mit geeigneten Partnern aus anderen Medikamentenklassen, sobald entsprechende Zulassungen erfolgt sind (Phase-III-Studien mit Angiogeneseinhibitoren befinden sich im Laufen). Lange mit Trifluridin/Tipiracil therapierte Patienten weisen oftmals weiterhin einen guten ECOG-Performance-Status auf und können als Viertlinientherapie häufig Regorafenib oder eine Rechallenge in Anspruch nehmen.4 In der Zulassungsstudie RECOURSE behielten 84% der mit Trifluridin/Tipiracil behandelten Patienten einen ECOG-Performance-Status 0–1 bei und waren daher fit genug für weiterführende Therapien.2
Fallbeispiel: Progression nach 6Jahren
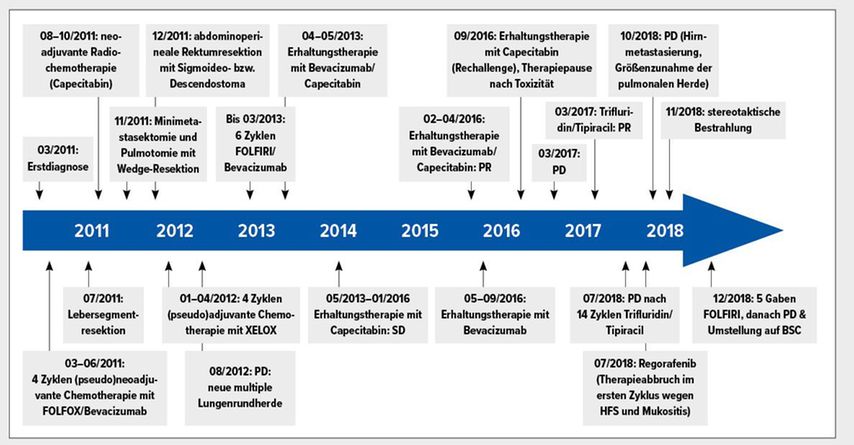
Bei einem 72-jährigen Patienten leiteten wir 2017 die Behandlung mit Trifluridin/Tipiracil ein, nachdem sechs Jahre zuvor im März 2011 ein metastasiertes Adenokarzinom des Rektums festgestellt worden war (endgültige postoperative Histologie: ypT3 N0 [0/16] M1b, G2, KRAS-mutiert, HER2/neu-negativ, mikrosatellitenstabil). Ab dem Diagnosezeitpunkt wurde zunächst eine Konversionstherapie mit FOLFOX/Bevacizumab über vier Zyklen durchgeführt (März bis Juni 2011), die im Juli 2011 von einer Lebersegmentresektion (Segment 7) sowie einer Minimetastasektomie und Wedge-Resektion bei Lungenmetastasen im November gefolgt war. Zudem erhielt der Patient eine neoadjuvante Radiochemotherapie (konkomitant mit Capecitabin) vor der geplanten abdominoperinealen Rektumresektion mit Sigmoideo- bzw. Descendostoma im Dezember 2011. Von Jänner bis April 2012 schloss sich die viermonatige (pseudo)adjuvante Behandlung mit Capecitabin plus Oxaliplatin (XELOX) an.
Bei Tumorfreiheit wurde Observanz eingeleitet, bereits im August 2012 manifestierten sich jedoch multiple Rundherde der Lunge. Sechs Zyklen FOLFIRI/Bevacizumab bewirkten eine partielle Remission bzw. Krankheitsstabilisierung. Als Erhaltungstherapie kam Capecitabin (die Kombination mit Bevacizumab war bei Stomablutung zunächst nicht möglich) über 2,5 Jahre bis zum Auftreten höhergradiger Toxizitäten (Tendinopathien, Hand-Fuß-Syndrom) im Jänner 2016 zur Anwendung. Nach dem Wechsel auf Bevacizumab wurde im Sommer 2016 noch einmal ein Therapieversuch mit Capecitabin (Rechallenge) gestartet und dann endgültig beendet. Dies war von einer längeren Therapiepause auf Patientenwunsch gefolgt.
Drittlinientherapie
Nach ca. einem halben Jahr Therapiefreiheit musste bei Krankheitsprogression (hepatal, abdominelle Lymphknoten) im März 2017 eine Entscheidung zwischen Regorafenib und Trifluridin/Tipiracil getroffen werden. Der Patient wies einen guten ECOG-Performance-Status von 0 auf, pflegte einen aktiven Lebensstil und wünschte keine Belastungen/Einschränkungen im Alltag durch die Therapie. Wir entschieden uns daher für die Verordnung von Trifluridin/Tipiracil, das ab März 2017 in einer Dosis von 75mg zweimal täglich zur Anwendung kam.
Unter dieser Behandlung konnte eine partielle Remission der pulmonalen Rundherde erreicht werden. Durch die orale Applikationsform ließen sich die Ambulanzbesuche auf ein Minimum reduzieren, und im Gegensatz zur vorherigen Anwendung von Capecitabin entwickelte der Patient kein Hand-Fuß-Syndrom.
Im September 2017 machte das Auftreten einer CT-morphologischen suspekten Milchglasverdichtung eine ergänzende pulmologische Vorstellung notwendig, wobei der Patient völlig asymptomatisch war. Die Abklärung ergab einen blanden Befund, der keine Therapieerweiterung erforderte. Eine Pilzinfektion konnte ausgeschlossen werden. Einmalig benötigte der Patient bei Neutropenie im September 2017 für einige Tage G-CSF (Filgrastim) und zeigte eine beginnende Alopezie, die sich im Verlauf aber ebenfalls stabilisierte und im Folgejahr nicht mehr angegeben wurde. Abgesehen davon manifestierten sich unter der Behandlung mit Trifluridin/Tipiracil keinerlei Toxizitäten. Der Patient blieb klinisch stabil und konnte seinen täglichen Aktivitäten uneingeschränkt nachgehen.
Weiterer Verlauf
Erst im Rahmen der Remissionskontrolle im Juli 2018 zeigte sich nach 14 Zyklen Trifluridin/Tipiracil 2x35mg/m2 eine Krankheitsprogression. Bei einem ECOG-Performance-Status von 0–1 erfolgte die Umstellung auf eine palliative Viertlinientherapie mit Regorafenib, die Behandlung musste jedoch aufgrund eines Hand-Fuß-Syndroms Grad III–IV und einer Mukositis Grad II bereits im ersten Zyklus abgebrochen werden. Nachdem Hirnmetastasen aufgetreten waren, erhielt der Patient im November 2018 eine stereotaktische Bestrahlung. Zuletzt kam eine palliative Folgelinie mit dosismodifiziertem FOLFIRI (66%) zum Einsatz, wobei nach fünf Gaben ein weiterer Progress der Hirnmetastasen Anlass zur Umstellung auf Best Supportive Care gab. Im April 2019 wurde der Patient auf unsere Palliativstation aufgenommen.
Insgesamt lässt sich bei der Betrachtung dieser Fallgeschichte festhalten, dass die Drittlinientherapie bei hoher Lebensqualität und Erhalt eines guten ECOG-Performance-Status bis zum neuerlichen Eintreten einer Progression 14 Monate lang wirksam war. In dieser Zeit manifestierten sich keine nicht dem Profil entsprechenden Nebenwirkungen, und der Patient konnte seinen aktiven Lebensstil aufrechterhalten.
Entgeltliche Einschaltung
Mit freundlicher Unterstützung durch Servier Austria GmbH
Literatur:
1 Fachinformation Lonsurf®, Stand Dezember 2020 2 Mayer RJ et al.: N Engl J Med 2015; 372: 1909-19 3 Van Cutsem E et al.: Ann Oncol 2016; 27(8): 1386-422 4 Klinischer Studienbericht: TPU-TAS-102-301-Protokoll (Phase-3-Studie RECOURSE); TAIHO Oncology, Inc.; Princeton, USA; 2014 (Data on File)