Biologika bei Asthma und COPD: Game-Changer in der personalisierten Therapie
Autor:
OA Dr. Christian Felix Summereder
Pneumologie
Ordensklinikum Linz Elisabethinen
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Biologika haben die Therapiemöglichkeiten für schweres Asthma transformiert und bieten nun auch für ausgewählte COPD-Patienten sowie bei diversen anderen inflammatorischen Erkrankungen wertvolle, zielgerichtete Optionen. Eine präzise Patientenauswahl bleibt der Schlüssel zum erfolgreichen Einsatz dieser innovativen Medikamente, die für viele Betroffene die Bezeichnung „Game-Changer“ verdienen.
Keypoints
-
Monoklonale Antikörper haben in den letzten Jahren eine Ära der personalisierten Therapiemöglichkeiten bei Asthma und COPD eingeläutet.
-
Biomarker wie Bluteosinophile, FeNO oder IgE-Sensibilisierung ermöglichen den Nachweis der Typ-2-Inflammation bei schwerem Asthma und stellen eine Indikation für die Biologikatherapie dar.
-
Ein Anteil der COPD-Patienten weist eine Eosinophilie auf, die mit häufigeren Exazerbationen assoziiert ist. Für diesen Phänotyp sind bereits Biologika als Add-on-Therapie zugelassen.
Status quo und Prävalenz
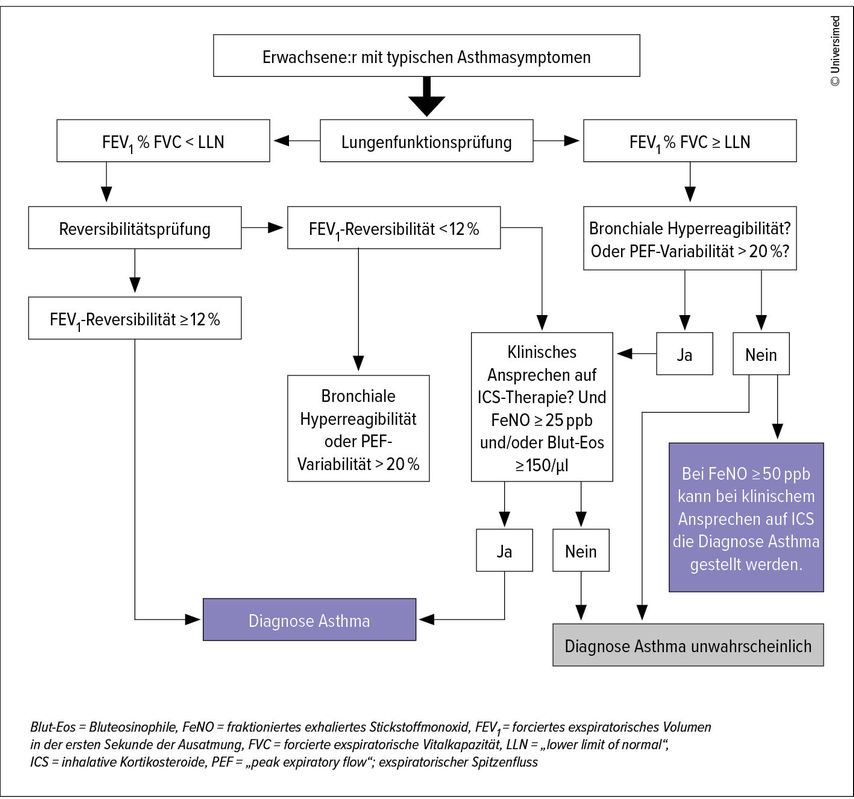
Atemwegserkrankungen wie Asthma bronchiale und die chronisch obstruktive Lungenerkrankung (COPD) stellen weltweit sowie in Österreich eine erhebliche gesundheitliche und sozioökonomische Belastung dar. Während Asthma schätzungsweise 5–7% der Gesamtbevölkerung betrifft, liefern spezifische österreichische Daten wie die bevölkerungsbasierte LEAD-Studie („Lung – hEart – sociAl – boDy“) aus Wien genauere Einblicke: Hier wurde eine Prävalenz des ärztlich diagnostizierten Asthmas von etwa 8–9% bei Erwachsenen festgestellt, was die hohe Krankheitslast unterstreicht. Ein relevanter Anteil dieser Asthmapatienten (ca. 5–10%) leidet an schwerem Asthma, das trotz optimierter Standardtherapie nur unzureichend kontrolliert ist und einen überproportional hohen Anteil der Krankheitskosten durch häufige Exazerbationen, Hospitalisierungen und oft notwendige, aber nebenwirkungsreiche systemische Kortikosteroidtherapien (OCS) verursacht. Abbildung 1 zeigt den Algorithmus der Asthmadiagnostik.
Abb. 1: Klinischer Algorithmus der Asthmadiagnostik bei Erwachsenen (modifiziert nach S2k-Leitlinie zur fachärztlichen Diagnostik und Therapie von Asthma 2023)
Auch bei COPD gibt es Patientengruppen, bei denen trotz maximaler inhalativer Therapie weiterhin häufig Exazerbationen auftreten. Die Entwicklung von Biologika, monoklonalen Antikörpern, die gezielt in spezifische Entzündungswege eingreifen, hat in den letzten Jahren die Therapiemöglichkeiten für diese schwer betroffenen Patienten revolutioniert und eine Ära der personalisierten Pneumologie eingeläutet.
Leitliniengerechte inhalative Basistherapie
Die Basis der medikamentösen Behandlung sowohl bei Asthma als auch bei COPD bildet die inhalative Therapie, deren Einsatz sich an aktuellen Leitlinien orientiert. Bei Asthma hat sich gemäß den Empfehlungen der Global Initiative for Asthma (GINA) die Verwendung von Budesonid/Formoterol oder Beclometason/Formoterol als Bedarfstherapie bei milder Erkrankung und als Erhaltungs- und Bedarfstherapie („maintenance and reliever therapy“; MART) in den höheren Therapiestufen etabliert.
Biologika kommen erst bei schwerem Asthma zum Einsatz, wenn trotz optimierter, hoch dosierter inhalativer Therapie (meist inhalatives Kortikosteroid + lang wirksamer Beta-2-Agonist, ggf. ergänzt mit einen lang wirksamen Muskarinantagonisten) keine ausreichende Krankheitskontrolle erreicht wird. Bei COPD steht gemäß Global Initiative for Chronic Obstructive Lung Disease (GOLD) die Bronchodilatation mittels lang wirksamer Muskarinantagonisten (LAMA) und/oder lang wirksamer Beta-2-Agonisten (LABA) im Vordergrund. Eine zusätzliche inhalative Kortikosteroidtherapie (ICS), meist als Teil einer Triple-Therapie (LAMA/LABA/ICS), wird für Patienten mit häufigen Exazerbationen und insbesondere bei Nachweis einer Eosinophilie empfohlen. Die hier diskutierten Biologika stellen bei COPD eine Add-on-Option für eine spezifische Subgruppe dar, die trotz maximaler inhalativer Therapie weiterhin Exazerbationen erleidet.
Die Rolle der FeNO-Messung als Biomarker
Neben der Bluteosinophilenzahl hat sich die Messung des fraktionierten exhalierten Stickstoffmonoxids (FeNO) als wertvoller nicht invasiv bestimmbarer Biomarker etabliert. FeNO spiegelt primär die durch Interleukin(IL)-4 und IL-13 getriggerte eosinophile Atemwegsinflammation wider und liefert Informationen zur systemischen Eosinophilie. Bei Asthma ist ein erhöhter FeNO-Wert ein Indikator für eine Typ-2-Inflammation und kann die Wahrscheinlichkeit eines Ansprechens auf inhalative Kortikosteroide (ICS) anzeigen. Wenngleich FeNO auch zur Therapieüberwachung genutzt werden kann, ist sein Stellenwert hierfür weniger klar definiert als für die Diagnostik und Phänotypisierung.
Bei COPD ist die Rolle von FeNO weniger etabliert: Obwohl es auch hier auf eine eosinophile Komponente hinweisen kann, wird zur Therapieentscheidung (z.B. ICS-Einsatz, Eignung für Biologika) gemäß aktuellen Leitlinien primär die Zahl der Bluteosinophilen herangezogen.
Biologika bei schwerem Asthma: Targeting der Typ-2-Inflammation
Die Pathophysiologie des schweren Asthmas ist heterogen, jedoch dominiert bei vielen Patienten eine sogenannte Typ-2-Inflammation. Diese wird durch Zytokine wie IL-4, IL-5 und IL-13 angetrieben und lässt sich oft durch Biomarker wie erhöhte Bluteosinophilenzahlen, erhöhten FeNO-Wert oder den Nachweis einer spezifischen IgE-Sensibilisierung charakterisieren (Abb. 2).
Abb. 2: Algorithmus zur Biologikatherapie bei schwerem Asthma (modifiziert nach S2k-Leitlinie zur fachärztlichen Diagnostik und Therapie von Asthma 2023)
1. Anti-IgE: Omalizumab
Als erstes zugelassenes Biologikum für Asthma bindet Omalizumab an freies Immunglobulin E (IgE). Es ist bei schwerem allergischem Asthma mit Sensibilisierung gegen >1 ganzjähriges Aeroallergen ab 6 Jahren zugelassen. Pivotalstudien wie die INNOVATE-Studie zeigten eine Reduktion der Rate schwerer Exazerbationen um etwa 50% im Vergleich zu Placebo (primärer Endpunkt).
2. Anti-IL-5/Anti-IL-5-Rezeptor: Mepolizumab, Benralizumab, Reslizumab
Diese Wirkstoffe zielen auf die eosinophile Inflammation. Mepolizumab bindet IL-5, Benralizumab bindet an den IL-5-Rezeptor alpha auf Eosinophilen und induziert so deren Zelltod. Beide sind für schweres eosinophiles Asthma zugelassen.
-
Mepolizumab: Die pivotalen Studien MENSA und SIRIUS belegten die Wirksamkeit durch eine Reduktion der klinisch signifikanten Exazerbationsrate um ca. 50% (MENSA, primärer Endpunkt) und eine mediane Reduktion der Dosis von oralen Kortikosteroiden (OCS) um 50% (SIRIUS, primärer Endpunkt).
-
Benralizumab: Die Zulassung stützte sich auf die Studien SIROCCO und CALIMA, die eine Reduktion der Exazerbationsrate um bis zu 51% zeigten (primärer Endpunkt), sowie ZONDA, die eine mediane Reduktion der OCS-Dosis um 75% erreichte (primärer Endpunkt).
Anti-IL-4/Anti-IL-13: Dupilumab
Durch die Blockade der gemeinsamen Rezeptor-Untereinheit für IL-4 und IL-13 inhibiert Dupilumab beide Zytokinwege. Die Zulassung erfolgte für schweres Asthma mit Nachweis einer Typ-2-Inflammation (Eosinophilie und/oder erhöhtes FeNO). Die Wirksamkeit wurde in QUEST (Reduktion schwerer Exazerbationen um ca. 47% und Verbesserung der Prä-Bronchodilatator-FEV1 um ca. 130–200 mL vs. Placebo bei Woche 12 als koprimäre Endpunkte) und VENTURE (mediane OCS-Reduktion um 70% vs. 42% unter Placebo als primärer Endpunkt) nachgewiesen.
Anti-TSLP: Tezepelumab
Tezepelumab blockiert das epitheliale Alarmin thymisches stromales Lymphopoietin (TSLP). Es ist für schweres Asthma zugelassen, unabhängig von Eosinophilen- oder FeNO-Grenzwerten. Die Phase-III-Studie NAVIGATOR zeigte eine signifikante Reduktion der annualisierten Asthmaexazerbationsrate um 56% in der Gesamtpopulation im Vergleich zu Placebo (primärer Endpunkt).
Biologika bei COPD: ein Ansatz für den eosinophilen Phänotyp
Ein signifikanter Anteil der COPD-Patienten weist trotz neutrophiler Dominanz eine Eosinophilie auf, assoziiert mit häufigeren Exazerbationen. Dies bildet die Rationale für den Einsatz von Biologika bei diesem „eosinophilen COPD-Phänotyp“.
Anti-IL-5(R)
-
Mepolizumab: Die Studien METREX undMETREO zeigten eine Reduktion der Ratemoderater/schwerer Exazerbationen um18–20% bei COPD-Patienten mit Eosinophilie >150 Zellen/µl bei Baseline oder >300 Zellen/μl im Vorjahr) im Vergleich zu Placebo (primärer Endpunkt). Mepolizumab ist als Add-on-Therapie für diesespezifische COPD-Population zugelassen.
-
Benralizumab: Die Phase-III-Studien GALATHEA und TERRANOVA erreichten ihren primären Endpunkt (Reduktion der Exazerbationsrate) in der untersuchten eosinophilen COPD-Population nicht. Eine Zulassung für COPD besteht derzeit nicht.
Anti-IL-4/Anti-IL-13 (Dupilumab)
Die Phase-III-Studien BOREAS und NOTUS zeigten bei COPD-Patienten mit Typ-2-Inflammation (Bluteosinophile ≥ 300 Zellen/μl) eine signifikante Reduktion der Rate moderater oder schwerer Exazerbationen um 30–34% im Vergleich zu Placebo (primärer Endpunkt).
Signifikante Verbesserungen bei FEV1 und Lebensqualität wurden ebenfalls beobachtet. Dupilumab ist basierend auf diesen Daten seit Kurzem auch für diese Indikation zugelassen.
Erweiterte Indikationsgebiete der Biologika
Der zielgerichtete Wirkmechanismus dieser Biologika hat zu Zulassungen auch in anderen Fachgebieten geführt, in denen die adressierten Entzündungswege eine Rolle spielen. Komorbiditäten sollten eine Entscheidungshilfe bei der Auswahl der richtigen Biologika darstellen (Abb. 2).
-
Omalizumab (Anti-IgE) ist neben Asthma auch zur Behandlung der chronischen spontanen Urtikaria (CSU) und der chronischen Rhinosinusitis mit Nasenpolypen (CRSwNP) zugelassen.
-
Mepolizumab (Anti-IL-5) hat Zulassungen für die eosinophile Granulomatose mit Polyangiitis (EGPA), das hypereosinophile Syndrom (HES) und CRSwNP.
-
Benralizumab (Anti-IL-5R) ist in der EU für schweres eosinophiles Asthma sowie für EGPA zugelassen (eine Zulassung für HES besteht z.B. in den USA, aber derzeit nicht durch die EMA).
-
Dupilumab (Anti-IL-4R) verfügt über ein breites Zulassungsspektrum, das neben Asthma und COPD auch atopische Dermatitis (AD), CRSwNP, eosinophile Ösophagitis (EoE) und Prurigo nodularis (PN) umfasst.
-
Tezepelumab (Anti-TSLP) ist aktuell ausschließlich für die Behandlung von schwerem Asthma zugelassen.
Bewertung und Ausblick: Paradigmenwechsel und neue Therapieziele
Für Patienten mit schwerem Typ-2-Asthma stellen Biologika zweifellos einen Paradigmenwechsel dar. Sie ermöglichen oft eine zuvor undenkbare Krankheitskontrolle, die weit über reine Symptomlinderung hinausgeht: Drastische Reduktion bis hin zur vollständigen Eliminierung des OCS-Bedarfs, eine signifikante Abnahme von Exazerbationen und Hospitalisierungen sowie bei einigen Patienten auch eine Verbesserung der Lungenfunktion werden regelmäßig beobachtet. Dies führt zu einer erheblichen Steigerung der Lebensqualität und ermöglicht oft die Rückkehr zu normalen Alltagsaktivitäten. Es wird diskutiert, inwieweit diese Therapien als erste Vertreter krankheitsmodifizierender antiasthmatischer Medikamente („disease-modifying anti-asthmatic drugs“; DMAAD) betrachtet werden können, da sie tief in die zugrunde liegende Pathophysiologie eingreifen und potenziell langfristige Effekte auf die Atemwegsinflammation und möglicherweise das „airway remodeling“ haben könnten. Ein realistisches und immer häufiger erreichbares Therapieziel für viele Patienten unter Biologika ist die klinische Remission – definiert als ein Zustand mit minimalen bis keinen Symptomen, keinen Exazerbationen, ohne OCS-Bedarf und mit minimalem Bedarf an Notfallmedikation bei stabiler Lungenfunktion. Eine anhaltende, therapiefreie Remission bleibt jedoch bislang die Ausnahme.
Bei COPD ist die Rolle der Biologika spezifischer: Mepolizumab und Dupilumab erweitern die Optionen für eine klar definierte Subgruppe mit eosinophilem Phänotyp und hohem Exazerbationsrisiko, sie ersetzen jedoch nicht die inhalative Basistherapie und adressieren nicht primär die Obstruktion oder das Emphysem.
Ungeachtet dieser Erfolge bleiben Herausforderungen: Die Optimierung prädiktiver Biomarker für das individuelle Ansprechen, das Management von Non-Respondern oder Partial-Respondern, die Langzeitwirkung auf das Atemwegs-Remodeling und die Sicherheit über viele Jahre, Strategien bei Therapiewechsel sowie die Kosten und der Zugang zur Therapie sind wichtige Themen. Direkte Vergleichsstudien zwischen den verschiedenen Biologika fehlen weiterhin.
Literatur:
beim Verfasser
Das könnte Sie auch interessieren:
Aktuelle Studien zur ILD-Therapie
Interstitielle Lungenkrankheit (ILD) ist der Oberbegriff für eine grosse und heterogene Gruppe von Krankheiten, die sich vorwiegend im distalen Bronchoalveolarraum manifestieren. Einige ...
Umweltbelastungen der Atemwege
Atemwege sind besonders anfällig für luftgetragene Schadstoffe wie Gase, Stäube und Allergene. Eine Studie untersuchte den Einfluss der Endotoxinbelastung in Klassenräumen auf die ...