Das Spektrum der zentralen vestibulären Syndrome im Überblick
Autor:
Prof. Dr. med. Alexander A. Tarnutzer
Leitender Arzt Neurologie
Kantonsspital Baden
E-Mail: alexander.tarnutzer@ksb.ch
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Schwindel ist eines der häufigsten Leitsymptome überhaupt und betrifft sowohl den Notfall wie auch die Praxis mit ca. 2–8% aller Konsultationen. Dabei bilden eine strukturierte Anamneseerhebung und gezielte klinische Untersuchung Schlüsselelemente. Die verte-brobasiläre Ischämie, die vestibuläre Migräne und ein somatoformer Schwindel («persistent postural-perceptual dizziness», PPPD) gehören zu den wichtigsten zentralen und funktionellen vestibulären Syndromen.
Keypoints
-
Beim Leitsymptom Schwindel sind eine strukturierte Vorgehensweise inkl. des gezielten Erfragens der Dauer und Häufigkeit der Episoden sowie der Provokationsfaktoren sowie eine fokussierte neurootologische Untersuchung einschliesslich der Suche nach subtilen okulomotorischen Zeichen essenziell.
-
Die Identifikation zentraler gefährlicher, potenziell lebensbedrohlicher Ursachen ist prioritär, beim akuten vestibulären Syndrom sind dies v.a. vertebrobasiläre Ischämien, Intoxikationen und ein akuter Thiaminmangel.
-
Die vestibuläre Migräne stellt die häufigste Ursache eines spontanen episodischen vestibulären Syndroms dar und sollte immer gezielt gesucht werden.
-
Bei Vorliegen eines PPPD oder eines MdDS («mal de débarquement syndrome») ist ein multimodaler Therapieansatz essenziell.
Patienten mit dem Leitsymptom Schwindel stellen sowohl in der Hausarztpraxis wie auch auf der Notfallstation oftmals eine Herausforderung dar. Dies sowohl aufgrund der meist schwer zu fassenden Symptomatik und der oft transienten (und nicht selten bereits wieder regredienten) Beschwerden als auch wegen der Vielzahl möglicher Differenzialdiagnosen aus verschiedensten Fachrichtungen. So ist es nicht erstaunlich, dass der Anteil unklarer oder rein deskriptiver Diagnosen hoch ist und die Anmeldung von Zusatzuntersuchungen oftmals niederschwellig oder gar voreilig erfolgt. Patienten mit Leitsymptom Schwindel binden deshalb überdurchschnittlich viele Ressourcen in der Praxis oder auf dem Notfall, was entsprechend hohe Kosten generiert und den Zeitaufwand erhöht.
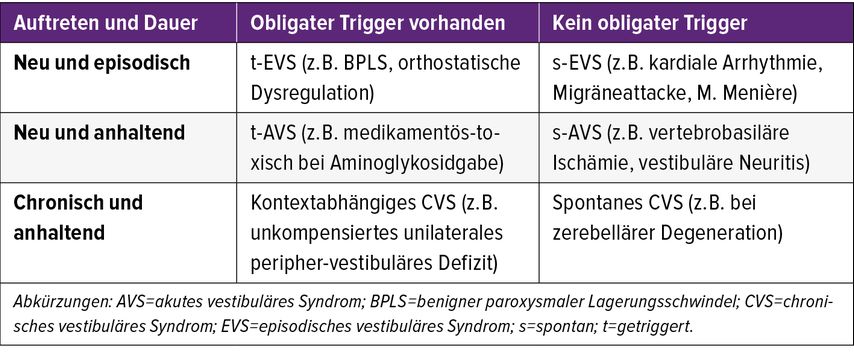
Eine strukturierte Herangehensweise an den Patienten mit Schwindel ist dementsprechend essenziell, um die korrekte Diagnose stellen zu können und um unnötige Diagnostiken und/oder Therapien zu vermeiden. Sehr bewährt hat sich hierfür in den letzten Jahren der sogenannte «TiTrATE approach», welcher 2015 erstmals von Jonathan Edlow und David Newman-Toker vorgestellt worden ist.1 Hierdurch lässt sich durch das Erfragen der Dauer und der Häufigkeit der einzelnen Schwindelattacken sowie das Vorhandensein (oder Fehlen) von Triggern eine erste Grobeinteilung in eine 3x2-Matrix vornehmen(Tab. 1).
Tab. 1: Verschiedene vestibuläre Syndrome basierend auf deren Dauer und Provokationsfaktoren (modifiziert nach Newman-Toker DE 2015)1
Im Folgenden soll auf zentrale Ursachen akuter und episodischer vestibulärer Syndrome eingegangen werden, mit einem besonderen Fokus auf häufige sowie gefährliche, potenziell lebensbedrohliche Ursachen.
Zentrale akute vestibuläre Syndrome
Ein akutes vestibuläres Syndrom (AVS) setzt das Vorliegen eines akut aufgetretenen, prolongierten (und anhaltenden) Schwindels mit begleitender Gangunsicherheit, Bewegungsintoleranz, Nausea/Vomitus sowie meist auch einem Nystagmus voraus.3 Pro Jahr stellen sich alleine in den USA ca. 250000 bis 500000 Patienten mit einem AVS auf einer Notfallstation vor. Schätzungen gehen davon aus, dass dem AVS ca. in jedem vierten Fall eine zentrale Ursache zugrunde liegt.3 Das Spektrum an zentralen Ursachen eines AVS ist breit und lässt sich – bezogen auf die zugrunde liegende Pathophysiologie – in drei grosse Gruppen einteilen:
-
strukturell
-
metabolisch-toxisch
-
funktionell
Bei den strukturellen Ursachen machen vertebrobasiläre Ischämien mit ca. 80% den grössten Anteil aus, während andere strukturelle Ursachen wie autoimmun-entzündliche Erkrankungen (ca. 10%) und hämorrhagische Schlaganfälle (ca. 4%) deutlich seltener zu finden sind.3 Ein abrupter Beginn, das Vorliegen von vaskulären Risikofaktoren (arterielle Hypertonie, Dyslipidämie, Diabetes mellitus, Nikotinkonsum, positive Familienanamnese) sowie zusätzliche fokal-neurologische Symptome und Befunde sprechen für eine zentrale zerebrovaskuläre Ursache. Eine bekannte entzündliche ZNS-Erkrankung macht hingegen eine demyelinisierende Läsion wahrscheinlicher, was sich ebenfalls (isoliert) als AVS präsentieren kann.4 Mögliche metabolisch-toxische Ursachen eines AVS umfassen Intoxikationen mit ZNS-wirksamen Medikamenten (Neuroleptika, Lithium, Antiepileptika wie z.B. Phenytoin oder Carbamazepin) oder Alkohol, die vestibuläre Migräne oder einen Thiaminmangel (Wernicke-Enzephalopathie).
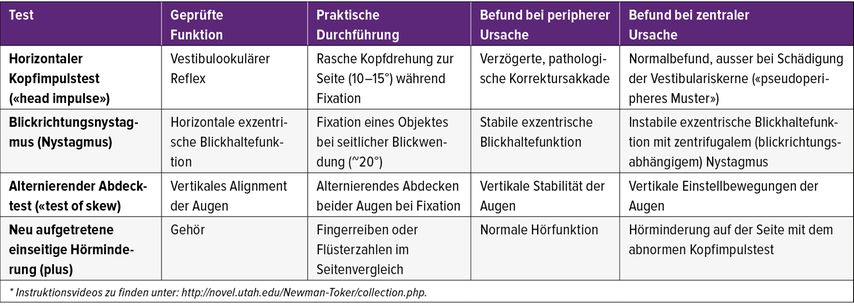
Bei der klinischen Beurteilung des Patienten mit AVS hat sich die Kombination einer strukturierten Anamneseerhebung mit Fokus auf das Timing der Symptome sowie das Vorliegen von Provokationsfaktoren (siehe auch «Timing and Triggers, TiTrATE approach»1) und die Prüfung subtiler okulomotorischer Zeichen (HINTS plus – «head-impulse test, nystagmus, test of skew») sowie zusätzlich die Prüfung des Gehörs, siehe Tabelle 2; alternativ STANDING5 sehr bewährt. Die Sensitivität der HINTS für einen Schlaganfall bei AVS liegt bei 95,3% (95% Konfidenzintervall [CI] =92,5–98,1), die Spezifität bei 92,6% (95% CI=88,6–96,5)6, für die HINTS plus ist die Sensitivität mit 97,2% nochmals leicht höher. Offensichtliche fokal-neurologische Zeichen finden sich hingegen nur bei ca. der Hälfte der Patienten.
Zusätzlich sollte auch eine Prüfung der Stand- und Gangataxie erfolgen und das Ausmass der Einschränkung graduiert werden (Grad 0–3).5 Ist basierend auf der klinisch-neurologischen Untersuchung von einer zentralen Ursache auszugehen, sollte der Patient auf eine Stroke Unit aufgenommen und weiter abgeklärt werden. Als Goldstandard zur Bestätigung bzw. zum Ausschluss einer ischämischen Genese gilt das MRI mit diffusionsgewichteter Sequenz (DWI). Dabei ist aber zu berücksichtigen, dass das frühe MRI des Neurocraniums (d.h. innerhalb der ersten 24–48h) bei ca. 15–20% der Patienten mit AVS falsch negativ sein kann6,7 und somit in Fällen mit klinisch weiterhin bestehendem Verdacht auf eine zentrale Ursache ein Verlaufs-MRI frühestens 72h nach Symptombeginn erfolgen sollte. Die Sensitivität der nativen Computertomografie (CT) für die Diagnose vertebrobasilärer Ischämien bei Patienten mit AVS beträgt nur ca. 29%; ein unauffälliges Nativ-CT des Neurocraniums schliesst eine ischämische Ursache keineswegs aus.7
Das Vorliegen eines beidseitig auffälligen Kopfimpulstests sowie eines Blickrichtungsnystagmus sollte an einen zugrunde liegenden Thiaminmangel denken lassen. Die HINTS können nach moderatem dezidiertem Training (in der Grössenordnung von 4–6h) mit vergleichbarer Sensitivität durchgeführt werden wie durch erfahrene Neurootologen,6 besteht hingegen keine Erfahrung in der Durchführung und Interpretation der HINTS, so ist deren Nutzen deutlich geringer. In der Akutdiagnostik des AVS wird zukünftig die quantitative okulomotorische Testung eine wichtige Rolle spielen. Werden die HINTS quantitativ erfasst, so lässt sich die Sensitivität derselben im Vergleich zu Experten erhöhen (100% vs. 91% Sensitivität).8
Die Therapie des AVS richtet sich nach der zugrunde liegenden Ursache, bei vertebrobasilärer Ischämie stehen die Suche nach einer Emboliequelle und die Sekundärprophylaxe im Vordergrund, bei Intoxikationen die Dosisanpassung der Medikation und bei der vestibulären Migräne die Akut- und Basismedikation. Besteht ein Verdacht auf einen Thiaminmangel, sollte umgehend eine hoch dosierte Vitamin- B1-Substitution (600–900mg als Kurzinfusion pro Tag) begonnen werden, um das Risiko für Spätfolgen (Korsakow-Syndrom) zu minimieren.
Handelt es sich hingegen um einen episodischen, durch Positionsänderungen hervorgerufenen Schwindel, so ist an einen benignen paroxysmalen Lagerungsschwindel (BPLS) zu denken und die Provokationsmanöver für die posterioren Bogengänge (Hallpike-Dix-Manöver) sowie für die lateralen Bogengänge (Supine-Roll-Manöver) sind durchzuführen.9
Zentrale episodische vestibuläre Syndrome
Die Differenzialdiagnose episodischer vestibulärer Syndrome (EVS) ist breit, eine erstere grobe Einteilung lässt sich in solche mit und ohne Trigger vornehmen. Während das häufigste getriggerte EVS durch eine peripher-vestibuläre Erkrankung – den BPLS – verursacht wird, stellt die vestibuläre Migräne die häufigste Ursache eines spontan auftretenden zentralen EVS dar.
Vestibuläre Migräne
Eine vestibuläre Migräne findet sich bei ca. 10% aller Patienten mit einer Neudiagnose einer Migräne, sie weist eine Lebenszeitprävalenz von bis zu 2,7% auf. Häufig ist die Erstmanifestation Jahre bis Jahrzehnte nach der Erstdiagnose eines Migränekopfschmerzes. Gemäss den diagnostischen Kritierien der International Headache Society (ICHD-3, Appendix 1.6.6)10 sind das Vorliegen der Diagnose einer Migräne sowie die Kombination von typischen Migränesymptomen (Migränekopfschmerzen, Lärm- und Lichtempfindlichkeit, visuelle Aura) in Kombination mit episodischem Schwindel von mittlerer oder hoher Intensität und einer Dauer von 5 Minuten bis 72 Stunden in mindestens jeder zweiten Episode erforderlich. Dabei ist zu erwähnen, dass die klinische Präsentation der vestibulären Migräne sehr variabel sein kann, sowohl bezüglich der Art der Schwindelbeschwerden (Drehschwindel, Schwankschwindel, Liftschwindel, lageabhängiger Schwindel etc.) wie auch hinsichtlich der Dauer der Episoden (Sekunden bis chronisch) und Begleitphänomene.
In der Attacke finden sich sehr oft (subtile) okulomotorische Zeichen wie ein positionsabhängiger Nystagmus (beinahe 100%), ein Spontannystagmus (70%) oder auch eine Gangataxie (95%).11 Je nach klinischem Bild kommen andere Differenzialdiagnosen infrage. Bestehen ein lageabhängiger Schwindel und Nystagmus, so besteht die Gefahr, eine vestibuläre Migräne mit einem BPLS zu verwechseln. Kommt es hingegen bei einem Patienten mit bekannter Migräne erstmals zu einer Episode mit prolongiertem Schwindel und zentralem Muster der HINTS, so kann die Abgrenzung zur ischämischen Ursache eines AVS am Patientenbett herausfordernd sein. Wichtig ist dabei zu erwähnen, dass für die Diagnose einer vestibulären Migräne mindestens fünf Episoden gemäss den diagnostischen Kriterien erforderlich sind.12 Besteht eine zusätzliche (subjektive) Hörminderung oder ein Völlegefühl im Ohr, so ist differenzialdiagnostisch in erster Linie an einen Morbus Menière zu denken.
Die Akuttherapie der vestibulären Migräne unterscheidet sich nicht wesentlich von derjenigen des akuten Migränekopfschmerzes und umfasst nebst diversen Akutanalgetika auch die Verwendung von Triptanen sowie zukünftig ggf. auch von CGRP-Antagonisten wie Zavegepant. Treten Episoden einer vestibulären Migräne regelmässig (d.h. mindestens 1–2x pro Monat) auf, so ist eine Basisbehandlung zur Reduktion der Attackenhäufigkeit und -intensität empfohlen. Bis dato finden sich kaum randomisierte, placebokontrollierte und verblindete Studien zur Prophylaxe der vestibulären Migräne. Therapieempfehlungen lehnen sich somit an diejenigen der Migränekopfschmerzbehandlung an und umfassen bekannte Substanzklassen wie Betablocker, Antidepressiva wie Venlafaxin oder Antiepileptika wie Lamotrigin.13 Kürzlich wurde in ersten Studien auch auf einen möglichen Nutzen von CGRP-Antagonisten sowie von Botulinumtoxin A – Applikation nach dem PREEMPT(«Phase 3 research evaluating migraine prophylaxis therapy»)-Schema – in der Behandlung der vestibulären Migräne hingewiesen. Diese neuen Ansätze sind aber noch nicht etabliert und bedürfen zudem einer Kostengutsprache durch die Krankenkasse.
Funktionelle zentrale Syndrome
An eine funktionelle Genese eines vestibulären Syndroms sollte v.a. bei chronischer Symptomatik (chronisches vestibuläres Syndrom) gedacht werden. Hierbei kommen mehrere Entitäten infrage, einschliesslich der «persistent postural-perceptual dizziness» (PPPD)14, des «mal de débarquement syndrome»(MdDS) und des sogenannten visuell-induzierten Schwindels («visually-induced dizziness», VID).
Davon abzugrenzen gilt es andere Ursachen eines chronischen vestibulären Syndroms, insbesondere eine persistierende unilaterale peripher-vestibuläre Unterfunktion, eine bilaterale vestibuläre Unterfunktion, eine Gangataxie im Rahmen einer peripheren Polyneuropathie, neurodegenerative Erkrankungen oder auch residuelle Symptome nach Schlaganfall oder Schädel-Hirn-Trauma.
«Persistent postural-perceptual dizziness»
In den vergangenen Jahrzehnten wurden für einen funktionellen chronischen Schwindel verschiedene Begriffe verwendet, einschliesslich eines phobischen Schwankschwindels, eines visuellen Schwindels, eines somatoformen Schwindels oder eben einer «persistent postural-perceptual dizziness» (PPPD). Die Einführung dezidierter diagnostischer Kriterien durch die Bárány Society (The International Society for Neuro-Otology) ermöglicht die einheitliche Diagnosestellung eines PPPD.14 Hierbei wird eine mindestens 3-monatige Beschwerdedauer mit Vorliegen eines Schwankschwindels oder einer Gangunsicherheit an den meisten Tagen mit Exazerbation in aufrechter Position, bei aktiven oder passiven Bewegungen sowie beim Auftreten komplexer, sich bewegender visueller Stimuli vorausgesetzt. Beschwerdefreie Intervalle dürfen bestehen. Wichtig ist die Identifikation eines vorausgehenden auslösenden Ereignisses im Sinne eines durchgemachten akuten, episodischen oder chronischen vestibulären Syndroms (z.B. eines BPLS, einer vestibulären Migräne oder einer akuten unilateralen Vestibulopathie), einer anderen neurologischen oder internistischen Erkrankung oder einer psychosozialen Belastungssituation. Die Symptomatik muss zudem zu einer relevanten funktionellen Beeinträchtigung und Belastung führen. Das mittlere Erkrankungsalter liegt bei 59,5 ± 15 Jahren, mit gehäuftem Auftreten bei Frauen.
Pathophysiologisch wird davon ausgegangen, dass die PPPD durch eine übermässige Gewichtung visueller und somatosensorischer Eingangssignale zu einer anhaltenden funktionellen Störung in der posturalen Kontrolle und der räumlichen Orientierung führt. Als Auslöser hierfür wird eine Störung der vestibulären Eingangssignale angenommen.14 Es werden im Folgenden eine übermässige Kontrolle und Korrektur der posturalen Stabilität postuliert, welche jedoch in der Erholungsphase nicht mehr als adaptiv und somit zielführend angesehen wird. Dementsprechend zielt die diagnostische Abklärung darauf ab, vorbestehende peripher- oder zentral-vestibuläre Defizite und somit einen möglichen Trigger zu erkennen. Das MRI des Neurocraniums ist dabei üblicherweise ohne wegweisende Befunde. Dabei ist zu beachten, dass die PPPD mit der initial auslösenden Erkrankung koexistieren kann. Die Abgrenzung zu einer chronifizierten vestibulären Migräne oder auch einem «mal de débarquement syndrome» kann dabei schwierig sein.
Aus therapeutischer Sicht wird ein multimodales Vorgehen propagiert, wobei jedoch Langzeitdaten zum Therapieansprechen fehlen. Eine gezielte Edukation über die Erkrankung und ihre zugrunde liegenden Mechanismen ist dabei empfohlen, auch betreffend vorgeschlagene therapeutische Massnahmen einschliesslich vestibulärer Rehabilitation, kognitiver Verhaltenstherapie und einer medikamentösen Therapie mit Fokus auf Antidepressiva wie Sertralin oder Venlafaxin. Mit diesen Massnahmen kann die Morbidität bei den meisten Patienten substanziell vermindert werden.
«Mal de débarquement syndrome»
Unter einem «mal de débarquement syndrome», MdDS, wird ein anhaltender oszillierender Schwank- oder Liftschwindel verstanden, welcher nach prolongierter Exposition gegenüber Bewegungen auftritt. Auslösend für ein MdDS sind mehrheitlich Reisen auf dem Wasser, vermehrt findet sich ein MdDS aber auch nach Flugreisen oder Überlandreisen. Bei Reexposition gegenüber Bewegungsreizen berichten viele Patienten über eine Abnahme des wahrgenommenen Schwindels, meist kommt es aber nach Sistieren der Bewegungsreize zu einer erneuten Exazerbation der Symptomatik. Die Prävalenz des MdDS ist bei Frauen deutlich höher als bei Männern und tritt am häufigsten zwischen dem 40. und 50. Lebensjahr auf.15 Bis zu 50% der Patienten mit MdDS erfüllen gleichzeitig auch die diagnostischen Kriterien der International Headache Society (IHS) für eine Migräne.
Gemäss den publizierten diagnostischen Kriterien für ein MdDS wird das Vorliegen eines Schwankschwindels nach Verlassen eines Schiffes, Flugzeuges oder Autos für mehr als 48 Stunden mit transienter Verbesserung durch die Exposition gegenüber passiven Bewegungsreizen gefordert. Besteht die Symptomatik für mehr als einen Monat, so wird von einem persistierenden MdDS gesprochen; sistiert die Symptomatik vor diesem Zeitpunkt, so wird dies als transientes MdDS bezeichnet. Hält die Symptomatik mehr als sechs Monate an, so sinkt die Wahrscheinlichkeit einer spontanen Remission deutlich. Für das MdDS existieren keine etablierten Behandlungsmassnahmen.
Experimentelle Ansätze einschliesslich transkranieller Magnetstimulation oder Readaptation des vestibulookulären Reflexes sind in Untersuchung. Ein Schwerpunkt der Behandlung ist aktuell die Modifikation des Lebensstils («lifestyle modification»), da eine Exazerbation der mit MdDS assoziierten Symptome unter emotionalem Stress und Schlafmangel beobachtet wurde. Des Weiteren wird auch der Einsatz von SSRI zur Behandlung des MdDS empfohlen,15 zum Nutzen von SNRI zur Behandlung des MdDS liegen keine Studiendaten vor. Von einem chronischen Einsatz von Benzodiazepinen, welche kurzfristig zu einer deutlichen Symptomregredienz führen können, wird aufgrund des Abhängigkeitspotenzials abgeraten.
Visuell induzierter Schwindel
Beim visuell induzierten Schwindel («visually-induced dizziness», VID) werden Schwindel und/oder räumliche Desorientiertheit oftmals durch komplexe, grossflächige und sich bewegende visuelle Stimuli im Gesichtsfeld ausgelöst. VID ist ein Syndrom oder eine Kombination von Symptomen und lässt sich in verschiedenen peripher- und zentral-vestibulären Erkrankungen beobachten. Die Behandlung richtet sich primär nach der zugrunde liegenden Ursache. Daneben besteht die Möglichkeit einer symptomorientierten, kombinierten Therapie, bestehend aus einer Desensibilisierung, einer kognitiven Verhaltenstherapie und einer vestibulären Physiotherapie.15
Zusammenfassung
Zentrale und funktionelle vestibuläre Syndrome weisen eine breite Differenzialdiagnose auf. Dementsprechend sind eine strukturierte Anamneseerhebung (z.B. nach dem TiTrATE-Schema) und die Suche nach subtilen okulomotorischen Zeichen (HINTS etc.) essenziell. Dabei ist die rasche Identifikation gefährlicher, potenziell lebensbedrohlicher Ursachen wie einer vertebrobasilären Ischämie, einer Intoxikation oder auch eines Thiaminmangels entscheidend für die Prognose.
Wird eine «persistent postural-perceptual dizziness» (PPPD) vermutetet, so ist die Suche nach Triggern essenziell und die Einleitung einer multimodalen Therapie ist erforderlich. Eine Abgrenzung zwischen einer vestibulären Migräne, welche die häufigste Ursache für ein spontanes episodisches vestibuläres Syndrom darstellt, und eines PPPD kann manchmal schwierig bis unmöglich sein. Die Therapie sollte sich dann auf die Aspekte mit dem grössten Einfluss auf die Lebensqualität des Patienten fokussieren.
Literatur:
1 Newman-Toker DE, Edlow JA: TiTrATE: A novel, evidence-based approach to diagnosing acute dizziness and vertigo. Neurol Clin 2015; 33(3): 577-99 2 ICD-11 (Mortality and Morbidity Statistics) [available from: https://icd.who.int/dev11/l-m/en#/http%3a%2f%2fid.who.int%2ficd%2fentity%2f1462112221 3 Tarnutzer AA et al.: Does my dizzy patient have a stroke? A systematic review of bedside diagnosis in acute vestibular syndrome. CMAJ 2011; 183(9): 571-92 4 Pula JH et al.: Multiple sclerosis as a cause of the acute vestibular syndrome. J Neurol 2013; 260(6): 1649-54 5 Tarnutzer AA, Edlow JA: Bedside testing in acute vestibular syndrome - evaluating HINTS plus and beyond; a critical review. Audiology Research 2023; 13(5): 670-85 6 Tarnutzer AA et al.: Impact of clinician training background and stroke location on bedside diagnostic test accuracy in the acute vestibular syndrome - a meta-analysis. Ann Neurol 2023; 94(2): 295-308 7 Shah VP et al.: Diagnostic accuracy of neuroimaging in emergency department patients with acute vertigo or dizziness: A systematic review and meta-analysis for the guidelines for reasonable and appropriate care in the emergency department. Acad Emerg Med 2023; 30(5): 517-30 8 Korda A et al.: Videooculography «HINTS» in acute vestibular syndrome: A prospective study. Front Neurol 2022; 13: 920357 9 Bhattacharyya N et al.: Clinical Practice Guideline: benign paroxysmal positional vertigo (Update). Otolaryngol Head Neck Surg 2017; 156(3_suppl): S1-S47 10 Headache Classification Committee of the International Headache Society (IHS): The International Classification of Headache Disorders, 3rd edition. Cephalalgia 2018; 38(1): 1-211 11 Young AS et al.: Clinical, oculographic, and vestibular test characteristics of vestibular migraine. Cephalalgia 2021; 41(10): 1039-52 12 Lempert T et al.: Vestibular migraine: Diagnostic criteria (update). J Vestib Res 2022; 32(1): 1-6 13 Smyth D et al.: Vestibular migraine treatment: a comprehensive practical review. Brain 2022; 145(11): 3741-54 14 Staab JP: Persistent postural-perceptual dizziness. Semin Neurol 2020; 40(1): 130-7 15 Cha YH: Chronic Dizziness. Continuum (Minneap Minn) 2021; 27(2): 420-46
Das könnte Sie auch interessieren:
Parkinsonprävention durch Lebensstilmodifikation
Noch bevor die ersten motorischen Symptome der Parkinsonkrankheit auftreten, beginnt die Erkrankung auf biologischer Ebene. Auch wenn bislang keine pharmakologische Neuroprotektion oder ...
Ist die ketogene Diät eine Präzisionsmedizin?
Die ketogenen Ernährungstherapien sind etablierte Behandlungsformen bei Epilepsie. Während sie primär bei therapierefraktären pädiatrischen Epilepsien eingesetzt werden, finden sie ...
Neues aus der Alzheimer’s Disease Drug Development Pipeline
Mit der weltweiten Zulassung der Amyloidantikörper Lecanemab und Donanemab ist erstmals eine kausale Behandlung der Alzheimerkrankheit möglich geworden. Die Behandlung setzt an der ...