Restgehörerhalt bei partieller Cochleaimplantation – chirurgische Aspekte und Langzeitergebnisse
Autor:
Prim. Univ.-Prof. Dr. Georg M. Sprinzl
Leiter der Universitätsklinik für Hals-, Nasen-, Ohrenhelkunde
Karl Landsteiner Privatuniversität für Gesundheitswissenschaften,
Universitätsklinikum St. Pölten
E-Mail: georg.sprinzl@stpoelten.lknoe.at
Vielen Dank für Ihr Interesse!
Einige Inhalte sind aufgrund rechtlicher Bestimmungen nur für registrierte Nutzer bzw. medizinisches Fachpersonal zugänglich.
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
Beim Vorliegen einer Hochtonschwerhörigkeit oder auch eines partiellen Hörverlustes wird durch den Einsatz kurzer und besonders flexibler Elektroden und strukturschonender Insertionstechniken das Restgehör durch elektrisch-akustische Stimulation (EAS) erhalten. EAS verbindet das Cochleaimplantat mit dem Hörgerät und dientzur Wiederherstellung der hohen Töne und zur Verstärkung der tiefen Töne. Im Rahmen einer Studie untersuchten wird die Langzeitergebnisse (bis zu 58 Monate) mit EAS bei 18 Patienten.
Keypoints
-
Langzeitergebnisse zeigen, dass Patienten mit partiellem Hörverlust signifikant von elektrisch-akustischer Stimulation profitieren.
-
Der Erhalt des vorhandenen Restgehörs kann durch besondere Operationstechniken und die Verwendung kürzerer, besonders flexibler Elektrodenarrays (Flex-20, Flex-24 und Flex-26) sowie mittels präoperativer Planung (OTOPLAN) erzielt werden.
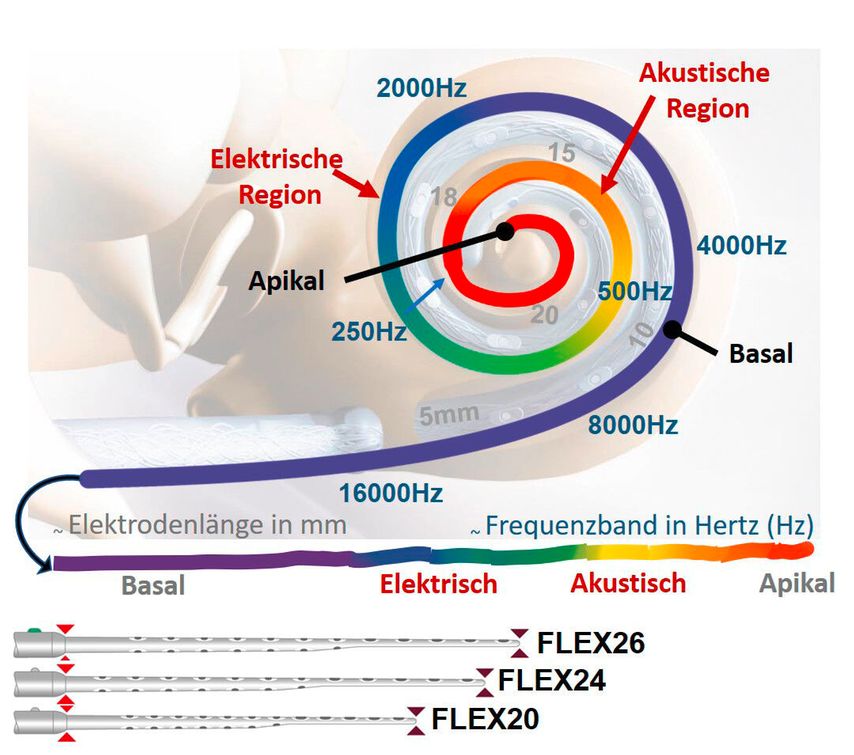
Seit einigen Jahrzehnten zählen Cochleaimplantate (CI) zur Standardbehandlung für Kinder und Erwachsene bei schwerem bis hochgradigem beidseitigem Hörverlust. Mit der Verbesserung der Technologie haben sich auch die Indikationskriterien für eine Cochleaimplantation erweitert, sodass heutzutage auch Patienten mit Restgehör, typischerweise in den tiefen Frequenzen, die nicht von Hörgeräten profitieren können, nun eine Kombination aus elektrischer und akustischer Stimulation (EAS) nutzen können.1 Diese Art von Hörverlust, bei der man hohe Töne nicht mehr bzw. nicht mehr gut hören kann, nennt man Hochtonschwerhörigkeit oder auch partiellen Hörverlust. Der potenzielle Vorteil der EAS-Anwendung, also die Kombination von Hörgerät (HG) und CI, besteht darin, dass tiefe Frequenzen, die für die Sprachwahrnehmung entscheidend sind, durch akustische Stimulation (mittels HG) und höhere Frequenzen durch elektrische Stimulation (mittels CI) verbessert werden. Um eine kombinierte elektrische und akustische Stimulation zu erreichen, wird ein kürzerer Elektrodenträger in die Scala tympani eingeführt, um das akustische Gehör apikal der Spitze des Trägers zu erhalten. Die Erhaltung des Restgehörs hängt davon ab, dass Teile der Cochlea (die mittlere Windung oder der Apex) noch funktionieren, was dadurch erreicht wird, dass die empfindliche Anatomie der Cochlea intakt bleibt, obwohl die Elektrode in die basale Cochleawindung eingeführt wird (Abb. 1).2–8 Die atraumatische Elektrodeneinführung kann durch die Verwendung flexibler und kürzerer Elektroden, die Einführung über das runde Fenster und das langsame und eine somit weitgehend traumalose Insertion der Elektrode erreicht werden. Zusätzlich werden Steroide verwendet, um Entzündungen zu verhindern. Es wurde berichtet, dass Probanden, die mit dieser Technik implantiert wurden, in schwierigen Hörsituationen besser abschneiden.1
Abb. 1: Das Bild im Hintergrund zeigt die Anatomie der Cochlea inkl. einer vollständig inserierten Elektrode mit Rundfensterzugang. Farblich dargestellt sind der Frequenzbereich bzw. das Frequenzband (Hz) (blaue Schrift) und die Elektrodenlänge (mm) (graue Schrift) innerhalb der Cochlea. Im unteren Teil sichtbar ist das aufgerollte Frequenzband zur ungefähren Visualisierung der drei verschiedenen verwendeten Elektroden für die Studienteilnehmer (Flex-26; Flex-24 und Flex-20) – nicht maßstabsgetreu
Chirurgische Aspekte
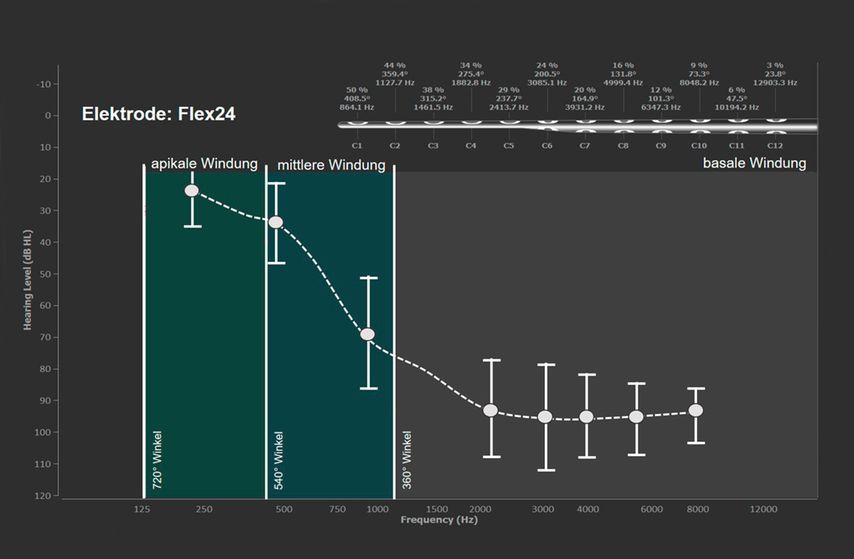
Zusätzlich zu den routinemäßigen chirurgischen Schritten, die bei der Standardcochleaimplantation angewandt werden (Mastoidektomie, hintere Tympanotomie, Rundfensterzugang), wird ein sanftes chirurgisches Verfahren angewandt, um das Cochleatrauma zu minimieren und den Erhalt des Restgehörs bei niedrigen Frequenzen zu maximieren. Zu den sanften chirurgischen Verfahren gehören die intraoperative Verabreichung von intravenösen Antibiotika und Kortikosteroiden, das Absaugen von Blut und Knochenstaub, das Auftragen einer Kortikosteroidlösung und eines Gleitmittels an der Einführungsstelle des runden Fensters sowie das besonders langsame und schonende Einführen der Elektrode. Die Elektrodenlänge wird bestimmt mittels präoperativer Reintonfrequenzbestimmung, kombiniert mit visualisierter anatomischer OTOPLAN-Planung, um die patientenspezifische Elektrodenvisualisierung und die automatische Kontakterkennung für den jeweiligen Frequenzbereich zu ermöglichen (Abb.2).
Abb. 2: Planungsansicht der OTOPLAN-Software mit darübergelegter Studienkohorte: durchschnittliches präoperatives Reintonaudiogramm inkl. Standardabweichung von 18 Patienten (weiß)
Langzeitergebnisse
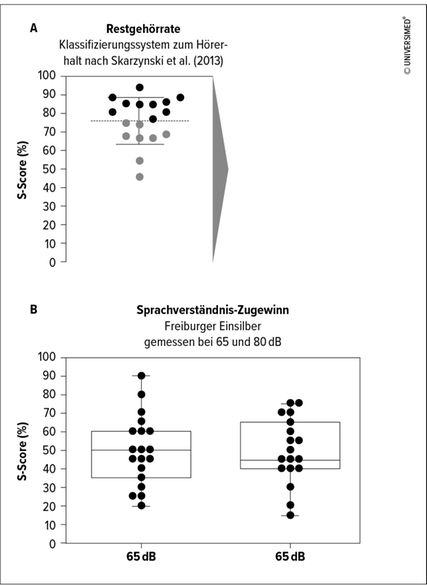
Abb. 3: Streudiagramm des S-Score für die einzelnen Patienten; A: vollständiger Restgehörerhalt (schwarze Kreise) und teilweiser Restgehörerhalt (graue Kreise); B: Boxplot der Patientenkohorte inkl. der einzelnen Ergebnisse zum Sprachverständniszugewinn getestet bei 65 dB und bei 80 dB (modifiziert nach Sprinzl GM et al. 2020)1
Der durchschnittliche Beobachtungszeitraum betrug 28,4±15,0 Monate (Spanne von 12 bis 58 Monaten). Eine Insertion der per OTOPLAN vorgeschlagenen Elektrode war bei allen 18 implantierten Patienten möglich. Den Probanden wurde entweder ein MED-EL-Concerto- oder MED-EL-Synchrony-Implantat mit einem Flex-20-, einem Flex-24- oder einem Flex-26-Elektrodenarray implantiert (Abb.1, MED-EL GmbH, Innsbruck/Österreich). Die Patienten wurden mit dem SONNET-Audioprozessor ausgestattet, der eine Akustikeinheit mit einem maßgefertigtem Ohrpassstück kombiniert, um eine spezielle akustische Stimulation in den niedrigen Frequenzen und eine elektrische Stimulation in den hohen Frequenzen zu ermöglichen.Um das Ausmaß des Restgehörs zu bestimmen, wurden die Hörschwellen vor und nach der Operation bei den Frequenzen 0,25, 0,5, 1, 2, 3, 4, 6 und 8kHz gemessen (Abb2). Zur quantitativen Bestimmung des Restgehörs nach Operation, dem sogenannten S-Score, wurde das Klassifizierungssystem nach Skarzynski etal. verwendet.6 Mit dem S-Score wird der Restgehörerhalt in vier Kategorien eingeteilt: 75% bis 100% Restgehörerhalt werden als vollständiger Hörerhalt eingestuft, 25% bis 75% als teilweiser Restgehörerhalt, 1% bis 25% als minimaler Hörerhalt und ein Wert von 0% bedeutet den vollständigen Hörverlust, sprich kein Erhalt des Restgehörs. Vollständiger Restgehörerhalt wurde bei 10 (55,6%) und teilweiser Restgehörerhalt bei 8 (44,4%) von den 18 untersuchten Personen erreicht (Abb.3A). Die Zugewinne bei mittleren Sprachverständnismessungen mittels FreiburgerEinsilber waren bei 65dB 49,25±18,459 und bei 80dB 49,47±17,23 (Abb. 3B).
Zusammenfassung
Diese Studie mit 18 Patienten über einen mittleren Beobachtungszeitraum von 28,4±15,0 Monaten (Spanne von 12 bis 58 Monaten) bestätigt, dass die Kombination von akustischer und elektrischer Stimulation über das EAS-System eine sichere, wirksame und vor allem stabile Behandlungsoption für Patienten mit partiellem Hörverlust darstellt. Für Erwachsene mit normalem bis mäßigem Hörverlust im Tieftonbereich und schwerem bis hochgradigem Hörverlust im Hochtonbereich, die von einer herkömmlichen Verstärkung nicht profitieren, erweist sich diese Behandlungsmethode als besonders nützlich. Das bis zu 58 Monate postoperativ gemessene stabile Resthörvermögen zeichnet sich durch hohe Sprachwahrnehmungswerte aus, was wiederum für den zukünftigen Einsatz von EAS-Technologie spricht.
Literatur:
1 Sprinzl GM et al.: Long-term hearing preservation in electric acoustic cochlear implant candidates. Otol Neurotol 2020; 41(6): 750-75 2 Dhanasingh A, Jolly C: An overview of cochlear implant electrode array designs. Hear Res 2017; 356: 93-103 3 Eshraghi AA et al.: Clinical, surgical, and electrical factors impacting residual hearing in cochlear implant surgery. Acta Otolaryngol 2017; 137(4): 384-8 4 Gantz BJ, Turner CW: Combining acoustic and electrical hearing. Laryngoscope 2003; 113(10): 1726-3 5 Gstoettner WK et al.: Ipsilateral electric acoustic stimulation of the auditory system: results of long-term hearing preservation. Audiol Neurootol 2006; 11(1): 49-56 6 Skarzynski H et al.: Towards a consensus on a hearing preservation classification system. Acta Otolaryngol Suppl 2013; (564): 3-13 7 von Ilberg CA et al.: Electric-acoustic stimulation of the auditory system: a review of the first decade. Audiol Neurootol 2011; 16(2): 1-30 8 Wanna GB et al.: Predictive factors for short- and long-term hearing preservation in cochlear implantation with conventional-length electrodes. Laryngoscope 2018; 128(2): 482-9
Das könnte Sie auch interessieren:
Wie Coaching den Fachärztemangel an medizinischen Abteilungen angehen kann
Hohe Arbeitsbelastung, Stress, schlechte Stimmung: An vielen Spitalskliniken ist das die tägliche Realität. Es ist daher nicht verwunderlich, dass viele Fachärzt:innen den Weg in die ...
Von „Klassikern“ bis zu „Raritäten“: Einführung in die Radiofrequenztherapie
Die Radiofrequenztherapie ist mittlerweile bei HNO-Eingriffen vielfältig einsetzbar. Aufgrund des steilen Temperaturgradienten wird das umliegende Gewebe geschont und es treten keine ...
AC102: ein vielversprechender Wirkstoffkandidat bei Hörsturz
Hörsturz führt häufig zu dauerhaftem Hörverlust und Begleiterkrankungen wie Tinnitus. Glukokortikoide werden für den Off-Label-Einsatz verschrieben, obwohl es keine klinischen Beweise ...