Lokoregional fortgeschrittene Oropharynxkarzinome
Autorinnen:
Dr. Elisa Thomas
PD Dr. med. habil. Annett Linge
Klinik und Poliklinik für Strahlentherapie und Radioonkologie
Medizinische Fakultät und Universitätsklinikum Carl Gustav Carus
Technische Universität Dresden
OncoRay – Nationales Zentrum für Strahlenforschung in der Onkologie Medizinische Fakultät und Universitätsklinikum Carl Gustav Carus
Technische Universität Dresden und Helmholtz-Zentrum Dresden Rossendorf, Dresden
Deutsches Konsortium für Translationale Krebsforschung (DKTK), Partnerstandort Dresden, und Deutsches Krebsforschungszentrum, Heidelberg
Nationales Zentrum für Tumorerkrankungen (NCT) Partnerstandort Dresden
Korrespondierende Autorin:
PD Dr. med. habil. Annett Linge
Sie sind bereits registriert?
Loggen Sie sich mit Ihrem Universimed-Benutzerkonto ein:
Sie sind noch nicht registriert?
Registrieren Sie sich jetzt kostenlos auf universimed.com und erhalten Sie Zugang zu allen Artikeln, bewerten Sie Inhalte und speichern Sie interessante Beiträge in Ihrem persönlichen Bereich
zum späteren Lesen. Ihre Registrierung ist für alle Unversimed-Portale gültig. (inkl. allgemeineplus.at & med-Diplom.at)
HPV-positive Oropharynxkarzinome sind sehr strahlensensitiv und zeigen ausgezeichnete Tumorkontrollraten. Anhand rezenter Daten ist davon auszugehen, dass betroffene Patienten nach aktuellem Therapiestandard überbehandelt werden. Für die Therapiedeeskalation zur Reduktion von Langzeittoxizitäten wurden verschiedene Ansätze untersucht.
Keypoints
-
Eine Dosisdeeskalation in Patienten mit HPV-positiven Oropharynxkarzinomen resultiert in hohen progressionsfreien 2-Jahres-Überlebensraten und in der Reduktion von Toxizitäten.
-
Deintensivierung der Strahlentherapie erscheint für (ausgewählte) Patienten mit HPV-positiven OPSCC erfolgreich, wobei die simultane Chemotherapie mit Cisplatin vorerst der Standard bleibt.
-
Die Kombination des HPV-Status mit weiteren Biomarkern zur biologischen Charakterisierung des Tumors ist für die „sichere“ Dosisdeeskalation (insbesondere bei primärer Radio[chemo]therapie und Nicht-OPSCC) erforderlich.
-
Weitere Phase-III-Studien sind für die Beurteilung notwendig.
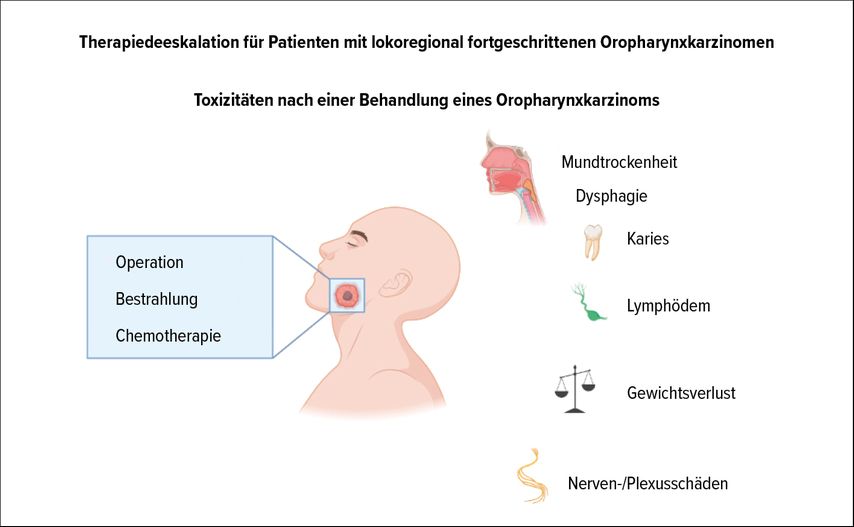
Patienten mit einem Plattenepithelkarzinom des Kopf-Hals-Bereiches werden interdisziplinär behandelt. In den frühen Stadien erfolgt in der Regel eine alleinige Operation. Sind postoperativ Risikofaktoren für ein erhöhtes Rezidivrisiko (großer Tumor, Lymphknotenbefall mit Kapselüberschreitung, keine vollständige Entfernung des Tumors im Gesunden) vorhanden, erhalten die Patienten eine adjuvante Bestrahlung, ggf. in Kombination mit einer Chemotherapie. Alternativ kann bei Inoperabilität oder auf Wunsch des Patienten auch eine alleinige Radiochemotherapie erfolgen. Die Nebenwirkungen einer solchen intensiven Tumortherapie sind oft irreversibel und beeinflussen die Lebensqualität der Patienten maßgeblich (Abb. 1).
Abb. 1: Frühe und späte (chronische) Nebenwirkungen einer Behandlung eines Oropharynxkarzinoms (modifiziert nach „Human Body Comparison“, created with BioRender.com, 2020)
Oropharynxkarzinome
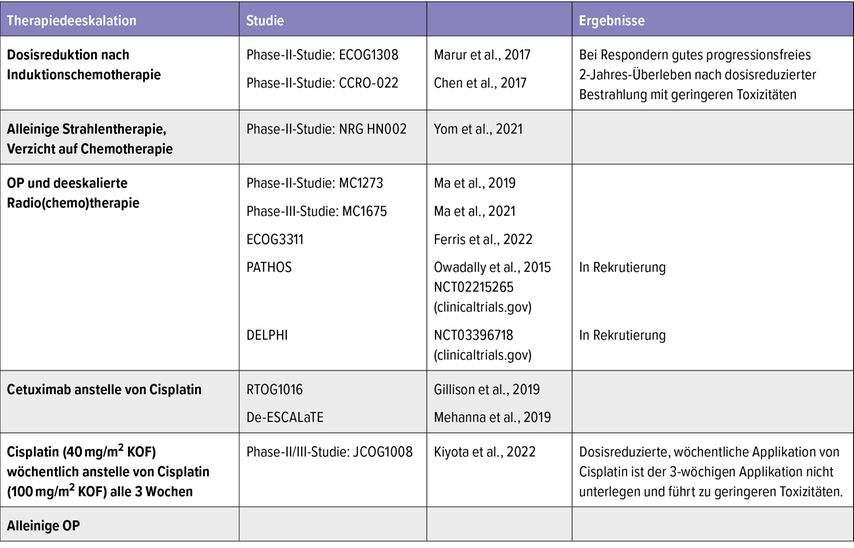
Eine Subgruppe der Kopf-Hals-Tumoren bilden die Oropharynxkarzinome, die sich im Bereich des Gaumens, der Tonsillen und am Zungengrund manifestieren. Wie bei anderen Plattenepithelkarzinomen gelten als Risikofaktoren karzinogene Substanzen wie Alkohol sowie Rauchen, aber auch eine HPV-Infektion. Studien konnten belegen, dass HPV-assoziierte Oropharynxkarzinome ein besseres Therapieansprechen zeigen und somit eine bessere Prognose aufweisen.1,2 Das wird in der aktuellen 8.TNM-Klassifikation berücksichtigt, die die HPV-assoziierten Oropharynxkarzinome als eigenständige Tumorentität aufführt. In einer aktuellen Arbeit konnte bestätigt werden, dass HPV-positive Tumoren sehr strahlensensitiv sind und exzellente Tumorkontrollraten3 aufweisen. Basierend auf diesen Erkenntnissen ist davon auszugehen, dass Patienten mit einem HPV-positiven Oropharynxkarzinom nach aktuellem Therapiestandard überbehandelt werden. Daher ist das Anliegen aktueller Studien, eine Therapiedeeskalation zur Reduktion von Langzeittoxizitäten, bei einer möglichst unverändert guten Tumorkontrolle, zu untersuchen. Hierzu gibt es verschiedene Ansätze. Es werden eine Reduktion der Strahlendosis nach Induktionschemotherapie, die Modifikation oder der Verzicht auf eine zusätzliche Chemotherapie zur Bestrahlung oder die alleinige Operation (Verzicht auf adjuvante Therapie) untersucht (Tab. 1).
Dosisdeeskalation nach Induktionschemotherapie
Eine Möglichkeit, die Therapie zu deeskalieren, ist die Applikation einer Induktionschemotherapie. In der ECOG1308-Studie wurden Patienten mit einem lokoregionär fortgeschrittenen Oropharynxkarzinom mit einer neoadjuvanten Chemotherapie vor primärer Radiochemotherapie behandelt. In 70% der Patienten konnte durch die Induktionschemotherapie (3 Zyklen Cisplatin, Paclitaxel, Cetuximab) eine klinische Komplettremission erreicht werden. In diesen Fällen wurde schließlich die Bestrahlungsdosis von 69,3Gy auf 54Gy reduziert. Vor allem bei Patienten mit <cT4, <cN2c und max. 10 „pack years“ konnte ein hervorragendes Therapieansprechen erreicht werden (progressionsfreies 2-Jahres-Überleben 96%). Die Reduktion der Dosis auf ≤54Gy resultierte in einer besseren Schluckfunktion der Patienten.4 Eine weitere ähnliche Studie (CCRO-022) konnte bei Patienten, die nach einer Induktionschemotherapie mit Carboplatin/Paclitaxel mindestens ein partielles Ansprechen zeigten, eine Dosisreduktion um 15–20% umsetzen. Auch diese Patienten zeigten ein sehr gutes progressionsfreies2-Jahres-Überleben von 93% und geringere therapiebedingte Toxizitäten.5
Alleinige Strahlentherapie
Um Therapienebenwirkungen zu reduzieren, untersucht die NRG-HN002-Studie die Durchführung einer alleinigen Strahlentherapie. In Patienten mit einem p16-positiven Oropharynxkarzinom und weniger als 10 „packyears“ wurde eine normofraktionierte oder hypofraktionierte Bestrahlung mit 60Gy als Therapie mit und ohne zusätzliche Cisplatin-basierte Chemotherapie verglichen. In der Radiochemotherapie-Gruppe zeigte sich im Vergleich zur alleinigen Strahlentherapie wiederum ein höheres progressionsfreies 2-Jahres-Überleben (90,5% vs. 87,6%). Zwar traten mehr akute Nebenwirkungen im Radiochemotherapie-Arm auf, jedoch ist zu beachten, dass es keine Unterschiede im Auftreten der irreversiblen Spätnebenwirkungen gab. Diese Studie belegt einen Benefit der zusätzlichen Chemotherapie.6
Deeskalation der postoperativen Radio(chemo)therapie
Eine Vielzahl von Studien befasst sich mit einer Deeskalation der Radiochemotherapie nach durchgeführter Operation. In der Phase-II-StudieMC1273 wurde bisher die deutlichste Dosisdeeskalation durchgeführt. Behandelt wurden Patienten mit einem p16-positiven Oropharynxkarzinom und maximal 10 „pack years“ nach R0-Resektion. Der primäre Endpunkt war wieder die lokoregionäre Kontrolle nach 2 Jahren. Im Falle einer extrakapsulären Extension (ECE) der Lymphknotenmetastasen nach Operation erfolgten eine Bestrahlung mit 36Gy und eine simultane Chemotherapie mit Docetaxel bzw. bei lymphovaskulärer oder perineuraler Invasion mit 30Gy und Docetaxel. Nach 2 Jahren lag das progressionsfreie Überleben bei 91,1% sowie die lokoregionale Kontrolle (LRC) bei 96,2%. Diese Ergebnisse sind mit historischen Kontrollen vergleichbar (z.B. LRC in der RTOG0234-Studie: 86,4%).7 In der darauf aufbauenden Phase-III-Studie MC1675wurde bei Patienten mit einem Oropharynxkarzinom mit intermediärem Risiko die dosisdeeskalierte Behandlung mit Docetaxel und 30Gy bzw. 36Gy (ECE) mit der Standardbehandlung mit Cisplatin und 60Gy hinsichtlich der Nebenwirkungen und des Therapieansprechens verglichen. Insgesamt zeigte sich eine Überlegenheit der Standardtherapie hinsichtlich des progressionsfreien und fernmetastasenfreien Überlebens sowie der lokalen Kontrolle. Dieser Unterschied wurde insbesondere in der Gruppe der pN2- und ECE-positiven Tumoren deutlich (progressionsfreies Überleben von 42,9% vs. 100%, lokoregionäre Kontrolle 77% vs. 100% sowie metastasenfreies Überleben von 59,4% vs. 100%).8
In der ECOG3311-Studie wurden die Patienten anhand des postoperativen Risikoprofils eingestuft und eine Dosisdeeskalation wurde durchgeführt. Bei Patienten mit einem Tumor mit niedrigem Risiko (pT1–2, pN0–1) erfolgte eine regelmäßige Tumornachsorge, bei intermediärem Risiko (knappe Schnittränder, ECE<1mm, 2–4 LK-Metastasen, Pn1, L1) erfolgte eine Randomisierung in eine 50-Gy- vs. 60-Gy-Gruppe sowie bei hohem Risiko (R1, ECE oder mind. 5 LK-Metastasen) eine simultane adjuvante Cisplatin-basierte Radiochemotherapie mit 66Gy. Die progressionsfreien Überlebensraten nach 2 Jahren waren bei niedrigem Risikoprofil 96,9% und hohem Risikoprofil 90,7%. In der intermediären Gruppe zeigten sich vergleichbare Werte in der 60- und 50-Gy-Gruppe (96% vs. 94,9%). Diese Studie verdeutlicht den Benefit einer Stratifizierung der Patienten. So konnten in der Hochrisiko-Gruppe nahezu die klinischen Ergebnisse der Niedrigrisiko-Gruppe erreicht werden.9
Auch in der PATHOS-Studie wurden die Patienten nach erfolgter Resektion eines Oropharynxkarzinoms in drei Gruppen entsprechend den Risikoprofilen eingeteilt.10 Die Patienten in der Gruppe mit niedrigem Risiko erhielten ebenso wie in der ECOG3311-Studie keine adjuvante Therapie. Patienten der Gruppe mit intermediärem Risiko wurden mit einer adjuvanten Bestrahlung entweder in Standarddosierung oder in reduzierter Dosierung behandelt und die Hochrisiko-Gruppe mit einer Radiochemotherapie oder alleiniger Bestrahlung. Die Daten zur Schluckfunktion und zum Überleben werden mit großem Interesse erwartet.
Eine weitere Studie, die sich aktuell in der Rekrutierungsphase befindet, ist die DELPHI-Studie (NCT03396718). In dieser multizentrischen Studie erfolgt eine zweistufige Dosisreduktion. Die primären Endpunkte sind frühe und späte Toxizitäten. Zudem erfolgt die Erfassung der Lebensqualität der Patienten.
Deeskalation der simultanen Systemtherapie
Neben der adjuvanten Bestrahlung wurde auch eine Modifikation der Systemtherapie untersucht. In der randomisierten, multizentrischen RTOG-1016-Studie wurden insgesamt über 700 Patienten mit einem p16-positiven Oropharynxkarzinom behandelt. Die Patienten wurden anhand von Risikofaktoren (T- und N-Status, Raucherstatus und ECOG) stratifiziert. Die Behandlung erfolgte dann in zwei Armen. Im Kontrollarm wurde eine Bestrahlung mit Cisplatin (100mg/m2 KOF, d1, d22) und im Experimentalarm mit Cetuximab (400mg/m2 KOF „loading dose“ + 250mg/m2 KOF/Woche) kombiniert. Es zeigte sich kein signifikanter Unterschied im Toxizitätsprofil beider Therapiearme, aber sowohl das progressionsfreie als auch das Gesamtüberleben und die lokale Kontrolle waren im Experimentalarm schlechter.11
Diese Ergebnisse werden von einer weiteren randomisierten Phase-III-Studie (De-ESCALaTE) gestützt, welche die simultane Systemtherapie untersucht. Insgesamt erhielten 334 Patienten mit einem HPV-positiven Oropharynxkarzinom eine normalfraktionierte Bestrahlung über 7 Wochen in insgesamt 32 Zentren. Im Kontrollarm erhielten die Patienten zur Bestrahlung 100mg/m2 KOF Cisplatin alle 3 Wochen und im Experimentalarm Cetuximab („loading dose“ von 400mg/m2 KOF und dann 250mg/m2 KOF wöchentlich). Verglichen wurden hier die Toxizitäten (Grad 3 und höher) nach 2 Jahren. Diese Studie ergab keine signifikanten Unterschiede im Toxizitätsprofil beider Therapiearme. Aber es zeigten sich auch hier im Experimentalarm mehr Rezidive sowie ein kürzeres Gesamtüberleben nach 2 Jahren (97,5% vs. 89,4%).12
Diese Studien bestätigen die aktuelle Standardchemotherapie mit Cisplatin. Um das Toxizitätsprofil der Chemotherapie mit Cisplatin zu evaluieren, erhielten Patienten mit einem sehr hohen Rezidivrisiko nach OP in der JCOG1008-Studie entweder eine simultane Radiochemotherapie mit Cisplatin 100mg/m2 KOF alle 3 Wochen oder mit Cisplatin 40mg/m2 KOF wöchentlich. Insgesamt wurden 261 Patienten eingeschlossen. Die 3. Interimsanalyse zeigte, dass die Behandlung mit Cisplatin 40mg/m2 KOF wöchentlich der Behandlung mit Cisplatin 100mg/m2 KOF dreiwöchentlich nicht unterlegen ist und seltener zu Neutropenien, Infektionen, der Beeinträchtigung der Nierenfunktion und des Hörvermögens führt.13
Zukünftige Therapiedeeskalationsansätze
Zukünftige Therapiedeeskalationsansätze bilden eine weitere Individualisierung der Therapie. Beispielsweise sollen mittels radiologischer Untersuchungen (PET-basierter Untersuchungen) hypoxische Areale detektiert werden, damit sie dann wieder zielgerichtet behandelt werden.14
Literatur:
1 Ang K et al.: Human papillomavirus and survival of patients with oropharyngeal cancer. N Engl J Med 2010; 363(1): 24-35 2 Lohaus F et al.: HPV16 DNA status is a strong prognosticator of loco-regional control after postoperative radiochemotherapy of locally advanced oropharyngeal carcinoma: results from a multicentre explorative study of the German Cancer Consortium Radiation Oncology Group (DKTK-ROG). Radiother Oncol 2014; 113(3): 317-23 3 Palma DA et al.: Assessment of toxic effects and survival in treatment deescalation with radiotherapy vs transoral surgery for HPV-associated oropharyngeal squamous cell carcinoma: the ORATOR2 phase 2 randomized clinical trial. JAMA Oncol 2022; 8(6): 1-7 4 Marur S et al.: E1308: phase II trial of induction chemotherapy followed by reduced-dose radiation and weekly cetuximab in patients with HPV-associated resectable squamous cell carcinoma of the orOpharynx – ECOG-ACRIN Cancer Research Group. J Clin Oncol 2017; 35(5): 490-7 5 Chen AM et al.: Reduced-dose radiotherapy for human papillomavirus-associated squamous carcioma of the oropharynx: a single-arm phase 2 study. Lancet oncol 2017; 18(6): 803-11 6 Yom SS et al.: Reduced-dose radiation therapy for HPV-associated oropharyngeal carcinoma (NRG Oncology HN002). J Clin Oncol 2021; 39(9): 956-65 7 Ma DJ et al.: Phase II evaluation of aggressive dose de-escalation for adjuvant chemoradiotherapy in human papillomavirus-associated oropharynx squamous cell carcinoma. J Clin Oncol 2019; 37(22): 1909-18 8 Ma DJ et al.: MC1675, a phase III evaluation of de-escalated adjuvant radiation therapy (DART) vs. standard adjuvant treatment for human papillomavirus associated oropharyngeal squamous cell carcinoma. Int J Radiat Oncol Biol Phys 2021; 111: 1324 9 Ferris RL et al.: Phase II randomized trial of transoral surgery and low-dose intensity modulated radiation therapy in resectable p16+ locally advanced oropharynx cancer: an ECOG-ACRIN Cancer Research Group Trial (E3311). J Clin Oncol 2022; 40(2): 138-49 10 Owadally W et al.: PATHOS: a phase II/III trial of risk-stratified, reduced intensity adjuvant treatment in patients undergoing transoral surgery for Human papillomavirus (HPV) positive oropharyngeal cancer. BMC Cancer 2015; 15: 602 11 Gillison ML et al.: Radiotherapy plus cetuximab or cisplatin in human papillomavirus-positive oropharyngeal cancer (NRG Oncology RTOG 1016): a randomised, multicentre, non-inferiority trial. Lancet 2019; 393(10166): 40-50 12 Mehanna H et al.: De-escalation after DE-ESCALATE and RTOG 1016: a head and neck cancer InterGroup Framework for Future de-escalation studies. J Clin Oncol 2020; 38(22): 2552-7 13 Kiyota N et al.: Weekly cisplatinplus radiation for postoperative head and neck cancer (JCOG1008): A multicenter, noninferiority, phase II/III randomized controlled trial. J Clin Oncol 2022; 40(18): 1980-90 14 Lee N et al.: Strategy of using intratreatment hypoxia imaging to selectively and safely guide radiation dose de-escalation concurrent with chemotherapy for locoregionally advanced human papillomavirus-related oropharyngeal carcinoma. Int J Radiat Oncol Biol Phys 2016; 96(1): 9-17
Das könnte Sie auch interessieren:
Vorgehensweise bei Verdacht auf eine auditive Verarbeitungsstörung (AVS)
Auditive Verarbeitungsstörungen (AVS) sind ein seit Jahren sehr kontrovers diskutiertes Thema, welches sowohl in der Diagnostik als auch in der Therapie mit uneinheitlichem Vorgehen ...
„Die HNO hat glücklicherweise keine Nachwuchsprobleme“
Prim. Prof. Dr. Fabian Sommer hat am 1. November 2024 die Leitung der Abteilung für Hals-, Nasen-, Ohrenheilkunde in Feldkirch, Vorarlbergs einziger HNO-Abteilung, übernommen. Im ...
Komplementäre & integrative Medizin bei Antibiotikaresistenzen und Pandemien
Komplementäre Behandlungsmethoden können zum Beispiel bei Atemwegsinfekten und Otitis media evidenzbasiert in multimodale Therapiekonzepte der HNO eingebunden werden – vor allem dann, ...